الصوديوم: الدليل العلمي الشامل لخصائصه، تفاعلاته، واستخداماته الصناعية

عنصر الصوديوم هو المعدن القلوي ذو العدد الذري 11 والرمز Na المشتق من اللاتينية Natrium. عزله السير همفري ديفي عام 1807 بالتحليل الكهربائي. يتميز بنشاط كيميائي استثنائي يجعله ينفجر عند ملامسة الماء، ومع ذلك يشكّل مركبه الأشهر — كلوريد الصوديوم — ملح الطعام الذي لا يخلو منه مطبخ واحد على وجه الأرض.
الخلاصة التنفيذية
التقط الفكرة فوراً
- افهم أن الصوديوم فلز قلوي عدده الذري 11 ويفقد إلكترونه الخارجي بسهولة شديدة.
- اربط هذا السلوك مباشرة بعنف تفاعله مع الماء والهواء والرطوبة.
ميّز التناقض الصحيح
- فرّق بين الصوديوم المعدني الخطير وكلوريد الصوديوم المستقر المستخدم كملح طعام.
- تذكّر أن خصائص المركب لا تساوي خصائص عناصره منفردة.
تتبّع التطبيقات المهمة
- لاحظ أن الصوديوم يُنتج صناعياً عبر خلية داونز ويخدم صناعات الكلور، الزجاج، الصابون، والبطاريات الناشئة.
- اربط لونه الأصفر المميز بخطوطه الطيفية ومصابيح بخار الصوديوم.
انتبه للصحة والسلامة
- اعرف أن أيونات الصوديوم أساسية للنبضات العصبية وتوازن السوائل.
- خفّض الإفراط الغذائي في الملح، ولا تتعامل مع الصوديوم المعدني إلا داخل مختبر مجهز وتحت إشراف مختص.
هل توقفت يوماً أمام فيديو لقطعة معدنية فضية تُلقى في بركة ماء فتشتعل وتنفجر بعنف، ثم اكتشفت أن هذا المعدن نفسه يختبئ داخل ملح الطعام الذي ترشّه على بيضتك كل صباح؟ هذا التناقض المذهل هو جوهر قصة عنصر الصوديوم. في هذا المقال ستفهم لماذا يتفاعل بهذه الشراسة، وكيف يعمل داخل خلاياك العصبية، وأين تستخدمه المصانع والمفاعلات النووية. ستخرج من هنا وأنت تنظر إلى ملّاحة المائدة بعين مختلفة تماماً.
تخيّل أن طالباً اسمه فهد يدرس الكيمياء في جامعة الملك سعود بالرياض. طلب منه أستاذه إحضار قطعة صغيرة من الصوديوم المعدني لتجربة مخبرية. فتح فهد العلبة فوجد القطعة مغمورة في سائل زيتي، فتعجّب: لماذا لا تُحفظ في علبة عادية مثل أي معدن؟ وحين أخرج الأستاذ شريحة رقيقة ووضعها في صحن ماء، اشتعلت شعلة صفراء ساطعة وتصاعد غاز بفرقعة مسموعة. في تلك اللحظة أدرك فهد أن هذا المعدن “حيّ” كيميائياً بطريقة لا تشبه أي معدن آخر شاهده. الخلاصة العملية: كل مرة ترى فيها لهباً أصفر في موقد الغاز أو في الألعاب النارية، فأنت غالباً تشاهد ذرات الصوديوم وهي تُطلق طاقتها الضوئية المميزة.
ما البطاقة التعريفية الكاملة لعنصر الصوديوم في الجدول الدوري؟
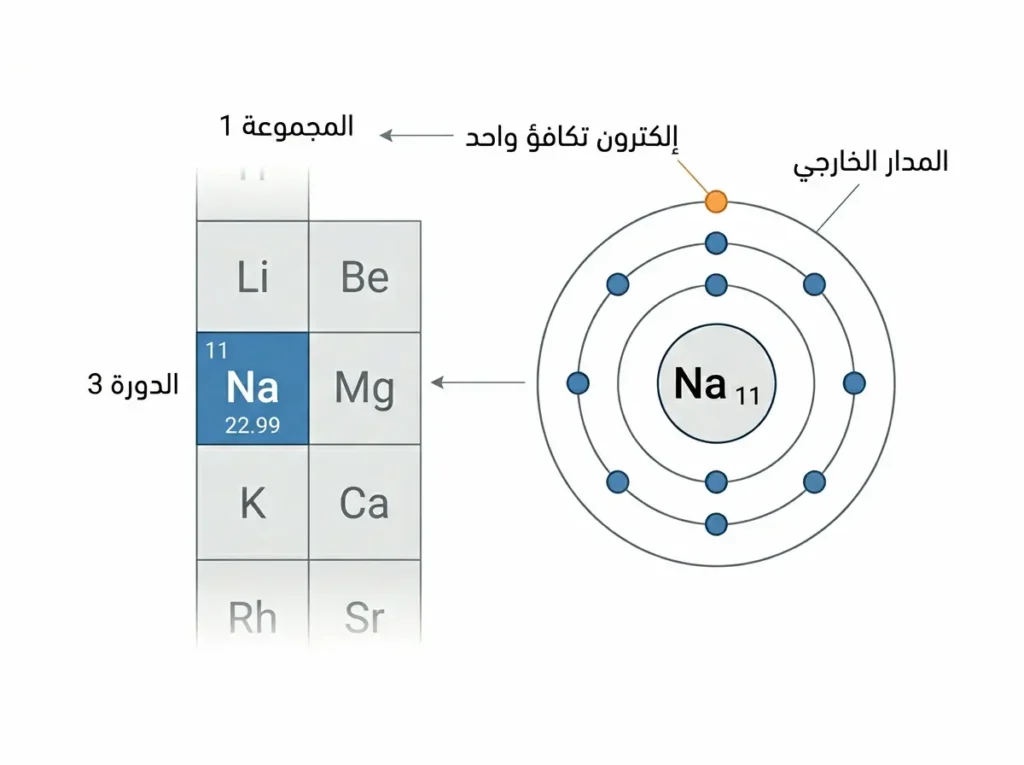
لنبدأ من الأساسيات التي يحتاجها كل طالب وباحث. الرمز الكيميائي لهذا العنصر هو Na، وهو اختصار لكلمة Natrium اللاتينية المشتقة بدورها من الكلمة المصرية القديمة “نطرون” التي كانت تشير إلى ملح كربونات الصوديوم المستخدم في التحنيط. العدد الذري يساوي 11، ما يعني أن نواة كل ذرة تحتوي على 11 بروتوناً. أما الكتلة الذرية فتبلغ نحو 22.99 وحدة كتل ذرية (u)، وهو أحادي النظير المستقر عملياً؛ إذ إن النظير الطبيعي السائد هو صوديوم-23.
يقع الصوديوم في الجدول الدوري للعناصر ضمن المجموعة الأولى (1A) والدورة الثالثة. هذا الموقع يضعه في عائلة الفلزات القلوية (Alkali Metals)، وهي العائلة الأكثر نشاطاً بين الفلزات. توزيعه الإلكتروني يُكتب:
1s2 2s2 2p6 3s1
لاحظ ذلك الإلكترون الوحيد في المدار 3s. هذا الإلكترون “الوحيد” هو مفتاح كل شيء. تخيّل شخصاً يحمل كرة ثقيلة في يد واحدة وهو واقف على حافة جسر: أقل دفعة ستجعله يُسقطها فوراً. هكذا تتصرف ذرة الصوديوم تماماً؛ فهي مستعدة للتخلي عن ذلك الإلكترون عند أدنى فرصة لتصل إلى حالة استقرار تشبه تركيب غاز النيون النبيل.
حقيقة علمية: طاقة التأين الأولى (First Ionization Energy) لعنصر الصوديوم تبلغ فقط 495.8 كيلوجول لكل مول، وهي من أدنى القيم بين جميع العناصر، ما يفسّر سهولة فقدانه لإلكترونه الخارجي ونشاطه الكيميائي العالي.
اقرأ أيضاً:
كيف اكتشف همفري ديفي الصوديوم وغيّر تاريخ الكيمياء؟
قبل عام 1807، كان الكيميائيون يعرفون مركبات الصوديوم جيداً — الصودا الكاوية والملح — لكن لم يتمكن أحد من عزل المعدن النقي. كان السؤال المحيّر: هل “القلويات” مواد بسيطة أم مركبة؟ الإجابة جاءت من مختبر المعهد الملكي في لندن (Royal Institution) على يد السير همفري ديفي (Sir Humphry Davy)، وهو عالم بريطاني لم يتجاوز التاسعة والعشرين من عمره آنذاك.
استخدم ديفي تقنية كانت ثورية في ذلك الوقت: التحليل الكهربائي (Electrolysis). مرّر تياراً كهربائياً قوياً عبر هيدروكسيد الصوديوم المنصهر، فلاحظ ظهور حبيبات معدنية لامعة براقة عند القطب السالب (الكاثود). يُروى أن ديفي قفز من فرحته حرفياً حين رأى تلك القطرات المعدنية تتشكل أمام عينيه. لقد كان يعلم أنه يشهد ميلاد عنصر جديد لم تره عين بشرية من قبل في صورته النقية. وفي الأسبوع نفسه عزل البوتاسيوم بالطريقة ذاتها، ما جعله أحد أغزر الكيميائيين اكتشافاً في التاريخ.
لماذا اختير الاسم Sodium وليس Natrium؟
هنا لطيفة لغوية تستحق التوقف. الاسم الإنكليزي Sodium مشتق من كلمة “سودا” (Soda)، بينما الرمز الكيميائي Na مأخوذ من Natrium اللاتينية. هذا الازدواج يحدث لأن اللغات الأوروبية لم تتفق على تسمية موحدة؛ فالألمان والروس يستخدمون Natrium، بينما يفضل الإنكليز والفرنسيون Sodium. ونحن في العربية نستخدم “صوديوم” تبعاً للتسمية الإنكليزية.
ومضة معرفية: لم يكن ديفي أكاديمياً تقليدياً؛ فقد بدأ حياته متدرباً عند صيدلاني في مدينة بنزانس بإنكلترا، وعلّم نفسه الكيمياء من الكتب قبل أن يصبح أحد أعظم الكيميائيين التجريبيين في القرن التاسع عشر.
اقرأ أيضاً: مايكل فاراداي: رائد الكهرومغناطيسية والتحليل الكهربائي
ما الخصائص الفيزيائية التي تجعل الصوديوم معدناً فريداً؟
أول ما يلفت انتباهك حين تمسك قطعة من الصوديوم النقي — بقفازات بالطبع — هو أنها طرية بشكل مدهش. يمكنك قطعها بسكين مطبخ عادي كما تقطع قطعة زبدة باردة. السطح المقطوع حديثاً يلمع بلون فضي ناصع، لكنه يفقد بريقه خلال ثوانٍ معدودة حين يتفاعل مع أكسجين الهواء ورطوبته ليتغطى بطبقة رمادية باهتة من الأكسيد.
الكثافة منخفضة بشكل لافت: 0.97 غرام لكل سنتيمتر مكعب فقط. هذا يعني أن الصوديوم يطفو على سطح الماء — تماماً كقطعة ثلج — لكن الفارق أن هذا “الجليد” المعدني يشتعل فور لمسه للماء! نقطة الانصهار تبلغ 97.8 درجة مئوية، ونقطة الغليان تصل إلى 883 درجة مئوية. بالمقارنة، الحديد ينصهر عند 1538 درجة، فالفارق هائل.
معلومة سريعة: الصوديوم موصل جيد للكهرباء والحرارة، وهذه الخاصية تحديداً هي التي تجعله مبرداً مثالياً في بعض أنواع المفاعلات النووية، كما سنرى لاحقاً في هذا المقال.
اقرأ أيضاً: عنصر الليثيوم: الدليل العلمي الشامل لخصائصه واستخداماته من الانفجار العظيم حتى ثورة التكنولوجيا
لماذا يتميز الصوديوم بنشاط كيميائي استثنائي؟
هنا نصل إلى خصائص الصوديوم الكيميائية، وهي الجزء الأكثر إثارة. فقد ذكرنا أن ذرته تمتلك إلكتروناً واحداً في غلافها الخارجي. هذا الإلكترون بعيد نسبياً عن النواة — ثلاثة مستويات طاقة تفصله عنها — ما يعني أن قوة جذب النواة له ضعيفة. كما أن كهرسلبيته (Electronegativity) على مقياس باولنغ تبلغ 0.93 فقط، وهي من أدنى القيم على الإطلاق. هذا الرقم يخبرنا أن الصوديوم لا يجذب الإلكترونات، بل يُقدّمها بسخاء شديد.
الفارق الحاسم بين النشاط الكيميائي والخطورة
ثمة خلط شائع يقع فيه كثيرون: النشاط الكيميائي العالي لا يعني بالضرورة أن المادة “سامة”. الصوديوم ليس ساماً بذاته، لكنه خطير ميكانيكياً لأن تفاعلاته عنيفة وطاردة للحرارة (Exothermic). على النقيض من ذلك، هناك مواد سامة للغاية لكنها مستقرة كيميائياً ولا تنفجر. إذاً الخطر هنا مرتبط بالعنف الحراري للتفاعل، لا بالسمية المباشرة. وهذا هو السبب الذي يجعل الكيميائيين يحفظون الصوديوم مغموراً في الكيروسين (Kerosene) أو زيوت معدنية خاملة تمنع وصول الرطوبة والأكسجين إليه.
نقطة تستحق الانتباه: لا تخلط بين كلوريد الصوديوم (ملح الطعام) وعنصر الصوديوم النقي. الأول مركب أيوني مستقر تماماً تأكله يومياً، والثاني معدن متفجر لا يُلمس بيد مكشوفة. الرابطة الأيونية القوية بين الصوديوم والكلور هي التي “تروّض” هذا المعدن الجامح.
| وجه المقارنة | الصوديوم العنصري (Na) | كلوريد الصوديوم (NaCl) |
|---|---|---|
| الطبيعة الكيميائية | عنصر فلزي قلوي نقي | مركب أيوني مستقر |
| الحالة عند درجة الغرفة | معدن طري فضي | بلورات صلبة بيضاء |
| السلوك مع الماء | يتفاعل بعنف وقد يشتعل | يذوب عادة دون انفجار |
| سبب الخطورة أو الأمان | يفقد إلكترونه الخارجي بسهولة شديدة | الأيونات مرتبطة في شبكة بلورية مستقرة |
| طريقة التخزين | تحت الزيت أو الكيروسين بعيداً عن الهواء والرطوبة | في عبوات عادية جافة |
| الاستخدام الأشهر | الاختزال، الصناعة، بعض التطبيقات النووية | الغذاء، الحفظ، الصناعة الكيميائية |
| التعامل المباشر | يتطلب معدات وقاية وإشرافاً مخبرياً | آمن غذائياً ضمن الحدود الصحية |
| المفهوم المفتاح | النشاط الكيميائي العالي | الاستقرار الأيوني |
اقرأ أيضاً:
كيف يتفاعل الصوديوم مع الماء ولماذا ينفجر؟
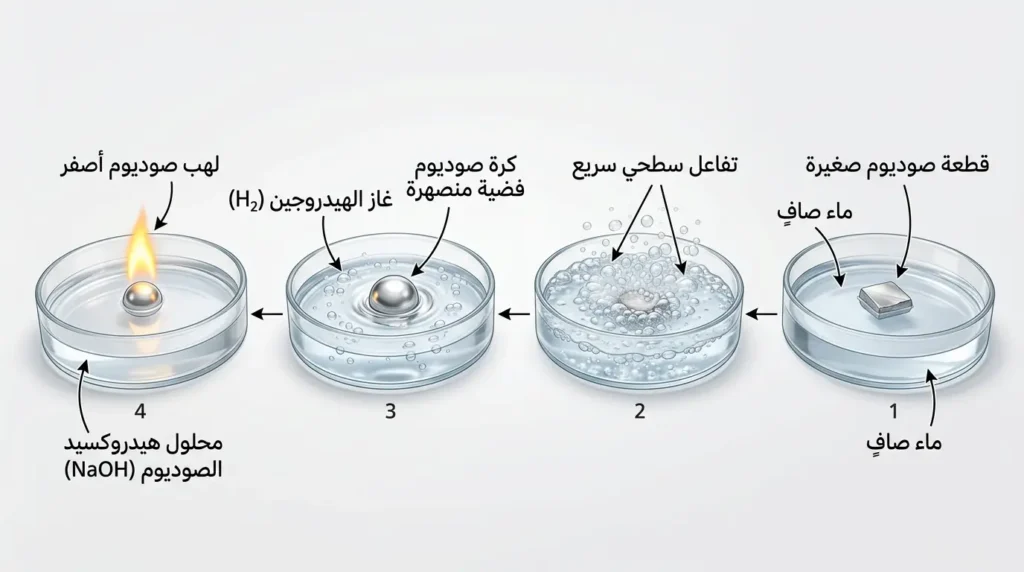
هذا هو التفاعل الأشهر على الإطلاق، والذي يجعل عيون طلاب الكيمياء تتسع دهشة في كل مرة. حين تُلقي قطعة صوديوم في الماء، تحدث سلسلة أحداث متتالية خلال أجزاء من الثانية:
أولاً، يطفو المعدن على السطح لأن كثافته أقل من كثافة الماء. ثانياً، يبدأ التفاعل فوراً مع جزيئات الماء. ثالثاً، تتصاعد حرارة هائلة تصهر المعدن وتحوّله إلى كرة فضية سائلة تتراقص على سطح الماء. رابعاً، يتصاعد غاز الهيدروجين (H₂) الذي يشتعل من شدة الحرارة مُطلقاً لهباً أصفر مميزاً. المعادلة الكيميائية تبدو بسيطة ظاهرياً:
2Na + 2H2O → 2NaOH + H2↑
لكن الميكانيكية الحقيقية أعقد مما تبدو. أظهرت دراسة منشورة في مجلة Nature Chemistry عام 2015 (Mason et al.) أن الانفجار لا يحدث فقط بسبب اشتعال الهيدروجين، بل لأن إلكترونات الصوديوم تقفز إلى الماء بسرعة هائلة فتُحدث “انفجاراً كولوميّاً” (Coulomb Explosion). ما يعني أن ذرات الصوديوم الموجبة تتنافر بعنف بعد فقدان إلكتروناتها، فتتناثر كشظايا دقيقة تزيد مساحة السطح المتفاعل بشكل مفاجئ، وهذا يُضخّم التفاعل بصورة انفجارية.
لماذا يظهر اللهب الأصفر تحديداً؟
هذا سؤال يغفل عنه كثيرون. اللون الأصفر البرتقالي ليس لوناً للهيدروجين المشتعل — فالهيدروجين النقي يحترق بلهب شفاف تقريباً — بل هو لون ذرات الصوديوم المتبخرة. حين تمتص ذرة الصوديوم طاقة حرارية، ينتقل إلكترونها إلى مستوى طاقة أعلى ثم يعود ليُصدر فوتوناً بطول موجي يبلغ 589 نانومتراً، وهو ما تراه عينك بلون أصفر ذهبي. هذا هو نفس المبدأ المستخدم في مصابيح بخار الصوديوم التي تُضيء شوارع المدن السعودية ليلاً بذلك اللون البرتقالي الدافئ المألوف.
اقرأ أيضاً: تفاعل الصوديوم مع الماء: تفاعل كيميائي متفجر
ماذا يحدث حين يلتقي الصوديوم بالأكسجين أو الهالوجينات أو الأحماض؟
التفاعل مع الأكسجين
لا يكتفي الصوديوم بتكوين الأكسيد العادي (Na₂O) حين يحترق في الهواء. في الحقيقة، الناتج الرئيس من احتراقه في وفرة من الأكسجين هو فوق أكسيد الصوديوم (Sodium Peroxide – Na₂O₂)، وهو مسحوق أصفر شاحب. وإذا أردت الحصول على الأكسيد العادي Na₂O، فعليك التحكم بكمية الأكسجين بعناية. فوق الأكسيد هذا مركب مثير للاهتمام؛ لأنه يتفاعل مع ثاني أكسيد الكربون ليُنتج الأكسجين:
2Na2O2 + 2CO2 → 2Na2CO3 + O2
هذه الخاصية استُخدمت فعلياً في الغواصات القديمة ومناجم التعدين لتجديد الهواء في الأماكن المغلقة. تخيّل: مركب كيميائي يمتص غاز الزفير ويُخرج أكسجيناً نقياً!
التفاعل مع الهالوجينات
حين يلتقي الصوديوم بغاز الكلور (Cl₂)، يحدث تفاعل عنيف ينتج عنه كلوريد الصوديوم — نعم، ملح الطعام ذاته:
2Na + Cl2 → 2NaCl
هذا التفاعل طارد للحرارة بشدة، ويُنتج شرارات بيضاء ساطعة. المفارقة العجيبة أن اتحاد معدن متفجر (الصوديوم) مع غاز سام خانق (الكلور) يُنتج مادة نأكلها يومياً! وهذا درس عميق في الكيمياء: خصائص المركب لا علاقة لها بخصائص عناصره المكوّنة.
التفاعل مع الأحماض
يتفاعل الصوديوم بقوة مع الأحماض المخففة، وينتج ملح الحمض المقابل وغاز الهيدروجين. مع حمض الهيدروكلوريك مثلاً:
2Na + 2HCl → 2NaCl + H2↑
لكن هذا التفاعل في المختبر أخطر من تفاعل الصوديوم مع الماء النقي؛ لأن الحمض يتفاعل بسرعة أكبر مع سطح المعدن. ولذلك لا يُجرى هذا التفاعل إلا بكميات صغيرة جداً وتحت إشراف صارم.
رقم لافت: ينتج تفاعل مول واحد فقط من الصوديوم (23 غراماً) مع الماء طاقة حرارية تبلغ نحو 184 كيلوجول. هذه الطاقة تكفي لرفع درجة حرارة لتر كامل من الماء بأكثر من 40 درجة مئوية دفعة واحدة.
اقرأ أيضاً:
- التفاعلات الكيميائية: ما أنواعها وكيف تحدث في كل لحظة؟
- عناصر الهالوجين: الخصائص، المركبات، والتطبيقات
العدسة العلمية الدقيقة – للمهتمين بالتفاصيل الأعمق
في الحالة الغازية، يمكن وصف سلوك إلكترون التكافؤ الوحيد لذرة الصوديوم بنموذج “الإلكترون شبه الهيدروجيني” (Hydrogenic Model)، لكن مع تطبيق تصحيح العيب الكمّي (Quantum Defect Correction) الذي يأخذ بعين الاعتبار اختراق الإلكترون 3s للطبقات الداخلية المملوءة. هذا التصحيح يجعل طاقة ربط الإلكترون الخارجي أعلى مما يتنبأ به نموذج بور البسيط بنحو 30%، وهو ما يفسّر الفارق الدقيق بين طاقة التأين المحسوبة نظرياً والمقاسة تجريبياً. خطوط الطيف الذري للصوديوم — وأشهرها الخط المزدوج D عند 589.0 و589.6 نانومتر — تنشأ من الفصل بالتفاعل المغزلي-المداري (Spin-Orbit Coupling)، وهو تأثير نسبوي بسيط لكنه قابل للقياس بدقة عالية. هذا الفصل الدقيق جعل خطوط الصوديوم أداة معيارية في المطيافية (Spectroscopy) لمعايرة الأجهزة البصرية منذ أكثر من قرن ونصف.
اقرأ أيضاً: ميكانيكا الكم: المبادئ الأساسية وتطبيقاتها
أين يختبئ الصوديوم في الطبيعة ولماذا لا نجده حراً أبداً؟
لن تجد قطعة صوديوم نقية ملقاة على الأرض مهما بحثت. السبب واضح الآن: نشاطه الكيميائي يجعله يتفاعل مع كل شيء حوله — الماء، الأكسجين، وحتى النيتروجين في درجات حرارة عالية. لكنه سادس أكثر العناصر وفرة في القشرة الأرضية، بنسبة تقارب 2.6% من كتلتها.
أكبر مخزن للصوديوم على كوكبنا هو المحيطات. يحتوي كل لتر من مياه البحر على نحو 10.8 غرامات من أيونات الصوديوم. فإذا تخيلت أن كل محيطات العالم جفّت فجأة، فستتبقى طبقة ملح سمكها عشرات الأمتار تُغطي قاع البحار بأكمله. كما أن البحيرات المالحة مثل البحر الميت تحتوي على تركيزات أعلى بكثير. أما المعادن الصخرية التي يتواجد فيها الصوديوم فأشهرها: الهاليت (Halite – NaCl)، وهو الملح الصخري الذي يُستخرج من المناجم تحت الأرض، والترونا (Trona – Na₃(CO₃)(HCO₃)·2H₂O) التي تُستخدم مصدراً لكربونات الصوديوم. في المملكة العربية السعودية، توجد رواسب ملحية ضخمة في مناطق عديدة، وتُعَدُّ صناعة الملح من الصناعات التقليدية العريقة في المنطقة الشرقية.
من المثير أن تعرف: بحسب تقديرات هيئة المسح الجيولوجي الأمريكية (USGS)، يُنتج العالم سنوياً أكثر من 290 مليون طن متري من الملح الصخري، ويُستخدم نحو 40% منها في الصناعات الكيميائية وليس في الغذاء.
اقرأ أيضاً: الصخور الرسوبية: التكوين، الأنواع، والأهمية الجيولوجية
كيف تُنتج المصانع الصوديوم النقي عبر خلية داونز؟
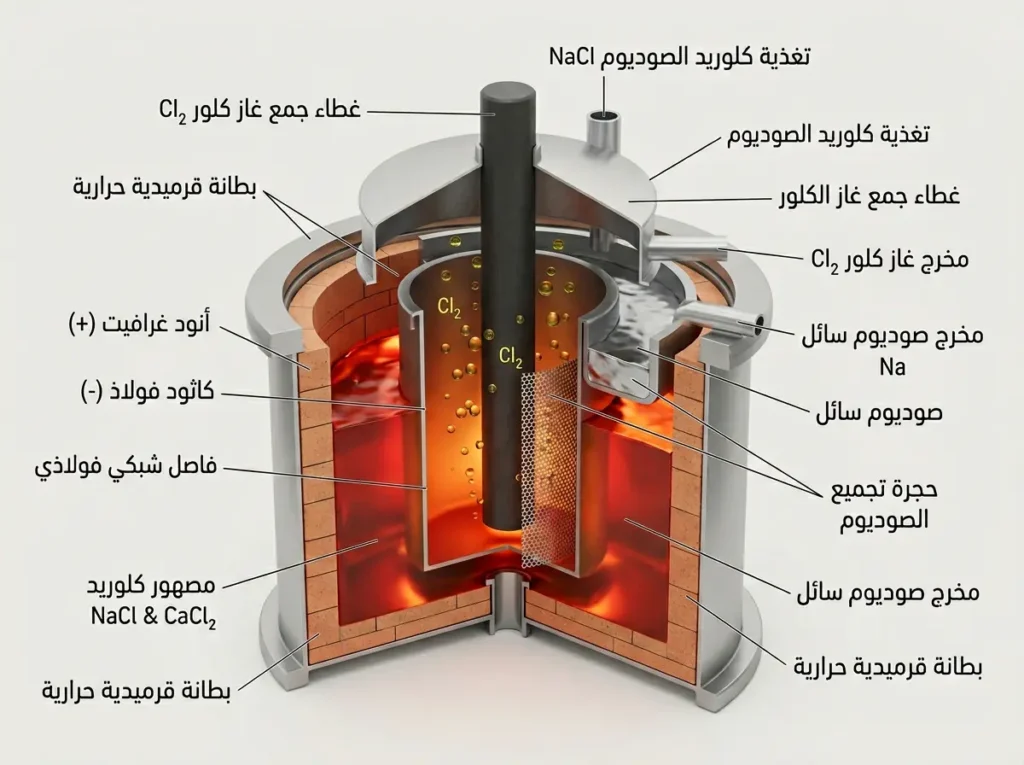
هنا ننتقل إلى واحدة من أذكى العمليات الصناعية في تاريخ الكيمياء. خلية داونز (Downs Cell) صُممت خصيصاً لاستخلاص الصوديوم المعدني من مصهور كلوريد الصوديوم عبر التحليل الكهربائي. فلماذا لا نُحلّل محلول ملح الطعام المذاب في الماء ببساطة؟ لأن الصوديوم المتحرر سيتفاعل فوراً مع الماء وينفجر قبل أن نتمكن من جمعه.
لذلك يُصهَر كلوريد الصوديوم عند درجة حرارة مرتفعة. لكن نقطة انصهار NaCl النقي تبلغ 801 درجة مئوية، وهي درجة عالية جداً تزيد التكلفة. الحل الذكي: يُضاف كلوريد الكالسيوم (CaCl₂) إلى الخليط ليخفض نقطة الانصهار إلى نحو 600 درجة مئوية، وهذا يوفر طاقة كبيرة.
خطوات إنتاج الصوديوم في خلية داونز
داخل الخلية، يوجد قطب سالب (كاثود) من الفولاذ وقطب موجب (أنود) من الغرافيت. عند مرور التيار الكهربائي:
- عند الكاثود: تُختزل أيونات الصوديوم (Na⁺) وتكتسب إلكتروناً لتتحول إلى صوديوم معدني سائل يطفو إلى الأعلى بسبب كثافته المنخفضة، فيُجمع في حجرة خاصة.
- عند الأنود: تتأكسد أيونات الكلوريد (Cl⁻) وتتحول إلى غاز الكلور (Cl₂) الذي يُجمع كمنتج ثانوي ذي قيمة تجارية عالية.
فاصل أسطواني من الفولاذ يفصل بين الكاثود والأنود لمنع اختلاط الصوديوم السائل مع غاز الكلور؛ لأن اختلاطهما يعني تفاعلاً عكسياً عنيفاً يُعيد تكوين كلوريد الصوديوم ويُبدد كل الطاقة المستثمرة.
لفتة علمية: الكلور المُنتج كمنتج ثانوي في خلية داونز ليس “فضلة” على الإطلاق. هو أحد أكثر الغازات طلباً في الصناعة الكيميائية؛ إذ يدخل في تصنيع المبيضات والبلاستيك (PVC) والمذيبات العضوية ومئات المنتجات الأخرى.
ما أشهر مركبات الصوديوم التي تُشكّل عصب الصناعة الحديثة؟
عنصر الصوديوم بصورته النقية مهم، لكن مركباته هي التي تُحرّك عجلة الصناعة فعلياً. لنستعرض أبرزها.
كلوريد الصوديوم (NaCl – Sodium Chloride): هو الأشهر بلا منازع. يُستخدم ليس فقط ملحاً للطعام، بل أيضاً في إذابة الجليد على الطرق في البلدان الباردة، وفي صناعة الكلور والصودا الكاوية عبر عملية كلور-قلوي (Chlor-Alkali Process). إنتاجه العالمي يجعله أحد أرخص المواد الكيميائية وأوسعها انتشاراً.
هيدروكسيد الصوديوم (NaOH – Sodium Hydroxide): يُعرف بالصودا الكاوية (Caustic Soda). إذا كنت قد صنعت صابوناً يدوياً أو شاهدت أحداً يفعل ذلك، فقد استخدم هذا المركب. يتفاعل مع الدهون والزيوت في عملية التصبّن (Saponification) لإنتاج الصابون والغليسرين. لكن استخداماته تتجاوز ذلك بمراحل: صناعة الورق، تنقية الألومنيوم من البوكسيت (عملية باير – Bayer Process)، معالجة المنسوجات، وإنتاج الأدوية. بحسب تقارير صناعية حديثة، يتجاوز الإنتاج العالمي من هيدروكسيد الصوديوم 70 مليون طن سنوياً.
كربونات الصوديوم (Na₂CO₃ – Sodium Carbonate): تُعرف بصودا الغسيل (Washing Soda) أو رماد الصودا (Soda Ash). تدخل في صناعة الزجاج — نعم، النافذة التي تنظر منها الآن تحتوي على صوديوم — وفي صناعة المنظفات ومعالجة المياه.
بيكربونات الصوديوم (NaHCO₃ – Sodium Bicarbonate): هي “بيكربونات الصودا” أو “صودا الخَبز” التي تستخدمها في إعداد الكعك. حين تسخّنها تتحلل وتُطلق غاز ثاني أكسيد الكربون الذي يصنع الفقاعات ويُعطي المعجنات قوامها الهشّ.
هيبوكلوريت الصوديوم (NaOCl – Sodium Hypochlorite): هو المادة الفعالة في مبيضات الغسيل مثل “الكلوركس” الشهير. محلوله المخفف يُستخدم على نطاق واسع في تعقيم مياه الشرب حول العالم.
اقرأ أيضاً: المحاليل المائية: المفهوم، الأنواع، والتطبيقات
| المركب | الصيغة | الاستخدام الرئيس | القطاع أو المثال التطبيقي | ملاحظة مهمة |
|---|---|---|---|---|
| كلوريد الصوديوم | NaCl | الغذاء والمواد الأولية الصناعية | ملح الطعام، عملية كلور-قلوي | أكثر مركبات الصوديوم شيوعاً |
| هيدروكسيد الصوديوم | NaOH | التصبن والمعالجة الكيميائية | الصابون، الورق، تنقية الألومينا | مادة كاوية قوية |
| كربونات الصوديوم | Na2CO3 | صناعة الزجاج والمنظفات | الزجاج التجاري، معالجة المياه | تُعرف برماد الصودا |
| بيكربونات الصوديوم | NaHCO3 | الخَبز والتنظيم الحمضي | المعجنات، بعض التطبيقات الطبية والمنزلية | تطلق CO2 عند التسخين |
| هيبوكلوريت الصوديوم | NaOCl | التعقيم والتبييض | مياه الشرب، مبيضات الغسيل | يجب استخدامه بتركيزات مناسبة |
| فوق أكسيد الصوديوم | Na2O2 | توليد الأكسجين وامتصاص CO2 | تطبيقات هواء مغلق تاريخية | مركب مؤكسد تفاعلي |
العلم في خدمتك: كيف تلاحظ الصوديوم في حياتك اليومية؟
هل تساءلت يوماً لماذا تبدو إضاءة شوارع مدينتك ليلاً بلون برتقالي مائل للصفرة وليست بيضاء كإضاءة المنزل؟ ذلك لأن كثيراً من مصابيح الشوارع — خصوصاً القديمة منها — هي مصابيح بخار الصوديوم (Sodium Vapor Lamps). تعمل بتسخين بخار الصوديوم داخل أنبوب زجاجي حتى تُصدر ذراته ذلك اللون الأصفر المميز عند الطول الموجي 589 نانومتراً.
جرّب أن تُمسك قليلاً من ملح الطعام بين إصبعيك وترشّه فوق لهب موقد الغاز في مطبخك — بحذر طبعاً. ستلاحظ أن اللهب يتحول فوراً إلى أصفر ساطع. هذا هو “اختبار اللهب” (Flame Test) الذي يستخدمه الكيميائيون للتعرف على وجود أيونات الصوديوم. كما أن انتشار الصوديوم في بيئتنا يجعل هذا اللون الأصفر “ملوِّثاً” شائعاً يُخفي ألوان لهب العناصر الأخرى، ولذلك يستخدم الكيميائيون زجاج الكوبالت الأزرق لتصفية الضوء الأصفر ورؤية ما خلفه.
اقرأ أيضاً: لون السماء: الفيزياء وراء الظاهرة
تحذير وإخلاء مسؤولية من خلية
يشرح هذا المقال مادة الصوديوم من منظور علمي وتعليمي فقط. لا ينبغي تنفيذ أي تجربة تتضمن الصوديوم المعدني، اللهب، القلويات الكاوية، أو الغازات التفاعلية خارج مختبر مجهز وتحت إشراف مختص مؤهل.
المعلومات الصحية الواردة هنا تعريفية ولا تُعد بديلاً عن استشارة الطبيب أو أخصائي التغذية، خصوصاً في حالات ارتفاع ضغط الدم، أمراض الكلى، اضطرابات الشوارد، أو الاشتباه بنقص الصوديوم أو زيادته.
إذا وقع تعرض كيميائي أو حرق أو ابتلاع غير مقصود، فاتبع بروتوكولات الطوارئ المحلية واطلب المساعدة الطبية فوراً. تعتمد خلية على مصادر علمية موثوقة، لكن التطبيق العملي مسؤولية المختبر والجهة المشرفة.
جرّب بنفسك: المختبر المنزلي
هذه تجربة بسيطة وآمنة تماماً يمكنك تنفيذها الآن. أحضِر شمعة وأشعلها، ثم خذ عود أسنان خشبياً وبلّل طرفه بالماء وغمسه في القليل من ملح الطعام العادي. قرّب الطرف المملّح من لهب الشمعة — ليس داخل اللهب بل عند حافته الخارجية. ستلاحظ فوراً ومضة صفراء زاهية. هذا هو طيف الانبعاث (Emission Spectrum) لأيونات الصوديوم حين تكتسب طاقة حرارية كافية. النتيجة المتوقعة: لهب أصفر لامع يظهر للحظة ثم يختفي حين يحترق الملح على طرف العود. المفهوم العلمي: الإلكترونات في ذرات الصوديوم تقفز إلى مستويات طاقة أعلى ثم تعود لتُصدر ضوءاً بطول موجي محدد.
كيف تستخدم الصناعة والتكنولوجيا عنصر الصوديوم النقي؟
استخدامات الصوديوم في الصناعة تتجاوز بكثير ما يتخيله معظم الناس. لنتعمق في أبرز هذه التطبيقات.
مبرّد المفاعلات النووية: في بعض أنواع المفاعلات النووية المتقدمة، يُسمّى “مفاعل السائل المعدني السريع” (Liquid Metal Fast Reactor)، يُستخدم الصوديوم المصهور كسائل تبريد بدلاً من الماء. فلماذا الصوديوم وليس الماء؟ لأن الصوديوم السائل ينقل الحرارة بكفاءة عالية جداً دون أن يتحول إلى بخار عند درجات حرارة تصل إلى 500 درجة مئوية — بينما الماء يغلي عند 100 درجة فقط. كما أن الصوديوم لا يُبطئ النيوترونات السريعة، وهذا ضروري لتشغيل هذا النوع من المفاعلات. المفاعل الفرنسي Superphénix والمفاعل الروسي BN-800 كلاهما يستخدمان هذه التقنية.
مصابيح بخار الصوديوم: ذكرناها سابقاً لكنها تستحق توسعاً. النوع “منخفض الضغط” (LPS) يُعطي ضوءاً أصفر نقياً شبه أحادي اللون، وكفاءته المضيئة من الأعلى بين جميع المصابيح: تصل إلى 200 لومن لكل واط. بينما النوع “عالي الضغط” (HPS) يُعطي طيفاً أوسع بلون أبيض مائل للذهبي، وهو الأكثر شيوعاً في إنارة الشوارع والطرق السريعة. في السعودية، شهدت السنوات الأخيرة تحولاً تدريجياً نحو إضاءة LED الأكثر كفاءة، لكن مصابيح بخار الصوديوم لا تزال حاضرة في كثير من المدن والقرى.
استخلاص معادن أخرى: يُستخدم الصوديوم في عملية كرول (Kroll Process) لاستخلاص التيتانيوم (Titanium) من كلوريده. التيتانيوم معدن خفيف وقوي يُستخدم في صناعة الطائرات والأطراف الصناعية. الصوديوم يختزل كلوريد التيتانيوم ليُحرر المعدن النقي، وهي عملية تحتاج حرارة عالية وظروفاً محكمة.
بطاريات الصوديوم-أيون (Sodium-Ion Batteries): هذا مجال بحثي ناشئ ومثير جداً. مع ازدياد الطلب على بطاريات تخزين الطاقة، بدأ العلماء يبحثون عن بدائل أرخص من بطاريات الليثيوم-أيون. الصوديوم أوفر بكثير وأكثر توفراً من الليثيوم. بحسب ورقة بحثية نُشرت في مجلة Nature Energy عام 2023 (Tarascon et al.)، حققت بعض نماذج بطاريات الصوديوم-أيون كثافة طاقة تقارب 160 واط·ساعة لكل كيلوغرام، وهو رقم يقترب من أداء بطاريات الليثيوم الأولى. الشركات الصينية بدأت فعلياً بإنتاج هذا النوع تجارياً منذ عام 2023.
هل تعلم؟ يُضاف الصوديوم المعدني أحياناً إلى وقود الصواريخ كعامل اختزال. كما أنه يُستخدم في تصنيع بعض المركبات العضوية الدوائية عبر تفاعل بيرش (Birch Reduction) الذي يعتمد على إذابة الصوديوم في الأمونيا السائلة.
اقرأ أيضاً: الثورة الصناعية الرابعة: الدليل العلمي الشامل للتقنيات التي تعيد صياغة مستقبل البشرية
الوجه الخفي: نظائر الصوديوم المشعة في خدمة الطب وتتبع الأعطال
لقد ذكرنا في البطاقة التعريفية للعنصر أن “صوديوم-23” هو النظير المستقر الوحيد، لكن ماذا عن النظائر المشعة التي يصنعها الفيزيائيون؟ هنا يبرز دور نظيرين في غاية الأهمية: صوديوم-22 وصوديوم-24. يتمتع صوديوم-24 بعمر نصف قصير يبلغ نحو 15 ساعة فقط، وهو ما يجعله أداة هندسية مثالية لتتبع التسربات في شبكات الأنابيب المعقدة تحت الأرض؛ إذ يُحقن في الأنابيب وتُتتبع إشعاعاته لتحديد موقع التسرب بدقة، ثم يختفي الإشعاع بسرعة فائقة دون ترك تلوث بيئي. أما في المجال الطبي، فيُستخدم كمتتبع إشعاعي (Radiotracer) لدراسة تدفق الدم ورصد اضطرابات الدورة الدموية، ليثبت الصوديوم أنه لا يضيء الشوارع فحسب، بل يضيء أيضاً طريق الأطباء داخل جسم الإنسان.
كيف يعمل الصوديوم داخل جسمك ولماذا لا تستطيع خلاياك العيش بدونه؟
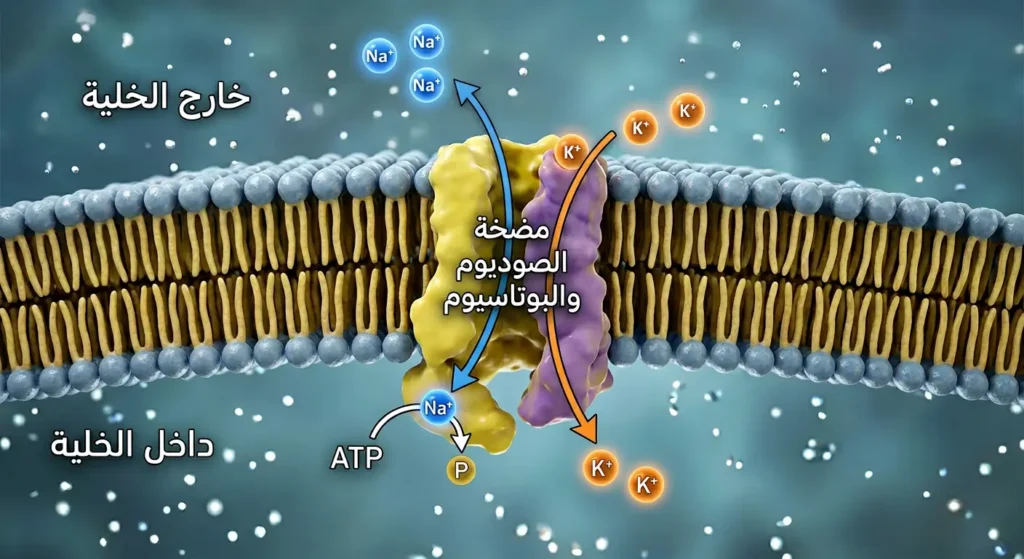
الآن ننتقل من عالم المصانع والمختبرات إلى عالم أكثر حميمية: جسمك أنت. الدور البيولوجي لعنصر الصوديوم أساسي لدرجة أن غيابه يعني الموت الفوري للخلايا. فما الذي يفعله بالضبط؟
مضخة الصوديوم والبوتاسيوم (Na⁺/K⁺-ATPase): تخيّل أن كل خلية في جسمك هي منزل له باب أمامي وباب خلفي. المضخة تعمل كحارس أمن ذكي: تطرد 3 أيونات صوديوم إلى خارج الخلية وتُدخل 2 أيون بوتاسيوم إلى داخلها في كل دورة عمل. هذا يُنشئ فرقاً في الجهد الكهربائي عبر غشاء الخلية يبلغ نحو -70 ميلي فولت. قد يبدو رقماً ضئيلاً، لكنه ضروري لكل نبضة عصبية ولكل انقباضة عضلية في جسمك.
حين يصلك منبه — لمسة ساخنة مثلاً — تنفتح قنوات الصوديوم (Voltage-Gated Sodium Channels) في الخلية العصبية فيندفع الصوديوم إلى الداخل بسرعة مذهلة، فينعكس الجهد الكهربائي ويتولد ما يُسمى “جهد الفعل” (Action Potential). هذه الإشارة تنتقل على طول العصب كموجة كهربائية بسرعة تصل إلى 120 متراً في الثانية — أي أسرع من سيارة تسير بسرعة 430 كيلومتراً في الساعة.
تنظيم ضغط الدم وتوازن السوائل: الكلى تتحكم بكمية الصوديوم في الجسم بدقة متناهية. حين تأكل وجبة مالحة، يرتفع تركيز الصوديوم في دمك، فيشعر جسمك بالعطش ليدفعك لشرب الماء وتخفيف التركيز. وإذا زاد الصوديوم بشكل مزمن، تحتفظ الكلى بمزيد من الماء، فيزداد حجم الدم، فيرتفع الضغط. هذه هي العلاقة المبسطة بين الملح وارتفاع ضغط الدم التي يُحذّر منها الأطباء. بحسب تقرير منظمة الصحة العالمية (WHO) لعام 2023، فإن تقليل استهلاك الملح إلى أقل من 5 غرامات يومياً يُقلل خطر أمراض القلب والسكتات الدماغية بشكل ملموس.
حقيقة علمية: يستهلك جسم الإنسان نحو 20–30% من طاقته الأيضية الإجمالية لتشغيل مضخات الصوديوم والبوتاسيوم فقط. في الدماغ، ترتفع هذه النسبة إلى أكثر من 50%. المضخة ليست ترفاً بيولوجياً، بل هي المحرك الأساسي لحياة الخلية.
اقرأ أيضاً:
- علم وظائف الأعضاء (Physiology): استكشاف آليات الحياة
- عملية الأيض (Metabolism): العمليات الكيميائية للحياة
عدو الزراعة الصامت: ماذا يفعل تراكم الصوديوم في التربة؟
في مفارقة عجيبة، ورغم أن خلاياك العصبية لا تستطيع العمل دون صوديوم، إلا أنه يُعدّ ألد أعداء النباتات! في المناطق الجافة وشبه الجافة، عندما تتراكم أيونات الصوديوم في الأراضي الزراعية (وهو ما يُعرف بصوديّة التربة أو Sodic Soils)، تحدث كارثة صامتة. تقوم أيونات الصوديوم بتفكيك البنية الفيزيائية للتربة، فتتحول إلى كتلة صلبة تمنع تدفق الماء وتخنق جذور النباتات. علاوة على ذلك، يتنافس الصوديوم مع عناصر ضرورية مثل البوتاسيوم والكالسيوم، فيمنع النبات من امتصاص غذائه. هذه المعركة الكيميائية في التربة تكبّد القطاع الزراعي العالمي خسائر بمليارات الدولارات سنوياً، وتدفع العلماء لابتكار طرق معالجة كيميائية — مثل إضافة الجبس الزراعي — لإزاحة هذا العنصر العنيد وغسل التربة منه.
ما المخاطر الحقيقية للتعامل مع الصوديوم النقي وكيف تحمي نفسك؟
التعامل مع عنصر الصوديوم في المختبر ليس مزحة. هذا المعدن يتطلب احتراماً كاملاً ومعرفة دقيقة بقواعد السلامة.
أولاً، يجب ارتداء نظارات واقية وقفازات مقاومة للمواد الكيميائية ومعطف مختبر مقاوم للنار. لا تلمس الصوديوم بيد مكشوفة أبداً؛ لأن رطوبة جلدك وحدها كافية لبدء تفاعل يُسبب حروقاً قلوية مؤلمة. ثانياً، استخدم أدوات جافة تماماً — ملقط معدني جاف أو سكين جافة — لقطع القطع الصغيرة. أي أثر للرطوبة على الأداة قد يُشعل التفاعل في يدك.
ماذا تفعل إذا وقع حادث؟
إذا لامس الصوديوم المعدني جلدك وتفاعل، فالناتج هو هيدروكسيد الصوديوم الكاوي. اغسل المنطقة المصابة بكميات كبيرة من الماء الجاري لمدة 15 دقيقة على الأقل. لا تحاول إزالة شظايا الصوديوم المتبقية على الجلد بيدك، بل اتركها تتفاعل تحت الماء الجاري. واطلب المساعدة الطبية فوراً.
للتخلص من نفايات الصوديوم في المختبر، لا تُلقِ القطع في سلة المهملات العادية ولا في حوض الغسيل. الطريقة الآمنة هي إذابتها ببطء شديد في كحول الأيزوبروبانول (Isopropanol) أو الإيثانول اللامائي؛ إذ يتفاعل الصوديوم مع الكحولات بلطف أكبر بكثير من تفاعله مع الماء. وبعض المختبرات تستخدم الرمل الجاف لتغطية قطع الصوديوم المتبقية ومنعها من التفاعل مع رطوبة الهواء.
نقطة تستحق الانتباه: لا تستخدم طفاية حريق مائية أو رغوية لإطفاء حريق ناجم عن الصوديوم. الماء سيزيد الحريق اشتعالاً. استخدم طفاية المعادن القلوية (Class D Fire Extinguisher) أو غطِّ النار بالرمل الجاف أو مسحوق كلوريد الصوديوم — والمفارقة الطريفة أن ملح الطعام يُطفئ حريق أبيه!
اقرأ أيضاً: الكيمياء البيئية: دراسة العمليات الكيميائية في البيئة
الخلاصة التطبيقية من خلية
بعد هذه الرحلة المعمّقة في عالم الصوديوم، إليك خلاصات عملية تستطيع استخدامها فوراً:
- ميّز بين العنصر والمركب دائماً. حين تقرأ خبراً يقول “الصوديوم يرفع ضغط الدم”، فالمقصود أيونات الصوديوم في ملح الطعام وليس المعدن النقي. هذا الفارق يمنعك من الخلط بين مادتين مختلفتين تماماً في السلوك والخصائص.
- اختبار اللهب أداة تعلّم فورية. يمكنك استخدام رشّة ملح فوق لهب الموقد لتوضيح مفهوم الطيف الذري لأبنائك أو زملائك. هذه التجربة البسيطة تربط النظرية بالملاحظة المباشرة بلا تكلفة.
- تابع تقنية بطاريات الصوديوم-أيون. هذا المجال يتطور بسرعة، وقد يُغيّر مشهد تخزين الطاقة المتجددة خلال السنوات القليلة المقبلة. قراءة الأخبار التقنية بهذه الخلفية ستجعلك تفهم أبعاد التنافس بين الليثيوم والصوديوم.
- لا تتجاهل إشارات جسمك المرتبطة بالصوديوم. العطش المفاجئ بعد وجبة مالحة ليس مجرد إحساس عشوائي، بل هو استجابة فسيولوجية دقيقة تهدف إلى حماية توازن السوائل في جسمك. فهم هذه الآلية يجعلك أكثر وعياً بعلاقتك مع الملح.
- احترم قواعد السلامة المخبرية. إذا كنت طالباً يتعامل مع الفلزات القلوية، فتذكّر أن الثقة الزائدة هي أخطر عدو في المختبر. الصوديوم لا يُعطي فرصة ثانية حين يلامس الماء.
- انظر إلى مصابيح الشارع بعين جديدة. ذلك اللون البرتقالي الليلي المألوف هو توقيع ذرات الصوديوم الكمومي. كل فوتون يصل إلى عينك يحمل بصمة طاقة محددة لا تُخطئها أجهزة المطيافية.
كيف يلخّص الصوديوم قصة الكيمياء بأسرها؟
في نهاية هذا المقال، أجد نفسي مندهشاً — رغم سنوات من دراسة الكيمياء — من قدرة عنصر واحد على الجمع بين هذا الكمّ من التناقضات. عنصر الصوديوم ينفجر في الماء لكنه يهدّئ أعصابك حرفياً عبر نبضاتك العصبية. يُخزَّن تحت الزيت خوفاً عليه من قطرة ماء، لكنه يسبح بالمليارات في كل قطرة من محيطات الأرض على هيئة أيونات مستقرة. معدن طري كالزبدة لكنه يُبرّد مفاعلات نووية عند درجات حرارة تصهر الفولاذ.
من همفري ديفي وهو يقفز فرحاً في مختبره عام 1807، إلى مهندسي البطاريات في شنغهاي وهم يصنعون بطاريات صوديوم-أيون عام 2025، يبقى هذا العنصر في قلب الابتكار البشري. وكل مرة ترشّ فيها ملحاً على طعامك، تذكّر أنك تمسك بين أصابعك نصف معادلة انفجارية روّضتها الطبيعة في رابطة أيونية محكمة.
شاركنا في التعليقات: هل جرّبت اختبار اللهب بملح الطعام؟ وما العنصر الكيميائي التالي الذي تودّ أن نكتب عنه بهذا العمق؟
بعد كل ما قرأته اليوم، أدعوك لتحويل هذه المعرفة إلى فعل: أرسل هذا المقال لصديق يدرس الكيمياء أو لمعلّم علوم تعرفه، واسأله عن تجربة الصوديوم في المختبر. المعرفة التي تُشارَك تتضاعف، والعلم الذي يبقى حبيساً في صفحة لا يُغيّر شيئاً.
اقرأ أيضاً:
- الذهب: ما الذي يجعل العنصر 79 أثمن معادن الأرض؟
- الكربون: ما الذي يجعله العنصر الأكثر تميزاً في الجدول الدوري؟
- الهيليوم: ما هو وما خصائصه ونظائره ولماذا لا يتفاعل مع بقية العناصر
الأسئلة الشائعة
ما الفرق بين الصوديوم والملح على الملصقات الغذائية؟
الصوديوم عنصر يدخل في تركيب الملح وغيره من المركبات. الملصقات الغذائية تذكر الصوديوم لأن التقييم الصحي يرتبط بكمية هذا العنصر لا بوزن الملح كله.
هل كل أنواع الملح تعطي كمية الصوديوم نفسها تقريباً؟
غالباً نعم مع فروق طفيفة فقط. ملح البحر وملح الهيمالايا قد يبدوان مختلفين، لكن محتواهما من الصوديوم يبقى متقارباً عند المقارنة بالوزن نفسه.
هل نقص الصوديوم في الدم حالة طبية طارئة؟
قد يصبح طارئاً إذا حدث سريعاً أو كان شديداً، لأنه قد يؤثر في الدماغ والوعي والتوازن. التشخيص والعلاج يجب أن يكونا طبياً لا منزلياً.
هل الرياضيون يحتاجون دائماً إلى تعويض الصوديوم بعد التمرين؟
لا دائماً. الحاجة تعتمد على مدة الجهد، شدة التعرق، الحرارة، وطبيعة الرياضة. في كثير من الحالات يكفي الطعام المتوازن والسوائل العادية.
هل ماء الشرب مصدر مهم للصوديوم في النظام الغذائي؟
عادة لا، إلا إذا كان الماء عالي الملوحة أو خاضعاً لظروف معالجة خاصة. المصدر الأكبر للصوديوم غالباً هو الأغذية المصنعة والملح المضاف.
هل بدائل الملح آمنة لمرضى الضغط؟
ليس دائماً. بعض بدائل الملح تعتمد على البوتاسيوم، وقد لا تناسب مرضى الكلى أو من يتناولون أدوية معينة. القرار الأفضل يكون بالتشاور مع الطبيب.
هل شطف الأطعمة المعلبة يقلل الصوديوم فعلاً؟
نعم، قد يخفض جزءاً ملحوظاً من الصوديوم السطحي أو الموجود في السائل الحافظ، لكنه لا يزيل الصوديوم المدمج داخل المنتج نفسه بالكامل.
هل بطاريات الصوديوم-أيون ستستبدل بطاريات الليثيوم قريباً؟
على الأرجح ستكملها أكثر مما ستستبدلها فوراً. تمتاز بتكلفة أقل ووفرة أعلى، لكن بعض تطبيقات الأداء العالي لا تزال تميل إلى الليثيوم.
هل الصوديوم المنخفض في منتج غذائي يعني دائماً أنه صحي؟
لا. قد يكون منخفض الصوديوم لكنه مرتفع السكر أو الدهون المشبعة أو السعرات. الحكم الصحي يحتاج قراءة الملصق الغذائي كاملاً.
هل يمكن علاج انخفاض الصوديوم بتناول الملح مباشرة في المنزل؟
ليس دائماً، وقد يكون خطيراً. علاج نقص الصوديوم يعتمد على السبب والسرعة والشدة، وقد يتطلب سوائل وريدية أو ضبطاً دقيقاً داخل منشأة طبية.
بيان المصداقية
أُعد هذا المقال في موقع خلية بالاعتماد على مصادر أكاديمية ومؤسسية موثوقة، تشمل أبحاثاً محكّمة، مراجع جامعية، وبيانات صادرة عن جهات علمية معترف بها مثل IUPAC وWHO وUSGS.
جرى التدقيق في المفاهيم الكيميائية والصناعية والحيوية الواردة في المقال مع مراعاة التمييز بين الصوديوم العنصري ومركباته، وتجنب التهويل أو التبسيط المخل أو الصور غير الدقيقة علمياً.
تاريخ إعداد النسخة الحالية: مايو 2026. تُحدَّث المادة عند ظهور بيانات مرجعية أحدث أو عند الحاجة إلى تحسينات تحريرية وعلمية.
معايير وبروتوكولات علمية مرجعية معتمدة
تم اعتماد هذه الأطر المرجعية بما يناسب موضوع المقالة حتى مايو 2026، مع استخدام الصياغة التعليمية دون تحويل النص إلى دليل تشغيلي ميداني.
المصادر والمراجع
- Mason, P. E., Uhlig, F., Vaněk, V., Buttersack, T., Bauerecker, S., & Jungwirth, P. (2015). Coulomb explosion during the early stages of the reaction of alkali metals with water. Nature Chemistry, 7(3), 250–254. https://doi.org/10.1038/nchem.2161
دراسة تكشف آلية الانفجار الكولومي عند تفاعل الصوديوم مع الماء. - Tarascon, J.-M. (2020). Na-ion versus Li-ion batteries: Complementarity rather than competitiveness. Joule, 4(8), 1616–1620. https://doi.org/10.1016/j.joule.2020.06.003
ورقة تحليلية عن مستقبل بطاريات الصوديوم-أيون مقابل الليثيوم-أيون. - Hwang, J.-Y., Myung, S.-T., & Sun, Y.-K. (2017). Sodium-ion batteries: Present and future. Chemical Society Reviews, 46(12), 3529–3614. https://doi.org/10.1039/C6CS00776G
مراجعة شاملة لتقنيات بطاريات الصوديوم-أيون ومكوناتها. - Skou, J. C. (1998). The identification of the sodium–potassium pump (Nobel Lecture). Angewandte Chemie International Edition, 37(17), 2320–2328. https://doi.org/10.1002/(SICI)1521-3773(19981002)37:17<2320::AID-ANIE2320>3.0.CO;2-2
محاضرة نوبل للعالم الذي اكتشف مضخة الصوديوم-بوتاسيوم. - Greenwood, N. N., & Earnshaw, A. (2012). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann.
كتاب مرجعي شامل في كيمياء العناصر يتناول الصوديوم بتفصيل واسع. - Housecroft, C. E., & Sharpe, A. G. (2018). Inorganic Chemistry (5th ed.). Pearson Education.
مرجع أكاديمي في الكيمياء غير العضوية يغطي خصائص الفلزات القلوية. - U.S. Geological Survey (USGS). (2024). Mineral Commodity Summaries: Salt. https://pubs.usgs.gov/periodicals/mcs2024/mcs2024-salt.pdf
تقرير رسمي عن إنتاج الملح عالمياً واحتياطياته. - World Health Organization (WHO). (2023). Guideline: Sodium intake for adults and children. https://www.who.int/publications/i/item/9789241504836
إرشادات المنظمة بشأن الحد الأقصى لاستهلاك الصوديوم اليومي. - National Science Foundation (NSF). (2022). Research on advanced nuclear reactor coolants. https://www.nsf.gov/
معلومات حول أبحاث سوائل التبريد المعدنية في المفاعلات النووية. - Holleman, A. F., Wiberg, E., & Wiberg, N. (2001). Inorganic Chemistry. Academic Press.
موسوعة كيميائية ألمانية مترجمة تُعَدُّ من أمهات المراجع في الكيمياء غير العضوية. - IUPAC. (2021). Periodic Table of the Elements. International Union of Pure and Applied Chemistry. https://iupac.org/what-we-do/periodic-table-of-elements/
المصدر الرسمي للجدول الدوري وبيانات العناصر. - Yabuuchi, N., Kubota, K., Dahbi, M., & Komaba, S. (2014). Research development on sodium-ion batteries. Chemical Reviews, 114(23), 11636–11682. https://doi.org/10.1021/cr500192f
مراجعة معمقة لأبحاث بطاريات الصوديوم. - Downs, J. C. (1924). Electrolytic process and cell. U.S. Patent No. 1,501,756. https://patents.google.com/patent/US1501756A/en
براءة اختراع خلية داونز الأصلية لاستخلاص الصوديوم. - MIT OpenCourseWare. (2020). Principles of Chemical Science: Alkali Metals. Massachusetts Institute of Technology. https://ocw.mit.edu/
مادة تعليمية مفتوحة من MIT عن الفلزات القلوية. - Matson, J. (2012). Sodium’s explosive secrets. Scientific American. https://www.scientificamerican.com/
مقال مبسط يشرح تفاعل الصوديوم مع الماء للقارئ غير المتخصص.
قراءات إضافية ومصادر للتوسع
- Cotton, F. A., Wilkinson, G., Murillo, C. A., & Bochmann, M. (1999). Advanced Inorganic Chemistry (6th ed.). Wiley.
لماذا نقترح عليك قراءته؟ هذا الكتاب — المعروف اختصاراً بـ “Cotton & Wilkinson” — يتناول كيمياء الصوديوم وعائلة الفلزات القلوية بعمق نظري وتجريبي لا تجده في مرجع آخر. مثالي لطالب الدراسات العليا. - Palacín, M. R. (2018). Battery materials design: An electrochemical challenge. Chemical Society Reviews, 47(13), 4924–4944. DOI: 10.1039/C7CS00889A.
لماذا نقترح عليك قراءته؟ مراجعة بحثية حديثة تضع بطاريات الصوديوم-أيون في سياق المقارنة مع تقنيات التخزين الأخرى، وتوضح التحديات المادية والكيميائية المتبقية. - Hille, B. (2001). Ion Channels of Excitable Membranes (3rd ed.). Sinauer Associates.
لماذا نقترح عليك قراءته؟ إذا أثار فضولك دور قنوات الصوديوم في النبضات العصبية، فهذا الكتاب يُعَدُّ المرجع الذهبي في فسيولوجيا القنوات الأيونية. كتبه بيرت هيل الذي كرّس حياته لهذا المجال، وهو لا غنى عنه لطلاب الفسيولوجيا وعلم الأعصاب.
سجل المراجعة والتحقق العلمي
يوضح هذا السجل أن المادة خضعت لمراجعة تخصصية، وتدقيق علمي، وتحقق من المراجع، وتحرير لغوي قبل النشر أو التحديث ضمن سياسة الجودة التحريرية في خلية.







