صناعة الأدوية: الدليل الشامل من أبحاث المختبرات إلى رفوف الصيدليات
كيف تتحول جزيئة كيميائية مجهولة إلى دواء يتناوله ملايين البشر يومياً؟

صناعة الأدوية هي منظومة علمية وتقنية متعددة التخصصات تشمل اكتشاف المركبات الفعالة، واختبارها مخبرياً وسريرياً، ثم تصنيعها وتوزيعها وفق معايير صارمة. تستغرق رحلة الدواء الواحد من المختبر إلى الصيدلية ما بين 10 و15 عاماً في المتوسط، وتتجاوز تكلفتها 2.6 مليار دولار وفقاً لتقديرات مركز تافتس لدراسة تطوير الأدوية.
- من كل 10,000 مركب كيميائي يُختبر، ينجح واحد فقط في الوصول إلى الصيدلية.
- رحلة الدواء من المختبر إلى السوق تستغرق 10 – 15 عاماً وتكلف أكثر من 2.6 مليار دولار.
- معدل النجاح الإجمالي للأدوية من التجارب السريرية إلى الموافقة لا يتجاوز 13.8%.
- الدواء الجنيس يحتوي على نفس المادة الفعالة بنفس الفعالية، وسعره أقل لأنه لم يتحمل تكاليف البحث.
- عبارة “أثبتت الدراسات” لا تعني شيئاً دون تحديد مرحلة التجربة — اسأل دائماً: أي مرحلة؟
- الإبلاغ عن أي أثر جانبي غير متوقع لهيئة الغذاء والدواء السعودية (SFDA) واجب وطني ويحمي الآخرين.
- الذكاء الاصطناعي أنجز مراحل اكتشاف أدوية في أقل من 18 شهراً بدلاً من 4 – 5 سنوات.
- تقنية كريسبر (CRISPR) دخلت السوق رسمياً عام 2023 بأول علاج جيني معتمد لفقر الدم المنجلي.
- أي منتج يدّعي علاج كل شيء دون تجارب سريرية موثّقة هو على الأرجح احتيال.
- ما ينجح في طبق بتري أو على فأر مختبر لا ينجح بالضرورة في جسم الإنسان.
هل تساءلت يوماً لماذا يبدو سعر بعض الأدوية مبالغاً فيه، أو لماذا تنتظر البشرية سنوات طويلة قبل أن يظهر علاج لمرض بعينه؟ الحقيقة أن خلف كل قرص صغير تبتلعه في ثوانٍ تختبئ قصة علمية معقدة ومذهلة، تبدأ بفكرة في ذهن باحث وتمر بآلاف التجارب والإخفاقات. هذا المقال سيأخذك في جولة داخل هذه القصة، ليس لتصبح صيدلانياً، بل لتفهم لماذا يستحق كل دواء فعّال أن تنظر إليه بعين مختلفة، ولتميّز بين الادعاءات الطبية الزائفة والعلم الحقيقي.
تخيّل أن “سارة”، طالبة صيدلة في جامعة الملك سعود بالرياض، تقرأ خبراً عن دواء جديد لعلاج سرطان الرئة حصل على موافقة وكالة الغذاء والدواء الأميركية (FDA). تتساءل: كيف وصل هذا الدواء إلى هنا؟ تبحث فتكتشف أن الباحثين بدأوا العمل عليه قبل 13 عاماً، وأن أكثر من 5,000 مركب كيميائي اختُبرت قبل أن ينجح واحد فقط، وأن تجاربه السريرية شملت أكثر من 8,000 مريض في 22 دولة. سارة الآن تنظر إلى علبة الدواء بطريقة مختلفة تماماً؛ إذ لم تعد ترى مجرد حبة بيضاء، بل ترى عقوداً من الجهد والتمويل والمخاطرة. وهذا بالضبط ما ستفعله أنت بعد قراءة هذا المقال.
كيف بدأت البشرية أول خطوة في صناعة الأدوية؟
قبل أن نغوص في تفاصيل المراحل الحديثة، دعني آخذك في لمحة سريعة عبر الزمن. لآلاف السنين، اعتمد الإنسان على النباتات والأعشاب لعلاج أمراضه. المصريون القدماء استخدموا لحاء شجر الصفصاف لتسكين الألم — وهو المصدر الطبيعي لما نعرفه اليوم بـالأسبرين. الأطباء العرب في العصر الذهبي الإسلامي، أمثال ابن سينا والرازي، صنّفوا مئات النباتات الطبية ووضعوا أسس الصيدلة كعلم منفصل عن الطب.
لكن النقلة الحقيقية حدثت في القرن التاسع عشر حين بدأ الكيميائيون بعزل المركبات الفعالة من النباتات. المورفين عُزل من الأفيون عام 1804، والكينين من لحاء شجرة السنكونا لعلاج الملاريا. ثم جاء الحدث الذي غيّر وجه الطب إلى الأبد: اكتشاف ألكسندر فليمنغ للبنسلين عام 1928. فليمنغ لاحظ أن عفناً أخضر قتل البكتيريا في طبق بتري بالصدفة! لكن — وهنا المفاجأة — احتاج العالم إلى أكثر من عشر سنوات إضافية قبل أن يتمكن هوارد فلوري وإرنست تشين من تحويل هذا الاكتشاف إلى دواء يمكن إنتاجه على نطاق واسع. هذا يعني أن الاكتشاف وحده لا يكفي؛ بل إن تحويله إلى منتج دوائي قابل للاستخدام هو التحدي الأكبر، وهو جوهر ما تقوم عليه صناعة الأدوية الحديثة.
ومضة معرفية: قبل اكتشاف المضادات الحيوية، كان خدش بسيط قد يتحول إلى عدوى قاتلة. البنسلين وحده أنقذ ما يُقدّر بأكثر من 200 مليون حياة منذ بدء استخدامه سريرياً في أربعينيات القرن العشرين.
اقرأ أيضاً:
ما الذي يحدث فعلاً في مرحلة اكتشاف الدواء وتصميمه؟
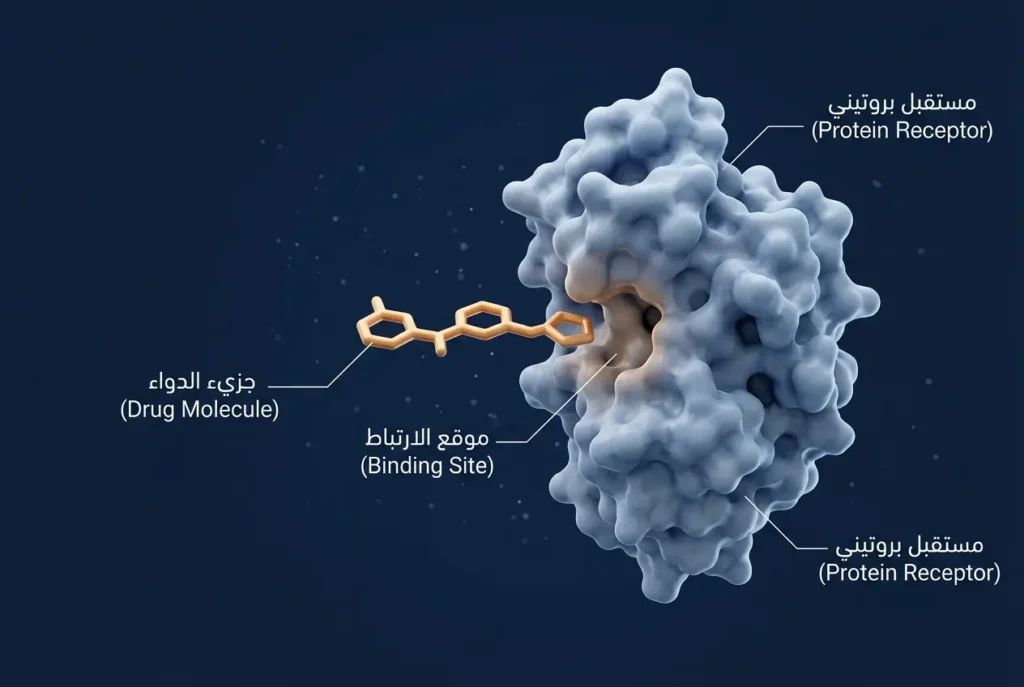
الخطوة الأولى: تحديد الهدف البيولوجي
هنا تبدأ القصة الحقيقية. قبل أن يصمم أي باحث جزيئة دوائية، عليه أولاً أن يفهم المرض على مستوى الخلايا والجزيئات. الخطوة الأولى تُسمى تحديد الهدف البيولوجي (Target Identification)، وتعني العثور على البروتين أو الإنزيم أو المستقبل الذي يلعب دوراً محورياً في حدوث المرض.
تخيّل الأمر هكذا: إذا كان المرض هو حريق في مبنى، فإن الهدف البيولوجي هو صنبور الغاز الذي يغذي النار. مهمة الباحث ليست إطفاء النار بالماء فقط، بل إيجاد ذلك الصنبور تحديداً وإغلاقه. هذا يتطلب فهماً عميقاً للمسارات الجزيئية (Molecular Pathways) داخل الخلية؛ أي سلسلة التفاعلات الكيميائية التي تؤدي في النهاية إلى ظهور أعراض المرض.
اكتشاف الجزيء الفعال ودور التقنية الحاسوبية
بعد تحديد الهدف، يبدأ البحث عن جزيء كيميائي يستطيع الارتباط بهذا الهدف وتعطيله أو تنشيطه. هذه المرحلة تُسمى “من الضربة إلى القائد” (Hit to Lead)؛ إذ يختبر الباحثون مكتبات ضخمة تحتوي على ملايين المركبات الكيميائية بحثاً عن “ضربة” — أي مركب يُظهر تفاعلاً مبدئياً مع الهدف.
في الماضي، كان هذا يتم يدوياً وببطء شديد. أما اليوم، فقد غيّرت الكيمياء الحاسوبية (Computational Chemistry) والمحاكاة الآلية قواعد اللعبة تماماً. البرمجيات المتقدمة تستطيع محاكاة شكل البروتين المستهدف ثلاثي الأبعاد، ثم “تجرب” ملايين الجزيئات افتراضياً لترى أيها يتناسب معه — كمن يجرب ملايين المفاتيح في قفل واحد، لكن بسرعة الحاسوب لا بسرعة اليد. تقنية الفرز عالي الإنتاجية (High-Throughput Screening – HTS) تسمح باختبار مئات الآلاف من المركبات في يوم واحد.
فقد أظهرت دراسة منشورة في مجلة Nature Reviews Drug Discovery عام 2019 أن استخدام المحاكاة الحاسوبية قلّص زمن المرحلة الأولى من اكتشاف الدواء بنسبة تصل إلى 40% في بعض الحالات. هذا الرقم مذهل حين تعرف أن كل شهر إضافي في التطوير قد يكلف شركات الأدوية ملايين الدولارات.
حقيقة علمية: من بين كل 10,000 مركب كيميائي يدخل مرحلة الاكتشاف المبكر، ينجح واحد فقط في الوصول إلى الصيدلية. هذه النسبة — 0.01% — تكشف حجم المقامرة العلمية المحسوبة التي تمارسها شركات الأدوية يومياً.
اقرأ أيضاً: تطبيقات الذكاء الاصطناعي في علم الأدوية: التحديات والفرص
الفرق الجوهري بين “اكتشاف” الدواء و”اختراعه”: لماذا التمييز مهم؟
ثمة خلط شائع يقع فيه كثيرون، بما فيهم بعض طلاب العلوم أنفسهم. كثيراً ما نسمع عبارة “اختراع دواء جديد”، لكن الدقة العلمية تقتضي التمييز. الأدوية لا تُخترع كما تُخترع الآلات؛ بل تُكتشف أولاً ثم تُطوّر وتُصمّم. الاكتشاف يعني العثور على مركب طبيعي أو تخليقي يُظهر فعالية ضد هدف بيولوجي معين. أما التطوير فيعني تحسين خصائص هذا المركب — ذوبانيته، ثباته، أمانه، وطريقة إيصاله إلى العضو المصاب — حتى يصبح صالحاً للاستخدام البشري.
هذا التمييز ليس ترفاً لغوياً. إنه يعكس فلسفة مختلفة تماماً في التفكير العلمي. المخترع يبني شيئاً من الصفر. أما مكتشف الدواء فهو أشبه بمنقّب عن الذهب: يعرف أن الذهب موجود في مكان ما داخل أطنان من الصخور، لكنه يحتاج إلى أدوات ذكية وصبر هائل لاستخراجه وتنقيته. وعليه فإن اكتشاف وتطوير الأدوية يجمع بين الحظ والمنهجية والإبداع في آن واحد.
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
كيف تُثبت التجارب قبل السريرية أن الدواء آمن قبل تجربته على البشر؟
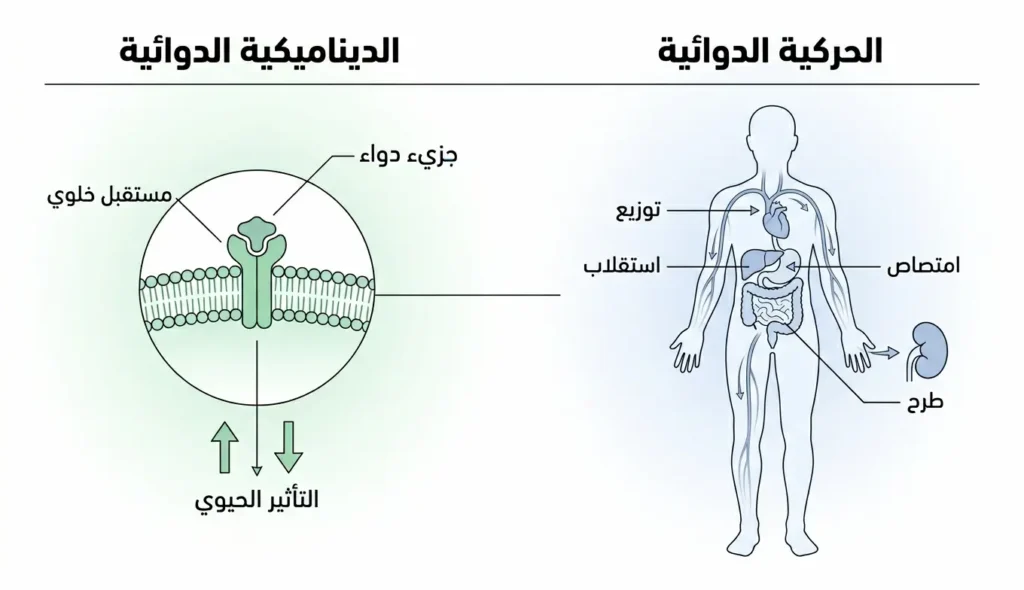
التجارب في المختبر والكائنات الحية
بعد أن يعثر الباحثون على مركب واعد، لا يمكنهم إعطاءه للبشر مباشرة. هنا تبدأ مرحلة حرجة تُسمى التجارب ما قبل السريرية (Preclinical Trials)، وتنقسم إلى نوعين رئيسين. النوع الأول هو التجارب المخبرية (In Vitro) — وتعني حرفياً “في الزجاج” — حيث تُختبر المادة على خلايا بشرية أو حيوانية في أطباق بتري أو أنابيب اختبار. الهدف هنا هو التأكد من أن الجزيء يتفاعل مع الهدف البيولوجي كما هو متوقع.
النوع الثاني هو التجارب على الكائنات الحية (In Vivo) — أي داخل جسم كائن حي، عادةً فئران أو جرذان مختبرية. في هذه المرحلة، يدرس العلماء أمرين بالغي الأهمية. الأول هو الحركية الدوائية (Pharmacokinetics – PK) — أي كيف يتعامل الجسم مع الدواء: كيف يُمتص، وكيف يتوزع في الأنسجة، وكيف يُستقلب في الكبد، وكيف يُطرح خارج الجسم. والثاني هو الديناميكية الدوائية (Pharmacodynamics – PD) — أي كيف يؤثر الدواء على الجسم: ما هي آليته في تعديل الوظائف البيولوجية.
فلنبسّط الأمر أكثر. الحركية الدوائية تجيب عن سؤال: “ماذا يفعل جسمك بالدواء؟”، بينما الديناميكية الدوائية تجيب عن سؤال: “ماذا يفعل الدواء بجسمك؟”. الفرق بينهما كالفرق بين أن تسأل: “كيف يتعامل منزلك مع ضيف جديد؟” و”كيف يغيّر هذا الضيف من أجواء المنزل؟”.
أخلاقيات التجارب على الحيوانات
لا يمكن الحديث عن مراحل تصنيع الدواء دون التطرق إلى الجانب الأخلاقي. التجارب على الحيوانات تخضع لقوانين صارمة جداً تُعرف بمبدأ الـ 3Rs: الاستبدال (Replacement) — أي استخدام بدائل حاسوبية أو خلوية كلما أمكن. التقليل (Reduction) — أي استخدام أقل عدد ممكن من الحيوانات. التحسين (Refinement) — أي تقليل المعاناة إلى أدنى حد. في المملكة العربية السعودية، تشرف لجان أخلاقيات البحث في الجامعات والمراكز البحثية — مثل مدينة الملك عبدالعزيز للعلوم والتقنية — على ضمان الالتزام بهذه المعايير.
نقطة تستحق الانتباه: بحسب تقرير صادر عن هيئة الغذاء والدواء السعودية (SFDA) عام 2024، تُلزم الهيئة جميع شركات الأدوية العاملة في المملكة بتقديم ملفات كاملة عن التجارب ما قبل السريرية قبل الموافقة على بدء أي تجربة سريرية على أراضيها.
اقرأ أيضاً: المنهج التجريبي: كيف تصمم تجربة علمية ناجحة وتحقق نتائج موثوقة؟
العدسة العلمية الدقيقة – للمهتمين بالتفاصيل الأعمق
دعني أصطحبك إلى مستوى أعمق من التفصيل. حين نتحدث عن تصميم جزيء دوائي، فإن الكيميائيين الطبيين (Medicinal Chemists) لا يعملون عشوائياً. هم يستخدمون مفهوماً محورياً يُسمى علاقة البنية بالفعالية (Structure-Activity Relationship – SAR). الفكرة ببساطة: كل تعديل صغير في التركيب الكيميائي للجزيء — إضافة مجموعة ميثيل هنا، أو إزالة ذرة كلور هناك — يُغيّر من خصائصه البيولوجية بشكل دراماتيكي. الأمر أشبه بضبط أوتار عود: تحريك الوتر ملليمتراً واحداً يغيّر النغمة كلياً.
كما أن هناك قاعدة شهيرة في مجال اكتشاف وتطوير الأدوية تُعرف بقاعدة ليبنسكي للخمسة (Lipinski’s Rule of Five)، وهي مجموعة معايير فيزيائية كيميائية تُستخدم للتنبؤ بما إذا كان المركب سيُمتص جيداً عبر الجهاز الهضمي عند تناوله فموياً. القاعدة تنص على أن الامتصاص الفموي الجيد يكون مرجحاً إذا كان الوزن الجزيئي أقل من 500 دالتون، ومعامل التوزيع اللوغاريتمي (LogP) أقل من 5، وعدد مجموعات مانحة الروابط الهيدروجينية أقل من 5، وعدد مجموعات مستقبلة الروابط الهيدروجينية أقل من 10. هذه القاعدة ليست قانوناً مطلقاً — فهناك أدوية ناجحة تنتهكها — لكنها تظل أداة فرز أولية قيّمة جداً.
في السنوات الأخيرة، بدأ الذكاء الاصطناعي يتدخل في هذه المرحلة بقوة. خوارزميات التعلم العميق (Deep Learning) تستطيع تحليل قواعد بيانات ضخمة من التفاعلات الجزيئية، واقتراح تعديلات بنيوية لم تخطر على بال الكيميائيين البشريين. شركة Insilico Medicine، على سبيل المثال، استخدمت الذكاء الاصطناعي لتحديد هدف بيولوجي جديد وتصميم جزيء دوائي وصل إلى التجارب السريرية في أقل من 30 شهراً — وهو زمن قياسي مقارنة بالمعتاد.
ما هي مراحل التجارب السريرية التي يجب أن يجتازها أي دواء جديد؟
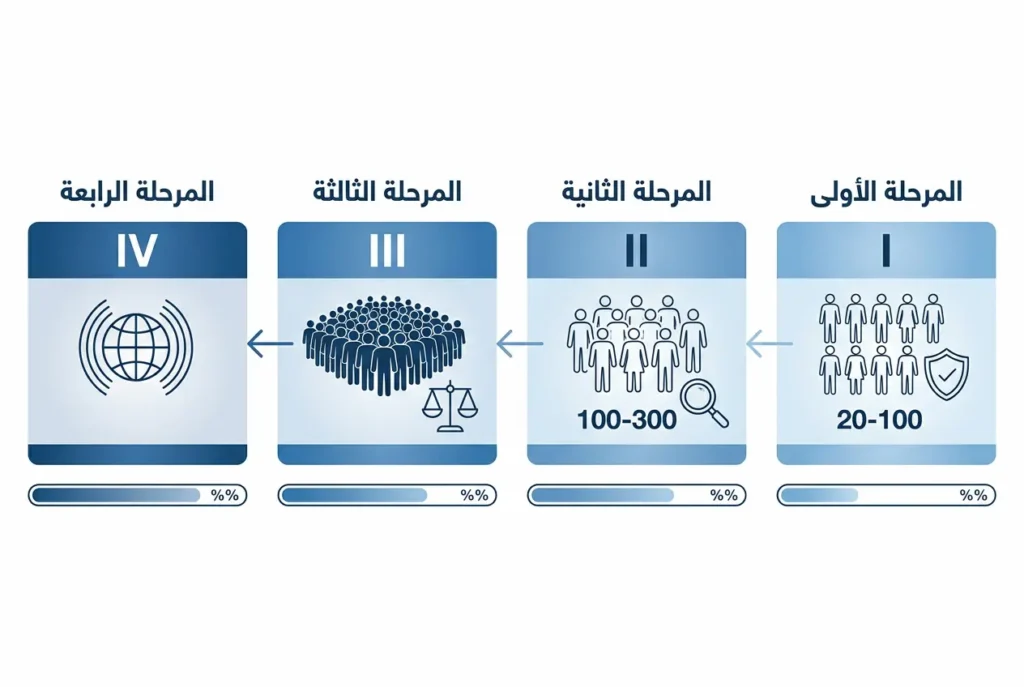
المرحلة الأولى: اختبار الأمان
هنا يُعطى الدواء لأول مرة لبشر حقيقيين. المرحلة الأولى من التجارب السريرية (Phase I Clinical Trials) تشمل عادةً ما بين 20 و100 متطوع سليم — نعم، أشخاص أصحاء وليسوا مرضى. الهدف ليس علاج مرض، بل الإجابة عن سؤال واحد محوري: هل هذا الدواء آمن للاستخدام البشري؟ يبدأ الأطباء بجرعات صغيرة جداً ثم يزيدونها تدريجياً، مع مراقبة دقيقة لأي أعراض جانبية. هذه المرحلة تستغرق عادةً من عدة أشهر إلى عام.
المرحلة الثانية: اختبار الفعالية
إذا أثبت الدواء أمانه، ينتقل إلى المرحلة الثانية (Phase II) التي تشمل ما بين 100 و300 مريض يعانون فعلاً من المرض المستهدف. هنا يتحول السؤال من “هل هو آمن؟” إلى “هل يعمل فعلاً؟”. يقيس الباحثون فعالية الدواء، ويحددون الجرعة المثلى، ويرصدون الأعراض الجانبية قصيرة المدى. نسبة كبيرة من الأدوية تسقط في هذه المرحلة — بحسب تقارير وكالة الغذاء والدواء الأميركية، يفشل نحو 70% من الأدوية في المرحلة الثانية.
رقم لافت: بحسب تحليل منشور في مجلة Biostatistics عام 2019، فإن معدل النجاح الإجمالي للأدوية من المرحلة الأولى للتجارب السريرية إلى حصولها على الموافقة التنظيمية لا يتجاوز 13.8%. أي أن من كل 7 أدوية تدخل التجارب على البشر، ينجو دواء واحد فقط تقريباً.
المرحلة الثالثة: التجربة الحاسمة
المرحلة الثالثة (Phase III) هي الامتحان الأكبر والأغلى. تشمل عادةً آلاف المرضى — أحياناً أكثر من 10,000 — موزعين في مراكز بحثية حول العالم. تُصمم هذه التجارب غالباً بمنهجية التجارب المعشاة ذات الشواهد المزدوجة التعمية (Randomized Double-Blind Placebo-Controlled Trials). فما معنى هذا؟
“المعشاة” تعني أن المرضى يُوزعون عشوائياً بين مجموعتين: مجموعة تتلقى الدواء الحقيقي، ومجموعة تتلقى علاجاً وهمياً (Placebo) أو الدواء القياسي الحالي. “المزدوجة التعمية” تعني أن لا المريض ولا الطبيب يعرف من يتلقى الدواء الحقيقي ومن يتلقى الوهمي. لماذا كل هذا التعقيد؟ لأن العقل البشري قادر على خداع الجسد! ظاهرة تأثير الدواء الوهمي (Placebo Effect) تُظهر أن بعض المرضى يتحسنون لمجرد اعتقادهم بأنهم يتلقون علاجاً. لذا، يجب التأكد من أن التحسن ناتج فعلاً عن الدواء وليس عن التوقع النفسي.
هذه المرحلة قد تستغرق من 3 إلى 5 سنوات وتكلف مئات الملايين من الدولارات. لكنها ضرورية لضمان أن الدواء فعّال وآمن على نطاق واسع.
اقرأ أيضاً: الإحصاء الاستدلالي: الاستنتاج من العينات إلى السكان
كيف تقرر الجهات التنظيمية الموافقة على دواء جديد أو رفضه؟
بعد اجتياز المرحلة الثالثة بنجاح، تقدم شركة الأدوية ملفاً ضخماً يُسمى طلب الدواء الجديد (New Drug Application – NDA) إلى الهيئة التنظيمية المختصة. في الولايات المتحدة، هذه الهيئة هي وكالة الغذاء والدواء (FDA). في أوروبا، هي وكالة الأدوية الأوروبية (EMA). وفي المملكة العربية السعودية، تضطلع هيئة الغذاء والدواء السعودية (SFDA) بهذا الدور المحوري.
حجم الملف المقدم قد يصدمك. نحن نتحدث عن ما يتراوح بين 100,000 و500,000 صفحة من البيانات العلمية والتحليلات الإحصائية ونتائج التجارب. فريق متخصص من العلماء والأطباء والإحصائيين في الهيئة التنظيمية يراجع كل هذه البيانات بدقة متناهية. المراجعة قد تستغرق من 6 أشهر إلى سنتين. في بعض الحالات الطارئة — كما رأينا مع لقاحات كوفيد-19 — تُستخدم مسارات مراجعة مُسرّعة تُسمى ترخيص الاستخدام الطارئ (Emergency Use Authorization – EUA)، لكنها لا تعني التنازل عن معايير السلامة؛ بل تعني إجراء المراجعة بالتوازي مع جمع البيانات بدلاً من الانتظار حتى اكتمالها.
معلومة سريعة: هيئة الغذاء والدواء السعودية (SFDA) أصبحت عضواً في مجلس التنسيق الدولي لتنظيم الأدوية (ICH) منذ عام 2018، مما يعني أن المعايير التنظيمية المطبقة في المملكة متوافقة مع أعلى المعايير الدولية.
اقرأ أيضاً: الاقتصاد السعودي: كيف تحول من الاعتماد على النفط إلى التنويع الشامل؟
ما هي ممارسات التصنيع الجيد للأدوية GMP ولماذا تُعَدُّ حاسمة؟

التحدي الهندسي في التوسعة
حين ينجح الدواء في التجارب السريرية ويحصل على الموافقة التنظيمية، تبدأ مرحلة جديدة لا تقل تعقيداً: التصنيع الدوائي على نطاق واسع (Manufacturing & Scale-Up). في المختبر، ينتج الباحثون غرامات قليلة من المادة الفعالة. لكن المصنع يحتاج إلى إنتاج أطنان. هذا التحول ليس مجرد “تكبير للوصفة” كما تفعل حين تضاعف مقادير كعكة؛ بل هو تحدٍّ هندسي وكيميائي معقد. التفاعلات الكيميائية التي تعمل بسلاسة في دورق صغير قد تفشل تماماً في مفاعل ضخم بسبب اختلاف ظروف الحرارة والضغط والتقليب.
هنا يأتي دور ممارسات التصنيع الجيد (Good Manufacturing Practice – GMP)، وهي مجموعة معايير صارمة تضمن أن كل حبة دواء تخرج من خط الإنتاج مطابقة تماماً للمواصفات من حيث النقاء والجرعة والثبات. تخيّل أنك في مطبخ مطعم خمس نجوم: كل طبق يجب أن يكون متطابقاً مع السابق في الطعم والشكل والحجم، دون أي اختلاف. هذا بالضبط ما تفعله معايير GMP في المصانع الدوائية.
الرقابة على كل مرحلة إنتاج
تشمل معايير GMP كل تفصيلة يمكنك تخيلها: من نظافة الهواء داخل غرف التصنيع (تُصفّى بفلاتر HEPA التي تحجز الجسيمات الأصغر من 0.3 ميكرومتر)، إلى تتبع كل خطوة إنتاجية بتوثيق مكتوب، إلى اختبار كل دفعة قبل خروجها من المصنع. أي انحراف — مهما كان بسيطاً — يعني إتلاف الدفعة بأكملها. في المملكة العربية السعودية، تجري هيئة الغذاء والدواء تفتيشات دورية ومفاجئة على مصانع الأدوية لضمان الالتزام بهذه المعايير.
من المثير أن تعرف: مصنع دوائي واحد قد يحتوي على أكثر من 10,000 جهاز استشعار يراقب درجة الحرارة والرطوبة والضغط في كل ركن، على مدار الساعة، طوال أيام السنة. أي تغيّر طفيف — حتى لو كان بدرجة مئوية واحدة — قد يُطلق إنذاراً ويوقف خط الإنتاج تلقائياً.
اقرأ أيضاً: مراقبة الجودة الإحصائية: الأدوات، التقنيات، والتطبيق
العلم في خدمتك: كيف تؤثر صناعة الأدوية على قراراتك اليومية؟
ربما تظن أن كل ما سبق يخص العلماء والمتخصصين فقط. لكن الحقيقة أن فهمك لهذه المراحل يؤثر مباشرة على قرارات تتخذها كل يوم. حين تذهب إلى الصيدلية ويخيّرك الصيدلي بين الدواء الأصلي (Brand-name) والدواء الجنيس (Generic)، هل تعرف الفرق بينهما فعلاً؟ الدواء الجنيس يحتوي على نفس المادة الفعالة بنفس الجرعة وبنفس المواصفات البيولوجية — لكنه يُباع بسعر أقل بكثير لأن الشركة المصنّعة لم تتحمل تكاليف البحث والتطوير الأصلية. هيئات الرقابة الدوائية تُلزم مصنّعي الأدوية الجنيسة بإثبات التكافؤ الحيوي (Bioequivalence) — أي أن الدواء يُمتص ويعمل في الجسم بالطريقة نفسها.
كما أن فهمك لمراحل التجارب السريرية يحميك من الوقوع ضحية لادعاءات طبية كاذبة. حين ترى إعلاناً عن “دواء معجزة” لم يُجرب إلا على عشرة أشخاص، ستعرف أن هذا يعني أنه لم يتجاوز حتى المرحلة الثانية. وحين تسمع أن دواءً ما “أثبت فعاليته في المختبر”، ستتذكر أن ما ينجح في طبق بتري لا ينجح بالضرورة في جسم الإنسان — الفارق بينهما كالفارق بين رسم خريطة لطريق والسير فيه فعلاً تحت المطر.
اقرأ أيضاً:
لماذا تستمر مراقبة الدواء حتى بعد طرحه في الأسواق؟
قد تتخيل أن القصة تنتهي حين يظهر الدواء في رفوف الصيدليات. لكنها في الحقيقة تبدأ فصلاً جديداً. المرحلة الرابعة من التجارب السريرية (Phase IV) — التي تُعرف أيضاً بمراقبة ما بعد التسويق أو اليقظة الدوائية (Pharmacovigilance) — تعني مراقبة الدواء على ملايين المستخدمين في الحياة الواقعية، بعيداً عن البيئة المضبوطة للتجارب السريرية.
لماذا هذا ضروري؟ لأن التجارب السريرية — مهما كانت واسعة — لا تستطيع رصد كل شيء. بعض الآثار الجانبية لا تظهر إلا بعد سنوات من الاستخدام. بعضها الآخر يصيب فئات محددة جداً من المرضى — كبار السن مثلاً، أو من يعانون من أمراض مزمنة متعددة — وهؤلاء غالباً لا يُشملون بأعداد كافية في التجارب الأولية.
تاريخ الرقابة الدوائية مليء بحالات سحب الأدوية من الأسواق بعد اكتشاف آثار جانبية خطيرة. من أشهر هذه الحالات دواء روفيكوكسيب (Rofecoxib – Vioxx) المضاد للالتهاب الذي سحبته شركة ميرك عام 2004 بعد أن أظهرت الدراسات زيادته لمخاطر النوبات القلبية. هذا الحدث وحده أعاد تشكيل قوانين الرقابة الدوائية حول العالم وجعل مراقبة ما بعد التسويق أكثر صرامة.
حقيقة علمية: هيئة الغذاء والدواء السعودية تشغّل نظاماً إلكترونياً للإبلاغ عن الآثار الجانبية يُتيح لأي مواطن أو مقيم الإبلاغ مباشرة عن أي أعراض غير متوقعة يلاحظها بعد تناول دواء ما. هذه التقارير تُغذي قاعدة بيانات عالمية تساعد في رصد المشكلات مبكراً.
اقرأ أيضاً: أمراض القلب: ما الذي يجب أن تعرفه لحماية قلبك؟
كم تكلف صناعة الأدوية حقاً، ولماذا تبدو الأسعار مرتفعة؟
اقتصاديات الأدوية عالم معقد ومثير للجدل. وفقاً لدراسة مركز تافتس (Tufts Center for the Study of Drug Development) المنشورة عام 2020، يبلغ متوسط تكلفة تطوير دواء جديد والحصول على موافقة تنظيمية له نحو 2.6 مليار دولار أميركي. هذا الرقم يشمل تكلفة الفشل — أي تكلفة كل المركبات التي لم تنجح في أثناء رحلة التطوير.
من ناحية أخرى، شركات الأدوية تحمي اكتشافاتها ببراءات اختراع دوائية (Pharmaceutical Patents) تمنحها حصرية التصنيع والتسويق لمدة تتراوح عادةً بين 15 و20 عاماً من تاريخ تقديم طلب البراءة. لكن — وهنا الأمر المهم — بما أن جزءاً كبيراً من هذه المدة يُستهلك في سنوات التطوير والتجارب السريرية والمراجعة التنظيمية، فإن الفترة الفعلية لحصرية البيع في السوق قد لا تتجاوز 7 إلى 12 عاماً.
بعد انتهاء فترة حماية براءة الاختراع، يحق لشركات أخرى تصنيع نسخ جنيسة من الدواء بتكلفة أقل بكثير. هذا هو الفرق بين الدواء الأصلي والدواء الجنيس الذي يسأل عنه كثيرون. الدواء الجنيس لا يحتاج إلى إعادة كل مراحل التطوير من الصفر — يكفي إثبات التكافؤ الحيوي — وبالتالي يُباع بسعر أقل بنسبة قد تصل إلى 80-90%.
في السعودية، تعمل هيئة الغذاء والدواء على تشجيع صناعة الأدوية الجنيسة محلياً ضمن رؤية المملكة 2030، التي تستهدف رفع نسبة التصنيع المحلي للأدوية. لقد بلغ حجم سوق الأدوية السعودي أكثر من 40 مليار ريال سعودي بحسب تقارير عام 2024، مما يجعله أكبر سوق دوائي في منطقة الشرق الأوسط.
اقرأ أيضاً: الثورة الصناعية الرابعة: الدليل العلمي الشامل للتقنيات التي تعيد صياغة مستقبل البشرية
جرّب بنفسك: المختبر المنزلي
هل تريد أن تفهم مبدأ الذوبانية (Solubility) الذي يُعَدُّ أحد أهم التحديات في تصميم الأدوية؟ جرّب هذه التجربة البسيطة. أحضر كوبين من الماء: واحد بارد من الثلاجة وآخر ساخن من السخان. أضف ملعقة سكر إلى كل كوب وقلّب. ستلاحظ أن السكر يذوب أسرع بكثير في الماء الساخن. الآن كرر التجربة بملعقة زيت زيتون بدلاً من السكر. ماذا يحدث؟ الزيت لا يذوب في الماء أبداً — لا الساخن ولا البارد.
هذا بالضبط ما يواجهه مصممو الأدوية. كثير من الجزيئات الدوائية الواعدة “لا تذوب في الماء” — أي أنها كارهة للماء (Hydrophobic). ولأن جسم الإنسان مكون من 60% ماء، فإن دواءً لا يذوب في الماء لن يُمتص جيداً من الأمعاء ولن يصل إلى مجرى الدم. لذا يضطر الكيميائيون إلى تعديل بنية الجزيء أو استخدام تقنيات صيدلانية خاصة — مثل تغليفه بجسيمات نانوية — لتحسين ذوبانيته. في المرة القادمة التي تتناول فيها حبة دواء، تذكّر أن وراء قدرتها على الذوبان في معدتك جهداً هندسياً مبهراً.
كيف يُعيد الذكاء الاصطناعي رسم مستقبل صناعة الأدوية؟
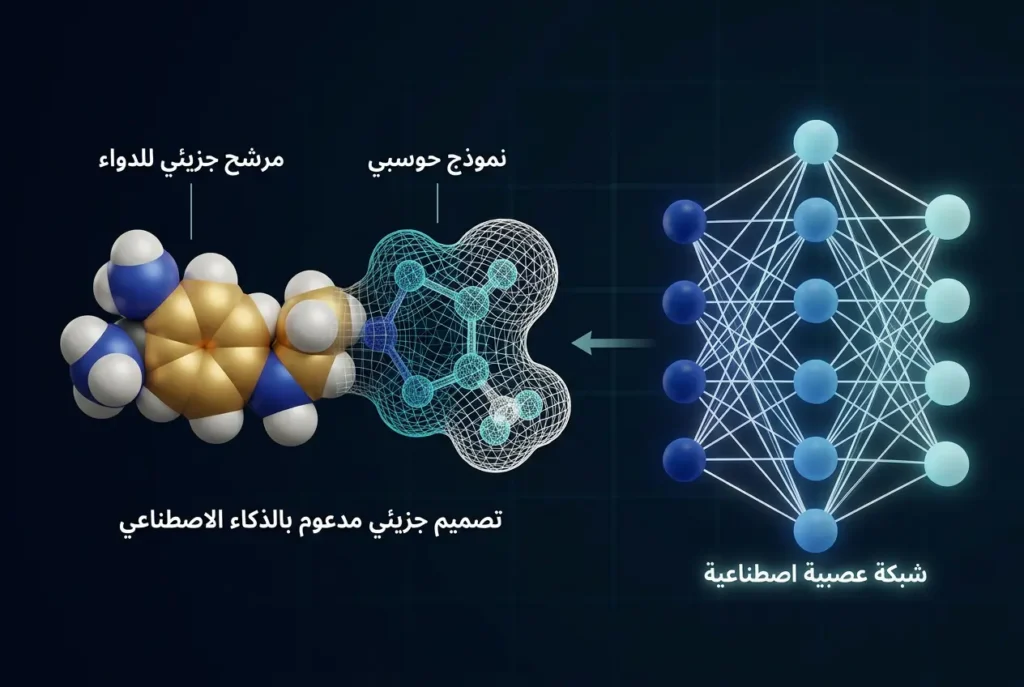
ثورة الذكاء الاصطناعي في اكتشاف الأدوية
نحن نعيش الآن في لحظة تاريخية فارقة. مستقبل الذكاء الاصطناعي في صناعة الأدوية لم يعد خيالاً علمياً، بل واقع يتسارع يوماً بعد يوم. في عام 2024، أُعلن عن أول دواء صُمم بالكامل بمساعدة الذكاء الاصطناعي ودخل المرحلة الثانية من التجارب السريرية — وهو مركب INS018_055 الذي طورته شركة Insilico Medicine لعلاج التليف الرئوي مجهول السبب (Idiopathic Pulmonary Fibrosis – IPF). ما كان يستغرق 4-5 سنوات في مرحلة الاكتشاف أُنجز في أقل من 18 شهراً.
خوارزميات التعلم الآلي (Machine Learning) تستطيع تحليل ملايين الأوراق البحثية وقواعد البيانات الجينومية في ساعات معدودة لتحديد أهداف بيولوجية جديدة. نماذج الذكاء الاصطناعي التوليدية (Generative AI) تقترح تراكيب جزيئية لم تُخلّق من قبل، مع التنبؤ بخصائصها الدوائية مسبقاً. هذا يختصر سنوات من العمل المخبري ويقلل التكاليف بنسب كبيرة.
الأدوية البيولوجية والعلاج الجيني
بالتوازي مع ثورة الذكاء الاصطناعي، تشهد صناعة الأدوية تحولاً جذرياً نحو الأدوية البيولوجية (Biologics). على عكس الأدوية الكيميائية التقليدية ذات الجزيئات الصغيرة، فإن الأدوية البيولوجية هي جزيئات كبيرة ومعقدة — كالأجسام المضادة وحيدة النسيلة (Monoclonal Antibodies) — تُنتج من خلايا حية. هذه الأدوية أحدثت ثورة في علاج أمراض مثل السرطان والروماتيزم والتصلب المتعدد.
أما العلاج الجيني (Gene Therapy) فيذهب أبعد من ذلك: بدلاً من معالجة أعراض المرض، يستهدف السبب الجذري عبر إصلاح أو استبدال الجين المعطوب. في عام 2023، وافقت وكالة الغذاء والدواء الأميركية على عقار كاسجيفي (Casgevy) — أول علاج جيني يعتمد على تقنية كريسبر (CRISPR-Cas9) لتعديل الجينات — وذلك لعلاج فقر الدم المنجلي. هذا الحدث يمثل فجراً جديداً في تاريخ الطب.
الطب الشخصي والدقيق
الطب الشخصي أو الدقيق (Personalized Medicine / Precision Medicine) يمثل المستقبل القادم بقوة. الفكرة ببساطة: بدلاً من وصف نفس الدواء لكل المرضى، يُصمم العلاج بناءً على الشفرة الوراثية للمريض نفسه. لماذا؟ لأن جيناتك تؤثر على طريقة استجابة جسمك للأدوية. بعض الأشخاص يحملون طفرات جينية تجعلهم يستقلبون دواءً معيناً ببطء شديد — مما يسبب تراكمه وزيادة آثاره الجانبية — بينما آخرون يستقلبونه بسرعة مفرطة فلا يستفيدون منه. علم الجينوم الدوائي (Pharmacogenomics) يدرس هذه الفروقات الفردية لتخصيص العلاج.
لفتة علمية: بحلول عام 2025، أصبح تحليل الجينوم الكامل متاحاً بتكلفة أقل من 200 دولار، مقارنة بثلاثة مليارات دولار حين أُكمل مشروع الجينوم البشري لأول مرة عام 2003. هذا الانخفاض الدراماتيكي في التكلفة يفتح الباب أمام تطبيقات الطب الشخصي على نطاق أوسع بكثير.
اقرأ أيضاً:
- الهندسة الوراثية: ما هي وكيف تُغيّر مستقبل البشرية؟
- علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
يقول المستشار الدوائي جاسم محمد مراد: “كل دواء تتناوله يمثل خلاصة جهد علمي استمر سنوات طويلة وعبر مراحل اختبار صارمة. فهم هذه المراحل لا يجعلك صيدلانياً، لكنه يجعلك مستهلكاً واعياً قادراً على التمييز بين العلاج الحقيقي والادعاء الزائف — وهذا الوعي في حد ذاته إنجاز صحي كبير.”
الخلاصة التطبيقية من خلية
بعد هذه الجولة المعمّقة في عالم اكتشاف وتطوير الأدوية، إليك أهم الخلاصات العملية التي يمكنك تطبيقها فوراً:
- لا تنخدع بعبارة “أثبتت الدراسات”: اسأل دائماً: أي مرحلة من التجارب السريرية وصل إليها هذا الدواء؟ نتيجة مخبرية في طبق بتري تختلف جذرياً عن تجربة سريرية واسعة النطاق. كثير من الإعلانات المضللة تستغل هذا الغموض.
- الدواء الجنيس ليس “تقليداً رخيصاً”: حين يعرض عليك الصيدلي بديلاً جنيساً، فاعلم أنه خضع لاختبارات التكافؤ الحيوي وحصل على موافقة الجهة التنظيمية. الفارق في السعر لا يعكس فارقاً في الجودة، بل فارقاً في تكاليف البحث والتطوير.
- أبلغ عن أي أثر جانبي غير متوقع: نظام الإبلاغ عن الآثار الجانبية في هيئة الغذاء والدواء السعودية متاح لكل مواطن ومقيم. بلاغك قد يساهم في اكتشاف مشكلة تؤثر على آلاف المرضى الآخرين.
- اسأل طبيبك عن بدائل الطب الشخصي: إذا كنت تعاني من عدم استجابة لدواء معين أو من آثار جانبية مفرطة، فقد يكون تحليل الجينوم الدوائي مفيداً في تحديد الدواء والجرعة الأنسب لجيناتك تحديداً.
- تعامل بحذر مع “الأدوية المعجزة” على وسائل التواصل: أي منتج يدّعي علاج كل شيء دون أن يمر بمراحل التجارب السريرية المعروفة هو على الأرجح احتيال. العلم الحقيقي لا يعد بالمعجزات.
- ادعم جهود التصنيع المحلي: حين تختار دواءً مصنّعاً محلياً في السعودية — وقد اجتاز رقابة SFDA — فأنت تدعم منظومة دوائية وطنية تقلل الاعتماد على الاستيراد وتعزز الأمن الدوائي للمملكة.
- اقرأ النشرة الداخلية: تلك الورقة المطوية داخل علبة الدواء ليست حشواً. إنها ملخص مكثف لكل ما اكتشفته التجارب السريرية عن هذا الدواء: آلية عمله، تفاعلاته، موانع استخدامه، وآثاره الجانبية المحتملة.
ما الأثر الحقيقي لصناعة الأدوية على حياة الإنسان المعاصر؟
لننظر إلى الصورة الكبرى. في عام 1900، كان متوسط عمر الإنسان عالمياً نحو 31 عاماً. اليوم، تجاوز 73 عاماً. هذه القفزة المذهلة لم تحدث بالصدفة. المضادات الحيوية أنقذت البشرية من الأوبئة البكتيرية. اللقاحات استأصلت أمراضاً كانت تفتك بالملايين كالجدري. أدوية القلب والسكري والسرطان حوّلت أمراضاً قاتلة إلى حالات مزمنة يمكن التعايش معها.
في المملكة العربية السعودية، ارتفع متوسط العمر المتوقع إلى أكثر من 77 عاماً بحسب بيانات الهيئة العامة للإحصاء لعام 2024، وهو مؤشر يعكس جودة المنظومة الصحية والدوائية. ومع تطوير المملكة لقدراتها في التصنيع الدوائي والبحث العلمي، يُتوقع أن تصبح لاعباً إقليمياً رئيساً في هذا القطاع خلال العقد القادم.
نقطة تستحق الانتباه: وفقاً لمنظمة الصحة العالمية (WHO)، لا يزال ثلث سكان العالم يفتقرون إلى إمكانية الحصول على الأدوية الأساسية. صناعة الأدوية ليست مجرد قطاع تجاري — إنها قضية عدالة صحية عالمية.
اقرأ أيضاً: الإحصاءات الحيوية (Vital Statistics): المفهوم، الأهمية، والتطبيقات
كل حبة دواء تتناولها هي ثمرة عقود من البحث والتجربة والمراجعة والتدقيق. هي نتيجة تعاون آلاف العلماء والأطباء والمهندسين والإحصائيين والمنظّمين. حين تُدرك هذا، تتغير نظرتك ليس فقط إلى الدواء، بل إلى العلم نفسه كمنظومة حماية للبشرية. ومع التطورات المتسارعة في الذكاء الاصطناعي والطب الشخصي والعلاج الجيني، فإن المستقبل يحمل وعوداً علمية حقيقية — لكنها وعود مبنية على المنهج العلمي الصارم، لا على الإثارة الإعلامية.
شاركنا رأيك في التعليقات: ما الدواء الذي غيّر حياتك أو حياة شخص تعرفه، وهل تساءلت يوماً عن قصته العلمية؟ وإن أعجبك هذا المقال، فشاركه مع طالب طب أو صيدلة أو أي شخص فضولي يستحق أن يعرف ما يختبئ خلف كل علبة دواء.
هل توقفت يوماً لتسأل نفسك: كم عالِماً ساهر أمضى لياليه لكي تصل إليك تلك الحبة التي تبتلعها في ثوانٍ معدودة؟
يلتزم موقع خليّة في إعداد محتواه العلمي بالمعايير الأكاديمية المعتمدة، ويعتمد على مصادر موثّقة من مجلات علمية محكّمة ومنظمات صحية دولية معترف بها، من بينها وكالة الغذاء والدواء الأميركية (FDA)، ووكالة الأدوية الأوروبية (EMA)، وهيئة الغذاء والدواء السعودية (SFDA)، ومنظمة الصحة العالمية (WHO).
يخضع كل مقال لمراجعة علمية متخصصة من قِبل هيئة تحرير مؤهّلة، ولمرحلتَي تدقيق علمي ولغوي قبل النشر. قائمة المصادر والمراجع مُدرجة في نهاية كل مقال للتحقق منها بشكل مستقل.
- ICH Q10 (2023) – مجلس التنسيق الدولي للتنظيم الدوائي: نظام جودة صناعة الأدوية الموحّد دولياً، المعتمد من FDA وEMA وSFDA.
- GMP – ممارسات التصنيع الجيد (WHO Technical Report Series, 2024): المرجع الدولي لمعايير إنتاج الأدوية وضمان جودتها.
- FDA Drug Development Process (2024): الإطار التنظيمي الرسمي لمراحل تطوير الأدوية والموافقة عليها.
- SFDA Pharmaceutical Regulations (2024): لوائح هيئة الغذاء والدواء السعودية المنظِّمة لتسجيل الأدوية ومراقبتها في المملكة العربية السعودية.
- Declaration of Helsinki (2013) – World Medical Association: المبادئ الأخلاقية الدولية الحاكمة للبحوث الطبية على البشر.
المصادر والمراجع
- DiMasi, J. A., Grabowski, H. G., & Hansen, R. W. (2016). Innovation in the pharmaceutical industry: New estimates of R&D costs. Journal of Health Economics, 47, 20–33. https://doi.org/10.1016/j.jhealeco.2016.01.012
دراسة مرجعية تقدّر تكلفة تطوير دواء جديد بنحو 2.6 مليار دولار. - Mullard, A. (2019). 2018 FDA drug approvals. Nature Reviews Drug Discovery, 18(2), 85–89. https://doi.org/10.1038/d41573-019-00014-x
تحليل سنوي لموافقات FDA وتوجهات صناعة الأدوية. - Zhavoronkov, A., et al. (2019). Deep learning enables rapid identification of potent DDR1 kinase inhibitors. Nature Biotechnology, 37(9), 1038–1040. https://doi.org/10.1038/s41587-019-0224-x
دراسة رائدة في استخدام الذكاء الاصطناعي لاكتشاف مثبطات كيناز جديدة. - Wouters, O. J., McKee, M., & Luyten, J. (2020). Estimated research and development investment needed to bring a new medicine to market, 2009-2018. JAMA, 323(9), 844–853. https://doi.org/10.1001/jama.2020.1166
دراسة نُشرت في JAMA تقدّر تكاليف البحث والتطوير الدوائي. - Hay, M., et al. (2014). Clinical development success rates for investigational drugs. Nature Biotechnology, 32(1), 40–51. https://doi.org/10.1038/nbt.2786
تحليل شامل لمعدلات النجاح والفشل في مراحل التجارب السريرية. - Fda.gov. (2024). The Drug Development Process. U.S. Food and Drug Administration. https://www.fda.gov/patients/learn-about-drug-and-device-approvals/drug-development-process
صفحة رسمية تشرح مراحل تطوير الأدوية من وجهة نظر الجهة التنظيمية. - World Health Organization. (2024). Access to medicines. https://www.who.int/health-topics/access-to-medicines
تقرير عن التحديات العالمية في الوصول إلى الأدوية الأساسية. - Saudi Food and Drug Authority (SFDA). (2024). Pharmaceutical Regulations. https://www.sfda.gov.sa
الموقع الرسمي لهيئة الغذاء والدواء السعودية ولوائح تنظيم الأدوية. - European Medicines Agency (EMA). (2024). How EMA evaluates medicines. https://www.ema.europa.eu/en/about-us/what-we-do/authorisation-medicines
شرح لآلية تقييم الأدوية في الاتحاد الأوروبي. - International Council for Harmonisation (ICH). (2024). Guidelines. https://www.ich.org/page/ich-guidelines
المعايير الدولية الموحدة لتسجيل المستحضرات الصيدلانية. - Lipinski, C. A. (2004). Lead- and drug-like compounds: the rule-of-five revolution. Drug Discovery Today: Technologies, 1(4), 337–341. https://doi.org/10.1016/j.ddtec.2004.11.007
الورقة المرجعية لقاعدة ليبنسكي للخمسة المستخدمة في تصميم الأدوية. - Hughes, J. P., et al. (2011). Principles of early drug discovery. British Journal of Pharmacology, 162(6), 1239–1249. https://doi.org/10.1111/j.1476-5381.2010.01127.x
مرجع أكاديمي شامل لمبادئ اكتشاف الأدوية المبكر. - Rang, H. P., et al. (2019). Rang & Dale’s Pharmacology (9th ed.). Elsevier.
كتاب مرجعي رئيس في علم الأدوية يُدرَّس في معظم كليات الصيدلة والطب حول العالم. - Patrick, G. L. (2023). An Introduction to Medicinal Chemistry (7th ed.). Oxford University Press.
كتاب أكاديمي يشرح أسس الكيمياء الطبية وتصميم الأدوية. - Stringer, J. L. (2017). Basic Concepts in Pharmacology: What You Need to Know for Each Drug Class (5th ed.). McGraw-Hill Education.
مرجع مبسّط للمفاهيم الأساسية في علم الأدوية لطلاب العلوم الصحية.
قراءات إضافية ومصادر للتوسع
- Drews, J. (2000). Drug discovery: a historical perspective. Science, 287(5460), 1960–1964. https://doi.org/10.1126/science.287.5460.1960
لماذا نقترح عليك قراءته؟ لأنه يقدم منظوراً تاريخياً عميقاً لتطور اكتشاف الأدوية من الصدفة إلى التصميم العقلاني، ويُعَدُّ من أكثر المقالات استشهاداً في هذا المجال. - Kola, I., & Landis, J. (2004). Can the pharmaceutical industry reduce attrition rates? Nature Reviews Drug Discovery, 3(8), 711–716. https://doi.org/10.1038/nrd1470
لماذا نقترح عليك قراءته؟ لأنه يحلل أسباب فشل الأدوية في مراحل التطوير المختلفة، ويقترح حلولاً منهجية لتقليل معدلات الاستنزاف — وهو موضوع محوري لكل من يريد فهم اقتصاديات الأدوية. - Schneider, G. (2018). Automating drug discovery. Nature Reviews Drug Discovery, 17(2), 97–113. https://doi.org/10.1038/nrd.2017.232
لماذا نقترح عليك قراءته؟ لأنه يقدم مراجعة شاملة ومحدّثة لدور الأتمتة والذكاء الاصطناعي في إعادة تشكيل مراحل اكتشاف الأدوية، وهو مرجع أساسي لفهم مستقبل هذه الصناعة.
إن كنت طالباً أو باحثاً أو مجرد قارئ فضولي وصلت إلى هذه السطور، فأنت بالفعل تملك الآن فهماً أعمق بكثير مما يملكه معظم الناس حول كيف تتم صناعة الأدوية كيميائياً وسريرياً وتنظيمياً. ندعوك لمشاركة هذا المقال مع من تعتقد أنه سيستفيد منه، ولا تتردد في ترك تعليقك أو سؤالك — فريق خلية العلمي جاهز للإجابة ومتحمس للنقاش معك.
المعلومات الواردة في هذا المقال ذات طابع علمي وتعليمي بحت، وتهدف إلى نشر الوعي الدوائي والمعرفة العلمية العامة حول آليات تطوير الأدوية وتصنيعها. لا تُعدّ هذه المعلومات بديلاً عن الاستشارة الطبية أو الصيدلانية المتخصصة، ولا ينبغي الاستناد إليها في اتخاذ قرارات علاجية فردية. يُرجى دائماً الرجوع إلى الطبيب أو الصيدلاني المختص قبل تناول أي دواء أو تعديل جرعة أو إيقاف علاج قائم. موقع خليّة غير مسؤول عن أي قرار صحي يُتخذ بناءً على ما ورد في هذا المحتوى.





