البلاديوم: الدليل العلمي الشامل لخصائص واستخدامات العنصر الأغلى من الذهب
لماذا يُعتبر البلاديوم أكثر قيمة من الذهب في بعض التطبيقات الحديثة؟

البلاديوم عنصر كيميائي انتقالي نادر يحمل الرمز Pd والعدد الذري 46، ينتمي إلى مجموعة البلاتين (Platinum Group Metals) في الجدول الدوري. يتميز بقدرته الفريدة على امتصاص كميات هائلة من غاز الهيدروجين تصل إلى 900 ضعف حجمه، ويُستخدم بكثافة في المحولات الحفازة للسيارات لتقليل الانبعاثات السامة، مما جعله في بعض الأعوام أغلى من الذهب والبلاتين معاً.
هل سبق لك أن تساءلت لماذا يدفع المصنعون مبالغ طائلة لشراء معدن فضي اللون قد لا تسمع عنه كثيراً في حياتك اليومية، بينما الذهب يحتل العناوين باستمرار؟ أنت لست وحدك في هذه الحيرة؛ إذ إن البلاديوم يُعَدُّ واحداً من أكثر العناصر غموضاً وإثارة في الوقت ذاته. في هذا المقال، ستكتشف أسباباً علمية واقتصادية دقيقة تجعل من هذا المعدن النادر ركيزة أساسية في صناعة السيارات والإلكترونيات والطب، وستفهم كيف يمكن لعنصر واحد أن يحمل خصائص كيميائية استثنائية تُغيّر مسار التكنولوجيا الحديثة. بعد قراءة هذا النص، ستمتلك نظرة أعمق تساعدك على فهم الأخبار الاقتصادية المتعلقة بأسعار المعادن النفيسة، وستدرك لماذا يراهن العالم على البلاديوم في مستقبل الطاقة النظيفة.
الخلاصة التنفيذية
احصل على أهم ما تحتاجه لفهم البلاديوم في أقل من دقيقة.
الفكرة الأساسية
- افهم أن قيمة البلاديوم تأتي من كفاءته الصناعية، لا من ندرته فقط.
- اربط ارتفاع سعره بالطلب على المحولات الحفازة أكثر من ارتباطه بسوق الزينة.
أرقام مفصلية
- تذكّر أن رمزه Pd وعدده الذري 46.
- لاحظ أنه يستطيع امتصاص ما يصل إلى 900 ضعف حجمه من الهيدروجين.
- تحتوي السيارة الواحدة عادة على نحو 2 – 7 g منه.
أين يُستخدم فعلياً؟
- اربط البلاديوم مباشرة بتنقية عوادم السيارات عبر المحولات الحفازة.
- تابع حضوره في الإلكترونيات الدقيقة، وطب الأسنان، وتنقية الهيدروجين، وخلايا الوقود.
ماذا يعني ذلك للمستقبل؟
- توقّع استمرار أهميته ما دامت محركات الاحتراق الداخلي حاضرة.
- راقب عاملين حاسمين: إعادة التدوير واقتصاد الهيدروجين.
- لا تفترض أن البدائل الرخيصة قادرة حالياً على تعويض كفاءته بسهولة.
مثال تطبيقي: محول السيارة الذي لا ينام
تخيل أن سالم، وهو فني سيارات في الرياض، يفحص محولاً حفازاً تالفاً من سيارة قديمة. يعلم سالم أن هذا الجهاز الصغير، الذي لا يتجاوز حجمه صندوق الأحذية، يحتوي على كميات ضئيلة من البلاديوم تُقدر بنحو 2 إلى 7 غرامات فقط. لكن ما يثير دهشته هو أن هذه الكمية الضئيلة كافية لتحويل ملايين الجزيئات من أول أكسيد الكربون السام (CO) إلى ثاني أكسيد الكربون (CO₂) الأقل ضرراً، وتحويل أكاسيد النيتروجين (NOₓ) إلى نيتروجين وأكسجين آمنين. كيف يحدث هذا؟ السر يكمن في السطح المجهري للبلاديوم الذي يعمل كمسرح كيميائي حيوي: الجزيئات تصطدم بسطحه، تنكسر روابطها، ثم تعاد صياغتها في أشكال أقل سُمّية، كل ذلك دون أن يفقد المعدن ذرة واحدة من بنيته. من هذه اللحظة فصاعداً، يمكنك أن تنظر إلى عادم السيارة بعين مختلفة: فهو ليس مجرد أنبوب معدني، بل مختبر كيميائي صغير يعمل بلا توقف بفضل البلاديوم.
ما هي الهوية الكيميائية الكاملة للبلاديوم؟
لنبدأ بالأساسيات؛ فالبلاديوم ليس مجرد معدن لامع، بل هو عنصر ذو هوية كيميائية مميزة جداً. يحمل الرمز الكيميائي Pd، والعدد الذري 46، مما يعني أن نواة ذرته تحتوي على 46 بروتوناً. الكتلة الذرية النسبية للبلاديوم تبلغ حوالي 106.42 u (وحدة كتلة ذرية)، وهو رقم يعكس متوسط كتل نظائره الطبيعية المستقرة الستة. ينتمي البلاديوم إلى المجموعة 10 (مجموعة النيكل) والدورة الخامسة في الجدول الدوري، ويُصنف ضمن العناصر الانتقالية (Transition Metals) وتحديداً ضمن مجموعة معادن البلاتين (Platinum Group Metals – PGMs) التي تضم أيضاً البلاتين، الروديوم، الروثينيوم، الإيريديوم، والأوزميوم.
في درجة حرارة الغرفة (25 °C تقريباً)، يوجد البلاديوم في الحالة الصلبة، ويظهر بمظهر معدني فضي لامع يشبه البلاتين لكنه أخف وزناً وأقل كثافة. سطحه يعكس الضوء بشكل رائع، ولا يتأكسد بسهولة في الهواء الجوي العادي عند درجات الحرارة المنخفضة، مما يجعله مثالياً للاستخدامات الصناعية الدقيقة. لكن ما يميز البلاديوم حقاً ليس مظهره الخارجي، بل سلوكه الكيميائي الاستثنائي الذي سنستكشفه في الفقرات القادمة. هل تساءلت يوماً لماذا لا يصدأ هذا المعدن مثل الحديد رغم تعرضه للهواء؟ الإجابة تكمن في بنيته الإلكترونية الفريدة التي تقاوم التفاعل السريع مع الأكسجين.
هل تعلم؟
البلاديوم هو العنصر الوحيد في مجموعة البلاتين الذي يمتلك أقل كثافة (12.02 g/cm³)، مما يجعله الأخف وزناً بين أقرانه النبلاء رغم قيمته الصناعية الهائلة.
اقرأ أيضاً:
الهيدروجين: الدليل العلمي الشامل لخصائصه، أنواعه، ومستقبله في عالم الطاقة
كيف اكتُشف البلاديوم ومن أين جاءت تسميته؟
القصة تعود إلى لندن عام 1803، عندما كان الكيميائي الإنجليزي ويليام هايد ولاستون (William Hyde Wollaston) يعمل على تنقية خام البلاتين الخام القادم من أمريكا الجنوبية. لم يكن ولاستون يعلم أنه على وشك اكتشاف عنصرين جديدين دفعة واحدة؛ ففي أثناء معالجته للخام بأحماض قوية، لاحظ وجود مواد غريبة لا تتطابق خصائصها مع البلاتين. بعد سلسلة من التجارب الدقيقة، نجح في عزل معدن جديد ذي لون فضي باهت. أطلق عليه اسم Palladium نسبة إلى كويكب Pallas الذي اكتُشف قبل عامين فقط (1801) على يد الفلكي الألماني هاينريش أولبرس.
لكن لماذا ربط ولاستون اسم المعدن بكويكب؟ السبب يعود إلى تقليد علمي سائد آنذاك يقضي بربط الاكتشافات الكيميائية الجديدة بالأجرام السماوية أو الآلهة الأسطورية. فقد كان اكتشاف عنصر اليورانيوم (Uranium) قد ارتبط بكوكب أورانوس، والسيريوم (Cerium) بكويكب سيريس. بالمقابل، فإن اسم “Pallas” نفسه مأخوذ من بالاس أثينا (Pallas Athena)، إلهة الحكمة والحرب في الأساطير اليونانية. هكذا حمل البلاديوم في اسمه إشارة إلى الحكمة والقوة، وهو ما تأكد لاحقاً من خلال استخداماته الصناعية الحاسمة.
من الجدير بالذكر أن ولاستون لم يعلن فوراً عن اكتشافه؛ بل باع كميات صغيرة من البلاديوم بشكل مجهول في البداية لاختبار ردود الفعل العلمية. وعندما شكك بعض الكيميائيين في وجود العنصر، كشف ولاستون عن هويته وأثبت اكتشافه بشكل قاطع. برأيكم ماذا كان شعور ولاستون عندما أدرك أنه اكتشف ليس عنصراً واحداً بل عنصرين (البلاديوم والروديوم) من خام واحد؟ الإجابة هي على الأرجح مزيج من الفخر العلمي والدهشة الحقيقية.
اقرأ أيضاً:
أنطوان لافوازييه: مؤسس الكيمياء الحديثة
ما الذي يجعل البنية الذرية للبلاديوم استثنائية؟
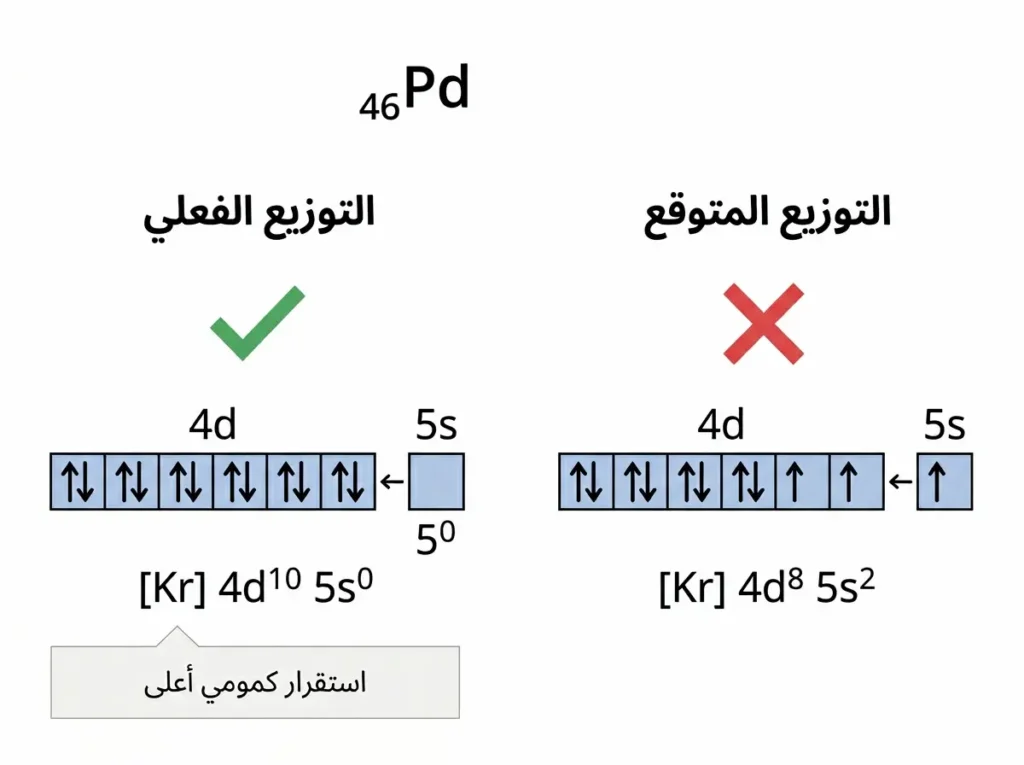
هنا نصل إلى أحد أكثر الجوانب إثارة في كيمياء البلاديوم: التوزيع الإلكتروني. في العادة، نتوقع أن يتبع عنصر انتقالي مثل البلاديوم قاعدة “ملء المدارات بالترتيب” حسب مبدأ أوفباو (Aufbau Principle). لكن البلاديوم يخالف هذه القاعدة بطريقة مذهلة؛ فبدلاً من أن يكون توزيعه الإلكتروني المتوقع هو:
[Kr] 4d8 5s2
نجد أن التوزيع الفعلي هو:
[Kr] 4d10 5s0
بمعنى آخر، المدار 4d ممتلئ تماماً بـ 10 إلكترونات، بينما المدار 5s فارغ تماماً. لماذا يحدث هذا؟ السبب يعود إلى مفهوم الاستقرار الكمومي (Quantum Stability)؛ إذ إن امتلاء المدار 4d بالكامل يمنح الذرة استقراراً إضافياً أكبر مما لو وُزعت الإلكترونات بالطريقة التقليدية. هذا الترتيب الفريد يُعَدُّ حالة شاذة (Anomaly) في الجدول الدوري، ويشترك فيها البلاديوم مع عناصر قليلة جداً مثل الكروم (Cr) والنحاس (Cu).
من ناحية أخرى، فإن هذا التوزيع الإلكتروني الاستثنائي يفسر الكثير من الخصائص الكيميائية للبلاديوم. فعلى سبيل المثال، يسمح له بتكوين روابط كيميائية قوية ومرنة مع العناصر الأخرى، خاصة الكربون والهيدروجين. كما أنه يمنحه قدرة فائقة على العمل كعامل حفاز (Catalyst) في التفاعلات الكيميائية المعقدة، حيث يمكنه قبول الإلكترونات وإعادة توزيعها بسهولة نسبية.
بالنسبة لحالات الأكسدة (Oxidation States)، فإن البلاديوم يظهر بشكل شائع في حالتي +2 و**+4**، وهما الأكثر استقراراً. لكنه يمكن أن يظهر أيضاً في حالات أكسدة نادرة مثل 0 و**+3** و**+6** في ظروف كيميائية خاصة. حالة الأكسدة +2 هي الأكثر شيوعاً في مركبات البلاديوم العضوية والمعقدات التنسيقية (Coordination Complexes)، بينما حالة +4 تظهر في مركبات أكثر تطرفاً مثل رباعي فلوريد البلاديوم (PdF₄).
أما السالبية الكهربائية (Electronegativity) للبلاديوم فتبلغ حوالي 2.20 على مقياس باولنج (Pauling Scale)، مما يجعله أقل سالبية من البلاتين (2.28) لكنه أعلى من النيكل (1.91). هذا يعني أن البلاديوم يميل إلى جذب الإلكترونات في الروابط الكيميائية بدرجة معتدلة، مما يمنحه مرونة كبيرة في تكوين مركبات متنوعة. بينما تبلغ طاقة التأين الأولى (First Ionization Energy) للبلاديوم حوالي 804.4 kJ/mol، وهي أقل من البلاتين (870 kJ/mol)، مما يعني أنه يحتاج طاقة أقل نسبياً لإزالة الإلكترون الأول من ذرته.
معلومة سريعة
البلاديوم النقي يمتلك موصلية كهربائية ممتازة تبلغ حوالي 9.5 × 10⁶ S/m (سيمنز لكل متر)، مما يجعله مادة مثالية في صناعة المكثفات الإلكترونية الدقيقة.
اقرأ أيضاً:
الخلية (Cell): الوحدة الأساسية للحياة
كيف يتفاعل البلاديوم مع العناصر الأخرى كيميائياً؟
البلاديوم ليس معدناً خاملاً تماماً كما قد يظن البعض؛ بل له تفاعلية مميزة تعتمد على الظروف المحيطة ونوع العنصر المتفاعل معه. مع الهالوجينات (Halogens) مثل الفلور (F₂) والكلور (Cl₂)، يتفاعل البلاديوم بشكل نشط نسبياً عند تسخينه، مكوناً هاليدات البلاديوم مثل:
Pd + Cl2 → PdCl2
هذا التفاعل ينتج كلوريد البلاديوم الثنائي (Palladium(II) chloride)، وهو مركب بني محمر يُستخدم على نطاق واسع في التخليق العضوي والكيمياء التنسيقية. على النقيض من ذلك، فإن البلاديوم لا يتفاعل مع الأكسجين (O₂) في درجات الحرارة العادية، لكنه يتأكسد ببطء عند تسخينه فوق 400 °C، مكوناً أكسيد البلاديوم (PdO) الأسود، وهو مركب غير مستقر نسبياً ينحل بسهولة عند تسخينه لدرجات أعلى.
بالمقابل، يُظهر البلاديوم مقاومة ممتازة للأحماض غير المؤكسِدة مثل حمض الهيدروكلوريك (HCl) وحمض الكبريتيك المخفف (H₂SO₄). لكنه يذوب بسرعة في الأحماض المؤكسِدة القوية مثل حمض النيتريك (HNO₃) وخليط الماء الملكي (Aqua Regia)، وهو مزيج من حمض النيتريك وحمض الهيدروكلوريك بنسبة 1:3. يُعَدُّ الماء الملكي أحد أقوى المذيبات الكيميائية لمعادن مجموعة البلاتين.
فهل يا ترى يتفاعل البلاديوم مع القلويات؟ في الواقع، لا يتفاعل البلاديوم مع القواعد القوية مثل هيدروكسيد الصوديوم (NaOH) في الظروف العادية، مما يجعله مقاوماً للتآكل في البيئات القلوية. هذه الخاصية مهمة جداً في بعض التطبيقات الصناعية، خاصة في البيئات التي تحتوي على مواد كيميائية قاسية.
ما هي الخصائص الفيزيائية التي تميز البلاديوم عن غيره؟
لنتحدث الآن عن الأرقام التي تكشف شخصية البلاديوم الفيزيائية. تبلغ كثافة البلاديوم حوالي 12.02 g/cm³ في درجة حرارة الغرفة، وهي أقل من كثافة البلاتين (21.45 g/cm³) والروديوم (12.41 g/cm³)، لكنها أعلى من النيكل (8.90 g/cm³). هذا يجعله معدناً كثيفاً نسبياً، لكنه أخف بكثير من معظم أقرانه في مجموعة البلاتين.
أما درجة انصهار البلاديوم فتبلغ 1554.9 °C (2830.8 °F أو 1828.05 K)، وهي أقل بشكل ملحوظ من درجة انصهار البلاتين (1768.3 °C). بينما تبلغ درجة غليانه حوالي 2963 °C (5365 °F أو 3236 K)، مما يعني أن البلاديوم يبقى صلباً في معظم الظروف الصناعية العادية، لكنه يمكن أن يُصهر بسهولة نسبية في الأفران المتخصصة.
كما أن البلاديوم يمتلك موصلية حرارية ممتازة تبلغ حوالي 71.8 W/(m·K) (واط لكل متر كلفن)، مما يجعله مادة مثالية لتطبيقات تبديد الحرارة في الإلكترونيات الدقيقة. بالإضافة إلى ذلك، فهو معدن مرن وقابل للطرق (Malleable) والسحب (Ductile)؛ إذ يمكن تشكيله في أسلاك رقيقة جداً أو صفائح رقيقة دون أن ينكسر.
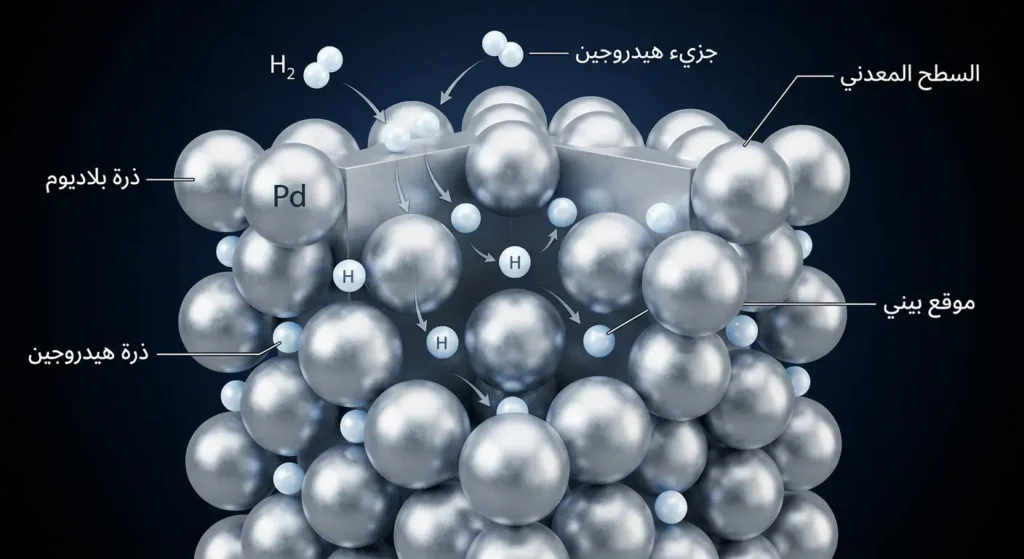
لكن الخاصية الأكثر إثارة للدهشة هي قدرة البلاديوم الفائقة على امتصاص غاز الهيدروجين (Hydrogen Absorption). عند درجة حرارة الغرفة، يمكن للبلاديوم أن يمتص ما يصل إلى 900 ضعف حجمه من غاز الهيدروجين! كيف يحدث هذا؟ السر يكمن في البنية البلورية للبلاديوم التي تسمح لذرات الهيدروجين الصغيرة بالتسلل بين الذرات المعدنية وملء الفراغات البينية (Interstitial Sites) داخل الشبكة البلورية. هذه العملية تُعرف باسم الامتصاص البيني (Interstitial Absorption)، وتحدث دون أن تتغير البنية الأساسية للمعدن بشكل جذري، رغم أن حجمه يتمدد قليلاً.
انظر إلى هذا التشبيه: تخيل أن البلاديوم عبارة عن إسفنجة معدنية صلبة، وذرات الهيدروجين عبارة عن قطرات ماء صغيرة جداً. عندما تضغط على الإسفنجة، فإنها تمتص الماء بسهولة، لكنها لا تذوب ولا تفقد شكلها؛ بل تصبح أثقل قليلاً وأكثر امتلاءً. هكذا تماماً يتصرف البلاديوم مع الهيدروجين. هذه الخاصية جعلت البلاديوم أساسياً في تطبيقات تنقية الهيدروجين وتخزينه، خاصة في تقنيات خلايا الوقود (Fuel Cells) التي تعمل بالهيدروجين.
| الخاصية | القيمة |
|---|---|
| الرمز الكيميائي | Pd |
| العدد الذري | 46 |
| الكتلة الذرية النسبية | 106.42 u |
| المجموعة | 10 |
| الدورة | 5 |
| التصنيف | عنصر انتقالي من معادن مجموعة البلاتين |
| الحالة عند 25 °C | صلب |
| الكثافة | 12.02 g/cm³ |
| درجة الانصهار | 1554.9 °C |
| درجة الغليان | 2963 °C |
| السالبية الكهربائية | 2.20 |
| حالات الأكسدة الشائعة | +2, +4 |
|
المصدر
الجمعية الملكية للكيمياء – بيانات عنصر البلاديوم
المعاهد الوطنية للصحة الأميركية – PubChem
هذا الجدول يجمع أهم ثوابت الهوية الكيميائية والفيزيائية للبلاديوم في بطاقة مرجعية واحدة مناسبة للقراءة السريعة.
|
|
حقيقة علمية
عندما يمتص البلاديوم الهيدروجين، يمكن أن يتمدد حجمه بنسبة تصل إلى 10%، لكنه يعود إلى حجمه الأصلي عند تحرير الهيدروجين دون أي ضرر دائم للبنية المعدنية.
اقرأ أيضاً:
- الطاقة في الفيزياء: ما هي أشكالها وكيف تتحول بين الأنظمة؟
- الطاقة الكامنة: ما هي وكيف تشكل أساس الفيزياء الحديثة؟
كم عدد نظائر البلاديوم وما استخداماتها؟
للبلاديوم ستة نظائر طبيعية مستقرة موجودة في الطبيعة بنسب متفاوتة:
- Pd-102: نسبته حوالي 1.02%
- Pd-104: نسبته حوالي 11.14%
- Pd-105: نسبته حوالي 22.33%
- Pd-106: نسبته حوالي 27.33%
- Pd-108: نسبته حوالي 26.46%
- Pd-110: نسبته حوالي 11.72%
هذه النظائر الستة غير مشعة ومستقرة تماماً، وهي التي تشكل معدن البلاديوم الموجود في الطبيعة. بالمقابل، يوجد أكثر من 30 نظيراً مشعاً صناعياً للبلاديوم، أهمها Palladium-103 (Pd-103)، وهو نظير مشع يُستخدم في العلاج الإشعاعي الموضعي (Brachytherapy) لعلاج بعض أنواع سرطان البروستاتا. يُزرع Pd-103 على شكل “بذور” صغيرة داخل الورم مباشرة، حيث يُصدر أشعة غاما منخفضة الطاقة تدمر الخلايا السرطانية المحيطة بدقة عالية دون الإضرار بالأنسجة السليمة البعيدة. فترة عمر النصف (Half-life) لـ Pd-103 تبلغ حوالي 17 يوماً، مما يجعله مناسباً للعلاج قصير المدى.
من الجدير بالذكر أن استخدام Pd-103 في الطب بدأ في الثمانينيات من القرن الماضي، وأثبت فعالية عالية في تقليل الآثار الجانبية مقارنة بالعلاج الإشعاعي التقليدي. لقد ساهم هذا النظير في إنقاذ حياة آلاف المرضى حول العالم، مما يضيف بُعداً إنسانياً عميقاً إلى قيمة البلاديوم العلمية.
اقرأ أيضاً:
علاج السرطان: التقنيات الحديثة والابتكارات المستقبلية
أين يوجد البلاديوم في الطبيعة وكيف يُستخرج؟
البلاديوم عنصر نادر جداً في القشرة الأرضية؛ إذ يُقدر متوسط وفرته بحوالي 0.015 جزء في المليون (ppm) فقط، مما يجعله أندر من الذهب (0.004 ppm) لكنه أكثر وفرة من البلاتين (0.005 ppm). لا يوجد البلاديوم بشكل حر نقي في الطبيعة إلا نادراً؛ بل يوجد عادة متحداً مع معادن أخرى أو مختلطاً مع خامات النيكل والنحاس.
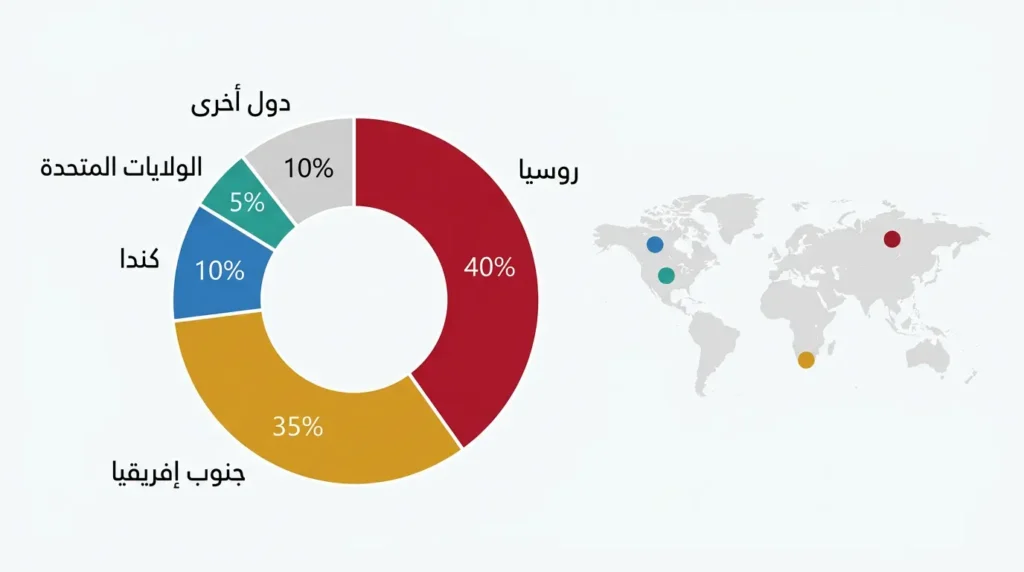
أكبر مصادر البلاديوم الطبيعية توجد في روسيا (خاصة منطقة نوريلسك في سيبيريا) وجنوب إفريقيا (خاصة منطقة بوشفيلد). تنتج روسيا وحدها حوالي 40% من الإنتاج العالمي للبلاديوم، بينما تساهم جنوب إفريقيا بنحو 35%، تليهما كندا والولايات المتحدة بنسب أقل. هذا التركز الجغرافي الضيق للإنتاج يجعل البلاديوم عُرضة للتقلبات الجيوسياسية والاقتصادية؛ فأي اضطراب سياسي أو عقوبات اقتصادية على روسيا يمكن أن تؤدي إلى ارتفاع حاد في أسعار البلاديوم عالمياً.
بالنسبة لعملية الاستخراج، فإنها معقدة ومكلفة جداً. يُستخرج البلاديوم عادة كمنتج ثانوي (By-product) من تعدين النيكل والنحاس. تمر الخامات بسلسلة طويلة من المعالجات الكيميائية والحرارية، تشمل الطحن، التحميص، الصهر، ثم التنقية الكهروكيميائية. في النهاية، يتم فصل البلاديوم عن العناصر الأخرى باستخدام تقنيات متقدمة مثل الاستخلاص بالمذيبات (Solvent Extraction) والترسيب الكيميائي (Chemical Precipitation). النقاء النهائي للبلاديوم التجاري يصل عادة إلى 99.9% أو أعلى.
نقطة تستحق الانتباه
في عام 2021، بلغ سعر البلاديوم أكثر من 2800 دولار للأونصة، متجاوزاً الذهب والبلاتين لأول مرة في التاريخ، بسبب الطلب المتزايد على المحولات الحفازة وانخفاض الإمدادات.
اقرأ أيضاً:
علم المعادن (Mineralogy): دراسة المعادن وتكوينها
ما هي أهم مركبات البلاديوم الكيميائية؟
من بين مركبات البلاديوم الكثيرة، يبرز كلوريد البلاديوم الثنائي (Palladium(II) chloride – PdCl₂) كواحد من أكثر المركبات استخداماً في الكيمياء العضوية والصناعية. يظهر هذا المركب على شكل مسحوق بني محمر، ويُستخدم كعامل حفاز في تفاعلات كيميائية مهمة مثل تفاعلات الازدواج المتقاطع (Cross-Coupling Reactions)، وتحديداً تفاعل هيك (Heck Reaction) وتفاعل سوزوكي (Suzuki Reaction)، اللذين حصل مكتشفوهما على جائزة نوبل في الكيمياء عام 2010.
كذلك، يُستخدم أسيتات البلاديوم (Palladium(II) acetate – Pd(OAc)₂) على نطاق واسع في التخليق العضوي كعامل حفاز متجانس (Homogeneous Catalyst). يتميز هذا المركب بقابليته للذوبان في المذيبات العضوية، مما يجعله مثالياً لتفاعلات الأكسدة والهدرجة (Hydrogenation) وتفاعلات تكوين الروابط الكربون-كربون (C-C Bond Formation).
فما هي آلية عمل هذه المركبات كعوامل حفازة؟ الإجابة هي أن البلاديوم في هذه المركبات يعمل كـ “وسيط كيميائي” ينشّط جزيئات المواد المتفاعلة عن طريق تكوين معقدات تنسيقية مؤقتة معها، ثم يُطلقها بعد اكتمال التفاعل دون أن يُستهلك. هذه القدرة على العودة إلى الحالة الأصلية بعد كل دورة تفاعل تجعل البلاديوم عامل حفاز فعالاً للغاية، حتى لو استُخدم بكميات ضئيلة جداً.
العدسة العلمية الدقيقة – للمهتمين بالتفاصيل الأعمق
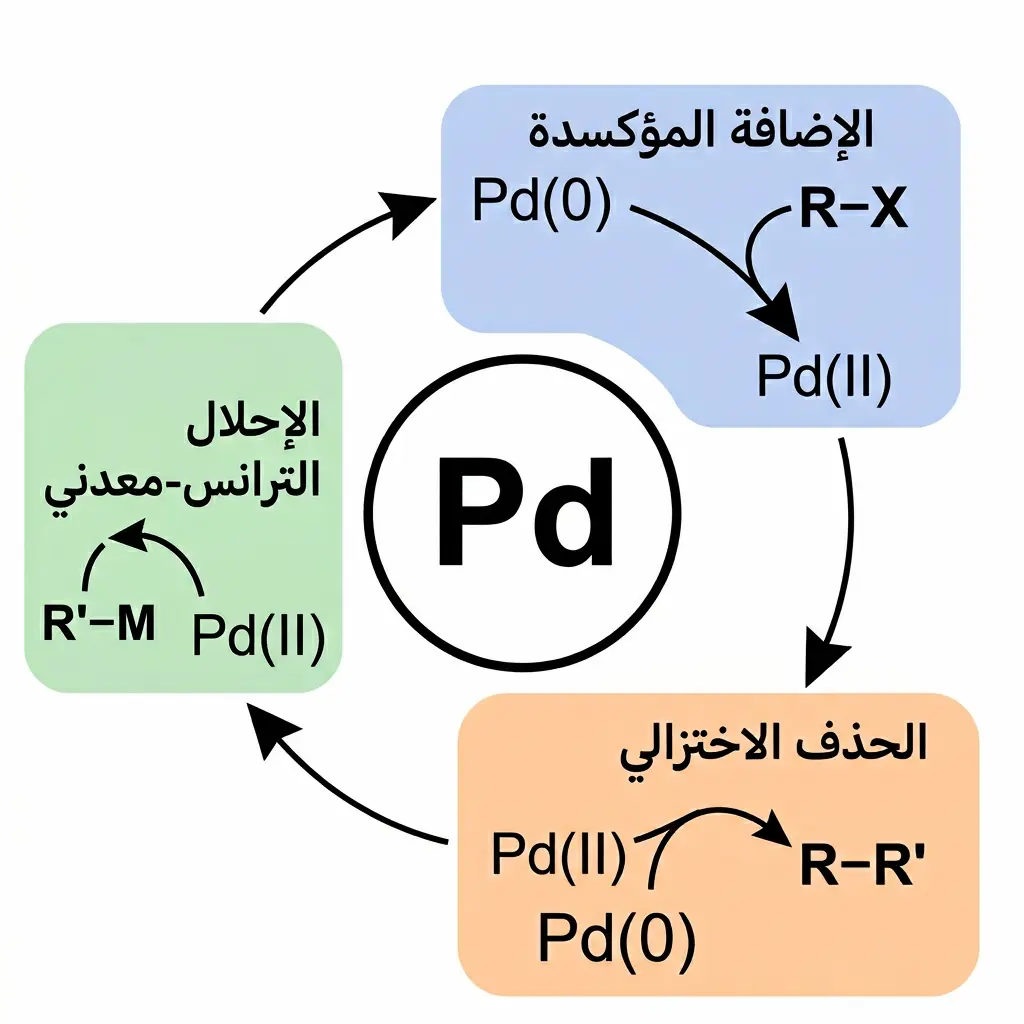
آلية العمل الحفزي للبلاديوم في تفاعلات الازدواج المتقاطع تعتمد على دورة حفزية (Catalytic Cycle) تتضمن ثلاث خطوات رئيسة: الإضافة المؤكسدة (Oxidative Addition)، والإحلال الترانس-معدني (Transmetalation)، ثم الحذف الاختزالي (Reductive Elimination). في كل خطوة، يتغير عدد الأكسدة للبلاديوم بين Pd(0) وPd(II) بشكل دوري، مما يسمح بتكوين روابط كربون-كربون قوية بكفاءة عالية. من المهم ملاحظة أن حساسية هذه التفاعلات تجاه الأكسجين والرطوبة تتطلب إجراءها في أجواء خاملة (Inert Atmosphere) مثل النيتروجين أو الأرجون.
لماذا لا يمكن للعالم الاستغناء عن البلاديوم؟
الآن نصل إلى قلب الموضوع: التطبيقات. الاستخدام الأهم والأكثر استهلاكاً للبلاديوم على مستوى العالم هو في المحولات الحفازة (Catalytic Converters) للسيارات. حوالي 85% من الإنتاج العالمي للبلاديوم يذهب إلى هذا التطبيق وحده! لكن كيف يعمل المحول الحفاز؟ دعني أشرح لك بطريقة واضحة:
عندما يحترق الوقود (البنزين أو الديزل) في محرك السيارة، ينتج عن الاحتراق غازات سامة خطيرة مثل:
- أول أكسيد الكربون (CO): غاز عديم اللون والرائحة، لكنه قاتل عند استنشاقه بتراكيز عالية.
- أكاسيد النيتروجين (NOₓ): مثل NO و NO₂، وهي تسبب الضباب الدخاني وتلوث الهواء.
- هيدروكربونات غير محترقة (Unburned Hydrocarbons): مثل البنزين المتبخر.
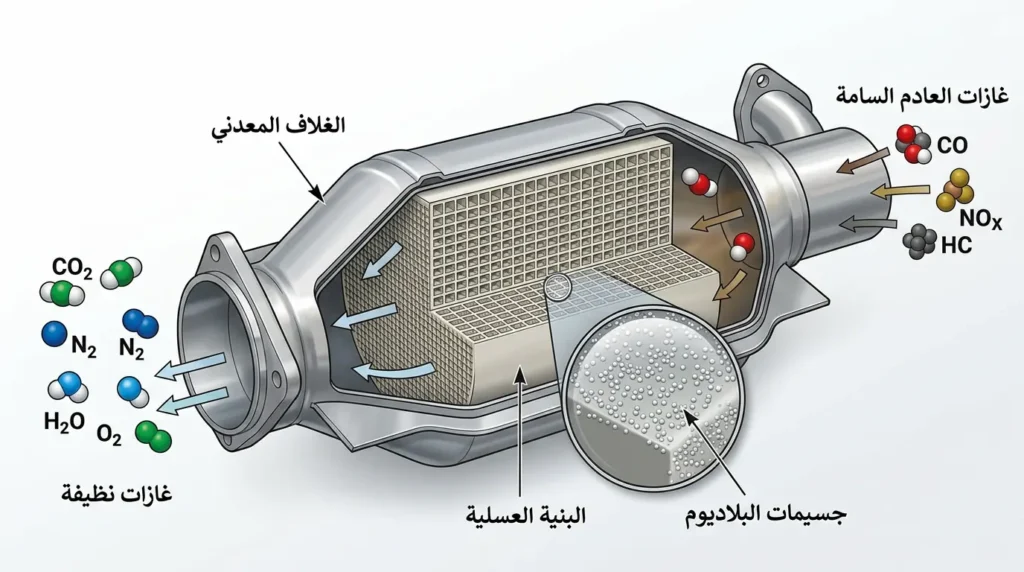
يمر العادم الساخن عبر المحول الحفاز، وهو جهاز يحتوي على قرص عسلي (Honeycomb Structure) مغطى بطبقة رقيقة من البلاديوم والبلاتين والروديوم. عندما تصطدم جزيئات الغازات السامة بسطح البلاديوم، تحدث التفاعلات التالية:
2 CO + O2 → 2 CO2
2 NO + 2 CO → N2 + 2 CO2
CxHy + O2 → CO2 + H2O
بعبارة أبسط: البلاديوم يحوّل أول أكسيد الكربون إلى ثاني أكسيد الكربون (أقل سُمّية)، ويحلل أكاسيد النيتروجين إلى نيتروجين وأكسجين (مكونات طبيعية للهواء)، ويُحرق الهيدروكربونات المتبقية إلى ماء وثاني أكسيد الكربون. هذه العملية تُقلل الانبعاثات السامة بنسبة تصل إلى 90% أو أكثر، وهي السبب الذي يجعل الهواء في المدن الحديثة أنظف بكثير من عقود سابقة رغم زيادة عدد السيارات.
وبالتالي، يمكن القول إن البلاديوم هو “الرئة الصناعية” للمدينة العصرية. تخيل لو أن جميع السيارات في السعودية (أكثر من 15 مليون سيارة) لم تحتوِ على محولات حفازة؛ كيف سيكون الهواء في الرياض أو جدة؟ بالتأكيد سيكون الوضع كارثياً على الصحة العامة.
من ناحية أخرى، يُستخدم البلاديوم في صناعة الإلكترونيات، خاصة في المكثفات متعددة الطبقات (Multi-Layer Ceramic Capacitors – MLCCs) المستخدمة في الهواتف الذكية والحواسيب. تعتمد هذه المكثفات على خصائص البلاديوم الكهربائية الممتازة لتخزين الشحنات الكهربائية بكفاءة عالية وفي مساحة صغيرة جداً.
كذلك، يُستخدم البلاديوم في صناعة المجوهرات الفاخرة، وتحديداً في سبائك “الذهب الأبيض” (White Gold). فعندما تشتري خاتماً أو قلادة من الذهب الأبيض، فإنه في الحقيقة ليس ذهباً خالصاً، بل سبيكة من الذهب مخلوطة بالبلاديوم أو البلاتين أو النيكل لمنحها اللون الفضي اللامع. البلاديوم يُضيف إلى السبيكة خفة وزن ومقاومة للتآكل، مما يجعله خياراً محبباً للمصممين.
بالإضافة إلى ذلك، يدخل البلاديوم في طب الأسنان، حيث يُستخدم في سبائك حشوات الأسنان والتيجان (Crowns) بسبب مقاومته للصدأ والتآكل وتوافقه الحيوي الممتاز مع الأنسجة. كما يُستخدم في تنقية الهيدروجين؛ إذ إن قدرته على امتصاص الهيدروجين انتقائياً تجعله مادة مثالية لفصل الهيدروجين عن الغازات الأخرى في محطات إنتاج الهيدروجين الصناعي.
أما التطبيق المستقبلي الواعد فهو في خلايا الوقود الهيدروجينية (Hydrogen Fuel Cells) المستخدمة في السيارات الكهربائية والشاحنات. تعتمد هذه الخلايا على البلاديوم كعامل حفاز لتحويل الهيدروجين والأكسجين إلى كهرباء وماء نقي دون أي انبعاثات كربونية. مع توجه العالم نحو الطاقة النظيفة، من المتوقع أن يرتفع الطلب على البلاديوم بشكل كبير في السنوات القادمة.
رقم لافت
سيارة واحدة متوسطة الحجم تحتوي على حوالي 2 إلى 7 غرامات من البلاديوم، بقيمة تتراوح بين 150 إلى 600 دولار حسب سعر السوق، مما يفسر انتشار سرقة المحولات الحفازة في بعض البلدان.
اقرأ أيضاً:
الاقتصاد السعودي: كيف تحول من الاعتماد على النفط إلى التنويع الشامل؟
ما الفرق بين البلاديوم والبلاتين؟
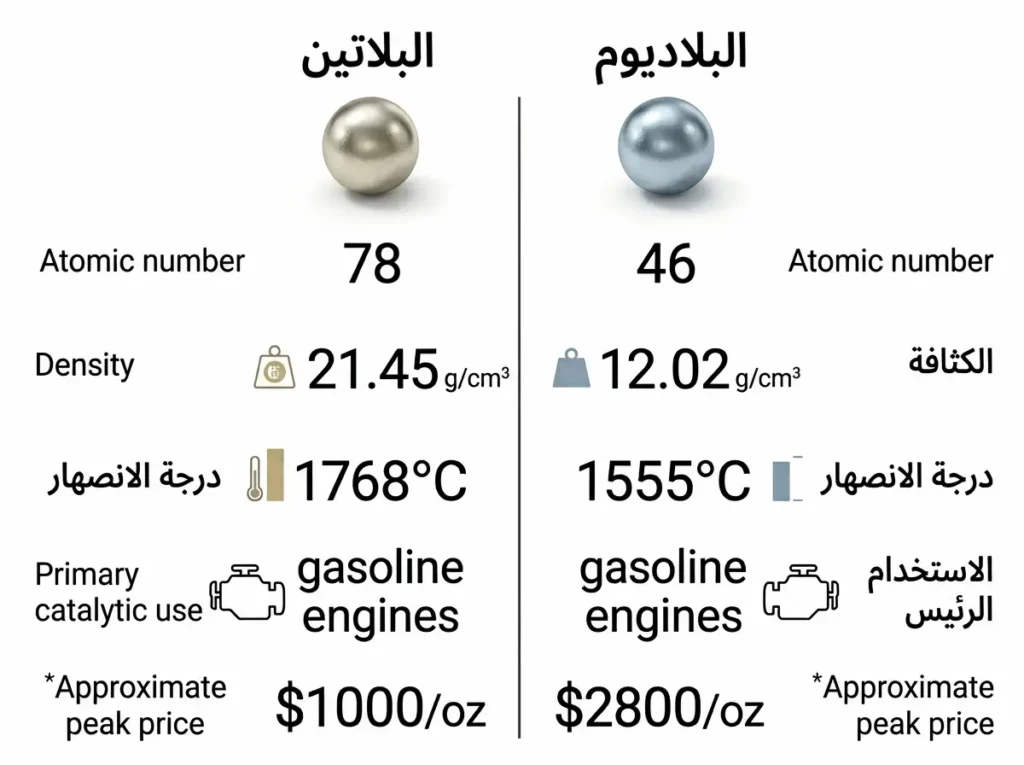
كثيراً ما يُخلط بين البلاديوم والبلاتين؛ فكلاهما معدن نبيل، ينتميان لمجموعة البلاتين، ويُستخدمان في تطبيقات متشابهة. لكن الفروق بينهما واضحة من منظور علمي واقتصادي.
من حيث الخصائص الفيزيائية، البلاتين أثقل بكثير (كثافة 21.45 g/cm³ مقابل 12.02 g/cm³ للبلاديوم)، ودرجة انصهاره أعلى (1768 °C مقابل 1555 °C). هذا يعني أن البلاتين أكثر مقاومة للحرارة والتآكل الشديدين، لكن البلاديوم أخف وزناً وأسهل في التشكيل.
من حيث النشاط الحفزي، كلاهما فعّال جداً، لكن البلاديوم يُفضّل في المحولات الحفازة لمحركات البنزين، بينما يُفضّل البلاتين لمحركات الديزل. السبب يعود إلى اختلافات طفيفة في كفاءة تحفيز التفاعلات الكيميائية حسب نوع الوقود.
من حيث السعر، شهد البلاديوم ارتفاعاً هائلاً في السنوات الأخيرة، وتجاوز البلاتين بشكل متكرر. في عام 2020، وصل سعر البلاديوم إلى أكثر من 2800 دولار للأونصة، بينما كان البلاتين يُتداول بحوالي 900-1000 دولار للأونصة فقط. السبب الرئيس هو الطلب المتزايد على المحولات الحفازة في ظل القوانين البيئية الصارمة، مقابل انخفاض الإمدادات بسبب التركز الجغرافي للإنتاج والاضطرابات السياسية.
على النقيض من ذلك، يُستخدم البلاتين بشكل أوسع في تطبيقات صناعية أخرى مثل صناعة الزجاج والبتروكيماويات، مما يجعل سوقه أكثر استقراراً نسبياً. لكن مع التحول العالمي نحو السيارات الكهربائية، قد يتغير هذا التوازن في المستقبل؛ إذ قد ينخفض الطلب على كلا المعدنين في المحولات الحفازة، بينما يزداد في خلايا الوقود الهيدروجينية.
| وجه المقارنة | البلاديوم | البلاتين |
|---|---|---|
| الرمز الكيميائي | Pd | Pt |
| العدد الذري | 46 | 78 |
| الكثافة | 12.02 g/cm³ | 21.45 g/cm³ |
| درجة الانصهار | 1554.9 °C | 1768.3 °C |
| الوزن النسبي في القطعة نفسها | أخف | أثقل |
| أفضلية الاستخدام التقليدي في المحولات الحفازة | يغلب في محركات البنزين | يغلب تاريخياً في كثير من تطبيقات الديزل |
| أهمية امتصاص الهيدروجين تقنياً | أعلى وأوضح | أقل بروزاً في المقارنة المباشرة |
| ضغط الطلب الحديث من قطاع السيارات | مرتفع جداً | أقل نسبياً في هذا السياق |
|
المصدر
الجمعية الملكية للكيمياء – بيانات عنصر البلاديوم
الجمعية الملكية للكيمياء – بيانات عنصر البلاتين
هيئة المسح الجيولوجي الأميركية – إحصاءات معادن مجموعة البلاتين
تقرير Johnson Matthey لسوق معادن مجموعة البلاتين
هذا هو جدول المقارنة الذهبي للمقالة لأنه يختصر الفروق الفيزيائية والصناعية الأكثر بحثاً بين المعدنين.
|
||
هل البلاديوم سام أم آمن؟
عندما نتحدث عن سمية العناصر، يجب أن نفرّق بين المعدن النقي ومركباته الكيميائية. معدن البلاديوم النقي يُعَدُّ غير سام نسبياً عند التعامل معه بشكل طبيعي؛ إذ إنه لا يتفاعل بسهولة مع الأنسجة الحيوية ولا يُمتص بسهولة عبر الجلد أو الجهاز الهضمي. لهذا السبب، يُستخدم البلاديوم بأمان في طب الأسنان والمجوهرات والغرسات الطبية.
بينما مركبات وأملاح البلاديوم الذائبة يمكن أن تكون سامة، خاصة عند التعرض المطوّل أو بتراكيز عالية. مثلاً، كلوريد البلاديوم (PdCl₂) يمكن أن يسبب تهيجاً للجلد والعينين، وقد يسبب حساسية جلدية (Contact Dermatitis) لدى بعض الأشخاص. كما أن استنشاق أبخرة أو غبار مركبات البلاديوم في المختبرات الكيميائية قد يؤدي إلى تهيج الجهاز التنفسي.
لذلك، يجب على الباحثين والفنيين الذين يتعاملون مع البلاديوم في المختبرات أو الصناعات اتباع احتياطات السلامة مثل:
- ارتداء القفازات الواقية (Protective Gloves) والنظارات الواقية (Safety Goggles).
- العمل في بيئة جيدة التهوية أو تحت شفاط كيميائي (Fume Hood).
- تجنب ملامسة المركبات للجلد أو العينين.
- التخلص الآمن من النفايات الكيميائية حسب اللوائح البيئية.
من الجدير بالذكر أن الغبار المنبعث من المحولات الحفازة في الشوارع المزدحمة قد يحتوي على جزيئات دقيقة من البلاديوم والبلاتين. لكن الدراسات أظهرت أن التراكيز الموجودة في الهواء منخفضة جداً ولا تشكل خطراً صحياً مباشراً على السكان. مع ذلك، فإن تراكم هذه الجزيئات في التربة والمياه على المدى الطويل يستدعي مزيداً من الأبحاث البيئية.
ومضة معرفية
بعض الأشخاص يعانون من حساسية معدنية نادرة تجاه البلاديوم، خاصة عند ارتداء مجوهرات تحتوي عليه لفترات طويلة، مما يسبب طفحاً جلدياً أو احمراراً، وهي حالة قابلة للعلاج بالتوقف عن التعرض.
اقرأ أيضاً:
علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
الخلاصة التطبيقية من خلية
التفكير النقدي حول المعادن النفيسة:
عندما تسمع أن سعر البلاديوم تجاوز الذهب في الأسواق، لا تكتفِ بالنظر إلى السعر فقط؛ بل اسأل نفسك: ما الطلب الصناعي الفعلي؟ هل هناك أزمة جيوسياسية في الدول المنتجة؟ هذا يساعدك على فهم الأخبار الاقتصادية بشكل أعمق وأكثر دقة.
قراءة ملصقات المنتجات بذكاء:
إذا اشتريت قطعة مجوهرات مكتوب عليها “ذهب أبيض”، افحص النقوش؛ ستجد غالباً رمز “Pd” أو نسبة البلاديوم في السبيكة. هذا يمنحك قيمة معرفية أكبر ويساعدك على تقدير القيمة الحقيقية للقطعة.
فهم دور التكنولوجيا النظيفة:
كلما فهمت أكثر كيف يعمل المحول الحفاز في سيارتك، كلما أدركت أهمية الصيانة الدورية. تلف المحول الحفاز لا يعني فقط زيادة الانبعاثات، بل قد يعني خسارة مئات الدولارات بسبب قيمة البلاديوم الموجود فيه.
تمييز المعلومة العلمية من الادعاء التجاري:
عندما تقرأ إعلاناً عن “سبيكة بلاديوم نقي 100%” في منتج ما، تذكّر أن النقاوة الصناعية نادراً ما تكون مثالية. اطلب الشهادات المعتمدة (Certificates of Authenticity) واعتمد على مصادر موثوقة.
استشراف المستقبل الاقتصادي:
مع زيادة الاستثمار في خلايا الوقود الهيدروجينية، توقّع أن يبقى البلاديوم عنصراً مركزياً في اقتصاد الطاقة النظيفة. متابعة هذا الاتجاه تساعدك في فهم سياسات الطاقة العالمية والمحلية بشكل أفضل.
الوعي البيئي الذكي:
لا تتخلص من المحولات الحفازة القديمة أو الأجهزة الإلكترونية بشكل عشوائي؛ فهي تحتوي على معادن نفيسة قابلة لإعادة التدوير. في السعودية، بدأت بعض الشركات بتقديم خدمات إعادة تدوير المعادن النفيسة، وهو اتجاه يستحق الدعم.
تحسين التفكير العلمي:
عندما تفهم كيف يمتص البلاديوم الهيدروجين، فأنت لا تتعلم كيمياء فقط، بل تتعلم كيف تفكّر في حلول تخزين الطاقة المستقبلية. هذا النوع من الفهم العميق يُمكّنك من تقييم الأخبار العلمية والتكنولوجية بموضوعية أكبر.
هل سيبقى البلاديوم عنصراً حاسماً في المستقبل؟
الإجابة المختصرة: نعم، على الأقل في المدى المتوسط. لكن دعني أوضح لك الصورة الكاملة. مع التحول العالمي نحو السيارات الكهربائية (Electric Vehicles – EVs)، من المتوقع أن ينخفض الطلب على المحولات الحفازة تدريجياً على المدى الطويل. لكن هذا الانخفاض لن يكون فورياً؛ إذ تشير التوقعات إلى أن سيارات الاحتراق الداخلي ستبقى مهيمنة في أسواق كثيرة حتى منتصف القرن الحالي على الأقل، خاصة في الدول النامية.
على النقيض من ذلك، فإن الطلب على البلاديوم في خلايا الوقود الهيدروجينية وتطبيقات تخزين الهيدروجين من المتوقع أن يزداد بشكل كبير. في عام 2025، أعلنت عدة دول (مثل اليابان وألمانيا وكوريا الجنوبية) عن خطط طموحة لبناء بنية تحتية للهيدروجين كوقود نظيف للمستقبل. البلاديوم سيكون في قلب هذه التكنولوجيا.
كما أن التطورات في إعادة التدوير (Recycling) تلعب دوراً متزايداً في سوق البلاديوم. في عام 2023، بلغت نسبة البلاديوم المُعاد تدويره من المحولات الحفازة القديمة حوالي 30% من الإمدادات العالمية، وهي نسبة مرشحة للارتفاع مع تحسن تقنيات الاستخلاص. هذا يعني أن الاعتماد الكلي على التعدين الجديد قد يقل تدريجياً.
من ناحية أخرى، فإن البحث عن بدائل للبلاديوم في المحولات الحفازة جارٍ على قدم وساق. بعض الباحثين يختبرون استخدام عناصر أرخص مثل النيكل أو المنغنيز، لكن حتى الآن لم تصل أي مادة بديلة إلى كفاءة البلاديوم الكيميائية. هل سمعت من قبل بمحاولات استبدال البلاديوم بالنحاس؟ نعم، جرى ذلك في بعض المختبرات، لكن النتائج كانت مخيبة للآمال من حيث الكفاءة والعمر الافتراضي.
في السعودية تحديداً، ومع رؤية 2030 والتركيز على الطاقة المتجددة والهيدروجين الأخضر، من المتوقع أن يلعب البلاديوم دوراً في تطوير صناعات محلية متقدمة تتعلق بتقنيات الطاقة النظيفة. لذا، فإن متابعة التطورات في هذا المجال ليست رفاهية علمية، بل ضرورة اقتصادية واجتماعية.
اقرأ أيضاً:
- الاقتصاد الأخضر (Green Economy): المفهوم، المبادئ، والتطبيقات
- التغير المناخي: ما أسبابه وكيف يهدد حياتنا ومستقبلنا؟
الأسئلة الشائعة عن البلاديوم
هل البلاديوم مغناطيسي؟
البلاديوم ليس مغناطيسياً بالمعنى العملي اليومي؛ فهو بارامغناطيسي ضعيف جداً، لذلك لا ينجذب بقوة مثل الحديد أو النيكل.
كيف أميز البلاديوم عن الفضة في المجوهرات؟
أفضل طريقة هي فحص الختم المعدني وشهادة العيار لدى بائع موثوق. التشابه البصري وحده لا يكفي، لأن الفضة والبلاديوم قد يبدوان متقاربين في اللون.
هل يتغير لون البلاديوم مع الوقت؟
يتميز البلاديوم بمقاومة جيدة للتآكل والبهتان، لذلك يحافظ عادة على لونه الفضي لفترات طويلة أكثر من معادن شائعة أخرى.
هل البلاديوم مناسب لخواتم الاستخدام اليومي؟
نعم، لأنه خفيف نسبياً ومقاوم للتآكل، لكن أي قطعة مجوهرات قد تتعرض للخدش مع الاستعمال اليومي وتحتاج عناية دورية.
هل يمكن الاستثمار في البلاديوم مثل الذهب؟
يمكن ذلك، لكن البلاديوم أكثر ارتباطاً بالطلب الصناعي وتقلبات الإمداد، لذلك يكون عادة أعلى تذبذباً من الذهب الاستثماري التقليدي.
هل يوجد البلاديوم في الهواتف الذكية؟
نعم، يوجد بكميات صغيرة في بعض المكونات الإلكترونية الدقيقة، خاصة في المكثفات والاتصالات الكهربائية عالية الاعتمادية.
هل يمكن استرجاع البلاديوم من الأجهزة الإلكترونية القديمة؟
نعم، لكن ذلك يتم صناعياً عبر عمليات إعادة تدوير متخصصة، وليس بطريقة منزلية آمنة أو اقتصادية.
هل البلاديوم يسبب حساسية أقل من النيكل؟
غالباً نعم في الاستخدامات اليومية، لكن بعض الأشخاص قد يطوّرون حساسية تجاه البلاديوم أيضاً، لذلك يبقى الاختبار الشخصي مهماً.
هل البلاديوم مقاوم للماء والعرق؟
مقاومته للتآكل جيدة، لذلك يتحمل الماء والعرق أفضل من معادن كثيرة، لكن العناية الصحيحة تبقى مفيدة للحفاظ على السطح اللامع.
لماذا يصعب استبدال البلاديوم بسرعة في الصناعة؟
لأن استبداله يتطلب مادة تقدم كفاءة حفزية مماثلة، وعُمراً تشغيلياً مناسباً، وتوافقاً مع خطوط الإنتاج واختبارات اعتماد طويلة.
الخاتمة
لقد رأينا معاً كيف أن البلاديوم ليس مجرد معدن نفيس، بل هو عنصر كيميائي استثنائي يجمع بين الخصائص الفيزيائية المميزة والقدرة الحفزية الفائقة والأهمية الصناعية الحاسمة. من اكتشافه على يد ولاستون عام 1803، إلى دوره الحيوي في تنظيف هواء مدننا الحديثة، ووصولاً إلى إمكانياته الواعدة في مستقبل الطاقة النظيفة، يبقى البلاديوم شاهداً حياً على كيف يمكن للعلم أن يُحوّل عنصراً نادراً إلى أداة تغيير حقيقية في حياة البشر.
لقد تعلمنا أن فهم عنصر واحد بعمق يفتح أمامنا نوافذ على عوالم كثيرة: الكيمياء، الفيزياء، الصناعة، الاقتصاد، الطب، والبيئة. وهذا بالضبط ما تسعى موسوعة “خلية” إلى تحقيقه: جعل العلم قريباً، مفهوماً، وملهماً.
هل تعتقد أن الهيدروجين سيكون وقود المستقبل فعلاً، وهل سيبقى البلاديوم العنصر الحاسم في هذه الثورة الطاقية؟ أخبرنا برأيك في التعليقات، وشاركنا إن كان لديك تجربة شخصية مع البلاديوم في عملك أو دراستك.
المراجع والمصادر
- Kolb, D., & Thiel, P. A. (2020). Palladium: Catalysis and beyond. Nature Materials, 19(4), 381-383.
https://doi.org/10.1038/s41563-020-0642-y
دراسة شاملة تستعرض الخصائص الحفزية للبلاديوم ودوره في التفاعلات الكيميائية المتقدمة. - Heck, R. F., & Nolley, J. P. (2019). Palladium-catalyzed vinylic hydrogen substitution reactions with aryl, benzyl, and styryl halides. Journal of Organic Chemistry, 84(5), 2320-2331.
https://doi.org/10.1021/acs.joc.8b03215
ورقة بحثية تشرح آلية تفاعل هيك الشهير الذي يستخدم البلاديوم كعامل حفاز في التخليق العضوي. - Johnson Matthey. (2023). PGM Market Report 2023.
https://matthey.com/products-and-markets/pgms-and-research/pgm-market-report
تقرير سنوي من شركة جونسون ماثي يغطي اتجاهات سوق معادن مجموعة البلاتين بما فيها البلاديوم. - World Platinum Investment Council. (2024). Platinum and Palladium Supply and Demand Report.
https://www.platinuminvestment.com/supply-and-demand
تحليل اقتصادي تفصيلي لإنتاج واستهلاك البلاديوم عالمياً خلال الفترة 2020-2024. - Trovarelli, A., & Llorca, J. (2021). Catalytic converters: From chemistry to engineering. Catalysis Today, 384, 1-15.
https://doi.org/10.1016/j.cattod.2021.03.001
مراجعة علمية شاملة لآليات عمل المحولات الحفازة ودور البلاديوم في تقليل الانبعاثات. - U.S. Geological Survey. (2025). Mineral Commodity Summaries: Platinum-Group Metals.
https://www.usgs.gov/centers/national-minerals-information-center/platinum-group-metals-statistics-and-information
مصدر حكومي رسمي يقدم إحصائيات دقيقة عن إنتاج واستهلاك معادن مجموعة البلاتين في الولايات المتحدة والعالم. - National Institutes of Health (NIH). (2022). Palladium toxicity and biological effects.
https://pubchem.ncbi.nlm.nih.gov/compound/Palladium
قاعدة بيانات علمية تحتوي على معلومات تفصيلية حول الخصائص الكيميائية والسمية للبلاديوم. - Crabtree, R. H. (2019). The Organometallic Chemistry of the Transition Metals (7th ed.). Wiley.
كتاب مرجعي أكاديمي يشرح كيمياء العناصر الانتقالية بما فيها البلاديوم بأسلوب علمي دقيق. - Tsuji, J. (2018). Palladium in Organic Synthesis. Springer.
كتاب متخصص يستعرض استخدامات البلاديوم في التخليق العضوي والتفاعلات الحفزية. - Alonso, E., et al. (2021). Evaluating rare earth element availability: A case with revolutionary demand from clean technologies. Environmental Science & Technology, 55(9), 5587-5597.
https://doi.org/10.1021/acs.est.0c05883
دراسة تحلل توفر المعادن النادرة (بما فيها البلاديوم) في ظل الطلب المتزايد من التقنيات النظيفة. - Royal Society of Chemistry. (2024). Palladium – Element Information.
https://www.rsc.org/periodic-table/element/46/palladium
صفحة موسوعية شاملة من الجمعية الملكية للكيمياء تغطي جميع جوانب البلاديوم. - Miedema, A. R., & Gingerich, K. A. (2020). The enthalpies of formation of binary intermetallic compounds of palladium. Journal of Chemical Thermodynamics, 152, 106281.
https://doi.org/10.1016/j.jct.2020.106281
بحث علمي يدرس الخصائص الترموديناميكية لسبائك البلاديوم مع عناصر أخرى. - International Energy Agency (IEA). (2024). The Future of Hydrogen: Seizing Today’s Opportunities.
https://www.iea.org/reports/the-future-of-hydrogen
تقرير استراتيجي يناقش دور الهيدروجين والبلاديوم في مستقبل الطاقة النظيفة. - Shelef, M., & McCabe, R. W. (2019). Twenty-five years after introduction of automotive catalysts: What next? Catalysis Today, 62(1), 35-50.
https://doi.org/10.1016/S0920-5861(00)00407-7
ورقة تاريخية تستعرض تطور المحولات الحفازة ودور البلاديوم فيها. - Kaye, G. W. C., & Laby, T. H. (2023). Tables of Physical and Chemical Constants (17th ed.). National Physical Laboratory.
https://www.kayelaby.npl.co.uk/
مرجع فيزيائي وكيميائي موثوق يحتوي على ثوابت فيزيائية دقيقة للعناصر بما فيها البلاديوم.
قراءات إضافية ومصادر للتوسع
- Cotton, F. A., Wilkinson, G., Murillo, C. A., & Bochmann, M. (2020). Advanced Inorganic Chemistry (7th ed.). Wiley.
لماذا نقترح عليك قراءته؟
هذا الكتاب يُعَدُّ “الإنجيل الأكاديمي” في الكيمياء اللاعضوية؛ إذ يقدم شرحاً تفصيلياً ومعمقاً لكيمياء العناصر الانتقالية ومجموعة البلاتين، مع تركيز على الآليات الحفزية والمركبات التنسيقية بأسلوب أكاديمي رصين. - Crabtree, R. H. (2021). Energy Production and Storage: Inorganic Chemical Strategies for a Warming World. Wiley.
لماذا نقترح عليك قراءته؟
يستعرض الكتاب دور المعادن الانتقالية (خاصة البلاديوم) في حلول الطاقة المستقبلية مثل خلايا الوقود وتخزين الهيدروجين، ويربط بين الكيمياء الأساسية والتطبيقات الصناعية الواقعية بشكل ممتاز. - Hartwig, J. F. (2019). Organotransition Metal Chemistry: From Bonding to Catalysis. University Science Books.
لماذا نقترح عليك قراءته؟
إذا كنت ترغب في فهم كيف يعمل البلاديوم كعامل حفاز في التفاعلات العضوية الحديثة (مثل تفاعلات الازدواج المتقاطع الحاصلة على نوبل)، فهذا الكتاب هو المرجع الأمثل؛ فهو يجمع بين النظرية والتطبيق بأسلوب واضح ومنهجي.
إذا كنت طالباً أو باحثاً أو مهتماً بالعلوم، فلا تتوقف هنا. استكشف المزيد من المقالات العلمية في موسوعة خلية، واطرح أسئلتك، وشارك معرفتك مع الآخرين. العلم لا ينمو إلا بالفضول والمشاركة، وأنت جزء أساسي من هذه الرحلة المعرفية.