ما هي البروتيوميات: وكيف تُحدث ثورة في الطب الحديث؟
كيف يكشف تحليل البروتينات أسرار الأمراض قبل ظهور أعراضها؟

تعريف مختصر
البروتيوميات (Proteomics) هي فرع من العلوم الحيوية يختص بدراسة مجموع البروتينات الموجودة في الخلية أو النسيج أو الكائن الحي في وقت محدد. يشمل هذا العلم تحليل بنية البروتينات ووظائفها وتفاعلاتها وتعديلاتها بعد الترجمة. تُستخدم تقنيات متقدمة كالطيف الكتلي (Mass Spectrometry) للكشف عن آلاف البروتينات دفعة واحدة. تُعَدُّ البروتيوميات أداة محورية في تشخيص الأمراض واكتشاف الأدوية والطب الشخصي.
هل شعرت يوماً بالإحباط وأنت تقرأ عن الجينات والحمض النووي دون أن تفهم لماذا يُصاب شخصان يحملان الجينات ذاتها بأمراض مختلفة تماماً؟ أنت لست وحدك في هذه الحيرة. الحقيقة أن الجينات ليست نهاية القصة، بل هي مجرد البداية. البروتينات هي التي تنفذ الأوامر فعلياً داخل جسمك؛ إذ تبني الأنسجة وتهضم الطعام وتحارب العدوى. لقد جاءت البروتيوميات لتملأ هذه الفجوة المعرفية الضخمة. في هذا المقال ستكتشف كيف يستطيع العلماء اليوم قراءة “لغة البروتينات” لتشخيص السرطان قبل سنوات من ظهوره، ولتصميم أدوية مخصصة لجسمك أنت تحديداً.
ما الفرق بين البروتيوميات والجينوميات؟
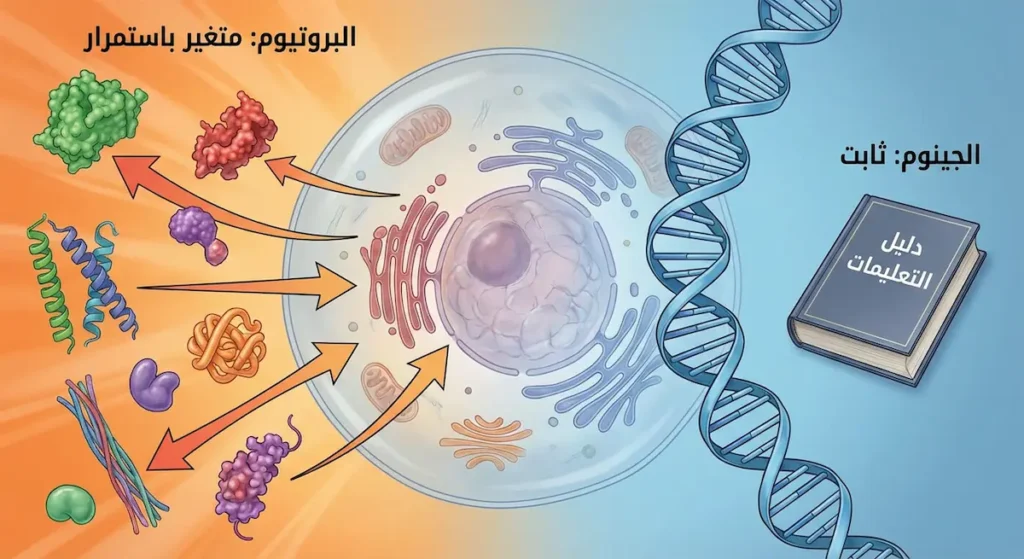
كثيراً ما يخلط المبتدئون بين هذين العلمين. الجينوميات (Genomics) تدرس الجينوم، أي مجموع الجينات في الكائن الحي. لكن الجينات مجرد “وصفات” مكتوبة بلغة الحمض النووي. البروتينات هي “الأطباق” الفعلية التي تُطهى من هذه الوصفات.
فكر في الأمر هكذا: لو كان جسمك مصنعاً، فإن الجينوم هو دليل التعليمات المخزن في الأرشيف. أما البروتيوم فهو العمال والآلات التي تعمل فعلياً على أرض المصنع. وإن أردت معرفة ما يحدث في المصنع الآن، فعليك مراقبة العمال لا قراءة الأرشيف فحسب.
الجينوم ثابت نسبياً طوال حياة الإنسان. على النقيض من ذلك، البروتيوم يتغير كل ثانية استجابةً للطعام والدواء والمرض والضغط النفسي وحتى الطقس. هذه الديناميكية تجعل البروتيوميات نافذة حية على صحة الجسم.
معلومة سريعة: يحتوي الجينوم البشري على نحو 20,000 جين فقط، لكن هذه الجينات تُنتج أكثر من مليون بروتين مختلف بسبب عمليات التعديل والتقطيع البديل (Alternative Splicing)!
كيف نشأ علم البروتيوميات وما محطاته التاريخية؟
لم تظهر البروتيوميات من فراغ. جذورها تعود إلى منتصف القرن العشرين حين بدأ العلماء دراسة البروتينات الفردية. لكن المصطلح ذاته لم يُصَغ إلا عام 1994 على يد الباحث الأسترالي مارك ويلكينز (Marc Wilkins).
في الخمسينيات والستينيات، طور العلماء تقنية الفصل الكهربائي (Electrophoresis) لفصل البروتينات حسب حجمها وشحنتها. كانت هذه التقنية بدائية لكنها فتحت الباب أمام فهم تنوع البروتينات. ثم جاءت السبعينيات بتقنية الفصل الكهربائي ثنائي البُعد (2D Gel Electrophoresis) التي سمحت بفصل مئات البروتينات في تجربة واحدة.
المنعطف الحقيقي حدث في أواخر الثمانينيات مع تطوير تقنيات الطيف الكتلي الملائمة للجزيئات البيولوجية الكبيرة. فقد حصل جون فين (John Fenn) وكويتشي تاناكا (Koichi Tanaka) على جائزة نوبل في الكيمياء عام 2002 تقديراً لإسهاماتهم في هذا المجال. بعد إتمام مشروع الجينوم البشري عام 2003، انتقل اهتمام المجتمع العلمي بقوة نحو البروتيوميات؛ إذ أدرك الباحثون أن معرفة الجينات وحدها لا تكفي لفهم الأمراض.
اقرأ أيضاً: علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
ما هو البروتيوم وكيف يختلف عن الجينوم؟
البروتيوم (Proteome) مصطلح يجمع بين كلمتي “بروتين” و”جينوم”. يُشير إلى المجموعة الكاملة من البروتينات التي تُنتجها خلية أو نسيج أو كائن حي في لحظة زمنية معينة وتحت ظروف محددة.
الجينوم كتاب مكتوب بحبر ثابت. البروتيوم أشبه بشاشة تتغير صورتها باستمرار. خلايا الكبد والدماغ والعضلات تحمل الجينوم ذاته، لكن بروتيومها مختلف تماماً. بل إن بروتيوم الخلية الواحدة يتغير حين تجوع أو تمرض أو تنقسم.
هذا التعقيد يمثل تحدياً هائلاً للباحثين. كما أنه يمثل فرصة ذهبية للطب؛ إذ يمكن رصد التغيرات البروتينية المرتبطة بالمرض قبل ظهور الأعراض السريرية بسنوات أحياناً.
حقيقة علمية: بروتيوم البلازما البشرية (بلازما الدم) يحتوي على أكثر من 10,000 بروتين مختلف، وتتراوح تراكيزها بفارق يصل إلى 10 مراتب عشرية (10 orders of magnitude)، مما يجعل تحليلها تحدياً تقنياً استثنائياً.
ما التقنيات المستخدمة في البروتيوميات؟
تعتمد البروتيوميات على ترسانة من التقنيات المتطورة. كل تقنية لها نقاط قوة وضعف، والباحثون عادة يجمعون بين عدة تقنيات للحصول على صورة شاملة.
الطيف الكتلي (Mass Spectrometry – MS)
يُعَدُّ الطيف الكتلي العمود الفقري للبروتيوميات الحديثة. تقوم هذه التقنية بتأيين جزيئات البروتين (تحويلها إلى أيونات مشحونة)، ثم قياس نسبة كتلتها إلى شحنتها (m/z). النتيجة هي “بصمة كتلية” فريدة لكل بروتين.
أشهر أنواع الطيف الكتلي المستخدمة تشمل: مطياف الكتلة الترادفي (Tandem MS أو MS/MS)، ومطياف وقت الطيران (Time-of-Flight أو TOF)، ومطياف المصيدة الأيونية (Ion Trap). التطورات الأخيرة في 2023 و2024 رفعت حساسية الأجهزة لدرجة الكشف عن بروتينات بتركيز أجزاء من المليار (nanomolar).

الفصل الكهربائي ثنائي البُعد (2D Gel Electrophoresis)
تقنية كلاسيكية لكنها لا تزال مفيدة. تفصل البروتينات في البُعد الأول حسب نقطة تساوي الكهربية (Isoelectric Point)، وفي البُعد الثاني حسب الكتلة الجزيئية. النتيجة خريطة ثنائية الأبعاد تظهر فيها البروتينات كنقاط منفصلة.
الكروماتوغرافيا السائلة (Liquid Chromatography – LC)
تُستخدم لفصل خليط البروتينات أو الببتيدات قبل إدخالها في الطيف الكتلي. الجمع بين الكروماتوغرافيا السائلة والطيف الكتلي (LC-MS) أصبح المعيار الذهبي في المختبرات الحديثة.
مصفوفات البروتين (Protein Microarrays)
تسمح بدراسة تفاعلات آلاف البروتينات في تجربة واحدة. تُستخدم خاصة في دراسة تفاعلات البروتين-البروتين وفي الكشف عن الأجسام المضادة.
لمحة تاريخية: أول جهاز طيف كتلي بُني عام 1912 على يد الفيزيائي البريطاني ج. ج. طومسون (J.J. Thomson)، لكن الأمر استغرق 80 عاماً حتى أصبحت التقنية قادرة على تحليل البروتينات الكبيرة!
اقرأ أيضاً: المجهر (Microscope): الاختراع، الأنواع، ودوره في العلم
ما أنواع البروتيوميات المختلفة؟
لقد تفرعت البروتيوميات إلى تخصصات فرعية، كل منها يركز على جانب معين من عالم البروتينات.
البروتيوميات التعبيرية (Expression Proteomics)
تدرس مستويات التعبير البروتيني، أي كمية كل بروتين في عينة معينة. تُستخدم للمقارنة بين الخلايا السليمة والمريضة، أو بين خلايا قبل العلاج وبعده. هذا النوع مهم جداً في أبحاث السرطان؛ إذ يكشف البروتينات التي يرتفع أو ينخفض تركيزها في الأورام.
البروتيوميات الهيكلية (Structural Proteomics)
تركز على تحديد البنية ثلاثية الأبعاد للبروتينات. فهم شكل البروتين ضروري لفهم وظيفته ولتصميم أدوية ترتبط به بدقة. تقنيات مثل الأشعة السينية البلورية (X-ray Crystallography) والمجهر الإلكتروني بالتبريد (Cryo-EM) أحدثت ثورة في هذا المجال.
برنامج ألفا فولد (AlphaFold) الذي طورته شركة ديب مايند (DeepMind) عام 2020 وتحديثاته في 2023 و2024 غيّر قواعد اللعبة تماماً؛ إذ يستطيع التنبؤ ببنية البروتينات بدقة تقارب التجربة المعملية.
البروتيوميات الوظيفية (Functional Proteomics)
تدرس وظائف البروتينات وتفاعلاتها مع بعضها ومع الجزيئات الأخرى. فهم شبكات التفاعل البروتيني (Protein Interaction Networks) يكشف كيف تعمل الخلية كنظام متكامل.

البروتيوميات السريرية (Clinical Proteomics)
تُطبق أدوات البروتيوميات في السياق الطبي. تشمل اكتشاف المؤشرات الحيوية (Biomarkers) للتشخيص والمتابعة والتنبؤ باستجابة المريض للعلاج.
كيف تُطبق البروتيوميات في الطب الحديث؟
مثال تطبيقي: اكتشاف سرطان المبيض مبكراً
تخيلي امرأة في الخامسة والأربعين تُدعى سميرة. لا تشكو من أي أعراض، لكنها قلقة لأن والدتها توفيت بسرطان المبيض. في الماضي، لم يكن أمام الأطباء سوى الانتظار حتى ظهور الأعراض أو إجراء فحوصات مكلفة وغير دقيقة.
اليوم، يمكن لمختبرات متخصصة تحليل بروتيوم بلازما دم سميرة. يبحث الباحثون عن نمط معين من البروتينات يُسمى “التوقيع البروتيومي” (Proteomic Signature). وجدت دراسات حديثة أن مجموعة من ستة بروتينات يمكنها الكشف عن سرطان المبيض في مراحله المبكرة بدقة تفوق 90%.
تُسحب عينة دم بسيطة من سميرة. تُفصل البروتينات باستخدام الكروماتوغرافيا السائلة، ثم تُحلل بالطيف الكتلي. الكمبيوتر يقارن “توقيعها البروتيومي” بقاعدة بيانات ضخمة. النتيجة تظهر خلال أيام: إما اطمئنان أو تنبيه مبكر يسمح بتدخل علاجي قبل أن يتحول الورم إلى مرحلة متقدمة.
هذا ليس خيالاً علمياً. مختبرات في أوروبا وأمريكا تُجري هذه الفحوصات فعلياً، وإن كانت التكلفة لا تزال مرتفعة نسبياً.
رقم مذهل: في عام 2024، نجح فريق بحثي دولي في تحديد أكثر من 12,000 بروتين في عينة دم بشرية واحدة باستخدام تقنيات البروتيوميات الحديثة، مقارنة بأقل من 1,000 بروتين قبل عقد واحد فقط!
اقرأ أيضاً: علاج السرطان: التقنيات الحديثة والابتكارات المستقبلية
ما دور البروتيوميات في اكتشاف الأدوية؟
صناعة الأدوية تواجه أزمة إنتاجية حقيقية. تكلفة تطوير دواء جديد تتجاوز 2 مليار دولار، ونسبة الفشل في المراحل السريرية تقارب 90%. البروتيوميات تقدم حلولاً واعدة لهذه المعضلة.
أولاً، تساعد في تحديد “الأهداف الدوائية” (Drug Targets). معظم الأدوية تعمل عبر الارتباط ببروتينات معينة في الجسم. فهم البروتيوم يكشف أي البروتينات تتغير في المرض، وبالتالي أيها يمكن استهدافه علاجياً.
ثانياً، تُستخدم في دراسة “الحركية الدوائية” (Pharmacokinetics). كيف يتفاعل الدواء مع بروتينات الجسم؟ هل يرتبط ببروتينات غير مستهدفة مسبباً آثاراً جانبية؟ البروتيوميات تجيب عن هذه الأسئلة.
ثالثاً، تدخل في مجال “الطب الشخصي” (Personalized Medicine). لماذا يستجيب مريض لدواء معين بينما لا يستجيب آخر؟ غالباً لأن بروتيوم كل منهما مختلف. تحليل بروتيوم المريض قبل العلاج يمكن أن يتنبأ باستجابته ويوجه اختيار الدواء الأمثل.
شركات أدوية كبرى مثل فايزر (Pfizer) ونوفارتس (Novartis) استثمرت مئات الملايين في مختبرات البروتيوميات خلال السنوات الأخيرة. الاتجاه واضح: مستقبل تطوير الأدوية مرتبط بهذا العلم.
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
كيف تُسهم البروتيوميات في فهم السرطان؟
السرطان ليس مرضاً واحداً، بل مئات الأمراض المختلفة. حتى الورم الواحد يحتوي على خلايا متباينة جينياً وبروتينياً. هذا التنوع يُعرف بـ”التباين الورمي” (Tumor Heterogeneity)، وهو سبب رئيس لفشل العلاجات ومقاومة الأدوية.
البروتيوميات تكشف هذا التنوع بتفاصيل غير مسبوقة. في 2023، نشر فريق من معهد برود (Broad Institute) دراسة حللت بروتيوم أكثر من 1,000 ورم بشري. وجدوا “توقيعات بروتينية” مميزة لكل نوع فرعي من السرطان، بعضها لم يكن معروفاً من قبل.
من جهة ثانية، تُستخدم البروتيوميات في مراقبة استجابة المريض للعلاج. بدلاً من انتظار أشهر لرؤية تقلص الورم في الأشعة، يمكن رصد تغيرات بروتينية في الدم خلال أسابيع تشير إلى فعالية العلاج أو فشله.
مشروع “أطلس بروتيوم السرطان” (Cancer Proteome Atlas) الذي أُطلق عام 2021 يهدف إلى رسم خريطة بروتينية شاملة لجميع أنواع السرطان. البيانات متاحة للباحثين حول العالم، مما يسرّع الاكتشافات.
هل تعلم؟ بعض أنواع السرطان تُفرز بروتينات معينة في الدم قبل سنوات من تشكل ورم يمكن رؤيته بالأشعة. البروتيوميات قادرة نظرياً على كشف هذه البروتينات، مما يفتح باب “الكشف المبكر جداً” (Very Early Detection).
ما التحديات التي تواجه علم البروتيوميات؟
رغم التقدم الهائل، يواجه هذا العلم عقبات كبيرة. فهم هذه التحديات ضروري لتقدير إنجازات الباحثين وتوقع مستقبل المجال.
تعقيد البروتيوم
كما ذكرنا، البروتيوم أكثر تعقيداً من الجينوم بمراتب. البروتين الواحد قد يوجد بعشرات الأشكال المختلفة بسبب التعديلات بعد الترجمة (Post-Translational Modifications) مثل الفسفرة (Phosphorylation) والغلكزة (Glycosylation). تتبع كل هذه الأشكال يتطلب تقنيات بالغة الحساسية.
النطاق الديناميكي الواسع
في بلازما الدم، يوجد بروتين الألبومين بتركيز هائل، بينما توجد بروتينات أخرى مهمة طبياً بتراكيز ضئيلة جداً. هذا الفارق الهائل يشبه محاولة سماع همسة في حفل روك صاخب. التقنيات الحالية تتحسن، لكن المشكلة لم تُحل كلياً.
التكلفة والوقت
أجهزة الطيف الكتلي المتقدمة تكلف مئات الآلاف وأحياناً ملايين الدولارات. تشغيلها يتطلب خبراء مدربين. تحليل البيانات الضخمة الناتجة يحتاج برمجيات متخصصة وقدرات حاسوبية عالية.
التوحيد القياسي
تختلف البروتوكولات بين المختبرات، مما يصعّب مقارنة النتائج. جهود توحيد المعايير جارية، لكن الطريق لا يزال طويلاً.
تخزين البيانات وتحليلها
تجربة بروتيومية واحدة قد تُنتج تيرابايتات من البيانات. تخزين هذه البيانات وتحليلها واستخراج معلومات مفيدة منها يتطلب أدوات المعلوماتية الحيوية (Bioinformatics) والذكاء الاصطناعي.
اقرأ أيضاً: البيانات الضخمة: كيف يحول الإحصاء ملايين الملاحظات إلى معرفة قابلة للتطبيق؟
ما أبرز الاتجاهات البحثية الحديثة في البروتيوميات؟
يشهد المجال تطورات متسارعة. إليك أبرز الاتجاهات التي تُشكل مستقبل هذا العلم في الفترة من 2023 إلى 2025.
البروتيوميات أحادية الخلية (Single-Cell Proteomics)
حتى وقت قريب، كان تحليل البروتيوم يتطلب آلاف أو ملايين الخلايا. النتيجة كانت “متوسطاً” يخفي التنوع بين الخلايا الفردية. التقنيات الجديدة سمحت بتحليل بروتيوم خلية واحدة، مما يكشف تفاصيل كانت مخفية.
في 2024، نشرت مجلة Nature Methods عدة تقنيات ثورية في هذا المجال. هذا الاتجاه مهم خاصة في أبحاث السرطان والمناعة؛ إذ يكشف تنوع الخلايا داخل الورم الواحد أو الاستجابة المناعية.
البروتيوميات المكانية (Spatial Proteomics)
لا يكفي معرفة أي بروتينات موجودة، بل أيضاً أين توجد داخل الخلية أو النسيج. تقنيات جديدة تجمع بين التصوير المجهري والطيف الكتلي لرسم خرائط مكانية للبروتينات.
تكامل البيانات متعددة الأوميكس (Multi-Omics Integration)
دمج بيانات البروتيوميات مع الجينوميات والترانسكريبتوميكس (دراسة الحمض النووي الريبوزي) والميتابولوميكس (دراسة الأيضات) يعطي صورة شاملة لبيولوجيا الخلية. هذا التكامل يتطلب أدوات حاسوبية متقدمة وتعاوناً بين تخصصات متعددة.
الذكاء الاصطناعي وتعلم الآلة
خوارزميات التعلم العميق (Deep Learning) أصبحت أداة أساسية في تحليل بيانات البروتيوميات. من التنبؤ ببنية البروتينات (ألفا فولد) إلى تحديد البروتينات من أطياف الكتلة إلى اكتشاف أنماط مرضية في البيانات الضخمة.
البروتيوميات السريرية في نقطة الرعاية (Point-of-Care Proteomics)
الحلم هو جهاز صغير في عيادة الطبيب يُحلل بروتيوم المريض في دقائق ويعطي نتائج فورية. التقنيات الحالية لم تصل لهذا المستوى بعد، لكن شركات ناشئة تعمل على تصغير الأجهزة وتبسيطها.
حقيقة مثيرة: في عام 2024، أعلنت شركة ناشئة أمريكية عن جهاز طيف كتلي بحجم جهاز الكمبيوتر المحمول، مقارنة بأجهزة تقليدية تحتل غرفة كاملة! التصغير المستمر سيجعل البروتيوميات في متناول مختبرات أكثر.
اقرأ أيضاً: التعلم الآلي والإحصاء: كيف يتكاملان لفهم البيانات وصنع القرار؟
كيف هو واقع البروتيوميات في العالم العربي؟
الحديث عن البروتيوميات لا يكتمل دون التطرق لواقعها في منطقتنا. الصورة فيها جوانب مضيئة وأخرى تحتاج لتطوير.
الإنجازات والمبادرات
بعض الدول العربية استثمرت بقوة في هذا المجال. المملكة العربية السعودية أنشأت مراكز بحثية متقدمة ضمن جامعة الملك عبدالله للعلوم والتقنية (كاوست) ومدينة الملك عبدالعزيز للعلوم والتقنية. الإمارات أيضاً لديها برامج طموحة في الطب الدقيق تعتمد على البروتيوميات. مصر والأردن ولبنان تضم باحثين متميزين نشروا دراسات في مجلات عالمية رفيعة.
التحديات الخاصة بالمنطقة
تكلفة الأجهزة والمواد الاستهلاكية مرتفعة جداً، خاصة للدول ذات الموارد المحدودة. هجرة الكفاءات (Brain Drain) تستنزف الخبرات المتراكمة. قلة التمويل البحثي المستمر تُعيق المشاريع طويلة المدى. كما أن البنية التحتية للمعلوماتية الحيوية لا تزال متواضعة في معظم الدول.
نصائح عملية للباحثين العرب المهتمين بالبروتيوميات
- ابدأ بالتعاون: لا تحاول بناء مختبر بروتيوميات كامل من الصفر. ابحث عن شراكات مع مراكز إقليمية أو دولية متقدمة.
- ركز على أسئلة بحثية فريدة: المنطقة العربية لديها تنوع جيني وأمراض ذات خصوصية محلية. دراسة بروتيوم هذه الأمراض يمثل فرصة للتميز.
- استثمر في المعلوماتية الحيوية: تحليل البيانات مهارة يمكن تعلمها بتكلفة أقل من شراء الأجهزة. كثير من البيانات البروتيومية متاحة مجاناً في قواعد بيانات عالمية.
- تابع المنح والفرص: منظمات مثل EMBO وHHMI تقدم منحاً للباحثين من الدول النامية.
- انضم للمجتمعات العلمية: جمعيات مثل HUPO (منظمة بروتيوم الإنسان) لديها مبادرات لدعم الباحثين الناشئين.
اقرأ أيضاً: مناهج البحث العلمي: ما أنواعها وكيف تختار المنهج المناسب
ما الفرق بين البروتيوميات والميتابولوميكس؟
سؤال يطرحه كثير من الطلاب. الميتابولوميكس (Metabolomics) تدرس الأيضات (Metabolites)، وهي الجزيئات الصغيرة الناتجة عن عمليات الأيض مثل السكريات والأحماض الأمينية والدهون.
العلاقة بين العلمين تكاملية. البروتينات (خاصة الإنزيمات) تُحفز التفاعلات الكيميائية الأيضية التي تُنتج الأيضات. التغيرات في البروتيوم تنعكس على الميتابولوم والعكس صحيح. الدمج بين العلمين يعطي صورة أكمل للحالة الفسيولوجية للخلية أو الكائن.
ما التعديلات بعد الترجمة ولماذا هي مهمة؟
التعديلات بعد الترجمة (Post-Translational Modifications – PTMs) هي تغييرات كيميائية تطرأ على البروتين بعد تصنيعه. تشمل أكثر من 400 نوع معروف، أشهرها:
- الفسفرة (Phosphorylation): إضافة مجموعة فوسفات، تتحكم في تنشيط البروتين أو تثبيطه.
- الغلكزة (Glycosylation): إضافة سكريات، تؤثر على استقرار البروتين وتفاعلاته.
- الأستلة (Acetylation): إضافة مجموعة أسيتيل، مهمة في تنظيم الجينات.
- اليوبيكويتين (Ubiquitination): وسم البروتين للتدمير.
هذه التعديلات تُغير وظيفة البروتين دون تغيير تسلسله. فهمها ضروري لفهم كيف تعمل الخلية فعلاً. دراسة التعديلات بعد الترجمة تُسمى أحياناً “فوسفوبروتيوميكس” (Phosphoproteomics) أو “غليكوبروتيوميكس” (Glycoproteomics) حسب نوع التعديل المدروس.
معلومة سريعة: خلل في عملية الفسفرة مرتبط بأكثر من 400 مرض بشري، بما في ذلك السرطان والسكري وألزهايمر. لذلك تُعَدُّ دراسة فوسفوبروتيوم الخلايا المريضة أولوية بحثية عالمية.
الأسئلة الشائعة حول البروتيوميات
ما الفرق بين البروتيوميات والجينوميات باختصار؟
الجينوميات تدرس الجينات (المادة الوراثية)، بينما البروتيوميات تدرس البروتينات (المنتجات الوظيفية للجينات). الجينوم ثابت نسبياً، أما البروتيوم فيتغير باستمرار حسب الظروف.
هل البروتيوميات تُستخدم في التشخيص الطبي حالياً؟
نعم، لكن بشكل محدود. بعض الفحوصات المعتمدة على البروتيوميات متاحة سريرياً، خاصة في تشخيص بعض أنواع السرطان وأمراض القلب. التوسع مستمر مع انخفاض التكاليف وتحسن التقنيات.
ما المؤهلات المطلوبة للعمل في مجال البروتيوميات؟
خلفية في الكيمياء الحيوية أو البيولوجيا الجزيئية أو الكيمياء التحليلية أساسية. مهارات المعلوماتية الحيوية والبرمجة أصبحت ضرورية أيضاً. درجة الماجستير أو الدكتوراه مطلوبة للمناصب البحثية المتقدمة.
كم يستغرق تحليل بروتيوم عينة واحدة؟
يختلف حسب عمق التحليل المطلوب. تحليل سريع قد يستغرق ساعات، بينما تحليل شامل عميق قد يحتاج أياماً أو أسابيع شاملة تحضير العينة ومعالجة البيانات.
ما أشهر قواعد البيانات البروتيومية؟
UniProt هي المرجع الأساسي لتسلسلات البروتينات ومعلوماتها. PRIDE Archive يخزن بيانات الطيف الكتلي الخام. Human Protein Atlas يوفر معلومات عن توزع البروتينات في الأنسجة البشرية.
هل يمكن للبروتيوميات التنبؤ بالأمراض قبل حدوثها؟
نظرياً نعم، وهذا هدف بحثي رئيس. عملياً، بعض الدراسات أظهرت إمكانية الكشف عن “توقيعات بروتينية” تسبق ظهور أمراض كالسكري والسرطان بسنوات. لكن الانتقال من البحث إلى التطبيق السريري الروتيني يحتاج مزيداً من الدراسات.
خاتمة
لقد قطعت البروتيوميات شوطاً هائلاً منذ صياغة مصطلحها قبل ثلاثة عقود. من تقنية معملية متخصصة إلى أداة تُشكل مستقبل الطب والصيدلة والبيولوجيا. التحديات لا تزال كبيرة: التعقيد الهائل للبروتيوم، والتكلفة المرتفعة، والحاجة لتوحيد المعايير. لكن التقدم التقني المتسارع، خاصة في الذكاء الاصطناعي والأجهزة المصغرة، يبشر بمستقبل مشرق.
بالنسبة للباحثين العرب، الفرصة متاحة للمساهمة في هذا المجال الواعد. الاستثمار في بناء الكفاءات والتعاون الإقليمي والدولي هو المفتاح. قد لا نملك كل الأجهزة المتطورة، لكننا نملك عقولاً قادرة على الإبداع وأسئلة بحثية فريدة تنتظر الإجابة.
فهل أنت مستعد للغوص في عالم البروتينات واكتشاف أسرار لا تزال مخفية في كل خلية من خلايا جسمك؟
أسئلة شائعة إضافية حول البروتيوميات
هل يمكن استخدام البروتيوميات في الكشف عن الأمراض المعدية والفيروسات؟
نعم، تُستخدم البروتيوميات في تحديد البروتينات الفيروسية والبكتيرية في عينات المرضى، مما يساعد في التشخيص السريع للعدوى. كما تُستخدم في دراسة استجابة الجسم المناعية للعدوى عبر رصد الأجسام المضادة والسيتوكينات، وهذا ما ساهم في فهم أعمق لفيروس كورونا المستجد خلال جائحة 2020.
ما العلاقة بين البروتيوميات وتقنية كريسبر للتعديل الجيني؟
تُستخدم البروتيوميات لتقييم نتائج التعديل الجيني بتقنية كريسبر عبر رصد التغيرات في مستويات البروتينات بعد التعديل. هذا التكامل يكشف ما إذا كان التعديل الجيني قد أدى فعلاً إلى التغيير البروتيني المطلوب، ويساعد في اكتشاف أي تأثيرات جانبية غير متوقعة على البروتينات الأخرى.
هل تختلف نتائج تحليل البروتيوم باختلاف وقت سحب العينة من المريض؟
نعم، البروتيوم يتأثر بشكل ملحوظ بالإيقاع اليومي والحالة الغذائية ومستوى النشاط البدني والأدوية المتناولة. لذلك تشترط البروتوكولات المعيارية سحب العينات في أوقات محددة وبعد صيام معين لضمان قابلية المقارنة بين النتائج.
كيف تُخزن عينات البروتيوم وما مدة صلاحيتها؟
تُخزن العينات عادة في درجة حرارة سالب 80 مئوية مع إضافة مثبطات إنزيمات التحلل البروتيني لمنع تدهور البروتينات. العينات المُحضرة بشكل صحيح يمكن أن تبقى صالحة لسنوات، لكن دورات التجميد والذوبان المتكررة تُقلل جودتها بشكل كبير.
هل يمكن تحليل بروتيوم الأنسجة الميتة أو المحفوظة تاريخياً؟
نعم، لكن بصعوبة أكبر. الأنسجة المثبتة بالفورمالين والمطمورة بالبارافين التي تُحفظ في المستشفيات لعقود يمكن تحليلها بتقنيات خاصة، وهذا يفتح إمكانية دراسة عينات تاريخية نادرة لفهم أمراض معينة بأثر رجعي.
ما الفرق بين البروتيوميات الكمية والنوعية؟
البروتيوميات النوعية تُحدد أي بروتينات موجودة في العينة دون قياس كمياتها، بينما البروتيوميات الكمية تقيس التركيز الدقيق لكل بروتين. التحليل الكمي أصعب تقنياً لكنه أكثر فائدة سريرياً لأنه يكشف التغيرات الطفيفة في مستويات البروتينات المرتبطة بالمرض.
هل البروتيوميات آمنة للمريض وما المخاطر المحتملة؟
البروتيوميات تحليل مخبري يُجرى على عينات مسحوبة مسبقاً، لذا لا توجد مخاطر إضافية على المريض تتجاوز مخاطر سحب الدم العادية. الاعتبار الأخلاقي الرئيس يتعلق بخصوصية البيانات الجينية والبروتينية وإمكانية استخدامها في التمييز التأميني أو الوظيفي.
كيف تُستخدم البروتيوميات في مجال التغذية والرياضة؟
تُستخدم لدراسة استجابة الجسم للأنظمة الغذائية المختلفة عبر رصد التغيرات البروتينية بعد تناول أطعمة معينة. في المجال الرياضي، تساعد في فهم آليات بناء العضلات والتعافي من الإصابات، كما تُستخدم في الكشف عن المنشطات المحظورة.
هل توجد تطبيقات للبروتيوميات خارج المجال الطبي؟
نعم، تُستخدم في الصناعات الغذائية للكشف عن غش المنتجات وتحديد مسببات الحساسية. كما تُستخدم في الزراعة لتطوير محاصيل مقاومة للجفاف والآفات، وفي الطب الشرعي لتحديد هوية الضحايا، وفي علم الآثار لتحليل بقايا الطعام في الأواني القديمة.
ما تكلفة تحليل البروتيوم الشامل للفرد الواحد حالياً؟
تتراوح التكلفة بين 500 و5000 دولار حسب عمق التحليل والتقنية المستخدمة والمختبر. الأسعار في انخفاض مستمر مع تطور التقنيات، ويُتوقع أن تصبح في متناول الاستخدام السريري الروتيني خلال العقد القادم.
إن وجدت هذا المقال مفيداً، شاركه مع زملائك المهتمين بالعلوم الحيوية. اترك تعليقاً بأسئلتك أو أفكارك حول مستقبل البروتيوميات في منطقتنا العربية. ولا تنسَ متابعة مقالاتنا القادمة عن تقنيات الطب الدقيق والمعلوماتية الحيوية.
المراجع
Aebersold, R., & Mann, M. (2016). Mass-spectrometric exploration of proteome structure and function. Nature, 537(7620), 347-355. https://doi.org/10.1038/nature19949
— مرجع أساسي يشرح مبادئ الطيف الكتلي في البروتيوميات من رائدين عالميين في المجال.
Graves, P. R., & Haystead, T. A. J. (2002). Molecular biologist’s guide to proteomics. Microbiology and Molecular Biology Reviews, 66(1), 39-63. https://doi.org/10.1128/MMBR.66.1.39-63.2002
— مقدمة شاملة للتقنيات الأساسية مناسبة للمبتدئين والباحثين من تخصصات مجاورة.
Pandey, A., & Mann, M. (2000). Proteomics to study genes and genomes. Nature, 405(6788), 837-846. https://doi.org/10.1038/35015709
— ورقة تاريخية مهمة توضح العلاقة بين الجينوميات والبروتيوميات وتضع الأساس النظري للمجال.
Liebler, D. C. (2002). Introduction to Proteomics: Tools for the New Biology. Humana Press.
— كتاب أكاديمي تعليمي ممتاز للطلاب والباحثين الجدد يغطي الأسس والتقنيات بأسلوب واضح.
Twyman, R. M. (2004). Principles of Proteomics. BIOS Scientific Publishers.
— كتاب جامعي شامل يغطي المبادئ النظرية والتطبيقية للبروتيوميات مع أمثلة تفصيلية.
Rodriguez, H., & Pennington, S. R. (2018). Revolutionizing precision oncology through collaborative proteogenomics and data sharing. Cell, 173(3), 535-539. https://doi.org/10.1016/j.cell.2018.04.018
— دراسة حديثة توضح تطبيقات البروتيوميات في أبحاث السرطان والتوجهات المستقبلية.
إخلاء المسؤولية: المعلومات الواردة في هذا المقال لأغراض تعليمية وتثقيفية فقط، ولا تُغني عن استشارة المتخصصين في التطبيقات السريرية أو البحثية.
جرت مراجعة هذا المقال من قبل فريق التحرير في موقعنا لضمان الدقة والمعلومة الصحيحة.