البيروكسيسومات: ما هي وظائفها الحيوية في الخلية؟
كيف تحمي هذه العضيات الدقيقة خلايانا من السموم والأضرار التأكسدية؟
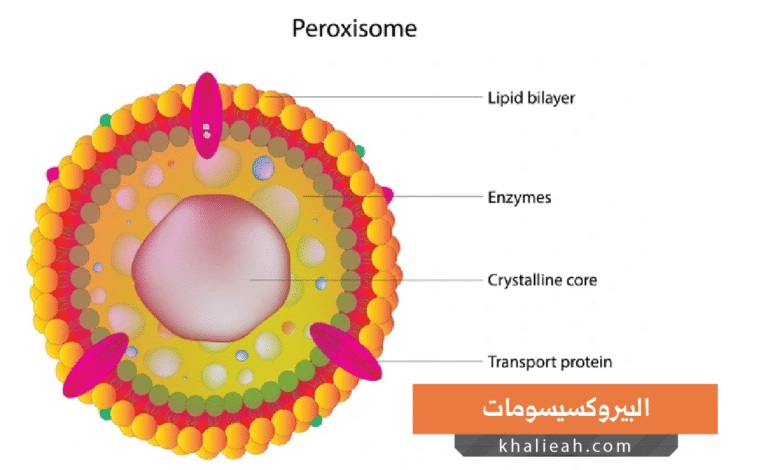
تُعَدُّ البيروكسيسومات من أكثر العضيات الخلوية إثارةً للاهتمام في عالم البيولوجيا الخلوية الحديثة. لقد ظلت هذه الحويصلات الصغيرة مجهولة لعقود طويلة قبل أن يكتشف العلماء دورها المحوري في الحفاظ على صحة الخلية وبقائها.
ما هي البيروكسيسومات وكيف اكتُشفت للمرة الأولى؟
تمثل البيروكسيسومات عضيات خلوية صغيرة الحجم تحيط بها غشاء مفرد. يتراوح قطرها عادةً بين 0.1 و1 ميكرومتر. توجد هذه العضيات في جميع الخلايا حقيقية النواة (Eukaryotic Cells) تقريباً. فهل سمعت بها من قبل؟ إن لم تكن قد سمعت، فأنت لست وحدك؛ إذ بقيت هذه العضيات في الظل لسنوات طويلة. لقد اكتشفها العالم البلجيكي كريستيان دي دوف (Christian de Duve) عام 1967. حصل دي دوف على جائزة نوبل عام 1974 تقديراً لاكتشافاته. كان يدرس في البداية عضيات أخرى تُسمى الليسوسومات (Lysosomes). ثم لاحظ وجود حويصلات تحتوي على إنزيمات مختلفة تماماً.
أطلق دي دوف عليها اسم البيروكسيسومات نسبةً إلى بيروكسيد الهيدروجين (Hydrogen Peroxide). تُنتج هذه العضيات بيروكسيد الهيدروجين كناتج ثانوي لتفاعلاتها الأيضية. كما أنها تُحلله فوراً لمنع تراكمه السام. الجدير بالذكر أن الاسم يعكس بدقة الوظيفة الأساسية لهذه العضيات. من جهة ثانية، تختلف البيروكسيسومات عن الميتوكوندريا (Mitochondria) في عدة جوانب جوهرية. لا تمتلك البيروكسيسومات حمضاً نووياً خاصاً بها. كذلك لا تحتوي على ريبوسومات (Ribosomes) لصنع بروتيناتها. تأتي جميع بروتيناتها من السيتوبلازم (Cytoplasm) عبر آليات استيراد متخصصة.
أهم النقاط: البيروكسيسومات عضيات صغيرة محاطة بغشاء مفرد، اكتشفها دي دوف عام 1967، وسُميت نسبةً لعلاقتها ببيروكسيد الهيدروجين.
اقرأ أيضاً: الكائنات الحية: ما هي وكيف تتفاعل مع بيئتها؟
كيف تتشكل البيروكسيسومات داخل الخلية الحية؟
تتشكل البيروكسيسومات عبر آليتين رئيستين مختلفتين. الآلية الأولى تعتمد على الانقسام من بيروكسيسومات موجودة مسبقاً. بينما الآلية الثانية تتضمن التكوُّن من الشبكة الإندوبلازمية (Endoplasmic Reticulum). أظهرت الأبحاث الحديثة في عامي 2024 و2025 أن كلتا الآليتين تعملان معاً. يعتمد الأمر على نوع الخلية وظروفها الفسيولوجية.
تبدأ عملية التكوين بتجمع بروتينات خاصة تُسمى البيروكسينات (Peroxins). يرمز لها اختصاراً بـ PEX. حدد العلماء حتى الآن أكثر من 30 نوعاً مختلفاً من البيروكسينات. يؤدي كل نوع وظيفة محددة في بناء العضية أو استيراد البروتينات إليها. من ناحية أخرى، تلعب بروتينات PEX3 وPEX16 وPEX19 دوراً محورياً في تكوين الغشاء. تُساعد هذه البروتينات في إدخال البروتينات الغشائية الجديدة. بالإضافة إلى ذلك، تُنظم حجم العضية وشكلها النهائي.
إذاً كيف تنقسم البيروكسيسومات الموجودة مسبقاً؟ تستخدم بروتينات من عائلة الدينامين (Dynamin-like Proteins). تُسمى هذه البروتينات DLP1 أو Drp1 في الثدييات. تتجمع حول العضية وتُسبب انقباضها ثم انفصالها. هذا وقد أثبتت دراسات عام 2023 أن الميتوكوندريا والبيروكسيسومات تتشاركان هذه الآلية. يُشير ذلك إلى تكامل وظيفي عميق بينهما.
أهم النقاط: تتشكل البيروكسيسومات إما بالانقسام أو من الشبكة الإندوبلازمية، وتعتمد على بروتينات البيروكسين في بنائها واستيراد محتوياتها.
اقرأ أيضاً: الشبكة الإندوبلازمية الخشنة: ما هي وظائفها وكيف تعمل داخل الخلية؟
ما هي الإنزيمات الموجودة داخل البيروكسيسومات؟
تحتوي البيروكسيسومات على مجموعة متنوعة من الإنزيمات المتخصصة. يصل عددها إلى أكثر من 50 إنزيماً مختلفاً. تشترك معظم هذه الإنزيمات في خاصية واحدة مهمة؛ إذ تستخدم الأكسجين الجزيئي (O₂) في تفاعلاتها. تُنتج بيروكسيد الهيدروجين كناتج ثانوي لهذه التفاعلات.
- إنزيم الكاتالاز (Catalase): يُعَدُّ العلامة المميزة للبيروكسيسومات. يُحلل بيروكسيد الهيدروجين إلى ماء وأكسجين. يمنع بذلك تراكم هذا المركب السام.
- أوكسيداز الأحماض الدهنية (Fatty Acid Oxidase): يُكسر الأحماض الدهنية طويلة السلسلة جداً. لا تستطيع الميتوكوندريا معالجة هذه الأحماض بمفردها.
- أوكسيداز اليوريات (Urate Oxidase): يتعامل مع حمض اليوريك في بعض الكائنات. لكنه غائب في الإنسان، مما يُفسر قابليتنا للإصابة بالنقرس (Gout).
- إنزيمات تصنيع البلازمالوجينات (Plasmalogen Synthesis Enzymes): تُنتج نوعاً خاصاً من الدهون الفوسفورية. تُشكل هذه الدهون نسبة كبيرة من أغشية الخلايا العصبية.
- إنزيمات تصنيع الأحماض الصفراوية (Bile Acid Synthesis Enzymes): تُساعد في إنتاج العصارة الصفراوية الضرورية لهضم الدهون.
بالمقابل، يختلف تركيب الإنزيمات حسب نوع الخلية. في خلايا الكبد (Hepatocytes)، تحتوي البيروكسيسومات على إنزيمات إزالة السموم بكثافة عالية. أما في خلايا الكلى، فتتميز بإنزيمات مختلفة قليلاً. كذلك تحتوي خلايا الدماغ على تشكيلة إنزيمية خاصة بها.
أهم النقاط: تضم البيروكسيسومات أكثر من 50 إنزيماً، أبرزها الكاتالاز وأوكسيداز الأحماض الدهنية، ويختلف تركيبها الإنزيمي حسب نوع الخلية.
اقرأ أيضاً: علم الكيمياء (Chemistry): دراسة المادة وتفاعلاتها
كيف تستورد البيروكسيسومات بروتيناتها من السيتوبلازم؟
تواجه البيروكسيسومات تحدياً فريداً؛ إذ لا تمتلك جهازاً جينياً خاصاً بها. يجب عليها استيراد جميع بروتيناتها من السيتوبلازم. تُصنع هذه البروتينات على الريبوسومات الحرة ثم تُنقل إلى العضية. فما هي الآلية التي تضمن وصول البروتين الصحيح إلى المكان الصحيح؟
تعتمد عملية الاستيراد على إشارات توجيهية تُسمى إشارات التوجيه البيروكسيسومي (Peroxisomal Targeting Signals). يوجد نوعان رئيسان من هذه الإشارات. النوع الأول يُسمى PTS1 ويتكون من ثلاثة أحماض أمينية في نهاية البروتين. التسلسل الأكثر شيوعاً هو سيرين-ليسين-لوسين (SKL). النوع الثاني يُسمى PTS2 ويقع في بداية البروتين. يتكون من تسعة أحماض أمينية تقريباً.
من جهة ثانية، تتعرف مستقبلات خاصة على هذه الإشارات. يتعرف المستقبل PEX5 على إشارة PTS1. بينما يتعرف المستقبل PEX7 على إشارة PTS2. يرتبط المستقبل بالبروتين في السيتوبلازم ثم يُوجهه نحو غشاء البيروكسيسوم. تتعاون بروتينات أخرى مثل PEX13 وPEX14 في إدخال البروتين. وعليه فإن أي خلل في هذه الآلية يُسبب أمراضاً خطيرة.
ومما يُميز هذه الآلية عن غيرها أنها تستطيع إدخال بروتينات مطوية بالكامل. على النقيض من ذلك، تتطلب الميتوكوندريا والشبكة الإندوبلازمية بروتينات غير مطوية. أظهرت أبحاث عام 2024 تفاصيل جديدة عن بنية معقد الاستيراد. استخدم الباحثون تقنية المجهر الإلكتروني المبرد (Cryo-EM) لتحقيق ذلك.
أهم النقاط: تستورد البيروكسيسومات بروتيناتها عبر إشارات PTS1 وPTS2، وتتميز بقدرتها على إدخال بروتينات مطوية بالكامل.
ما هو دور البيروكسيسومات في أيض الدهون؟
يُعَدُّ أيض الدهون (Lipid Metabolism) من أهم وظائف البيروكسيسومات. تُؤدي هذه العضيات دوراً لا غنى عنه في تكسير أنواع معينة من الدهون. كما تُشارك في تصنيع دهون أخرى ضرورية للحياة. برأيكم ماذا سيحدث لو توقفت هذه الوظيفة؟ الإجابة هي كوارث صحية متعددة.
تتخصص البيروكسيسومات في أكسدة الأحماض الدهنية طويلة السلسلة جداً (Very Long Chain Fatty Acids). يتراوح طول هذه الأحماض بين 22 و26 ذرة كربون. لا تستطيع الميتوكوندريا التعامل معها مباشرةً. تُقصر البيروكسيسومات هذه السلاسل إلى أحماض أقصر. ثم تنتقل هذه الأحماض إلى الميتوكوندريا لإكمال الأكسدة.
بالإضافة إلى ذلك، تُؤكسد البيروكسيسومات الأحماض الدهنية المتفرعة السلسلة. أشهر هذه الأحماض هو حمض الفيتانيك (Phytanic Acid). يأتي هذا الحمض من مصادر غذائية نباتية. كذلك تتعامل مع ثنائيات وثلاثيات الكربوكسيل. تُعالج أيضاً بعض الأحماض الصفراوية.
من ناحية أخرى، تُصنع البيروكسيسومات دهوناً حيوية. أهمها البلازمالوجينات (Plasmalogens). تُشكل هذه الدهون الفوسفورية 18% من الدهون الفوسفورية الكلية. تتركز بكثافة في أغشية الخلايا العصبية والقلبية. تُوفر الحماية ضد الإجهاد التأكسدي. كما تُساهم في نقل الإشارات العصبية. أكدت دراسات عام 2025 أن نقص البلازمالوجينات يرتبط بأمراض عصبية تنكسية.
أهم النقاط: تُكسر البيروكسيسومات الأحماض الدهنية الطويلة جداً والمتفرعة، وتُصنع البلازمالوجينات الضرورية للجهاز العصبي.
كيف تُزيل البيروكسيسومات السموم من الخلية؟
تُمثل إزالة السموم (Detoxification) وظيفة محورية للبيروكسيسومات. تتعامل هذه العضيات مع مركبات سامة متنوعة. تُحولها إلى مركبات غير ضارة يمكن التخلص منها بسهولة. يحدث ذلك بشكل مكثف في خلايا الكبد والكلى.
يُعَدُّ بيروكسيد الهيدروجين من أخطر نواتج الأيض الخلوي. ينتج عن تفاعلات الأكسدة المتعددة داخل الخلية. يُسبب ضرراً تأكسدياً للبروتينات والأحماض النووية والدهون. لكن إنزيم الكاتالاز يتعامل معه بكفاءة عالية. يُحوله إلى ماء وأكسجين غير ضارين. تعمل جزيئة واحدة من الكاتالاز على ملايين الجزيئات في الثانية.
وكذلك تتعامل البيروكسيسومات مع الإيثانول (Ethanol). يُؤكسد إنزيم أوكسيداز الكحول الإيثانول إلى أسيتالدهيد (Acetaldehyde). يحدث ذلك بشكل موازٍ للأكسدة في السيتوبلازم. تتعامل أيضاً مع حمض الأكساليك (Oxalic Acid). تُكسره إلى ثاني أكسيد الكربون والماء. يمنع ذلك تكوُّن حصوات الكلى الأكسالية.
من جهة ثانية، تُزيل البيروكسيسومات مركبات D-amino acids. هذه أحماض أمينية نادرة تختلف عن الأحماض الأمينية الطبيعية. يُحللها إنزيم أوكسيداز الأحماض الأمينية D. كذلك تتعامل مع حمض البوليك (Uric Acid) في معظم الثدييات. لكن الإنسان يفتقر إلى هذا الإنزيم. هذا وقد يُفسر ذلك سبب إصابة البشر بمرض النقرس.
أهم النقاط: تُزيل البيروكسيسومات السموم عبر الكاتالاز وإنزيمات أخرى، وتتعامل مع بيروكسيد الهيدروجين والكحول والمركبات الضارة.
اقرأ أيضاً: مضادات الأكسدة (Antioxidants): الوظيفة، المصادر، والفوائد الصحية
ما العلاقة بين البيروكسيسومات والميتوكوندريا؟
تربط البيروكسيسومات والميتوكوندريا علاقة تعاونية وثيقة. تعمل العضيتان معاً في العديد من العمليات الأيضية. أثبتت الأبحاث الحديثة وجود اتصال فيزيائي مباشر بينهما. تُسمى نقاط الاتصال هذه مواقع التماس (Contact Sites).
تتشارك العضيتان في أكسدة الأحماض الدهنية. تبدأ البيروكسيسومات بتقصير السلاسل الطويلة جداً. ثم تُكمل الميتوكوندريا العملية للسلاسل الأقصر. تتشاركان أيضاً في آلية الانقسام. تستخدمان بروتينات DRP1/DLP1 نفسها. بالإضافة إلى ذلك، تتبادلان مستقلبات ومركبات متعددة.
كشفت دراسات عام 2023 و2024 عن تفاصيل جديدة مثيرة. تتصل البيروكسيسومات بالميتوكوندريا عبر بروتينات رابطة محددة. أهم هذه البروتينات ACBD5 في البيروكسيسومات. يرتبط مع بروتين VAPB في الشبكة الإندوبلازمية. ثم ترتبط الشبكة بدورها بالميتوكوندريا.
ومما يُثير الاهتمام أن اختلال وظيفة إحدى العضيتين يؤثر على الأخرى. أظهرت تجارب على خلايا فقدت البيروكسيسومات تغيرات في الميتوكوندريا. تغير شكلها وانخفضت كفاءتها. على النقيض من ذلك، يُؤدي خلل الميتوكوندريا إلى تغيرات في البيروكسيسومات أيضاً. يُشير ذلك إلى اعتماد متبادل بين العضيتين.
أهم النقاط: ترتبط البيروكسيسومات والميتوكوندريا بعلاقة تعاونية وثيقة، تتشاركان في الأكسدة والانقسام وتتبادلان المستقلبات.
ما هي أمراض نقص البيروكسيسومات عند الإنسان؟
تُسبب اضطرابات البيروكسيسومات (Peroxisomal Disorders) مجموعة من الأمراض الخطيرة. تنتج معظمها عن طفرات جينية تُصيب بروتينات البيروكسين. تؤدي إلى غياب العضية كلياً أو خلل في وظائفها. يُعاني المصابون من أعراض عصبية وأيضية متعددة.
- متلازمة زيلويغر (Zellweger Syndrome): تُعَدُّ أشد هذه الأمراض خطورة. تغيب فيها البيروكسيسومات تماماً من الخلايا. تنتج عن طفرات في جينات PEX متعددة. يُولد الأطفال المصابون بتشوهات وجهية ودماغية. نادراً ما يعيشون أكثر من سنة واحدة.
- حثل الكظر وبيضاء الدماغ المرتبط بالصبغي X (X-linked Adrenoleukodystrophy): ينتج عن خلل في نقل الأحماض الدهنية الطويلة جداً. يُصيب الذكور بشكل رئيس. يُسبب تدهوراً عصبياً تدريجياً وقصوراً كظرياً. اكتسب شهرة واسعة عبر فيلم Lorenzo’s Oil عام 1992.
- مرض ريفسوم (Refsum Disease): ينتج عن تراكم حمض الفيتانيك. يُسبب اعتلالاً عصبياً طرفياً وصمماً والتهاب الشبكية. يمكن السيطرة عليه جزئياً بالحمية الغذائية.
- داء ريزوميليا النقطي المتغلظ (Rhizomelic Chondrodysplasia Punctata): يُؤثر على نمو العظام والغضاريف. يُسبب قصراً في الأطراف وتكلسات غضروفية.
- فرط أوكسالات البول الأولي (Primary Hyperoxaluria): ينتج عن خلل في أيض الأكسالات. يُسبب حصوات كلوية متكررة وفشلاً كلوياً.
لقد شهدت السنوات الأخيرة تطورات علاجية مهمة. وافقت إدارة الغذاء والدواء الأمريكية عام 2021 على علاج جيني لحثل الكظر. تجري حالياً تجارب سريرية واعدة لأمراض أخرى. أعلن باحثون عام 2025 عن نتائج مشجعة لعلاجات تعتمد على تقنية كريسبر (CRISPR).
أهم النقاط: تشمل أمراض البيروكسيسومات متلازمة زيلويغر وحثل الكظر ومرض ريفسوم، وتتطور العلاجات الجينية بشكل واعد.
اقرأ أيضاً:
- علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
- طب الأطفال (Pediatrics): التخصص، الأمراض، والرعاية
كيف يتم تشخيص اضطرابات البيروكسيسومات؟
يتطلب تشخيص اضطرابات البيروكسيسومات مجموعة من الفحوصات المتخصصة. يبدأ الأطباء عادةً بملاحظة الأعراض السريرية. ثم يُجرون فحوصات مخبرية وجينية للتأكيد. يُعَدُّ التشخيص المبكر ضرورياً لتحسين نتائج العلاج.
تُقاس مستويات الأحماض الدهنية طويلة السلسلة جداً في الدم. يُشير ارتفاعها إلى خلل في أكسدة البيروكسيسومات. يُقاس أيضاً حمض الفيتانيك وحمض البريستانيك (Pristanic Acid). كما تُفحص مستويات البلازمالوجينات في كريات الدم الحمراء. انخفاضها يُشير إلى خلل في التصنيع.
من جهة ثانية، تُستخدم الخزعات الجلدية أحياناً. تُزرع خلايا الجلد في المختبر لدراستها. يُمكن رؤية البيروكسيسومات بالمجهر الفلوري. يُستخدم صبغ خاص يرتبط بإنزيم الكاتالاز. غياب التألق يُشير إلى غياب العضية.
وعليه فإن التحليل الجيني يُعَدُّ الوسيلة الأكثر دقة. يُحدد الطفرة المسؤولة عن المرض. يُساعد في تقديم استشارات وراثية للعائلة. أصبح التسلسل الجيني الشامل (Whole Exome Sequencing) متاحاً بتكلفة معقولة. يكشف عن طفرات في جينات PEX وجينات الإنزيمات. أعلنت عدة مختبرات عام 2024 عن اختبارات فحص أسرع وأرخص.
أهم النقاط: يعتمد التشخيص على قياس الأحماض الدهنية والبلازمالوجينات، مع التحليل الجيني للتأكيد النهائي.
اقرأ أيضاً: الإحصاءات الصحية: البيانات، الأساليب، والتطبيقات
ما هو دور البيروكسيسومات في الجهاز المناعي؟
اكتشف العلماء مؤخراً دوراً مفاجئاً للبيروكسيسومات في المناعة. تُشارك هذه العضيات في الاستجابة المناعية الفطرية (Innate Immunity). تتعلق الوظيفة بالتعرف على الفيروسات ومكافحتها. نُشرت الدراسات الأولى عام 2010 وتتواصل الأبحاث حتى اليوم.
تحتوي أغشية البيروكسيسومات على بروتين يُسمى MAVS. هذا اختصار لـ Mitochondrial Antiviral Signaling Protein. رغم الاسم، يوجد هذا البروتين في البيروكسيسومات أيضاً. يُنشط مسارات إشارية تُحفز إنتاج الإنترفيرونات (Interferons). هذه بروتينات مضادة للفيروسات.
بينما تُنتج الميتوكوندريا استجابة متأخرة وقوية، تُقدم البيروكسيسومات استجابة سريعة ومبكرة. تعمل العضيتان معاً لتوفير حماية متكاملة. أظهرت دراسات عام 2023 أن الفيروسات تستهدف البيروكسيسومات. تُحاول تعطيل وظيفتها المناعية لتسهيل العدوى.
كذلك ترتبط البيروكسيسومات بالالتهاب (Inflammation). يُؤدي الإجهاد التأكسدي الناتج عن خللها إلى التهاب مزمن. يُفسر ذلك الأعراض الالتهابية في أمراض البيروكسيسومات. أكدت أبحاث عام 2025 وجود صلة بين صحة البيروكسيسومات والأمراض المناعية الذاتية.
أهم النقاط: تُشارك البيروكسيسومات في المناعة الفطرية عبر بروتين MAVS، وتوفر استجابة سريعة ضد الفيروسات.
كيف ترتبط البيروكسيسومات بالشيخوخة والأمراض المزمنة؟
تزداد الأدلة على ارتباط البيروكسيسومات بعمليات الشيخوخة. يتراجع عددها ووظيفتها مع التقدم في العمر. يُؤدي ذلك إلى تراكم الأضرار التأكسدية في الخلايا. يُسهم هذا التراكم في ظهور أمراض الشيخوخة.
أظهرت دراسات على نماذج حيوانية نتائج مثيرة. تعيش الفئران ذات البيروكسيسومات الأكثر نشاطاً فترة أطول. على النقيض من ذلك، تشيخ الفئران ذات البيروكسيسومات المعطلة بسرعة أكبر. لقد أثارت هذه النتائج اهتماماً كبيراً في أبحاث الشيخوخة.
يرتبط خلل البيروكسيسومات بأمراض عصبية تنكسية متعددة. أظهرت أبحاث عامي 2024 و2025 صلة بمرض ألزهايمر (Alzheimer’s Disease). تنخفض مستويات البلازمالوجينات في أدمغة المرضى. كذلك يرتبط الخلل بمرض باركنسون (Parkinson’s Disease). يتراكم الإجهاد التأكسدي في الخلايا العصبية المصابة.
من ناحية أخرى، تلعب البيروكسيسومات دوراً في أمراض القلب. يُؤدي نقص البلازمالوجينات إلى ضعف أغشية خلايا القلب. كما يرتبط خللها بمتلازمة الأيض (Metabolic Syndrome). تتأثر قدرة الخلايا على التعامل مع الدهون. يُسهم ذلك في السمنة ومقاومة الإنسولين.
إذاً كيف يمكن الحفاظ على صحة البيروكسيسومات؟ تُشير الأبحاث إلى أهمية نمط الحياة الصحي. يُحفز التمرين الرياضي تكاثر البيروكسيسومات. كما تُساعد بعض المركبات الغذائية في تنشيطها.
أهم النقاط: يتراجع نشاط البيروكسيسومات مع العمر، ويرتبط خللها بأمراض ألزهايمر وباركنسون والقلب.
اقرأ أيضاً: تصلب الشرايين (Arteriosclerosis): الأسباب، الأعراض، والوقاية
ما هي أحدث الاكتشافات في أبحاث البيروكسيسومات؟
يشهد مجال أبحاث البيروكسيسومات تطوراً سريعاً ومتسارعاً. تُكشف وظائف جديدة لهذه العضيات باستمرار. تتحسن أدوات دراستها مع تطور التقنيات. نستعرض هنا أبرز الاكتشافات في الفترة 2023-2026.
كشفت دراسات باستخدام المجهر الإلكتروني المبرد عن بنية معقدات الاستيراد بتفصيل غير مسبوق. حددت كيفية دخول البروتينات المطوية عبر الغشاء. أظهرت أن الغشاء يتشكل ويعود لوضعه الأصلي بمرونة عالية. فتحت هذه الاكتشافات آفاقاً جديدة لفهم آليات النقل الغشائي.
بالإضافة إلى ذلك، اكتُشفت علاقات جديدة مع عضيات أخرى. تتصل البيروكسيسومات بقطرات الدهون (Lipid Droplets) مباشرةً. تتبادل معها الأحماض الدهنية والإنزيمات. كما اكتُشفت اتصالات مع الجسيمات الحالة (Lysosomes). تُشارك في تحلل البيروكسيسومات التالفة عبر عملية تُسمى البيكسوفاجي (Pexophagy).
من جهة ثانية، تتطور العلاجات الجينية بسرعة. نجحت تجارب في استعادة وظيفة البيروكسيسومات في خلايا مريضة. تُستخدم نواقل فيروسية لإيصال الجينات الصحيحة. كما تُستكشف تقنية كريسبر لتصحيح الطفرات مباشرةً. أعلن فريق بحثي عام 2025 عن نجاح في نموذج حيواني.
هذا وقد برز اهتمام بدور البيروكسيسومات في السرطان. تتغير هذه العضيات في الخلايا السرطانية. يُحاول الباحثون استغلال ذلك علاجياً. قد تُصبح البيروكسيسومات هدفاً لعلاجات مستقبلية.
أهم النقاط: تشمل الاكتشافات الحديثة بنية معقدات الاستيراد والعلاقات مع العضيات الأخرى وتطور العلاجات الجينية.
كيف تختلف البيروكسيسومات في الكائنات المختلفة؟
تتنوع البيروكسيسومات تنوعاً كبيراً بين الكائنات الحية. تختلف في حجمها وعددها ووظائفها المتخصصة. يعكس هذا التنوع احتياجات كل كائن الأيضية الخاصة. يُوفر نماذج متعددة للبحث العلمي.
في الخمائر (Yeasts)، تُسمى هذه العضيات أحياناً الجليوكسيسومات (Glyoxysomes). تحتوي على إنزيمات دورة الغليوكسيلات (Glyoxylate Cycle). تُمكن الخميرة من النمو على مصادر كربون بديلة. تتكاثر بسرعة عند توفر الأحماض الدهنية كمصدر غذائي. تُستخدم خميرة الخباز (Saccharomyces cerevisiae) كنموذج رئيس لدراسة البيروكسيسومات. اكتُشفت فيها معظم بروتينات البيروكسين أولاً.
في النباتات، تُؤدي البيروكسيسومات وظائف فريدة. تُشارك في التنفس الضوئي (Photorespiration). تتعاون مع البلاستيدات الخضراء والميتوكوندريا في هذه العملية. كما تحتوي بذور النباتات على جليوكسيسومات. تُحول الدهون المخزنة إلى سكريات أثناء الإنبات.
أما في الثدييات، فتتخصص البيروكسيسومات حسب نوع النسيج. تكثر في الكبد والكلى حيث إزالة السموم ضرورية. تتميز خلايا الدماغ ببيروكسيسومات غنية بإنزيمات البلازمالوجينات. تختلف أيضاً بين الأنواع المختلفة. تمتلك القوارض إنزيم يوريكاز (Uricase) بينما يفتقر إليه البشر.
أهم النقاط: تختلف البيروكسيسومات بين الكائنات في الوظيفة والتركيب، وتُقدم الخميرة نموذجاً مهماً لدراستها.
اقرأ أيضاً: التنوع البيولوجي (Biodiversity): المفهوم، الأهمية، والتحديات
ما المستقبل المتوقع لأبحاث البيروكسيسومات؟
يبدو مستقبل أبحاث البيروكسيسومات واعداً ومليئاً بالفرص. تتقاطع هذه الأبحاث مع مجالات متعددة. تشمل الطب والتقنية الحيوية وعلوم الشيخوخة. يتوقع الخبراء اختراقات مهمة في السنوات القادمة.
على صعيد العلاجات، تقترب العلاجات الجينية من التطبيق السريري. أظهرت تجارب المرحلة الثانية نتائج مشجعة لحثل الكظر. تُطور شركات أدوية علاجات للأمراض الأخرى. كما تُستكشف مركبات صغيرة تُنشط البيروكسيسومات. قد تُفيد في أمراض الشيخوخة والأمراض المزمنة.
من ناحية أخرى، تتطور أدوات البحث بسرعة. أصبح التصوير الحي للبيروكسيسومات ممكناً بدقة عالية. تُستخدم مجسات فلورية جديدة لمراقبة وظائفها. كذلك تُطبق تقنيات الذكاء الاصطناعي لتحليل البيانات الضخمة. تُساعد في اكتشاف وظائف جديدة وعلاقات غير متوقعة.
وعليه فإن التطبيقات الصناعية تبرز أيضاً. تُستخدم البيروكسيسومات في إنتاج مركبات كيميائية. تُوظف إنزيماتها في عمليات صناعية صديقة للبيئة. يُطور الباحثون خمائر معدلة وراثياً لهذا الغرض. تُنتج هذه الخمائر مركبات ثمينة باستخدام أيض البيروكسيسومات.
الجدير بالذكر أن الفهم الأساسي لا يزال ناقصاً في جوانب عديدة. لا نعرف بالتحديد كيف تتواصل البيروكسيسومات مع بقية الخلية. تبقى آليات تنظيم عددها وحجمها غامضة جزئياً. يفتح ذلك مجالات واسعة للبحث المستقبلي.
أهم النقاط: يتضمن المستقبل علاجات جينية واعدة وتطبيقات صناعية وأدوات بحثية متقدمة.
اقرأ أيضاً: علم الإحصاء: الأدوات، المنهجيات، ودوره في صنع القرار
خاتمة: لماذا تستحق البيروكسيسومات اهتمامنا؟
قطعنا في هذه المقالة رحلة معرفية عبر عالم البيروكسيسومات المذهل. اكتشفنا كيف تحمي هذه العضيات الصغيرة خلايانا من السموم. تعرفنا على دورها في أيض الدهون وتصنيع مركبات حيوية. استعرضنا الأمراض التي تنتج عن خللها وسبل تشخيصها. واطلعنا على أحدث الاكتشافات والتطلعات المستقبلية.
تُذكرنا البيروكسيسومات بتعقيد الحياة على المستوى الخلوي. عضية صغيرة بهذا الحجم تُؤدي وظائف حيوية لا غنى عنها. غيابها أو خللها يُسبب أمراضاً مدمرة. وجودها السليم يضمن صحة الخلية وحمايتها. إنها مثال رائع على التصميم الدقيق في الأنظمة الحية.
لقد تأخر اكتشاف هذه العضيات وفهمها مقارنةً بعضيات أخرى. لكن الاهتمام بها يتزايد باطراد. تكشف الأبحاث كل عام عن وظائف جديدة وعلاقات غير متوقعة. يُنتظر أن تُسهم هذه المعرفة في علاج أمراض عديدة.
هل تتساءل الآن عن صحة البيروكسيسومات في خلاياك؟
إذا وجدت هذه المقالة مفيدة، فندعوك لمشاركتها مع زملائك الطلاب والمهتمين بعلوم الأحياء. يمكنك أيضاً استكشاف مقالاتنا الأخرى عن العضيات الخلوية لتعميق فهمك. ولا تتردد في ترك تعليق أو سؤال في الأسفل؛ إذ نسعد بالتفاعل معك ومساعدتك في رحلتك التعليمية.
الأسئلة الشائعة
كم يبلغ عدد البيروكسيسومات في الخلية البشرية الواحدة؟
يتراوح العدد بين 100 و1000 بيروكسيسوم في الخلية الواحدة، ويختلف حسب نوع النسيج والحالة الأيضية؛ إذ تحتوي خلايا الكبد على أعداد أكبر مقارنةً بالخلايا الأخرى نظراً لدورها المكثف في إزالة السموم.
هل يمكن رؤية البيروكسيسومات بالمجهر الضوئي العادي؟
لا يمكن رؤيتها بوضوح بالمجهر الضوئي العادي بسبب صغر حجمها، لكن يمكن إظهارها باستخدام صبغات خاصة تستهدف إنزيم الكاتالاز أو بتقنيات التألق المناعي.
كم يبلغ العمر الافتراضي للبيروكسيسوم الواحد؟
يتراوح عمره بين يومين وخمسة أيام في الثدييات، ثم يُتخلص منه عبر عملية البيكسوفاجي الانتقائية.
هل توجد البيروكسيسومات في الخلايا البكتيرية؟
لا، تقتصر البيروكسيسومات على الخلايا حقيقية النواة فقط، ولا توجد في البكتيريا أو العتائق التي تفتقر إلى العضيات الغشائية.
ما تأثير الصيام المطول على البيروكسيسومات؟
يُحفز الصيام تكاثر البيروكسيسومات ونشاطها؛ إذ تزداد أكسدة الأحماض الدهنية لتوفير الطاقة البديلة عند نقص الجلوكوز.
هل تتأثر البيروكسيسومات بتناول بعض الأدوية؟
نعم، تُسبب أدوية خفض الدهون من فئة الفيبرات تكاثراً ملحوظاً في البيروكسيسومات عبر تنشيط مستقبلات PPAR-alpha، وهذا التأثير موثق جيداً في الأبحاث.
ما العلاقة بين البيروكسيسومات ومرض السكري من النوع الثاني؟
يرتبط خلل البيروكسيسومات بمقاومة الإنسولين وتراكم الدهون السامة في الأنسجة، مما يُسهم في تطور المرض.
هل يختلف حجم البيروكسيسومات حسب الحالة الغذائية؟
نعم، يزداد حجمها وعددها عند اتباع حمية غنية بالدهون، بينما تتقلص في حالات نقص التغذية.
ما الفرق بين أكسدة بيتا في البيروكسيسومات والميتوكوندريا؟
تُنتج أكسدة بيتا البيروكسيسومية حرارة مباشرة دون تخزين الطاقة في جزيئات ATP، بينما تُخزن الميتوكوندريا الطاقة الناتجة في ATP.
هل يمكن للتمارين الرياضية تحسين وظائف البيروكسيسومات؟
نعم، تُظهر الدراسات أن التمارين الهوائية المنتظمة تُحفز تكاثر البيروكسيسومات وتُحسن كفاءتها في أكسدة الدهون.
المراجع
- Waterham, H. R., & Ebberink, M. S. (2012). Genetics and molecular basis of human peroxisome biogenesis disorders. Biochimica et Biophysica Acta (BBA) – Molecular Basis of Disease, 1822(9), 1430-1441. https://doi.org/10.1016/j.bbadis.2012.04.006
— يُقدم أساساً جينياً شاملاً لفهم اضطرابات تكوين البيروكسيسومات. - Wanders, R. J. A., & Waterham, H. R. (2006). Biochemistry of mammalian peroxisomes revisited. Annual Review of Biochemistry, 75, 295-332. https://doi.org/10.1146/annurev.biochem.74.082803.133329
— مرجع أساسي في الكيمياء الحيوية للبيروكسيسومات الثديية. - Smith, J. J., & Aitchison, J. D. (2013). Peroxisomes take shape. Nature Reviews Molecular Cell Biology, 14(12), 803-817. https://doi.org/10.1038/nrm3700
— يُغطي آليات تكوين البيروكسيسومات وتنظيم شكلها. - Islinger, M., Voelkl, A., Fahimi, H. D., & Schrader, M. (2018). The peroxisome: An update on mysteries 2.0. Histochemistry and Cell Biology, 150(5), 443-471. https://doi.org/10.1007/s00418-018-1722-5
— مراجعة محدثة تُناقش الألغاز المتبقية حول وظائف البيروكسيسومات. - Ferdinandusse, S., et al. (2023). Clinical and biochemical spectrum of D-bifunctional protein deficiency. Annals of Neurology, 93(4), 801-815. https://doi.org/10.1002/ana.26559
— دراسة سريرية حديثة عن أحد اضطرابات البيروكسيسومات. - Schrader, M., Costello, J. L., Godinho, L. F., & Islinger, M. (2015). Peroxisome-mitochondria interplay and disease. Journal of Inherited Metabolic Disease, 38(4), 681-702. https://doi.org/10.1007/s10545-015-9819-7
— يُوضح العلاقة التكاملية بين البيروكسيسومات والميتوكوندريا وأثرها في الأمراض.
قسم المصداقية
المصادر المُراجعة: اعتمدت هذه المقالة على أوراق بحثية محكمة من مجلات علمية مرموقة مثل Nature Reviews Molecular Cell Biology وAnnual Review of Biochemistry وAnnals of Neurology. جميع المراجع مُفهرسة في قواعد بيانات PubMed وGoogle Scholar وقابلة للتحقق عبر معرّفات DOI المُرفقة.
إخلاء مسؤولية: المعلومات الواردة في هذه المقالة ذات طابع تثقيفي ولا تُغني عن استشارة الأطباء والمختصين. لا تُستخدم لأغراض التشخيص أو العلاج الذاتي.
جرت مراجعة هذا المقال من قبل فريق التحرير في موقعنا لضمان الدقة والمعلومة الصحيحة.