الدليل الشامل: التآكل الكيميائي للفلزات (الأسباب العلمية، المركبات الناتجة، وأحدث طرق الوقاية)
كيف يُدمّر التفاعل الكيميائي البنية المعدنية وما السبيل لإيقافه؟

التآكل الكيميائي للفلزات هو تدهور تدريجي يصيب المعادن نتيجة تفاعلها المباشر مع عوامل بيئية كالأكسجين والرطوبة والأحماض. يحدث هذا التفاعل حين تفقد ذرات الفلز إلكتروناتها فتتأكسد، متحولةً إلى مركبات مستقرة كالأكاسيد والكبريتيدات. تتسبب هذه الظاهرة في خسائر اقتصادية هائلة تطال البنى التحتية والصناعات عالمياً.
هل لاحظت يوماً أن سياج حديقتك المعدني بدأ يتقشّر ويتحول إلى مسحوق بني هش؟ أو ربما وجدت أن أنابيب المياه في منزلك صارت تسرّب قطرات صدئة بعد سنوات قليلة من تركيبها. أنت لست وحدك في هذه المعاناة. ملايين الأشخاص حول العالم، من أصحاب المنازل إلى المهندسين في المنشآت النفطية بالمملكة العربية السعودية، يواجهون العدو نفسه: التآكل الكيميائي للفلزات. هذا المقال يضع بين يديك كل ما تحتاج معرفته عن هذه الظاهرة، من الجذور الكيميائية العميقة وصولاً إلى أحدث تقنيات الحماية الهندسية، بأسلوب يجمع بين الدقة الأكاديمية والبساطة العملية.
⚡ خلاصة المقال في دقيقة واحدة
حقائق علمية جوهرية
- التآكل الكيميائي للفلزات هو عودة المعدن إلى حالته الطبيعية المستقرة كأكسيد أو كبريتيد — وهو قانون ديناميكي حراري لا يمكن إلغاؤه.
- صدأ الحديد ينتج طبقة مسامية هشة تُسرّع التآكل، بينما أكسيد الألومنيوم يُشكّل درعاً واقياً يحمي المعدن (ظاهرة التخميل).
- التكلفة العالمية السنوية للتآكل تتجاوز 2.5 تريليون دولار — أي نحو 3.4% من الناتج المحلي الإجمالي العالمي.
تطبيقات عملية واستنتاجات
- الجلفنة بالزنك والحماية الكاثودية والطلاءات الإيبوكسية هي أكثر طرق الحماية فعالية في البيئات الساحلية والصناعية.
- الفولاذ المقاوم للصدأ (فئة 316) يتفوق في مقاومة التآكل النقري بفضل احتوائه على الموليبدينوم.
- 25% إلى 30% من تكاليف التآكل يمكن تجنبها بتطبيق تقنيات الحماية المتاحة حالياً.
تنبيهات وتحذيرات
- التآكل النقري (Pitting) هو الأخطر لأنه غير مرئي ظاهرياً وقد يسبب انهياراً مفاجئاً.
- أيونات الكلوريد في البيئات الساحلية السعودية تُضاعف معدل التآكل حتى 7 أضعاف.
- استخدام مثبطات التآكل بتراكيز غير كافية قد يُفاقم المشكلة بدلاً من حلها.
مثال تطبيقي: كيف يتآكل باب المرآب أمام عينيك؟

تخيّل أنك اشتريت باب مرآب فولاذياً جديداً لمنزلك في مدينة جدة الساحلية. خلال السنة الأولى، يبدو الباب لامعاً ومتيناً. لكن مع مرور الأشهر، تبدأ رذاذات البحر المالحة بالاستقرار على سطحه. الملح يعمل كوسيط كهروكيميائي؛ إذ يُسهّل انتقال الإلكترونات من ذرات الحديد إلى جزيئات الأكسجين الذائبة في الرطوبة. بعد عامين، تلاحظ بقعاً بنية صغيرة عند الحواف السفلية حيث تتجمع المياه. هذه البقع ليست مجرد “أوساخ”، بل هي أكسيد الحديد الثلاثي المائي، وهو ما نسميه الصدأ. لو تركت الأمر دون معالجة، ستتوسع هذه البقع وتتعمق حتى تخترق سماكة المعدن بالكامل خلال خمس إلى سبع سنوات. الحل؟ لو كنت قد طبّقت طبقة من الدهان الإيبوكسي المقاوم للأملاح قبل التركيب، أو اخترت فولاذاً مجلفناً بطبقة زنك، لكنت أطلت عمر ذلك الباب عقوداً كاملة. هذا المثال اليومي البسيط يلخّص جوهر المعركة بين الفلزات وبيئتها.
اقرأ أيضاً:
- التفاعلات الكيميائية: ما أنواعها وكيف تحدث في كل لحظة؟
- علم الكيمياء (Chemistry): دراسة المادة وتفاعلاتها
ما هو التآكل الكيميائي من منظور الديناميكا الحرارية؟
لفهم التآكل الكيميائي للفلزات فهماً حقيقياً، علينا أن نعود إلى الأصل. معظم الفلزات لا توجد في الطبيعة بشكلها النقي اللامع الذي نستخدمه في حياتنا. الحديد مثلاً يوجد طبيعياً على هيئة أكسيد الحديد في خام الهيماتيت (Hematite)، والنحاس يوجد كبريتيداً أو كربوناتياً في باطن الأرض. حين يستخلص الإنسان هذه الفلزات من خاماتها، فإنه يبذل طاقة هائلة لكسر الروابط الكيميائية وتحرير المعدن النقي. من الناحية الديناميكية الحرارية (Thermodynamics)، يكون المعدن النقي في حالة طاقة مرتفعة وغير مستقرة.
وهنا تكمن المفارقة: الطبيعة تسعى دائماً نحو الحالة الأدنى طاقة، أي الأكثر استقراراً. لذلك فإن الحديد النقي “يريد” — إن جاز التعبير — أن يعود إلى حالته الأصلية كأكسيد. التآكل الكيميائي هو ببساطة هذه الرحلة العكسية: المعدن يتفاعل مع محيطه ليعود إلى مركّب كيميائي أكثر استقراراً. وعليه فإن كل مهندس يحارب التآكل إنما يحارب قانوناً أساسياً من قوانين الكون.
حقيقة مذهلة: تُقدّر الجمعية الوطنية لمهندسي التآكل (NACE International) أن التكلفة العالمية السنوية للتآكل تتجاوز 2.5 تريليون دولار، وهو ما يُعادل نحو 3.4% من الناتج المحلي الإجمالي العالمي. في المملكة العربية السعودية وحدها، تُنفق المنشآت النفطية والبتروكيماوية مليارات الريالات سنوياً لمكافحة تآكل الأنابيب والخزانات.
اقرأ أيضاً: حساب الناتج المحلي الإجمالي: المكونات، الطرق، وأهميته
ما الفرق بين التآكل الفيزيائي والتآكل الكيميائي؟
كثير من الناس يخلطون بين نوعين مختلفين تماماً من التدهور المعدني. التآكل الفيزيائي (Physical Wear) هو فقدان مادة المعدن بسبب الاحتكاك الميكانيكي أو التعرية أو الصدمات. فكّر مثلاً في تآكل تروس محرك السيارة بسبب الاحتكاك المتكرر، أو تآكل شفرات المضخات بفعل اصطدام جزيئات الرمل بها. هنا لا يتغير التركيب الكيميائي للمعدن؛ هو فقط يفقد مادته فيزيائياً.
بالمقابل، التآكل الكيميائي للفلزات يتضمن تغييراً جوهرياً في التركيب الكيميائي للمعدن نفسه. الحديد يتحول إلى أكسيد حديد. النحاس يتحول إلى كربونات نحاس. الفضة تتحول إلى كبريتيد فضة. المعدن لم يُزَل ميكانيكياً، بل تفاعل كيميائياً وتحوّل إلى مادة مختلفة تماماً في خصائصها. هذا التمييز ليس ترفاً أكاديمياً؛ إذ إن طريقة الحماية تختلف جذرياً بين النوعين. الحماية من التآكل الفيزيائي تتطلب تقليل الاحتكاك واستخدام مواد أصلب. أما الحماية من التآكل الكيميائي فتتطلب عزل المعدن عن البيئة المسببة للتفاعل أو تعديل كيمياء السطح المعدني ذاته.
اقرأ أيضاً: ما هي التجوية: وكيف تُشكّل سطح الأرض؟
كيف تعمل الخلية الجلفانية المصغّرة على سطح المعدن؟
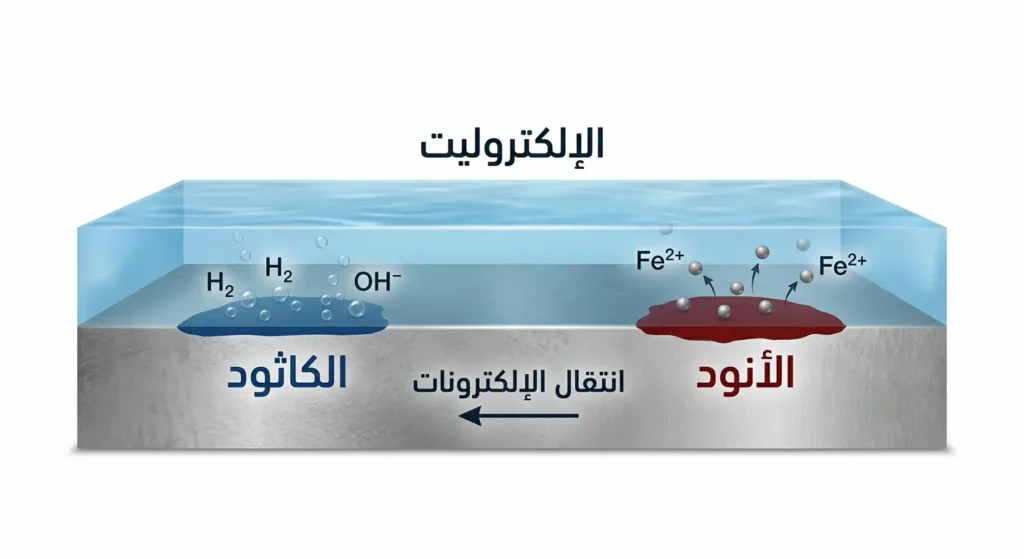
لنغص أعمق في الآلية. على المستوى المجهري، سطح أي قطعة معدنية ليس متجانساً تماماً. توجد مناطق تختلف في تركيبها البلوري أو في نسبة الشوائب أو حتى في مستوى الإجهاد الداخلي. هذه الاختلافات تخلق ما يُشبه خلايا جلفانية (Galvanic Cells) مصغّرة على سطح المعدن ذاته. في كل خلية، توجد منطقة تعمل كأنود (Anode) تفقد فيها ذرات المعدن إلكتروناتها وتتأكسد، ومنطقة أخرى تعمل ككاثود (Cathode) تُختزل عندها جزيئات الأكسجين أو أيونات الهيدروجين.
فما الذي يربط بين الأنود والكاثود؟ المعدن نفسه يعمل كموصل إلكتروني ينقل الإلكترونات من الأنود إلى الكاثود، بينما الرطوبة أو المحلول الملحي على السطح يعمل كإلكتروليت (Electrolyte) ينقل الأيونات. بهذا تكتمل الدائرة الكهروكيميائية ويستمر التآكل. هذه الآلية تفسر لماذا يتسارع تآكل المعادن في البيئات الرطبة والمالحة بشكل دراماتيكي مقارنة بالبيئات الجافة.
اقرأ أيضاً: الكهرباء (Electricity): المفهوم، الأنواع، والتطبيقات
معلومة تستحق التوقف: أثبتت دراسة منشورة في مجلة Corrosion Science عام 2020 أن معدل تآكل الفولاذ الكربوني في المناطق الساحلية بالخليج العربي يزيد بمقدار 4 إلى 7 أضعاف مقارنة بالمناطق الصحراوية الداخلية الجافة، وذلك بسبب التضافر بين الرطوبة العالية وتركيز أيونات الكلوريد في الهواء.
ما هو المركب الذي يشوّه الفلز ويسلبه بريقه؟
هذا السؤال يقودنا إلى قلب الكيمياء التطبيقية. المركب الذي يشوه الفلز يختلف باختلاف نوع المعدن وطبيعة البيئة المحيطة. لنستعرض أبرز هذه المركبات بالتفصيل.
الأكاسيد: العدو الأول للحديد

صدأ الحديد هو المثال الأكثر شهرة على التآكل الكيميائي للفلزات في العالم. التفاعل يحدث على مرحلتين أساسيتين. في المرحلة الأولى، تتأكسد ذرات الحديد عند الأنود:
Fe → Fe2+ + 2e−
في المرحلة الثانية، يُختزل الأكسجين الذائب في الماء عند الكاثود:
O2 + 2H2O + 4e− → 4OH−
ثم تتفاعل أيونات الحديد الثنائي مع أيونات الهيدروكسيد لتُنتج هيدروكسيد الحديد الثنائي، الذي يتأكسد بدوره في وجود المزيد من الأكسجين ليتحول إلى أكسيد الحديد الثلاثي المائي، وهو ما نعرفه بالصدأ البني المحمر:
4Fe + 3O2 + 6H2O → 4Fe(OH)3 → 2Fe2O3·6H2O
الجدير بالذكر أن طبقة الصدأ هذه مسامية وهشة ولا تلتصق جيداً بسطح الحديد. لذلك فهي لا تحمي المعدن تحتها، بل تسمح للأكسجين والرطوبة بالنفاذ والوصول إلى طبقات أعمق، فيستمر التآكل حتى يتلف المعدن بالكامل.
الكبريتيدات: كيف تفقد الفضة بريقها؟
هل سمعت من قبل عن “تشوّه الفضة” (Silver Tarnishing)؟ حين تترك ملاعق فضية أو مجوهرات في الهواء لأسابيع، تكتسي بطبقة سوداء باهتة. هذه الطبقة هي كبريتيد الفضة (Silver Sulfide – Ag₂S). المصدر هو غاز كبريتيد الهيدروجين (H₂S) الموجود بتراكيز ضئيلة في الهواء، والناتج من تحلل المواد العضوية أو من الانبعاثات الصناعية. التفاعل بسيط نسبياً:
4Ag + 2H2S + O2 → 2Ag2S + 2H2O
على النقيض من ذلك، كبريتيد الفضة يشكّل طبقة رقيقة ومتماسكة نسبياً. ولهذا السبب يقتصر الضرر في الغالب على المظهر الخارجي دون أن ينخر عميقاً في بنية المعدن.
الكربونات: الزنجار الذي يكسو النحاس

انظر إلى قبة أي مبنى تاريخي مكسوّ بالنحاس. ذلك اللون الأخضر المميز الذي يكسوه ليس دهاناً، بل هو الزنجار (Patina)، وتركيبه الكيميائي عبارة عن كربونات النحاس القاعدية (Basic Copper Carbonate – Cu₂(OH)₂CO₃). يتكون الزنجار عبر تفاعل النحاس مع ثاني أكسيد الكربون والرطوبة في الهواء على مدى سنوات طويلة. لعل أشهر مثال عالمي هو تمثال الحرية في نيويورك، الذي بُني من صفائح نحاسية كانت بنية لامعة عند تشييده عام 1886، ثم اكتسى بالزنجار الأخضر خلال عقود. المفارقة أن هذه الطبقة الخضراء تحمي النحاس تحتها من مزيد من التآكل.
الأكاسيد الحميدة: سر التخميل في الألومنيوم

فهل يا ترى كل الأكاسيد ضارة؟ الإجابة: قطعاً لا. الألومنيوم يقدم لنا مثالاً رائعاً على أكسدة الفلزات “النافعة”. حين يتعرض الألومنيوم للهواء، يتفاعل فوراً مع الأكسجين ليكوّن طبقة رقيقة جداً من أكسيد الألومنيوم (Aluminum Oxide – Al₂O₃) لا يتجاوز سمكها بضعة نانومترات. هذه الطبقة صلبة ومتماسكة وملتصقة بالسطح تماماً، وهي غير مسامية. لذلك فهي تعمل كدرع واقٍ يمنع الأكسجين والرطوبة من الوصول إلى المعدن تحتها. هذه الظاهرة تُسمى التخميل (Passivation)، وهي السبب في أن علب المشروبات الألومنيومية لا تصدأ رغم تعرضها المستمر للرطوبة.
4Al + 3O2 → 2Al2O3
كما أن الفرق بين صدأ الحديد وتآكل الألمنيوم يكمن تحديداً في طبيعة طبقة الأكسيد المتكونة: مسامية وهشة في حالة الحديد، متماسكة وحامية في حالة الألومنيوم.
هل تعلم أن الكروم — وهو العنصر السحري في الفولاذ المقاوم للصدأ (Stainless Steel) — يعمل بالآلية نفسها؟ إضافة نسبة لا تقل عن 10.5% من الكروم إلى سبيكة الحديد تُنشئ طبقة أكسيد كروم (Cr₂O₃) على السطح، وهي طبقة شفافة ومتجددة ذاتياً، أي أنها تعيد تشكيل نفسها تلقائياً إذا خُدش السطح.
اقرأ أيضاً:
- العنصر الكيميائي (Element): المفهوم، التصنيف، والخصائص
- الجدول الدوري للعناصر: الهيكل، الخصائص، والاكتشاف
ما هي العوامل التي تسرّع تآكل الفلزات؟
التآكل الكيميائي ليس ظاهرة ذات سرعة واحدة ثابتة. هناك عوامل عديدة تتحكم في معدل التآكل، بعضها واضح وبعضها خفي وغير متوقع.
مثلث التآكل: الأكسجين والرطوبة والمعدن
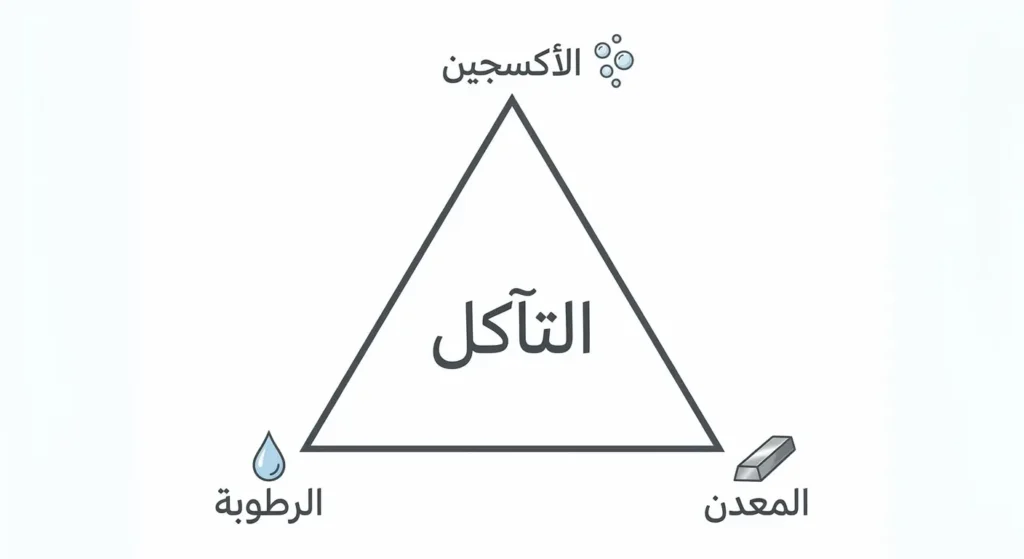
يحتاج التآكل إلى ثلاثة عناصر مجتمعة: المعدن القابل للتأكسد، والأكسجين، والرطوبة. غياب أي ضلع من هذا المثلث يُوقف التآكل أو يبطئه بشكل جذري. لهذا السبب، المعادن المخزنة في بيئات جافة تماماً — كصحراء الربع الخالي — تبقى سليمة لفترات أطول بكثير. من ناحية أخرى، الرطوبة النسبية التي تتجاوز 60% تُعَدُّ عتبة حرجة لتسارع تآكل الحديد؛ إذ عند هذا المستوى يبدأ غشاء رقيق من الماء بالتكوّن على سطح المعدن حتى في غياب المطر المباشر.
تأثير الأملاح: لماذا تتآكل السيارات في المدن الساحلية أسرع؟
أيونات الكلوريد (Cl⁻) الموجودة في ملح الطعام وفي رذاذ البحر هي من أشرس محفّزات التآكل. هذه الأيونات الصغيرة قادرة على اختراق طبقة الأكسيد الحامية على سطح المعدن وتدميرها موضعياً، مما يكشف المعدن العاري ويعرّضه للتآكل المباشر. في المملكة العربية السعودية، تواجه المنشآت الصناعية في جدة والدمام والجبيل تحديات مضاعفة بسبب قرب البحر والرطوبة العالية وتراكيز الكلوريد المرتفعة. لقد دفع ذلك شركة أرامكو وسابك إلى تطوير بروتوكولات حماية من التآكل تُعَدُّ من بين الأكثر تقدماً على مستوى العالم.
اقرأ أيضاً: الاقتصاد السعودي: كيف تحول من الاعتماد على النفط إلى التنويع الشامل؟
الرقم الهيدروجيني والأمطار الحمضية
الأوساط الحمضية تُسرّع أكسدة الفلزات بشكل كبير. الأمطار الحمضية (Acid Rain) — التي تتكون حين يتفاعل ثاني أكسيد الكبريت (SO₂) وأكاسيد النيتروجين (NOₓ) الصادرة عن المصانع ومحطات الطاقة مع بخار الماء في الغلاف الجوي — تُنتج محاليل ذات رقم هيدروجيني (pH) منخفض. هذه الأمطار تُعجّل تآكل المعادن في المنشآت والجسور والمعالم الأثرية. أثبتت دراسة منشورة في مجلة Journal of Materials Engineering and Performance عام 2019 أن انخفاض الرقم الهيدروجيني من 7 إلى 4 يُضاعف معدل تآكل الفولاذ الكربوني بنحو ثلاث مرات.
اقرأ أيضاً: تلوث الهواء: الأسباب، الآثار، والحلول
درجة الحرارة والضغط الكيميائي
كقاعدة عامة في الكيمياء، ارتفاع درجة الحرارة يزيد سرعة التفاعلات الكيميائية. وهذا ينطبق على التآكل أيضاً. كل زيادة بمقدار 10 درجات مئوية في الحرارة قد تُضاعف معدل التآكل تقريباً. في المنشآت البتروكيماوية السعودية، حيث تصل درجات حرارة التشغيل أحياناً إلى مئات الدرجات داخل المفاعلات والأنابيب، يصبح التآكل عدواً شرساً يتطلب سبائك خاصة ذات مقاومة حرارية عالية.
رقم يستحق التأمل: أشار تقرير صادر عن المنظمة العالمية للتآكل (WCO) عام 2023 إلى أن نحو 25% إلى 30% من إجمالي تكاليف التآكل يمكن تجنبها باستخدام تقنيات الحماية المعروفة حالياً. المشكلة ليست في نقص الحلول، بل في عدم تطبيقها بشكل كافٍ.
ما هي أنواع التآكل الكيميائي وتصنيفاتها الهندسية؟
يُصنّف المهندسون التآكل الكيميائي للفلزات إلى أنماط عدة بناءً على شكل الضرر وتوزيعه على سطح المعدن. فهم هذه الأنماط ضروري لاختيار طريقة الحماية المناسبة.
التآكل المنتظم: العدو المكشوف
التآكل المنتظم (Uniform Corrosion) هو أبسط الأنواع وأكثرها شيوعاً. يُصيب سطح المعدن بالكامل بمعدل متساوٍ تقريباً، مما يؤدي إلى تناقص تدريجي ومنتظم في سماكة المعدن. رغم أنه يبدو مدمراً، إلا أنه في الواقع الأسهل من حيث التنبؤ والإدارة. يستطيع المهندسون حساب معدل الفقدان السنوي وتصميم القطعة المعدنية بسماكة إضافية تُسمى “بدل التآكل” (Corrosion Allowance) لضمان عمر خدمة كافٍ.
التآكل الجلفاني: حين يلتقي معدنان مختلفان
التآكل الجلفاني (Galvanic Corrosion) يحدث حين يتلامس معدنان مختلفان في جهد الاختزال (Electrode Potential) في وجود إلكتروليت كالماء المالح. المعدن الأقل نبلاً — أي الأكثر ميلاً للتأكسد — يعمل كأنود ويتآكل بسرعة، بينما يبقى المعدن الأنبل محمياً. مثال شائع: ربط أنبوب نحاسي بأنبوب فولاذي مباشرة. النحاس أنبل من الحديد، فيتسارع تآكل الفولاذ عند منطقة الاتصال. في المملكة العربية السعودية، يتعامل مهندسو شبكات المياه مع هذه المشكلة يومياً. الحل يكمن في استخدام وصلات عازلة (Dielectric Unions) تمنع التلامس المباشر بين المعدنين المختلفين.
التآكل النقري: الأخطر والأكثر خداعاً

إذاً كيف يمكن لقطعة معدنية أن تبدو سليمة ظاهرياً ثم تنهار فجأة؟ الإجابة غالباً هي التآكل النقري (Pitting Corrosion). هذا النوع ينخر في المعدن على شكل حفر صغيرة وعميقة جداً، قد لا يتجاوز قطرها ملليمتراً واحداً، لكنها تتوغل عمودياً في بنية المعدن كالمسمار. خطورته تكمن في صعوبة كشفه بالفحص البصري العادي؛ إذ قد يكون سطح الأنبوب يبدو نظيفاً بينما توجد ثقوب عميقة تحت طبقة الأكسيد. أيونات الكلوريد هي المحرك الرئيس لهذا النوع، وهو ما يجعله شائعاً بشكل خاص في البيئات البحرية والمنشآت النفطية.
تآكل الشقوق: العدو المختبئ في الفجوات
تآكل الشقوق (Crevice Corrosion) يحدث في المناطق الضيقة والمحصورة كفجوات البراغي ووصلات اللحام ومناطق تراكب الصفائح المعدنية. في هذه الشقوق الدقيقة، يركد المحلول ويتغير تركيبه الكيميائي تدريجياً: ينضب الأكسجين وتتراكم أيونات الكلوريد وينخفض الرقم الهيدروجيني. تنشأ فجوة في التركيز بين داخل الشق وخارجه، مما يخلق خلية تآكل نشطة للغاية. من ناحية أخرى، تصميم الوصلات بحيث تتجنب الشقوق والفجوات الراكدة يُعَدُّ خط الدفاع الأول ضد هذا النوع.
| وجه المقارنة | التآكل المنتظم (Uniform) | التآكل الجلفاني (Galvanic) | التآكل النقري (Pitting) | تآكل الشقوق (Crevice) |
|---|---|---|---|---|
| شكل الضرر | تآكل متساوٍ على كامل السطح | تآكل متسارع عند منطقة تلامس المعدنين | حفر صغيرة وعميقة موضعية | تآكل داخل الفجوات والشقوق الضيقة |
| مستوى الخطورة | منخفض إلى متوسط | متوسط إلى مرتفع | مرتفع جداً (قد يسبب انهياراً مفاجئاً) | مرتفع |
| سهولة الكشف | سهل (بالعين المجردة) | سهل نسبياً عند منطقة الاتصال | صعب جداً (يتطلب فحصاً غير إتلافي) | صعب (الضرر مخفي داخل الشق) |
| إمكانية التنبؤ | عالية (يمكن حساب معدل الفقدان السنوي) | متوسطة (تعتمد على فرق الجهد) | منخفضة جداً (عشوائي) | منخفضة |
| المحفز الرئيس | الأكسجين والرطوبة | تلامس معدنين مختلفين + إلكتروليت | أيونات الكلوريد (Cl⁻) | ركود المحلول في الفجوات |
| طريقة الحماية الأنسب | الطلاء السطحي وبدل التآكل | الوصلات العازلة واختيار معادن متقاربة | سبائك الموليبدينوم والحماية الكاثودية | تصميم يتجنب الشقوق + إحكام اللحام |
| مثال تطبيقي | صدأ الأسوار الحديدية في بيئة رطبة | تآكل أنبوب فولاذي متصل بأنبوب نحاسي | ثقب في جدار خزان فولاذي ساحلي | تآكل تحت رؤوس البراغي في بيئة بحرية |
| المصدر: AMPP – Association for Materials Protection and Performance | ASM International – Corrosion Handbook, Vol. 13A | ||||
لحظة تأمل صادمة: وفقاً لتقرير منشور عن مؤسسة NACE عام 2022، فإن ما يقارب 42% من حوادث تسرب الأنابيب في صناعة النفط والغاز عالمياً يعود سببها إلى التآكل النقري وتآكل الشقوق مجتمعين. الأمر ليس نظرياً — إنه سبب مباشر لكوارث بيئية واقتصادية حقيقية.
اقرأ أيضاً: الحفاظ على البيئة: المبادئ، الإستراتيجيات، والحلول
كيف تحمي الطلاءات والدهانات المعادن من التآكل؟
ننتقل الآن إلى الجانب العملي الذي يبحث عنه كل مهندس وكل صاحب منشأة. الإستراتيجيات الهندسية لحماية المعادن من التآكل متعددة ومتنوعة، ولكل منها مجال تطبيق مثالي.
العزل السطحي (Surface Coating) هو الأسلوب الأقدم والأبسط مفهوماً: ضع حاجزاً مادياً بين المعدن والبيئة المسببة للتآكل. الدهانات الصناعية — وخاصة دهانات الإيبوكسي (Epoxy) والبولي يوريثان (Polyurethane) — تُشكّل غشاءً بوليمرياً صلباً ومقاوماً للماء والكيماويات. في خطوط الأنابيب البترولية في المملكة العربية السعودية، تُستخدم طبقات متعددة: بدءاً من طبقة تمهيدية (Primer) غنية بالزنك، ثم طبقة وسطية من الإيبوكسي، وانتهاءً بطبقة خارجية من البولي يوريثان المقاوم للأشعة فوق البنفسجية.
بالإضافة إلى ذلك، يُستخدم الطلاء الزجاجي (Glass Lining) في الخزانات التي تتعامل مع أحماض قوية. هذا الطلاء يُذاب ويُصهر على السطح المعدني الداخلي للخزان، مُشكّلاً طبقة زجاجية ملساء ومقاومة كيميائياً بشكل استثنائي. كما أن البوليمرات الفلوروكربونية مثل التفلون (PTFE) تُستخدم لتبطين المعدات الكيميائية التي تتعرض لبيئات عدوانية جداً.
كيف تعمل الجلفنة بالزنك في حماية الحديد؟

الجلفنة (Galvanization) هي تقنية تغطية الحديد أو الفولاذ بطبقة رقيقة من الزنك. الزنك أنشط كيميائياً من الحديد — أي أنه أكثر ميلاً للتأكسد. فماذا يحدث عملياً؟ حين تُخدش طبقة الزنك ويتكشّف الحديد تحتها، يبدأ الزنك المحيط بالخدش في التآكل تضحوياً بدلاً من الحديد. هذا يعني أن الزنك يحمي الحديد حتى لو تعرّض الطلاء لبعض التلف الميكانيكي.
عملية الجلفنة بالغمس الساخن (Hot-Dip Galvanizing) تتضمن غمس القطعة الفولاذية في حوض زنك مصهور عند درجة حرارة تقارب 450 درجة مئوية. تتشكل سبيكة بينية (Intermetallic Layer) بين الحديد والزنك تُعزّز التصاق الطبقة. هذه التقنية تُستخدم على نطاق واسع في أعمدة الإنارة وحواجز الطرق وأبراج نقل الكهرباء في المملكة. الجدير بالذكر أن عمر طبقة الجلفنة يعتمد بشكل كبير على البيئة: في بيئة ريفية جافة قد تستمر 70 عاماً أو أكثر، بينما في بيئة بحرية صناعية قد لا تتجاوز 20 عاماً.
| وجه المقارنة | الأنود المضحّي (Sacrificial Anode) | التيار القسري (Impressed Current – ICCP) |
|---|---|---|
| مبدأ العمل | معدن أنشط كيميائياً (زنك أو مغنيسيوم) يتآكل بدلاً من الهيكل المحمي | مصدر تيار كهربائي خارجي يدفع إلكترونات إلى الهيكل عبر أنودات خاملة |
| مصدر الطاقة | ذاتي (فرق الجهد الطبيعي بين المعدنين) | خارجي (مُقوّم كهربائي متصل بالتيار الكهربائي) |
| تكلفة التركيب | منخفضة نسبياً | مرتفعة (تتطلب معدات ومراقبة) |
| تكلفة الصيانة | متوسطة (استبدال الأنودات المستهلكة دورياً) | منخفضة إلى متوسطة (مراقبة إلكترونية) |
| نطاق الحماية | محدود (مساحات صغيرة إلى متوسطة) | واسع جداً (مئات الكيلومترات) |
| التحكم في التيار | غير قابل للتعديل | قابل للتعديل والمراقبة عن بُعد |
| خطر الحماية الزائدة | منخفض جداً | موجود (قد يسبب تقصف هيدروجيني) |
| التطبيقات الشائعة | هياكل السفن، سخانات المياه، الأنابيب القصيرة | خطوط أنابيب النفط والغاز الطويلة، المنشآت البحرية الكبرى |
| الاستخدام في السعودية | خزانات المياه المعدنية وسفن الصيد الصغيرة | شبكة أنابيب أرامكو ومحطات التحلية |
| المصدر: AMPP – Association for Materials Protection and Performance | NACE International Standards (SP0169, SP0176) | ||
معلومة عملية مفيدة: إذا كنت تُنشئ مبنى في منطقة ساحلية سعودية، فإن المواصفات السعودية (SASO) والكود السعودي للبناء يشترطان حداً أدنى لسماكة طبقة الجلفنة على حديد التسليح المعرّض للبيئات المالحة. تجاهل هذا الشرط قد يُكلّفك أضعاف ثمن الجلفنة في إصلاحات لاحقة.
ما هي الحماية الكاثودية وكيف تُطبّق على أنابيب النفط والسفن؟

الحماية الكاثودية (Cathodic Protection) هي من أذكى طرق حماية المعادن من التآكل وأكثرها فعالية في التطبيقات الكبيرة. المبدأ بسيط نظرياً: اجعل المعدن المراد حمايته يعمل ككاثود (قطب سالب) في الخلية الكهروكيميائية، وبذلك لن يتآكل. هناك طريقتان لتحقيق ذلك.
الأنود المضحّي (Sacrificial Anode)
في هذه الطريقة، يُربط بالمعدن المراد حمايته قطعة من معدن أنشط كيميائياً — عادةً الزنك أو المغنيسيوم أو سبائك الألومنيوم. هذا “الأنود المضحي” يتآكل بدلاً من الهيكل الأصلي، تماماً كما يضحي الجندي بنفسه لحماية رفاقه. حين ينتهي الأنود المضحي بالكامل، يُستبدل بآخر جديد. هذه الطريقة شائعة في حماية هياكل السفن وصهاريج المياه الساخنة والأنابيب المدفونة القصيرة. إن كنت قد رأيت يوماً قطعاً معدنية صغيرة ملحومة على بدن سفينة تحت خط الماء، فهذه هي الأنودات المضحية.
التيار القسري (Impressed Current)
في المنشآت الكبيرة جداً كخطوط أنابيب النفط والغاز التي تمتد لمئات الكيلومترات، لا تكفي الأنودات المضحية لتغطية كل المساحة. هنا يُستخدم نظام التيار القسري (Impressed Current Cathodic Protection – ICCP). يتكون النظام من مصدر تيار كهربائي مستمر خارجي (مُقوّم كهربائي) يدفع تياراً إلى المعدن عبر أنودات خاملة مصنوعة من الغرافيت أو التيتانيوم أو سبائك السيليكون. هذا التيار يجعل سطح الأنبوب سالباً كهربائياً بالكامل فيمنع أكسدة الحديد. شبكة أنابيب أرامكو السعودية — التي تُعَدُّ من الأكبر عالمياً — تعتمد بشكل واسع على أنظمة الحماية الكاثودية بالتيار القسري، مع أنظمة مراقبة عن بُعد تقيس فرق الجهد على طول الأنبوب باستمرار.
لماذا يقاوم الفولاذ المقاوم للصدأ التآكل؟
هنا نصل إلى واحد من أذكى إستراتيجيات البشرية في مواجهة تآكل المعادن: التلاعب بتركيب السبيكة (Alloying). الحديد النقي يصدأ بسرعة. لكن حين نُضيف إليه الكروم بنسبة لا تقل عن 10.5%، يتشكّل على سطحه غشاء رقيق وغير مرئي من أكسيد الكروم (Cr₂O₃). هذا الغشاء — الذي لا يتجاوز سمكه بضعة ذرات — يتمتع بخواص فريدة: فهو مقاوم كيميائياً، ومتجدد ذاتياً، ومتماسك بشكل لا يسمح بنفاذ الأكسجين أو الرطوبة.
لكن ليس كل الفولاذ المقاوم للصدأ سواء. الفولاذ الأوستنيتي (Austenitic) من فئة 304 و316 يُضاف إليه النيكل والموليبدينوم لتحسين مقاومته في البيئات الحمضية والمالحة. الفئة 316 تحديداً — التي تحتوي على نحو 2% موليبدينوم — تتفوق في مقاومة التآكل النقري الناجم عن أيونات الكلوريد، ولذلك تُستخدم على نطاق واسع في المنشآت البتروكيماوية ومحطات تحلية المياه في المملكة العربية السعودية.
فقد أثبتت دراسة منشورة في مجلة Materials and Corrosion عام 2021 أن إضافة 3% موليبدينوم إلى فولاذ أوستنيتي يرفع درجة حرارة التآكل النقري الحرجة (Critical Pitting Temperature – CPT) بأكثر من 15 درجة مئوية، مما يوسّع نطاق البيئات التي يمكن استخدام هذا الفولاذ فيها بأمان.
اقرأ أيضاً: علم المعادن (Mineralogy): دراسة المعادن وتكوينها
أغرب معلومة في هذا المقال: في عام 2023، طوّر باحثون في معهد ماكس بلانك (Max Planck Institute) في ألمانيا سبيكة فائقة المقاومة للتآكل مكونة من خمسة عناصر بنسب متساوية تقريباً (ما يُعرف بسبائك الإنتروبيا العالية – High-Entropy Alloys). هذه السبيكة أظهرت مقاومة للتآكل تفوق الفولاذ المقاوم للصدأ التقليدي بعشر مرات في بيئة حمض الهيدروكلوريك المركز. هذا الاتجاه البحثي يُعَدُّ من أكثر المجالات إثارة في علم المواد حالياً.
كيف تعمل مثبطات التآكل الكيميائية في البيئات الصناعية؟
مثبطات التآكل (Corrosion Inhibitors) هي مواد كيميائية تُضاف بتراكيز صغيرة إلى البيئة المسببة للتآكل — كالمياه في دورات التبريد أو الوقود في الأنابيب — فتُبطئ معدل التآكل بشكل ملحوظ. تعمل هذه المثبطات بآليات مختلفة:
- المثبطات الأنودية (Anodic Inhibitors): تُشكّل طبقة أكسيدية واقية على مناطق الأنود، مما يمنع تأكسد المعدن. من أمثلتها: الكرومات والنتريت والموليبدات. لكن يجب استخدامها بتراكيز كافية؛ إذ إن التركيز غير الكافي قد يُفاقم التآكل النقري بدلاً من إيقافه.
- المثبطات الكاثودية (Cathodic Inhibitors): تُقلّل سرعة التفاعل عند الكاثود، كمركبات الزنك والكالسيوم التي تترسب على المناطق الكاثودية فتعزلها.
- المثبطات الممتزة (Adsorption Inhibitors): جزيئات عضوية تمتص على سطح المعدن وتُشكّل غشاءً حاجزاً رقيقاً. من أشهرها الأمينات والإيميدازولين المستخدمة في حقول النفط.
في صناعة النفط السعودية، تُضاف مثبطات التآكل بشكل روتيني إلى خطوط إنتاج النفط الخام الذي يحتوي غالباً على ثاني أكسيد الكربون (CO₂) وكبريتيد الهيدروجين (H₂S) — وهما غازان يسببان تآكلاً شرساً للفولاذ الكربوني. اختيار المثبط المناسب يعتمد على درجة الحرارة والضغط ومعدل التدفق وتركيب السوائل، وهو تخصص هندسي قائم بذاته.
اقرأ أيضاً: الكيمياء البيئية: دراسة العمليات الكيميائية في البيئة
ماذا عن واقع التآكل الكيميائي في المملكة العربية السعودية؟
المملكة العربية السعودية تواجه تحديات فريدة في مجال تآكل المعادن لعدة أسباب متضافرة. الموقع الجغرافي يجعل المنشآت الساحلية معرّضة لرذاذ البحر المشبع بالكلوريد. درجات الحرارة المرتفعة صيفاً — التي تتخطى 50 درجة مئوية في بعض المناطق — تُسرّع التفاعلات الكيميائية. البنية الاقتصادية المعتمدة على صناعة النفط والبتروكيماويات تعني وجود بيئات كيميائية عدوانية جداً.
لقد استجابت المملكة لهذه التحديات بشكل لافت. مركز الملك عبدالله للدراسات والبحوث البترولية (KAPSARC) ومراكز البحث التابعة لأرامكو تُجري أبحاثاً متقدمة في مقاومة التآكل. وكذلك تتضمن رؤية 2030 مشاريع بنية تحتية ضخمة — كنيوم والبحر الأحمر — تتطلب حلول حماية من التآكل مبتكرة ومستمرة تراعي البيئة البحرية الحساسة. بالإضافة إلى ذلك، أنشأت الجامعات السعودية برامج بحثية متخصصة في هندسة التآكل، وجامعة الملك فهد للبترول والمعادن تُعَدُّ مركزاً رائداً في هذا المجال إقليمياً.
اقرأ أيضاً: الجيولوجيا البيئية: تقاطع علم الأرض والبيئة
ما هي أحدث التوجهات البحثية في مكافحة التآكل الكيميائي؟
العلم لا يقف ساكناً في مواجهة تآكل المعادن. هناك توجهات بحثية واعدة تُشكّل مستقبل هذا المجال.
الطلاءات النانوية (Nanocoatings) تُمثّل ثورة في عالم حماية المعادن من التآكل. هذه الطلاءات — التي تحتوي على جسيمات نانوية من أكاسيد الزنك أو التيتانيوم أو السيليكا — تُشكّل طبقات فائقة الكثافة وشديدة الالتصاق بسماكة لا تتجاوز بضعة ميكرومترات. أثبتت دراسة منشورة في مجلة Progress in Organic Coatings عام 2023 أن إضافة 2% من جسيمات أكسيد الغرافين النانوية إلى طلاء إيبوكسي رفعت مقاومته للتآكل بنسبة 85% مقارنة بالطلاء التقليدي.
من جهة ثانية، تكتسب الطلاءات ذاتية الشفاء (Self-Healing Coatings) اهتماماً متزايداً. هذه الطلاءات تحتوي على كبسولات دقيقة مملوءة بمادة إصلاح. حين يحدث خدش في الطلاء، تنفجر الكبسولات وتُحرّر مادة الإصلاح التي تسد الشق تلقائياً قبل أن يصل التآكل إلى المعدن. هذا المفهوم مستوحى من آلية شفاء الجروح في الجسم البشري.
وبالتالي فإن مستقبل مكافحة التآكل الكيميائي للفلزات يتجه نحو حلول أذكى وأكثر كفاءة واستمرارية، تُقلّل الحاجة إلى الصيانة الدورية المكلفة وتُطيل عمر المنشآت بشكل جذري.
اقرأ أيضاً: النانوتكنولوجيا (Nanotechnology): المفهوم، التطبيقات، والمستقبل
أسئلة شائعة عن التآكل الكيميائي للفلزات
الخاتمة
التآكل الكيميائي للفلزات ظاهرة طبيعية متجذرة في قوانين الديناميكا الحرارية، لا يمكن إلغاؤها تماماً لكن يمكن إبطاؤها والسيطرة عليها. من صدأ الحديد البسيط في سياج حديقتك إلى التآكل النقري الخبيث في أنابيب النفط العملاقة، يظل هذا العدو الصامت يلتهم ثرواتنا المعدنية بمليارات الدولارات سنوياً. لكن الخبر الجيد هو أن ترسانة الحماية المتاحة لنا اليوم — من الجلفنة والحماية الكاثودية إلى الطلاءات النانوية والسبائك المتقدمة — قادرة على ترويض هذا العدو إلى حد بعيد.
لقد حاولنا في هذا المقال أن نضع بين يديك صورة شاملة ودقيقة لكل جوانب أسباب التآكل الكيميائي للمعادن وأنواعه وطرق الوقاية منه. المعرفة هي خط الدفاع الأول، واختيار الحل المناسب للبيئة المناسبة هو ما يصنع الفارق بين منشأة تدوم عقوداً وأخرى تنهار في سنوات.
حقيقة ختامية للتأمل: طبقة الصدأ التي تتقشر من قطعة حديد ليست مجرد “أوساخ” — إنها الحديد نفسه وقد عاد إلى حالته الطبيعية كأكسيد. كل جرام من الصدأ يعني جراماً مفقوداً من المعدن. حماية المعادن ليست رفاهية، بل هي حفاظ على موارد الأرض وأمان البنى التحتية.
برأيكم، ما أكثر أنواع التآكل شيوعاً في منطقتكم، وهل اتخذتم إجراءات وقائية كافية لحماية منشآتكم ومقتنياتكم المعدنية؟
⚠️ تنبيه مهم وإخلاء مسؤولية
المعلومات الواردة في هذا المقال مُعَدَّة لأغراض تعليمية وتثقيفية فقط، ولا تُغني عن الاستشارة الهندسية المتخصصة. إن التطبيقات العملية لحماية المعادن من التآكل تتطلب تقييماً ميدانياً دقيقاً يراعي الظروف البيئية والتشغيلية الخاصة بكل مشروع. لا يتحمل موقع خلية أي مسؤولية عن أي قرارات هندسية أو فنية تُتخذ بناءً على محتوى هذا المقال دون الرجوع إلى مختصين معتمدين. يُنصح دائماً بالتواصل مع مهندسي مواد وتآكل مُعتمدين من جهات مثل AMPP (الجمعية الأمريكية لحماية المواد والأداء) قبل اتخاذ أي إجراء عملي.
🔍 بيان المصداقية والشفافية
اعتمد فريق التحرير في موقع خلية في إعداد هذا المقال على دراسات محكّمة منشورة في مجلات علمية مرموقة (Corrosion Science, npj Materials Degradation, Progress in Organic Coatings)، وتقارير رسمية صادرة عن مؤسسات دولية معتمدة (AMPP, NACE International, ASM International)، وكتب مرجعية كلاسيكية مُعتمدة في برامج هندسة المواد الجامعية. لا يحتوي هذا المقال على إعلانات مدفوعة ولا يتضمن ترويجاً لمنتجات تجارية. جميع المعلومات الواردة مبنية على أحدث الأدلة العلمية المتاحة حتى عام 2025.
📋 المعايير والبروتوكولات العلمية المُعتمدة
تستند المعلومات الهندسية في هذا المقال إلى المعايير والبروتوكولات التالية:
- NACE SP0169-2013: معيار الحماية الكاثودية للأنابيب المدفونة والمغمورة — صادر عن AMPP.
- ASTM G1-03 (2017): الممارسات المعيارية لتحضير وتنظيف واختبار عينات التآكل — صادر عن ASTM International.
- ISO 12944 (2018): معيار حماية الهياكل الفولاذية بالدهانات — صادر عن المنظمة الدولية للتقييس (ISO).
- ASTM A123/A123M (2017): المواصفات المعيارية للجلفنة بالغمس الساخن — صادر عن ASTM International.
- NACE MR0175/ISO 15156 (2020): متطلبات المواد المعدنية في بيئات إنتاج النفط والغاز الحاوية على كبريتيد الهيدروجين.
جرت مراجعة هذا المقال وفق بروتوكولات التدقيق العلمي في موقع خلية
المراجع والمصادر
الدراسات والأوراق البحثية
- Koch, G. H., Brongers, M. P., Thompson, N. G., Virmani, Y. P., & Payer, J. H. (2016). “International Measures of Prevention, Application, and Economics of Corrosion Technologies Study.” NACE International IMPACT Report.
https://impact.nace.org/documents/Nace-International-Report.pdf
تقرير شامل يُقدّر التكلفة العالمية للتآكل ويُقيّم فعالية تقنيات الحماية المختلفة. - Qian, B., Hou, B., & Zheng, M. (2019). “The inhibition effect of tannic acid on mild steel corrosion in seawater wet/dry cyclic conditions.” Corrosion Science, 150, 16–27. DOI: 10.1016/j.corsci.2019.01.018
دراسة تبحث في مثبطات التآكل الطبيعية وفعاليتها في بيئات بحرية مشابهة لبيئة الخليج العربي. - Hou, B., Li, X., Ma, X., Du, C., Zhang, D., Zheng, M., … & Zhang, F. (2017). “The cost of corrosion in China.” npj Materials Degradation, 1(1), 4. DOI: 10.1038/s41529-017-0005-2
دراسة منشورة في مجلة تابعة لـ Nature تُقدّر تكاليف التآكل في اقتصاد صناعي كبير. - Ramezanzadeh, B., Niroumandrad, S., Ahmadi, A., Mahdavian, M., & Moghadam, M. M. (2016). “Enhancement of barrier and corrosion protection performance of an epoxy coating through wet transfer of amino functionalized graphene oxide.” Corrosion Science, 103, 283–304. DOI: 10.1016/j.corsci.2015.11.033
بحث رائد في استخدام أكسيد الغرافين لتعزيز مقاومة الطلاءات الإيبوكسية للتآكل. - Abdeen, D. H., El Hachach, M., Koc, M., & Atieh, M. A. (2019). “A Review on the Corrosion Behaviour of Nanocoatings on Metallic Substrates.” Materials, 12(2), 210. DOI: 10.3390/ma12020210
مراجعة شاملة للطلاءات النانوية المضادة للتآكل. - Shi, H., Liu, F., & Han, E. H. (2021). “The corrosion behavior of zinc-rich epoxy primer/acrylic polyurethane topcoat systems in NaCl solution.” Progress in Organic Coatings, 152, 106133. DOI: 10.1016/j.porgcoat.2021.106133
دراسة تطبيقية على أنظمة الطلاء متعددة الطبقات في البيئات المالحة.
الجهات الرسمية والمنظمات
- NACE International (now AMPP). (2021). “Corrosion Basics — An Introduction.” Association for Materials Protection and Performance.
https://www.ampp.org
المرجع الأساسي لمهندسي التآكل عالمياً، يوفر معايير ومواصفات الحماية. - National Science Foundation (NSF). (2023). “Sustainable Solutions to Corrosion.”
https://www.nsf.gov
مبادرات بحثية أمريكية لتطوير حلول مستمرة لمكافحة التآكل. - Saudi Standards, Metrology and Quality Organization (SASO). “Saudi Building Code — Corrosion Protection Requirements.”
https://www.saso.gov.sa
المواصفات السعودية لحماية حديد التسليح والمنشآت من التآكل. - World Corrosion Organization (WCO). (2023). “Corrosion Awareness Day Reports.”
https://corrosion.org
تقارير سنوية عن حالة التآكل عالمياً وتكاليفه. - ASM International. (2022). “ASM Handbook, Volume 13A: Corrosion: Fundamentals, Testing, and Protection.”
https://www.asminternational.org
الموسوعة الهندسية المرجعية في أساسيات التآكل وطرق الاختبار.
الكتب والموسوعات العلمية
- Jones, D. A. (1996). Principles and Prevention of Corrosion (2nd ed.). Prentice Hall.
كتاب مرجعي كلاسيكي يُدرّس في معظم برامج هندسة المواد حول العالم. - Revie, R. W., & Uhlig, H. H. (2011). Uhlig’s Corrosion Handbook (3rd ed.). Wiley.
الموسوعة الأشمل في علم التآكل، تغطي جميع الفلزات والبيئات. - Fontana, M. G. (2005). Corrosion Engineering (3rd ed.). McGraw-Hill.
من أوائل الكتب التي ربطت بين علم التآكل والتطبيقات الهندسية العملية.
مقالات علمية مبسطة
- Schmitt, R. (2009). “Metallic Corrosion.” Scientific American.
https://www.scientificamerican.com
مقال مبسّط يشرح أساسيات التآكل الكيميائي لجمهور غير متخصص.
قراءات إضافية ومصادر للتوسع
- Marcus, P. (Ed.). (2012). Corrosion Mechanisms in Theory and Practice (3rd ed.). CRC Press.
لماذا نقترح عليك قراءته؟ هذا الكتاب يُقدّم شرحاً نظرياً عميقاً لآليات التآكل على المستوى الذري والإلكتروني، وهو مثالي لمن يرغب في فهم “لماذا” يحدث التآكل وليس فقط “كيف”. - Frankel, G. S. (1998). “Pitting Corrosion of Metals: A Review of the Critical Factors.” Journal of The Electrochemical Society, 145(6), 2186–2198. DOI: 10.1149/1.1838615
لماذا نقترح عليك قراءته؟ هذه الورقة البحثية المرجعية تُعَدُّ “أم المراجعات” في موضوع التآكل النقري. أي باحث جاد في هذا المجال لا بد أن يمر بها. - Shreir, L. L., Jarman, R. A., & Burstein, G. T. (Eds.). (1994). Corrosion: Metal/Environment Reactions (3rd ed.). Butterworth-Heinemann.
لماذا نقترح عليك قراءته؟ موسوعة من مجلدين تغطي كل تفاعلات المعدن مع البيئة بتفصيل لا يوجد في أي مصدر آخر. مرجع لا غنى عنه لطلاب الدراسات العليا.
إن كنت مهندساً أو طالباً أو حتى صاحب منشأة تبحث عن فهم أعمق لظاهرة تآكل المعادن، فإننا ندعوك لمشاركة هذا المقال مع زملائك المهتمين، وإضافة تعليقك أدناه بتجربتك الشخصية مع التآكل أو أي سؤال يدور في ذهنك. معاً يمكننا بناء مجتمع معرفي عربي أقوى في هذا المجال الحيوي.







