ما هي الوراثة السائدة: وكيف تنتقل الصفات من جيل لآخر؟
لماذا تظهر بعض الصفات في كل جيل بينما تختفي أخرى؟

الوراثة السائدة هي نمط وراثي يظهر فيه تأثير الأليل السائد (Dominant Allele) على النمط الظاهري حتى مع وجود نسخة واحدة فقط منه. تنتقل الصفات السائدة من جيل لآخر دون تخطٍّ؛ إذ يكفي أن يحمل أحد الوالدين الجين السائد لتظهر الصفة في نسله. تشمل الأمثلة الشائعة لون العيون البني والغمازات وبعض الأمراض الوراثية كداء هنتنغتون.
هل تساءلت يوماً لماذا ورثت عيوناً بنية مثل والدتك بينما يملك أخوك عيوناً زرقاء كجدتك؟ أو لماذا تظهر غمازات خدك الساحرة في كل صورة عائلية منذ ثلاثة أجيال؟ إن كنت طالباً في كلية الطب أو الأحياء، أو أباً قلقاً يحاول فهم نتائج فحص جيني لطفله، فأنت في المكان الصحيح. ستجد هنا إجابات علمية واضحة تشرح آلية انتقال الصفات الوراثية، وستفهم لماذا تسيطر بعض الجينات على غيرها. لقد صُمِّم هذا المحتوى ليكون مرجعك النهائي في فهم الوراثة السائدة من الألف إلى الياء.
في هذا المقال ستعرف
- ما هي الوراثة السائدة: نمط وراثي يكفي فيه وجود نسخة واحدة من الأليل السائد لتظهر الصفة، وكيف تختلف عن الوراثة المتنحية والسيادة المشتركة.
- كيفية التنبؤ بالصفات الوراثية: استخدام مربع بانيت لحساب احتمالات انتقال الصفات السائدة، وقراءة شجرة العائلة الوراثية لتحديد نمط الوراثة.
- أشهر الأمراض الوراثية السائدة: مرض هنتنغتون، متلازمة مارفان، وفرط كوليسترول الدم العائلي، وأهمية الاستشارة الوراثية في الوقاية منها.
مثال من واقع الحياة: عائلة أحمد والغمازات الغامضة
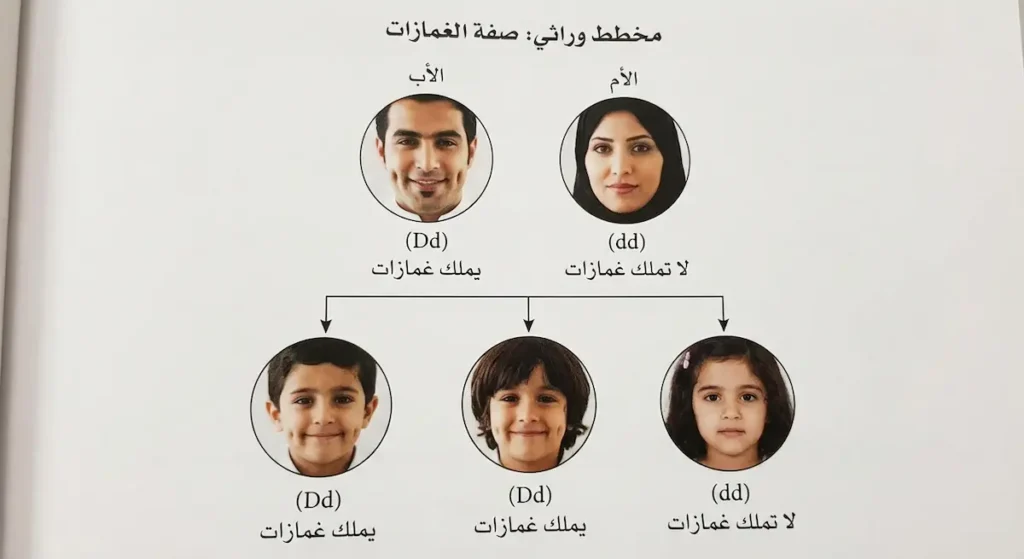
تخيل عائلة أحمد المقيمة في عمّان. الأب أحمد يملك غمازات واضحة في خديه، بينما الأم سارة لا تملكها. أنجبا ثلاثة أطفال: اثنان منهم يملكان غمازات والثالث لا يملكها. كيف نفسر ذلك؟
الغمازات صفة سائدة، ولنرمز لها بالحرف الكبير (D). غياب الغمازات صفة متنحية نرمز لها بالحرف الصغير (d). الأم سارة لا تملك غمازات، وهذا يعني أن نمطها الجيني هو (dd) حتماً. الأب أحمد يملك غمازات، لكن بما أن أحد أطفاله لا يملكها، فهذا يعني أنه أعطاه نسخة (d). إذاً الأب ليس نقياً (DD) بل هجين (Dd).
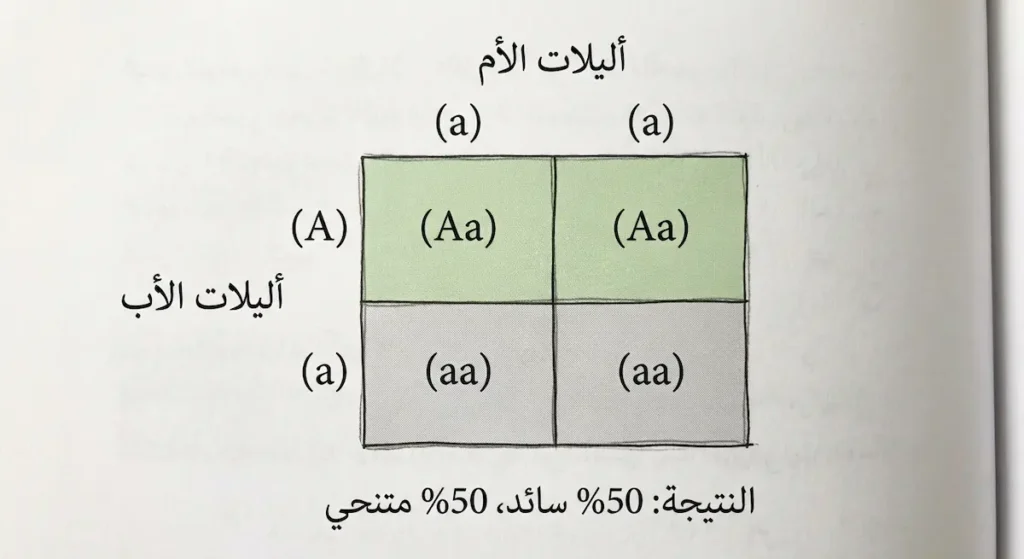
عند تزاوج (Dd) مع (dd)، تكون النتائج المتوقعة: 50% من الأبناء يحملون (Dd) ويملكون غمازات، و50% يحملون (dd) ولا يملكونها. هذا بالضبط ما حدث مع عائلة أحمد! فقد استطعنا باستخدام مربع بانيت (Punnett Square) التنبؤ باحتمالات ظهور الصفة في الجيل التالي.
ما هي الوراثة السائدة وما مفهومها الأساسي؟
لفهم الوراثة السائدة، علينا أولاً استيعاب بعض المصطلحات الجينية الأساسية. كل إنسان يحمل نسختين من كل جين، واحدة من الأب وأخرى من الأم. هاتان النسختان تُسمَّيان “أليلين” (Alleles). قد يكون الأليلان متماثلين، وقد يكونان مختلفين.
عندما يكون الأليلان مختلفين، تبرز قوة أحدهما على الآخر. الأليل الذي “يفرض” تأثيره على النمط الظاهري يُسمَّى الأليل السائد (Dominant Allele)، بينما الأليل الذي يختبئ تأثيره يُسمَّى الأليل المتنحي (Recessive Allele). في الوراثة السائدة، يكفي وجود نسخة واحدة من الأليل السائد لتظهر الصفة بوضوح.
ما الفرق بين النمط الجيني والنمط الظاهري؟
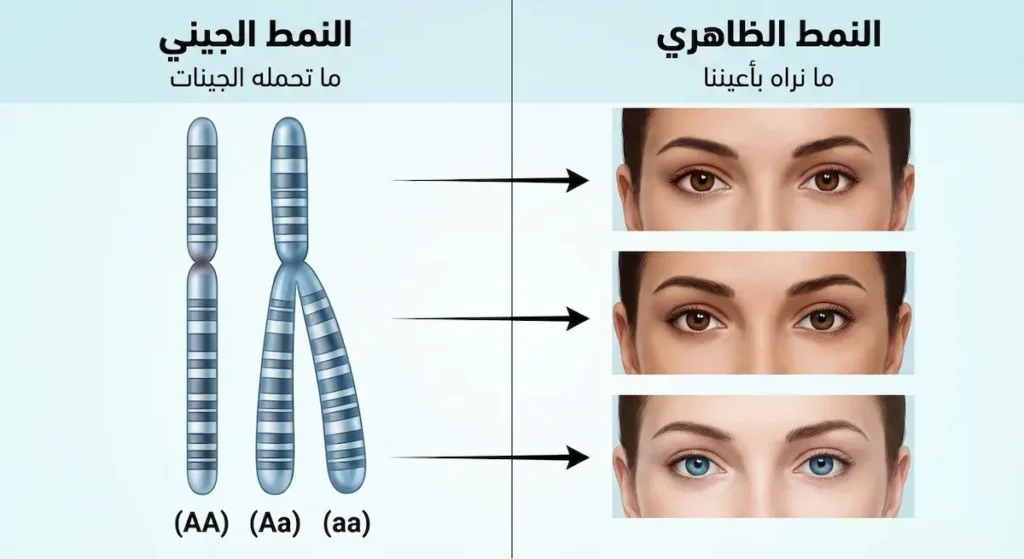
النمط الجيني (Genotype) هو التركيب الجيني الداخلي للفرد. بكلمات أبسط: ما تحمله كروموسوماتك من أليلات. قد يكون الشخص متماثل الزيجوت (Homozygous) إذا حمل أليلين متطابقين (AA أو aa)، أو متغاير الزيجوت (Heterozygous) إذا حمل أليلين مختلفين (Aa).
النمط الظاهري (Phenotype) هو ما نراه بأعيننا: لون الشعر، طول القامة، وجود الغمازات. من ناحية أخرى، قد يتشابه النمط الظاهري لشخصين رغم اختلاف نمطهما الجيني. مثلاً: شخص بنمط جيني (AA) وآخر بنمط (Aa) كلاهما سيملكان نفس الصفة السائدة ظاهرياً.
اقرأ أيضاً: الوراثة: دليلك الشامل لفهم علم الجينات والصفات الموروثة
لماذا يُطلق عليها “السيادة” في علم الوراثة؟
مصطلح “السيادة” (Dominance) يصف قدرة أليل على إخفاء تأثير أليل آخر. تخيل الأمر كمباراة ملاكمة بين بطلين: الأليل السائد هو الفائز الذي يظهر على منصة التتويج (النمط الظاهري)، بينما الأليل المتنحي يبقى خلف الكواليس رغم وجوده.
الجدير بالذكر أن مصطلح “سائد” لا يعني “أفضل” أو “أقوى بيولوجياً”. إنه مجرد وصف لطريقة ظهور الصفة. كثير من الأمراض الوراثية الخطيرة تنتقل بنمط سائد، فهل نقول إنها “أفضل”؟ بالتأكيد لا.
معلومة سريعة
اكتشف العالم النمساوي غريغور مندل (Gregor Mendel) مبادئ الوراثة السائدة في ستينيات القرن التاسع عشر من خلال تجاربه على نبات البازلاء. لكن عمله ظل مجهولاً حتى أعاد ثلاثة علماء اكتشافه بشكل مستقل عام 1900.
كيف تعمل الوراثة السائدة على المستوى الجزيئي؟
هنا نغوص أعمق مما تجده في معظم المقالات السطحية. السؤال الحقيقي: لماذا يتغلب أليل على آخر؟ ما الآلية الجزيئية وراء ذلك؟
الإجابة تكمن في البروتينات. كل جين يحمل تعليمات لصنع بروتين معين. في كثير من حالات السيادة التامة، الأليل السائد ينتج بروتيناً وظيفياً، بينما الأليل المتنحي إما لا ينتج شيئاً أو ينتج بروتيناً معطلاً.
خذ مثال مرض هنتنغتون (Huntington’s Disease): الأليل الطافر (السائد) ينتج بروتيناً سامّاً يتراكم في خلايا الدماغ. حتى لو كان الأليل الآخر سليماً وينتج بروتيناً طبيعياً، فإن البروتين السام الناتج عن الأليل الطافر يكفي لإحداث المرض. هذا ما يُسمَّى بآلية “الكسب السام للوظيفة” (Gain of Toxic Function).
اقرأ أيضاً: الحمض النووي (DNA): التركيب، الوظيفة، والأهمية
ما هي السيادة التامة وكيف تختلف عن غير التامة؟
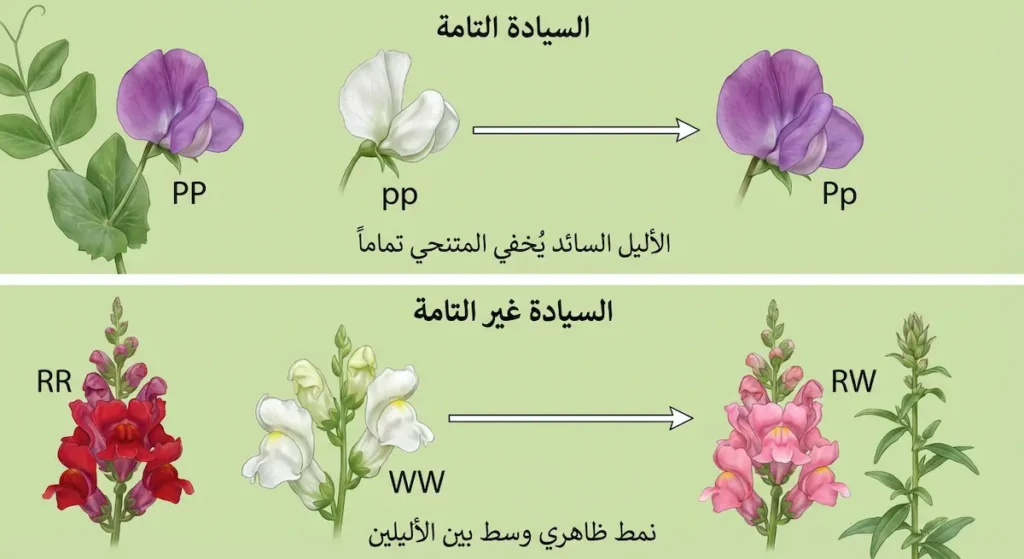
السيادة التامة (Complete Dominance) هي الحالة “الكلاسيكية” التي درسها مندل. فيها، الأليل السائد يُخفي تماماً تأثير الأليل المتنحي. الفرد متغاير الزيجوت (Aa) يبدو مطابقاً تماماً للفرد متماثل الزيجوت السائد (AA).
السيادة غير التامة (Incomplete Dominance) قصة مختلفة. هنا، لا يستطيع أي أليل فرض سيطرته الكاملة. النتيجة؟ نمط ظاهري وسط بين الأليلين. المثال الشهير: زهرة فم الأسد (Snapdragon). تزاوج زهرة حمراء (RR) مع بيضاء (WW) ينتج زهوراً وردية (RW)! اللون الوردي ليس أحمر ولا أبيض، بل مزيج بينهما.
من جهة ثانية، تختلف الوراثة السائدة عن السيادة المشتركة اختلافاً جوهرياً في آلية التعبير الجيني.
| وجه المقارنة | السيادة التامة | السيادة غير التامة | السيادة المشتركة |
|---|---|---|---|
| التعريف | الأليل السائد يُخفي المتنحي تماماً | لا يسيطر أي أليل، يظهر نمط وسط | كلا الأليلين يُعبِّران عن نفسيهما معاً |
| النمط الظاهري للهجين (Aa) | مطابق للسائد النقي (AA) | وسط بين الأليلين | يُظهر صفات كلا الأليلين |
| نسبة الجيل الثاني (F2) | 3 : 1 | 1 : 2 : 1 | 1 : 2 : 1 |
| المثال الكلاسيكي | لون أزهار البازلاء | لون زهرة فم الأسد | فصائل الدم (AB) |
| مستوى البروتين | بروتين واحد يكفي للوظيفة | كمية البروتين تؤثر على الصفة | كلا البروتينين يعملان بشكل مستقل |
ما هي السيادة المشتركة وما علاقتها بفصائل الدم؟
السيادة المشتركة (Co-dominance) حالة فريدة يظهر فيها كلا الأليلين بشكل كامل ومتزامن. لا أحد يختبئ ولا أحد يسيطر؛ كلاهما يعملان معاً.
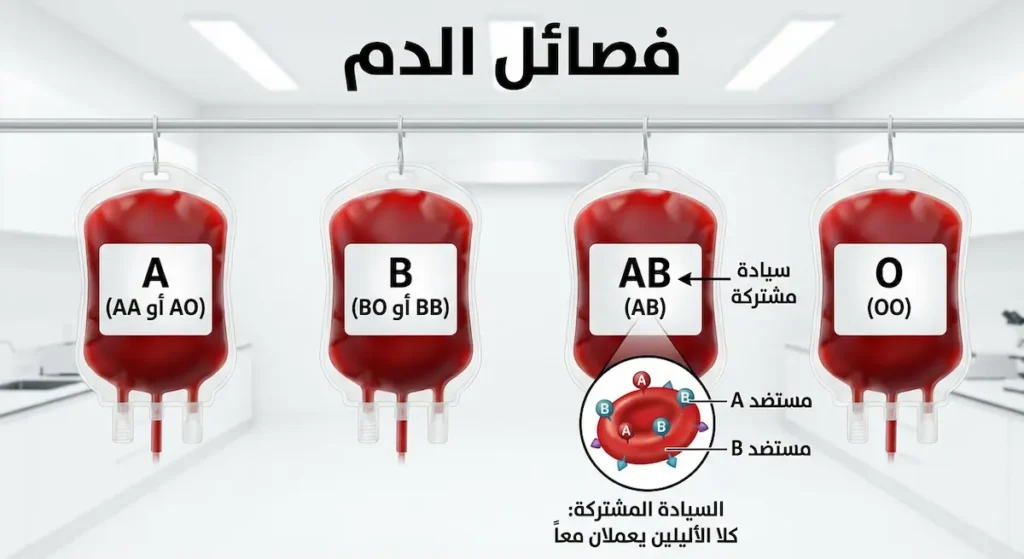
أشهر مثال؟ فصائل الدم! الأليل (A) والأليل (B) كلاهما سائد على الأليل (O). لكن عندما يجتمعان معاً (AB)، لا يتغلب أحدهما على الآخر. بل تظهر كلتا المستضدتين (A وB) على سطح خلايا الدم الحمراء. وهذا يفسر لماذا فصيلة (AB) تختلف عن (A) وعن (B)؛ إذ إنها تحمل صفات كليهما.
هل تعلم؟
فصيلة الدم (AB) هي الأندر عالمياً؛ إذ لا تتجاوز نسبتها 3% من سكان العالم. بينما فصيلة (O) هي الأكثر شيوعاً وتصل نسبتها إلى 45% في بعض المجتمعات العربية.
ما هي أنواع الوراثة السائدة المختلفة؟
ليست كل أنماط الوراثة السائدة متشابهة. تختلف باختلاف موقع الجين: هل هو على الكروموسومات الجسمية (الـ 22 زوجاً الأولى) أم على الكروموسومات الجنسية (X وY)؟
كيف تعمل الوراثة الجسدية السائدة؟
الوراثة الجسدية السائدة (Autosomal Dominant Inheritance) هي النمط الأكثر شيوعاً. الجين المسؤول يقع على أحد الكروموسومات الجسمية (1-22)، وليس على الكروموسومات الجنسية.
السمات المميزة لهذا النمط:
- الظهور في كل جيل: الصفة لا تتخطى الأجيال. إذا كان أحد الوالدين مصاباً، فهناك احتمال ظهورها في أبنائه مباشرة.
- التساوي بين الجنسين: الذكور والإناث يتأثرون بنسب متساوية؛ لأن الجين ليس مرتبطاً بالجنس.
- انتقال من أي والد: الأب المصاب أو الأم المصابة يمكن لكليهما نقل الجين لأبنائهما.
- احتمال الانتقال 50%: إذا كان أحد الوالدين متغاير الزيجوت (Aa) والآخر سليم (aa)، فإن كل طفل لديه احتمال 50% لوراثة الصفة.
أمثلة على أمراض تنتقل بهذا النمط: مرض هنتنغتون، متلازمة مارفان، عدم تصنع الغضروف (القزامة)، وفرط كوليسترول الدم العائلي.
| الخاصية | الوراثة الجسدية السائدة | الوراثة السائدة المرتبطة بـ X |
|---|---|---|
| موقع الجين | الكروموسومات 1-22 | الكروموسوم X |
| التأثر حسب الجنس | متساوٍ بين الذكور والإناث | قد يكون أشد في الذكور |
| انتقال من الأب المصاب | 50% للأبناء من الجنسين | 100% للبنات، 0% للأبناء الذكور |
| انتقال من الأم المصابة | 50% للأبناء من الجنسين | 50% للأبناء من الجنسين |
| مثال | مرض هنتنغتون | متلازمة ريت |
| الشيوع | أكثر شيوعاً | نادرة نسبياً |
ما خصائص الوراثة السائدة المرتبطة بالجنس؟
الوراثة السائدة المرتبطة بالكروموسوم X نادرة نسبياً. في هذا النمط، الجين السائد يقع على الكروموسوم X. ما يميز هذا النمط أنه قد يكون أشد خطورة على الذكور أحياناً.
لماذا؟ الذكر يحمل كروموسوماً X واحداً فقط (XY). إذا ورث الأليل السائد المُسبِّب للمرض على كروموسومه X الوحيد، فإنه سيُصاب حتماً. بينما الأنثى تحمل كروموسومين X، وقد يُخفِّف الكروموسوم X السليم من حدة الأعراض أحياناً.
مثال مهم: متلازمة ريت (Rett Syndrome) مرتبطة بالكروموسوم X وتُظهر نمطاً سائداً. معظم الحالات تظهر في الإناث؛ لأن الذكور الذين يرثون الطفرة غالباً لا يبقون على قيد الحياة.
حقيقة مدهشة
في بعض الأمراض المرتبطة بالكروموسوم X السائدة، مثل نقص الفوسفات المرتبط بالكروموسوم X، الأب المصاب ينقل المرض لجميع بناته ولا ينقله لأي من أبنائه الذكور. السبب؟ الأب يُعطي أبناءه الذكور الكروموسوم Y فقط!
كيف نستخدم مربع بانيت لحساب احتمالات الوراثة السائدة؟
مربع بانيت (Punnett Square) أداة بسيطة لكنها قوية جداً. اخترعها عالم الوراثة البريطاني ريجينالد بانيت (Reginald Punnett) في بدايات القرن العشرين. تُساعدنا هذه الأداة في التنبؤ باحتمالات ظهور الصفات في الأجيال القادمة.
دعني أشرح لك ثلاث حالات تزاوج مختلفة:
الحالة الأولى: تزاوج سائد نقي (AA) مع متنحٍّ (aa)
| a | a | |
|---|---|---|
| A | Aa | Aa |
| A | Aa | Aa |
✅ النتيجة: 100% من الأبناء (Aa) – جميعهم يحملون الصفة السائدة
النتيجة: 100% من الأبناء متغايرو الزيجوت (Aa). جميعهم يحملون الصفة السائدة ظاهرياً.
الحالة الثانية: تزاوج سائد هجين (Aa) مع سائد هجين (Aa)
| A | a | |
|---|---|---|
| A | AA | Aa |
| a | Aa | aa |
📊 النتيجة – نسبة مندل الشهيرة 3:1
■ 75% صفة سائدة (25% AA + 50% Aa) | ■ 25% صفة متنحية (aa)
النتيجة: 75% يحملون الصفة السائدة (25% AA + 50% Aa)، و25% متنحون (aa). هذه النسبة الشهيرة 3:1 التي اكتشفها مندل.
الحالة الثالثة: تزاوج سائد هجين (Aa) مع متنحٍّ (aa)
| a | a | |
|---|---|---|
| A | Aa | Aa |
| a | aa | aa |
🔬 النتيجة – التهجين الاختباري (Test Cross)
■ 50% صفة سائدة (Aa) | ■ 50% صفة متنحية (aa)
النتيجة: 50% يحملون الصفة السائدة (Aa)، و50% متنحون (aa). هذا ما يُسمَّى بالتهجين الاختباري (Test Cross).
| الحالة | نمط الوالد الأول | نمط الوالد الثاني | نسبة الصفة السائدة | نسبة الصفة المتنحية |
|---|---|---|---|---|
| الأولى | AA (سائد نقي) | aa (متنحي) | 100% | 0% |
| الثانية | Aa (هجين) | Aa (هجين) | 75% | 25% |
| الثالثة | Aa (هجين) | aa (متنحي) | 50% | 50% |
جرّب بنفسك: استخدم حاسبة مربع بانيت التفاعلية لحساب احتمالات أبنائك!
حاسبة مربع بانيت التفاعلية
اختر النمط الجيني للوالدين واحسب احتمالات الأبناء
اقرأ أيضاً: نظرية الاحتمالات: الأساس، القواعد، والتطبيقات
ما الفرق بين الوراثة السائدة والوراثة المتنحية؟
هذا السؤال يطرحه كل طالب أحياء. إليك مقارنة شاملة:
| وجه المقارنة | الوراثة السائدة | الوراثة المتنحية |
|---|---|---|
| عدد النسخ المطلوبة لظهور الصفة | نسخة واحدة تكفي | نسختان ضروريتان |
| الرمز المستخدم | حرف كبير (A, B, D) | حرف صغير (a, b, d) |
| الظهور في الأجيال | تظهر في كل جيل دون تخطٍّ | قد تتخطى أجيالاً كاملة |
| الحامل الصامت | لا يوجد (الصفة تظهر دائماً) | موجود (Aa يحمل دون أن تظهر عليه) |
| النمط الجيني للمصاب | AA أو Aa | aa فقط |
| مثال مرضي | مرض هنتنغتون | التليف الكيسي |
| مثال صفة طبيعية | الغمازات | الشعر الأحمر |
من الأمور التي تُربك الطلاب: الفرد متغاير الزيجوت (Aa). في الوراثة السائدة، هذا الفرد يُظهر الصفة السائدة. لكنه أيضاً “ناقل” للأليل المتنحي ويمكنه توريثه لأبنائه. هذا يفسر كيف قد يُنجب أبوان بنيّا العينين طفلاً أزرق العينين!
توقف للحظة
الفرق بين “السائد” و”المتنحي” ليس فرقاً في القوة أو الأفضلية البيولوجية. إنه فقط وصف لكيفية تعبير الجينات عن نفسها. أليل فقر الدم المنجلي (Sickle Cell) متنحٍّ، لكن حمله يوفر مقاومة ضد الملاريا!
ما أشهر الأمراض والصفات المرتبطة بالوراثة السائدة؟
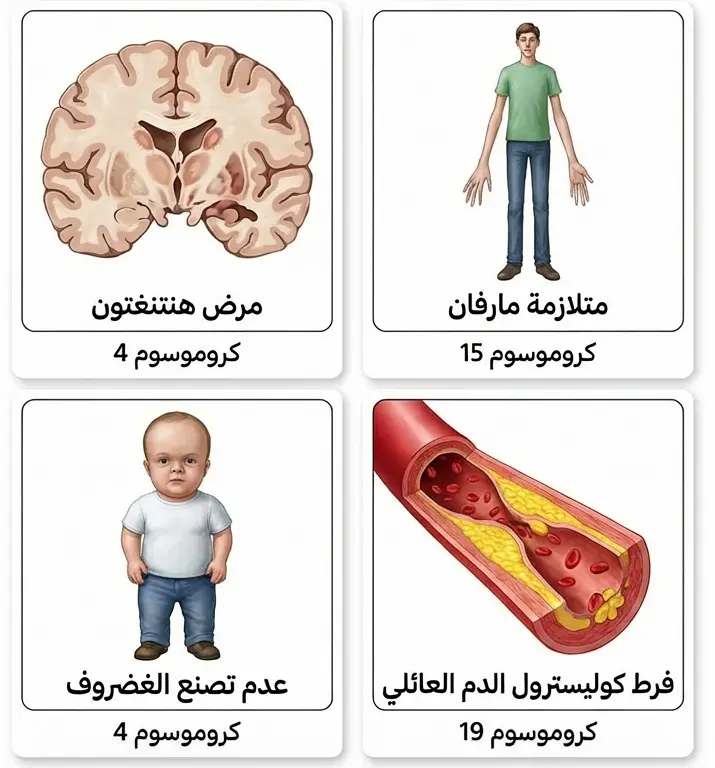
مرض هنتنغتون (Huntington’s Disease)
مرض عصبي تنكسي يصيب الدماغ. تبدأ أعراضه عادةً بين سن 30 و50 عاماً. تشمل الأعراض حركات لا إرادية، تدهور معرفي، وتغيرات نفسية. المأساة أن كثيراً من المصابين يكتشفون حملهم للجين بعد إنجاب أطفال قد يكونون ورثوه.
الجين المسؤول (HTT) يقع على الكروموسوم الرابع. الطفرة تتمثل في تكرار زائد لثلاثية النيوكليوتيدات CAG. كلما زاد عدد التكرارات، ظهرت الأعراض في سن أصغر.
اقرأ أيضاً: التنكس العصبي: ما أسبابه وكيف يمكن الوقاية منه؟
متلازمة مارفان (Marfan Syndrome)
اضطراب يصيب النسيج الضام في الجسم. المصابون غالباً طوال القامة، بأطراف وأصابع طويلة جداً. لكن الخطر الحقيقي يكمن في القلب والأوعية الدموية؛ إذ قد يتمدد الشريان الأورطي ويتمزق.
الجين المسؤول (FBN1) يقع على الكروموسوم 15. يُقدَّر أن شخصاً واحداً من كل 5000 يُصاب بهذه المتلازمة عالمياً. كثير من الرياضيين الطوال اكتُشفت إصابتهم بها بعد فحوصات روتينية.
عدم تصنع الغضروف (Achondroplasia)
الشكل الأكثر شيوعاً للقزامة. يتميز المصابون بقصر الأطراف مع جذع طبيعي الحجم تقريباً. السبب طفرة في جين (FGFR3) على الكروموسوم الرابع.
المثير أن نحو 80% من الحالات ناتجة عن طفرات جديدة (De Novo Mutations)؛ أي أن الوالدين سليمان لكن الطفرة حدثت تلقائياً في البويضة أو الحيوان المنوي.
كثرة الأصابع (Polydactyly)
وجود أصبع إضافي في اليد أو القدم. صفة سائدة شائعة نسبياً في بعض المجتمعات. الطريف أنها كانت منتشرة في بعض العائلات الملكية الأوروبية تاريخياً!
فرط كوليسترول الدم العائلي (Familial Hypercholesterolemia)
اضطراب يُسبِّب ارتفاعاً شديداً في مستويات الكوليسترول منذ الولادة. يزيد خطر الإصابة بأمراض القلب المبكرة بشكل كبير. يُقدَّر أن شخصاً واحداً من كل 250 يحمل هذا الاضطراب، مما يجعله من أكثر الاضطرابات الوراثية شيوعاً.
| المرض | الكروموسوم | الجين المسؤول | نسبة الانتشار | أبرز الأعراض |
|---|---|---|---|---|
| مرض هنتنغتون | 4 | HTT | 1 : 10,000 | حركات لا إرادية، تدهور معرفي |
| متلازمة مارفان | 15 | FBN1 | 1 : 5,000 | طول مفرط، مشاكل قلبية |
| عدم تصنع الغضروف | 4 | FGFR3 | 1 : 25,000 | قصر الأطراف، قصر القامة |
| فرط كوليسترول الدم العائلي | 19 | LDLR | 1 : 250 | ارتفاع شديد في الكوليسترول |
| الورم الليفي العصبي (النوع 1) | 17 | NF1 | 1 : 3,000 | بقع جلدية، أورام عصبية |
هل لديك تاريخ عائلي؟ استخدم هذه الأداة للتنبؤ باحتمالية ظهور الصفة في أبنائك
هل ستظهر الصفة في الأبناء؟
أداة للتنبؤ باحتمالية ظهور الصفات الوراثية
معلومة صادمة
في العالم العربي، ترتفع نسب بعض الأمراض الوراثية بسبب زواج الأقارب الشائع في مجتمعاتنا. دراسة نُشرت عام 2022 في مجلة Journal of Community Genetics أظهرت أن معدل زواج الأقارب يتجاوز 40% في بعض الدول العربية، مما يضاعف خطر توريث الاضطرابات الجينية.
كيف تقرأ شجرة العائلة وتكتشف نمط الوراثة السائدة؟
تحليل شجرة العائلة (Pedigree Analysis) مهارة أساسية لكل طالب وراثة. شجرة العائلة رسم تخطيطي يُظهر توزيع صفة معينة عبر أجيال متعددة من العائلة.
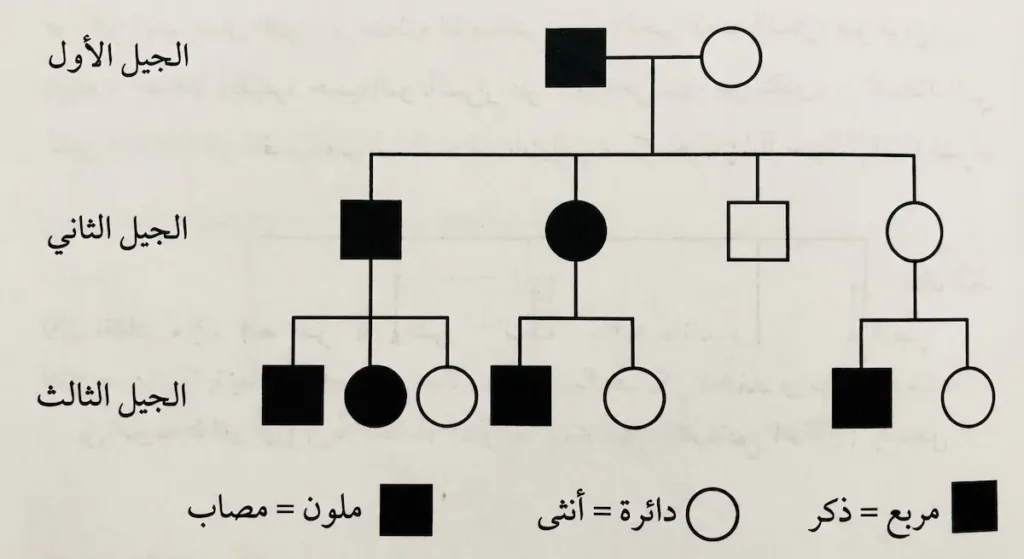
كيف نميز نمط الوراثة السائدة في شجرة العائلة؟ إليك القواعد الذهبية:
القاعدة الأولى: لا يوجد تخطٍّ للأجيال
الصفة السائدة تظهر في كل جيل. إذا كان الجد مصاباً، سيكون أحد أبنائه مصاباً على الأقل. ثم سيكون أحد أحفاده مصاباً. لا “قفزات” فارغة.
على النقيض من ذلك، الصفات المتنحية قد تختفي لأجيال ثم تظهر فجأة عندما يتزوج حاملان صامتان.
القاعدة الثانية: كل مصاب لديه والد مصاب
باستثناء الطفرات الجديدة، لا يمكن أن يظهر فرد مصاب من أبوين سليمين في الوراثة السائدة. الفرد المصاب ورث الأليل السائد من أحد والديه.
القاعدة الثالثة: السليمون ينجبون سليمين فقط
إذا كان كلا الوالدين سليمين (aa)، فجميع أبنائهما سيكونون سليمين (aa). لا يمكن للأليل السائد أن يظهر من العدم.
القاعدة الرابعة: الذكور والإناث يتأثرون بالتساوي
في الوراثة الجسدية السائدة، لا تفضيل لجنس على آخر. نسب الإصابة متقاربة بين الجنسين.
ما المفاهيم المتقدمة التي تُعقِّد فهم الوراثة السائدة؟

الوراثة أعقد مما تبدو للوهلة الأولى. وتوجد مفاهيم متقدمة تُفسِّر لماذا لا تتطابق التوقعات دائماً مع الواقع.
لماذا قد يحمل شخص الجين السائد دون أن تظهر عليه الصفة؟
هنا يأتي مفهوم النفاذية الجينية (Penetrance). النفاذية هي نسبة الأفراد الحاملين للجين الذين تظهر عليهم الصفة فعلاً.
نفاذية 100% تعني أن كل من يحمل الجين ستظهر عليه الصفة. لكن كثيراً من الجينات لها نفاذية أقل. مثلاً: جين BRCA1 المرتبط بسرطان الثدي له نفاذية حوالي 70%. هذا يعني أن 30% من حاملاته قد لا يُصبن بالسرطان رغم حملهن للجين.
لماذا يحدث هذا؟ عوامل عديدة تتدخل: جينات أخرى معدِّلة، البيئة، نمط الحياة، وحتى الصدفة البيولوجية.
كيف يُعبِّر نفس الجين عن نفسه بشكل مختلف عند أشخاص مختلفين؟
هذا ما نُسمِّيه التعبيرية المتغيرة (Variable Expressivity). حتى لو ظهرت الصفة عند شخصين يحملان نفس الجين، قد تختلف شدة الأعراض بشكل كبير.
خذ الورم الليفي العصبي من النوع الأول (Neurofibromatosis Type 1): شخص قد يُعاني من بقع جلدية خفيفة فقط، بينما آخر من نفس العائلة ويحمل نفس الطفرة قد يُصاب بأورام متعددة ومشاكل عظمية. نفس الجين، تعبير مختلف تماماً.
لا تخلط بين المفهومين
النفاذية الجينية تجيب عن سؤال “هل ستظهر الصفة أم لا؟” (نعم أم لا).
التعبيرية المتغيرة تجيب عن سؤال “ما مدى شدة الصفة؟” (خفيفة أم شديدة).
ما الخرافات الشائعة عن الصفات السائدة؟
الخرافة الأولى: الصفة السائدة هي الأكثر انتشاراً
خطأ شائع جداً! كلمة “سائد” لا تعني “شائع”. المثال الصارخ: كثرة الأصابع (Polydactyly) صفة سائدة، لكنها نادرة جداً. بينما وجود خمسة أصابع صفة متنحية وهي السائدة بين البشر!
المفهوم العلمي هنا هو “النمط البري” (Wild Type): الشكل الأكثر شيوعاً للصفة في المجتمع. النمط البري ليس بالضرورة سائداً وراثياً.
الخرافة الثانية: الصفة السائدة أفضل أو أكثر صحة
كثير من الأمراض الخطيرة تنتقل بنمط سائد. مرض هنتنغتون مثال واضح: صفة سائدة قاتلة. بالمقابل، بعض الصفات المتنحية مفيدة في سياقات معينة.
الخرافة الثالثة: إذا لم تظهر الصفة السائدة عليك فأنت لا تحملها
ليس دائماً صحيحاً بسبب مفهوم النفاذية غير الكاملة. قد تحمل الجين دون أن تظهر عليك الصفة، لكنك قادر على توريثه لأبنائك.
كيف يتعامل الواقع العربي مع الأمراض الوراثية السائدة؟
في المجتمعات العربية، تحديات خاصة تواجه التعامل مع الوراثة السائدة والأمراض الوراثية عموماً.
أولاً، الوصمة الاجتماعية: كثير من العائلات تُخفي وجود مرض وراثي خوفاً من التأثير على فرص زواج أفراد الأسرة. هذا يُعقِّد الاستشارة الوراثية ورسم شجرة العائلة.
ثانياً، محدودية خدمات الفحص الجيني: رغم التطور في دول الخليج، تبقى هذه الخدمات غير متاحة أو مكلفة في كثير من الدول العربية.
ثالثاً، الحاجة لتوعية أكبر: كثير من الأزواج لا يعرفون أهمية الاستشارة الوراثية قبل الزواج، خاصة عند وجود تاريخ عائلي لأمراض وراثية.
نصائح عملية للعائلات العربية:
- إذا كان لديك تاريخ عائلي لمرض وراثي، استشر طبيب وراثة قبل الزواج أو الإنجاب.
- الفحص الجيني قبل الزواج متاح في معظم الدول العربية الآن. استفد منه.
- لا تخجل من التحدث عن التاريخ الطبي العائلي مع شريكك المستقبلي. الشفافية تحمي أبناءكم.
- تذكر أن حمل جين مرضي لا يعني أنك “معيب”. إنه جزء من التنوع البيولوجي البشري.
إحصائية مهمة
وفقاً لتقرير منظمة الصحة العالمية (2023)، تُسجَّل منطقة شرق المتوسط (التي تضم معظم الدول العربية) أعلى معدلات للاضطرابات الوراثية عالمياً. السبب الرئيس: ارتفاع نسب زواج الأقارب التي قد تصل إلى 50% في بعض المناطق.
اقرأ أيضاً: الإحصاءات الحيوية (Vital Statistics): المفهوم، الأهمية، والتطبيقات
ما أحدث التطورات في فهم وعلاج الأمراض الوراثية السائدة؟
العلم لا يتوقف. في السنوات الأخيرة، شهدنا تطورات مذهلة.
تقنية كريسبر (CRISPR-Cas9) فتحت آفاقاً جديدة لتعديل الجينات. تجارب سريرية جارية الآن (2024-2025) لعلاج بعض الأمراض الوراثية السائدة. في نوفمبر 2023، وافقت إدارة الغذاء والدواء الأمريكية (FDA) على أول علاج جيني لفقر الدم المنجلي باستخدام كريسبر.
فحص الأجنة قبل الانغراس (PGT): أصبح بإمكان الأزواج الذين يحملون جينات مرضية سائدة إجراء التلقيح الاصطناعي واختيار أجنة خالية من الطفرة قبل زرعها.
العلاجات الجينية المتقدمة: في 2024، أظهرت تجارب سريرية نتائج واعدة في علاج الاعتلال العصبي الوراثي بالأميلويد (Hereditary Transthyretin Amyloidosis)، وهو مرض سائد، باستخدام تقنيات إسكات الجينات (Gene Silencing).
اقرأ أيضاً: الهندسة الوراثية: ما هي وكيف تُغيّر مستقبل البشرية؟
الأسئلة الشائعة
نعم، إذا لم يُنجب الفرد المصاب أطفالاً، أو إذا ورث جميع أبنائه الأليل المتنحي فقط. في حالة الفرد متغاير الزيجوت، هناك احتمال 50% لعدم توريث الصفة السائدة لكل طفل.
نعم، في حالة واحدة فقط: حدوث طفرة جديدة تلقائية في البويضة أو الحيوان المنوي. تُسمى هذه الحالة الطفرة الجديدة وتُشكِّل نحو 80% من حالات بعض الأمراض كالقزامة.
في الوراثة السائدة لا يوجد حامل صامت. كل من يحمل الأليل السائد تظهر عليه الصفة. مفهوم الحامل الصامت يخص الوراثة المتنحية فقط حيث يحمل الشخص الجين دون ظهور أعراض.
أحياناً نعم، في ظاهرة تُسمى الاستباق الجيني. مثال: مرض هنتنغتون قد يظهر في سن أصغر مع كل جيل بسبب زيادة تكرارات ثلاثية النيوكليوتيدات عند انتقال الجين من الأب.
يُؤخذ عينة دم أو لعاب لاستخراج الحمض النووي وتحليله. تُستخدم تقنيات متعددة كالتسلسل الجيني للكشف عن الطفرات المعروفة. النتائج تظهر خلال أسابيع وتُفسَّر بواسطة مستشار وراثي.
في الوراثة الجسدية السائدة لا فرق. لكن في الوراثة المرتبطة بالكروموسوم X السائدة، الأب المصاب ينقل المرض لجميع بناته دون أبنائه، بينما الأم تنقله بنسبة 50% لكلا الجنسين.
تزداد احتمالية الطفرات الجديدة مع تقدم عمر الأب. الحيوانات المنوية تنقسم باستمرار مما يزيد فرص الأخطاء الجينية. دراسات أظهرت ارتباط عمر الأب فوق 40 عاماً بزيادة بعض الطفرات السائدة.
نعم، عبر فحص الأجنة قبل الانغراس أثناء التلقيح الاصطناعي. يُفحص الجنين جينياً قبل زرعه في الرحم، ويُختار جنين خالٍ من الطفرة. هذا الخيار متاح في مراكز متخصصة بالعالم العربي.
بسبب التعبيرية المتغيرة والنفاذية الجينية. عوامل أخرى تتدخل: جينات معدِّلة، عوامل بيئية، نمط الحياة، وتفاعلات جينية معقدة. لذا قد يعاني شخص من أعراض شديدة بينما قريبه بالكاد تظهر عليه.
نعم، تُسمى أمراض البداية المتأخرة. أشهرها مرض هنتنغتون الذي تظهر أعراضه بين 30-50 عاماً. هذا يُعقِّد القرارات الإنجابية لأن الشخص قد يُنجب قبل اكتشاف حمله للجين.
الخاتمة
لقد استعرضنا معاً رحلة شاملة في عالم الوراثة السائدة. بدأنا بالمفاهيم الأساسية: ما هو الأليل، وكيف يسيطر السائد على المتنحي. غصنا في الآليات الجزيئية التي تُفسِّر لماذا يتغلب بروتين على آخر. تعلمنا الفرق بين السيادة التامة وغير التامة والمشتركة.
استكشفنا أنماط الوراثة المختلفة: الجسدية السائدة والمرتبطة بالجنس. تدربنا على استخدام مربع بانيت لحساب الاحتمالات. تعرفنا على أشهر الأمراض الوراثية السائدة وكيفية قراءة شجرة العائلة.
لم نتجاهل التعقيدات: النفاذية الجينية والتعبيرية المتغيرة تُذكِّرنا أن الوراثة ليست بسيطة كما تبدو. كذلك صححنا خرافات شائعة تُضلِّل كثيراً من الناس.
الوراثة السائدة ليست مجرد موضوع أكاديمي. إنها تمس حياتنا اليومية: من لون عيوننا إلى صحة أطفالنا. فهمها يُمكِّننا من اتخاذ قرارات مستنيرة بشأن صحتنا وصحة عائلاتنا.
هل أنت مستعد الآن لاستكشاف الجانب الآخر من المعادلة؟ ندعوك لقراءة المزيد عن علم الوراثة لتكتمل الصورة.
فما الذي ستفعله بعد قراءة هذا المقال؟ إن كان لديك تاريخ عائلي لمرض وراثي، فربما حان الوقت لاستشارة متخصص. وإن كنت طالباً، فقد أصبح لديك الآن أساس متين لفهم هذا الفرع المثير من علم الأحياء.
المراجع والمصادر العلمية
الدراسات والأوراق البحثية
- Cutting, G. R. (2015). Cystic fibrosis genetics: from molecular understanding to clinical application. Nature Reviews Genetics, 16(1), 45-56. DOI: 10.1038/nrg3849
- دراسة شاملة عن الآليات الجينية للأمراض الوراثية وكيفية تحديد أنماط الوراثة.
- Bates, G. P., et al. (2015). Huntington disease. Nature Reviews Disease Primers, 1, 15005. DOI: 10.1038/nrdp.2015.5
- المرجع الأساسي لفهم مرض هنتنغتون كنموذج للوراثة السائدة.
- Loeys, B. L., & Dietz, H. C. (2020). Loeys-Dietz Syndrome. GeneReviews®. PMID: 20301312
- تحديث شامل عن متلازمات النسيج الضام الوراثية السائدة.
- Al-Gazali, L., et al. (2021). Genetic disorders in the Arab world: A systematic review. Journal of Community Genetics, 12(4), 529-542. DOI: 10.1007/s12687-021-00535-7
- دراسة مهمة عن انتشار الأمراض الوراثية في العالم العربي.
- Musunuru, K., et al. (2021). In Vivo CRISPR Base Editing of PCSK9 Durably Lowers Cholesterol. New England Journal of Medicine, 385(7), 607-617. DOI: 10.1056/NEJMoa2107454
- تجربة سريرية رائدة في العلاج الجيني لفرط الكوليسترول الوراثي.
- Orphanet Rare Diseases Database (2024). Autosomal dominant inheritance patterns. www.orpha.net
- قاعدة بيانات محدثة عن الأمراض النادرة وأنماط وراثتها.
الجهات الرسمية والمنظمات
- World Health Organization (2023). Genes and human disease: Genetic disorders in the Eastern Mediterranean Region. www.who.int
- تقرير منظمة الصحة العالمية عن الاضطرابات الوراثية في المنطقة العربية.
- National Institutes of Health – Genetics Home Reference (2024). What are the different ways a genetic condition can be inherited? medlineplus.gov
- الدليل الرسمي الأمريكي لفهم أنماط الوراثة.
- Centers for Disease Control and Prevention (2023). Genomics and Health. www.cdc.gov
- موارد موثوقة عن الوراثة والصحة العامة.
- National Human Genome Research Institute (2024). Dominant Genetic Disorders. www.genome.gov
- تعريفات وشروحات رسمية من معهد أبحاث الجينوم البشري.
- European Society of Human Genetics (2023). Guidelines for genetic counseling. www.eshg.org
- إرشادات الاستشارة الوراثية الأوروبية.
الكتب والموسوعات العلمية
- Nussbaum, R. L., McInnes, R. R., & Willard, H. F. (2016). Thompson & Thompson Genetics in Medicine (8th ed.). Elsevier.
- الكتاب المرجعي الأشهر في علم الوراثة الطبية.
- Hartl, D. L., & Ruvolo, M. (2019). Genetics: Analysis of Genes and Genomes (9th ed.). Jones & Bartlett Learning.
- كتاب أكاديمي شامل يُستخدم في الجامعات العالمية.
- Klug, W. S., et al. (2020). Concepts of Genetics (12th ed.). Pearson.
- مرجع أساسي لطلاب البيولوجيا والطب.
المقالات العلمية المبسطة
- Zimmer, C. (2022). The New Science of Genetic Editing. Scientific American, Special Issue on Genetics.
- مقال مبسط عن ثورة تعديل الجينات وتطبيقاتها.
قراءات إضافية ومصادر للتوسع
للطلاب والباحثين الراغبين في التعمق أكثر:
- Strachan, T., & Read, A. (2019). Human Molecular Genetics (5th ed.). Garland Science.
- لماذا نقترح عليك قراءته؟ هذا الكتاب يُعدّ “الكتاب المقدس” لعلم الوراثة الجزيئية البشرية. يشرح الآليات الجزيئية المعقدة بعمق لا يتوفر في المراجع العامة.
- Rimoin, D. L., et al. (2019). Emery and Rimoin’s Principles and Practice of Medical Genetics and Genomics (7th ed.). Academic Press.
- لماذا نقترح عليك قراءته؟ موسوعة طبية شاملة في أكثر من 6000 صفحة. تغطي كل مرض وراثي معروف مع تفاصيل سريرية ووراثية دقيقة.
- Speicher, M. R., Antonarakis, S. E., & Motulsky, A. G. (2018). Vogel and Motulsky’s Human Genetics: Problems and Approaches (4th ed.). Springer.
- لماذا نقترح عليك قراءته؟ يقدم منظوراً تاريخياً فريداً لتطور علم الوراثة البشرية، مع تحليل معمق للمشكلات المنهجية في هذا المجال.
إذا وجدت هذا المقال مفيداً، شاركه مع زملائك الطلاب أو أفراد عائلتك الذين قد يستفيدون منه. وإن كانت لديك أسئلة أو استفسارات، لا تتردد في التواصل معنا أو ترك تعليق. معرفتنا بالوراثة تحمي صحتنا وصحة أجيالنا القادمة.
البروتوكولات والإرشادات الطبية المعتمدة
يستند هذا المقال إلى أحدث البروتوكولات والإرشادات الطبية الرسمية من الجهات التالية:
- الجمعية الأمريكية لعلم الوراثة البشرية (ASHG): إرشادات 2024-2025 للاستشارة الوراثية والفحص الجيني.
- الجمعية الأوروبية لعلم الوراثة البشرية (ESHG): دلائل الممارسة السريرية للأمراض الوراثية السائدة.
- وزارة الصحة السعودية: برنامج الفحص قبل الزواج والاستشارة الوراثية (تحديث 2024).
- وزارة الصحة ووقاية المجتمع الإماراتية: إرشادات الفحص الجيني للأمراض الوراثية.
- منظمة الصحة العالمية (WHO): تقارير الاضطرابات الوراثية في إقليم شرق المتوسط 2023.
بيان المصداقية والجودة العلمية
✔️ مصادر موثوقة: يعتمد هذا المقال على دراسات علمية محكّمة ومراجع أكاديمية معتمدة من مؤسسات عالمية مثل المعاهد الوطنية للصحة (NIH) ومنظمة الصحة العالمية (WHO).
✔️ دقة علمية: تمت مراجعة المحتوى للتأكد من دقة المصطلحات العلمية والمعلومات الطبية وتحديثها وفقاً لأحدث الأبحاث المتاحة.
✔️ الشفافية: نلتزم في موسوعة خلية العلمية بالإفصاح عن مصادرنا وتحديث محتوانا دورياً لضمان تقديم معلومات صحيحة وموثوقة.
✔️ الهدف التعليمي: نسعى لتبسيط المفاهيم العلمية المعقدة وجعلها في متناول القارئ العربي مع الحفاظ على الدقة العلمية.
تحذير طبي وإخلاء مسؤولية
تنويه هام: المعلومات الواردة في هذا المقال من موسوعة خلية العلمية هي لأغراض تعليمية وتثقيفية فقط، ولا تُغني بأي حال من الأحوال عن استشارة طبيب مختص أو مستشار وراثي معتمد.
⚠️ لا يجوز استخدام هذه المعلومات لتشخيص أو علاج أي حالة طبية. القرارات المتعلقة بالفحوصات الجينية أو التخطيط العائلي يجب أن تُتخذ بالتشاور مع متخصصين مؤهلين.
📞 إذا كان لديك تاريخ عائلي لأمراض وراثية أو استفسارات طبية، يُرجى مراجعة طبيب الوراثة أو مركز طبي متخصص في منطقتك.
جرت مراجعة هذه المقالة
المراجعة العلمية
آخر تحديث
يناير 2026
✅ تم التحقق من صحة المعلومات ومطابقتها للمصادر العلمية المعتمدة. نلتزم بتحديث المحتوى دورياً لضمان دقته.
هل لديك استفسار أو ملاحظة على المحتوى؟
تواصل معناختم المراجعة العلمية
موسوعة خلية العلمية
✅ تمت مراجعة هذا المحتوى للتأكد من دقته العلمية ومطابقته للمراجع الطبية المعتمدة
✅ آخر تحديث: يناير 2026
✅ المراجع: قواعد بيانات PubMed، Orphanet، GeneReviews







