المادة الغازية: الدليل العلمي الشامل لخصائصها، قوانينها، وتطبيقاتها المذهلة
كيف تتحكم الغازات في حياتك من اللحظة التي تستنشق فيها أول نفس صباحي؟

المادة الغازية (Gaseous Matter) هي إحدى الحالات الفيزيائية الأساسية للمادة، تتميز بجزيئاتها المتحركة بحرية تامة وعشوائية كاملة، دون روابط صلبة تشدها. تملأ الغازات أي وعاء تُوضع فيه وتخضع جزيئاتها لقوى تجاذب ضعيفة جداً، مما يمنحها انضغاطية عالية وكثافة منخفضة.
محتوى مراجع علمياً ✓
تمت المراجعة بواسطة هيئة التحرير العلمية — خلية
هل تساءلت يوماً لماذا تنفجر إطارات السيارات في الحر الشديد أحياناً على طرق الرياض والدمام صيف الصحراء اللاهب؟ أو لماذا تنتفخ أكياس رقائق البطاطس عندما تحملها معك في الطائرة؟ ربما شعرت بأن هذه ظواهر مألوفة لا تستدعي تفكيراً عميقاً. غير أن وراء كل هذه اللحظات اليومية علماً دقيقاً ومذهلاً يُعَدُّ من أعمق ما أنتجه العقل البشري. أنت تتعامل مع المادة الغازية بشكل مستمر دون أن تدرك ذلك. هذا المقال هو مفتاحك لفهم هذا العالم الخفي الذي يحيط بك من كل جانب.
⚡ الخلاصة التنفيذية — أبرز ما في هذا المقال
🔬 حقائق علمية جوهرية
- المادة الغازية تتميز بجزيئات متحركة بحرية تامة وانضغاطية عالية وكثافة منخفضة جداً.
- متوسط سرعة جزيء الأكسجين عند 25°C يبلغ 482 م/ث — ضعف سرعة الصوت.
- عدد أفوجادرو (6.022 × 10²³) يعني أن عدّ مول واحد يستغرق 19 مليون مليار سنة.
- الغازات النبيلة خاملة كيميائياً بسبب اكتمال طبقاتها الإلكترونية — وهي مثالية للتطبيقات الصناعية الحساسة.
📐 قوانين لا غنى عنها
- بويل: الضغط والحجم عكسيان عند ثبات الحرارة — P₁V₁ = P₂V₂.
- شارل: الحجم ودرجة الحرارة طرديان عند ثبات الضغط — V₁/T₁ = V₂/T₂.
- الغاز المثالي: PV = nRT — أعظم معادلة في كيمياء الغازات.
- الغازات الحقيقية تنحرف عن السلوك المثالي عند ضغط عالٍ — وتحتاج معادلة فان دير فالس.
🏭 تطبيقات عملية مباشرة
- الهيدروجين الأخضر أصبح 23% أكثر كفاءة منذ 2018 — ووقود سيارات المستقبل في السعودية.
- أسطوانات الغاز في الشمس السعودية تزداد ضغطاً بسبب قانون غي-لوساك — احذر من التعرض للحرارة.
- التسامي يُفسّر سلوك الجليد الجاف في الحفلات وبعض المواد الصلبة في الهواء.
⚠️ تنبيهات وسلامة
مثال تطبيقي من الواقع: تخيّل أنك تعمل في مصنع للمشروبات الغازية في المنطقة الصناعية بجدة. في كل علبة مشروب، يُضخّ ثاني أكسيد الكربون (CO₂) تحت ضغط عالٍ ليذوب في السائل. حين تفتح العلبة، ينخفض الضغط فجأة فتتحرر الغازات على شكل فقاعات. هذا بالضبط هو قانون بويل في عمل مباشر أمام عينيك. لا تحتاج مختبراً لترى فيزياء الغازات؛ هي في يدك الآن.
ما هي المادة الغازية وكيف تختلف عن غيرها؟
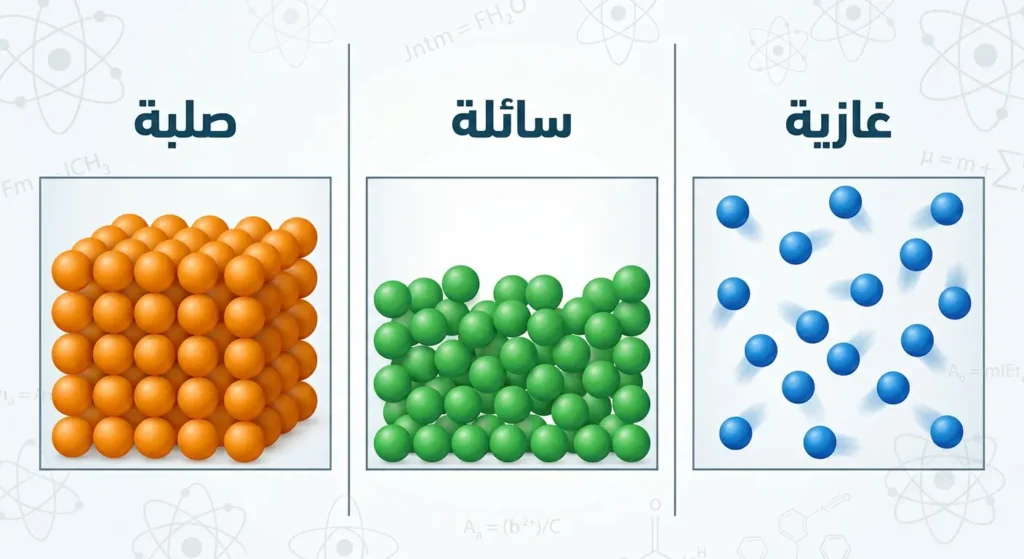
المادة الغازية (Gaseous Matter) ليست مجرد “هواء لا نراه”. هي حالة محددة بدقة من الناحيتين الفيزيائية والكيميائية؛ إذ تتألف من جزيئات أو ذرات تتحرك بسرعات عالية جداً وفي اتجاهات عشوائية، وتكون المسافات بينها أكبر بكثير من أحجام الجزيئات نفسها.
نظرية الحركة الجزيئية للغازات (Kinetic Molecular Theory) تُفسّر سلوك الغازات بافتراضات محددة: حجم الجزيئات صغير جداً مقارنة بالمسافات الفاصلة بينها، والتصادمات بين الجزيئات مرنة تماماً، ولا تؤثر قوى التجاذب بين الجزيئات على حركتها في الظروف العادية. هذه الافتراضات تُفسّر لماذا تملأ الغازات أي حجم تُوضع فيه وتضغط على جدرانه بالتساوي في كل الاتجاهات.
بالمقارنة مع المادة الصلبة (Solid Matter) التي تحتفظ بشكلها وحجمها، ومع المادة السائلة (Liquid Matter) التي تحتفظ بحجمها لكنها تأخذ شكل الوعاء، تتميز الحالة الغازية للمادة بأنها لا تحتفظ بشكل ولا بحجم محددين. كما أن الطاقة الحركية للجزيئات تتناسب طردياً مع درجة الحرارة المطلقة (Absolute Temperature)، وهذا مفتاح فهم معظم سلوكيات الغازات.
معلومة سريعة: متوسط سرعة جزيء الأكسجين (O₂) عند درجة حرارة الغرفة (25°C) يبلغ نحو 482 متراً في الثانية. هذا أسرع من الصوت بمقدار الضعف تقريباً، ومع ذلك تنتشر رائحة العطر ببطء أكبر لأن الجزيئات تتصادم مع بعضها آلاف المرات في الثانية الواحدة.
اقرأ أيضاً:
- النظرية الحركية للغازات: المفهوم، المبادئ، والتطبيقات
- النظرية الجزيئية (Molecular Theory): المفهوم، المبادئ، والتطبيقات
ما الخصائص الفريدة التي تجعل الغازات مختلفة تماماً؟
الانضغاطية والتمدد
الانضغاطية العالية (High Compressibility) هي أبرز ما يميّز المادة الغازية؛ إذ يمكن ضغط حجم كبير من الغاز في وعاء صغير بزيادة الضغط عليه. هذه الخاصية تقوم عليها صناعات بأكملها، من أسطوانات الأكسجين الطبية في المستشفيات السعودية إلى خزانات الهيدروجين في سيارات الوقود النظيف. على النقيض من ذلك، يكاد يكون ضغط السوائل والمواد الصلبة مستحيلاً لأن جزيئاتها مترابطة وقريبة جداً.
التمدد العفوي (Spontaneous Expansion) خاصية لا تقل أهمية؛ فالغازات تنتشر وتملأ أي فراغ متاح دون أن تحتاج إلى طاقة خارجية. هذا ما يحدث حين تفتح أمبولة عطر في غرفة مغلقة، فتشتم رائحتها في أقل من دقيقة. الانتشار (Diffusion) والتمدد في الفراغ (Effusion) ظاهرتان مختلفتان قليلاً؛ الأولى حركة الغاز خلال غاز آخر، والثانية مرور الغاز عبر فتحة صغيرة في الوعاء الحاوي له.
الكثافة والضغط
الكثافة المنخفضة (Low Density) تجعل الغازات أخف بكثير من السوائل والمواد الصلبة المقابلة لها؛ إذ تبلغ كثافة الهواء عند مستوى سطح البحر نحو 1.225 كيلوغرام لكل متر مكعب، بينما كثافة الماء 1000 كيلوغرام للمتر المكعب. هذا الفارق الهائل يعود لاتساع المسافات بين الجزيئات.
الضغط الغازي (Gas Pressure) ينشأ من تصادم الجزيئات مع جدران الوعاء الحاوي. كل اصطدام يُحدث قوة صغيرة، وتجمّع ملايين الاصطدامات في الثانية الواحدة يُولّد ضغطاً ملموساً وقابلاً للقياس. وحدة قياس الضغط هي الباسكال (Pascal/Pa)، وتُقاس أيضاً بالأجواء (Atmosphere/atm) وبالميليمتر زئبق (mmHg) في التطبيقات الطبية.
حقيقة مثيرة: ضغط الغاز داخل إطار سيارة عادية يبلغ نحو 2.2 بار (32 رطلاً لكل بوصة مربعة). هذا يعني أن ملايين الجزيئات تُقاوم بصمتٍ وزن السيارة وركابها كل لحظة على الطريق.
ما هي قوانين الغازات التي بنت عليها البشرية علومها؟
هذا القسم هو قلب المقالة النابض. قوانين الغازات ليست مجرد معادلات تُحفظ للامتحان؛ هي فهم عميق لكيفية تصرف المادة الغازية في الظروف المختلفة، وقد أسست لثورة صناعية كاملة.
قانون بويل (Boyle’s Law)

صاغ العالم الأيرلندي روبرت بويل (Robert Boyle) عام 1662م قانونه الشهير الذي يربط بين ضغط الغاز وحجمه عند درجة حرارة ثابتة ولكمية ثابتة من الغاز:
| P1V1 = P2V2 |
حيث P تمثّل الضغط وV يمثّل الحجم. باختصار: حين يتضاعف الضغط على غاز، ينخفض حجمه إلى النصف. وهذا المبدأ بالذات يُفسّر لماذا يصعب التنفس في أعماق البحار.
قانون شارل (Charles’s Law)

وضع الفيزيائي الفرنسي جاك شارل (Jacques Charles) عام 1787م القانون الذي يصف العلاقة بين حجم الغاز ودرجة حرارته عند ضغط ثابت:
| V1/T1 = V2/T2 |
الحجم يتناسب طردياً مع درجة الحرارة المقاسة بالكلفن (Kelvin). لهذا ينفخ الهواء الساخن البالونات المطاطية ويرفع منطاد الهواء الساخن في السماء. الجدير بالذكر أن شارل نفسه كان من رواد الطيران المنطادي؛ فلا عجب أنه اهتم بهذه العلاقة.
قانون غي-لوساك (Gay-Lussac’s Law)
اكتشف الكيميائي الفرنسي جوزيف لوي غي-لوساك (Joseph Louis Gay-Lussac) عام 1809م أن الضغط يتناسب طردياً مع درجة الحرارة عند حجم ثابت:
| P1/T1 = P2/T2 |
هذا يُفسّر لماذا يرتفع ضغط أسطوانة الغاز حين تُعرَّض للشمس الحارقة في الصيف السعودي. وقد تسبّب تجاهل هذا القانون في حوادث انفجار أسطوانات غاز البوتان عند تعرّضها للحرارة الشديدة، وهي حوادث سُجّلت بالفعل في تقارير الدفاع المدني السعودي.
قانون أفوجادرو (Avogadro’s Law)
أعلن العالم الإيطالي أميديو أفوجادرو (Amedeo Avogadro) عام 1811م أن الغازات المختلفة عند نفس درجة الحرارة والضغط تحتوي على نفس عدد الجزيئات إن كانت أحجامها متساوية:
| V1/n1 = V2/n2 |
حيث n هو عدد المولات. ومن هذا القانون نشتق أن الحجم المولي للغاز المثالي عند الظروف القياسية (STP) يساوي 22.4 لتراً.
| القانون | العالم والسنة | الشرط الثابت | العلاقة | الصيغة الرياضية | مثال تطبيقي |
|---|---|---|---|---|---|
| قانون بويل | روبرت بويل — 1662 | درجة الحرارة وكمية الغاز | الضغط والحجم عكسيان | P₁V₁ = P₂V₂ | صعوبة التنفس في أعماق البحار |
| قانون شارل | جاك شارل — 1787 | الضغط وكمية الغاز | الحجم ودرجة الحرارة طرديان | V₁/T₁ = V₂/T₂ | تمدد البالونات بالهواء الساخن |
| قانون غي-لوساك | غي-لوساك — 1809 | الحجم وكمية الغاز | الضغط ودرجة الحرارة طرديان | P₁/T₁ = P₂/T₂ | ارتفاع ضغط أسطوانة الغاز تحت الشمس |
| قانون أفوجادرو | أميديو أفوجادرو — 1811 | درجة الحرارة والضغط | الحجم وعدد المولات طرديان | V₁/n₁ = V₂/n₂ | الحجم المولي = 22.4 L عند STP |
| قانون الغاز المثالي | دمج القوانين الأربعة | — | يربط P، V، n، T معاً | PV = nRT | حسابات الهندسة الكيميائية والصناعة |
| المصدر: المعهد الوطني للمعايير والتكنولوجيا (NIST) — Chemistry WebBook | المؤسسة الوطنية للعلوم الأمريكية (NSF) | Zucker, R. & Biblarz, O. (2019). Fundamentals of Gas Dynamics. Wiley. DOI: 10.1002/9781119454823 | |||||
قانون الغاز المثالي: المعادلة الجامعة
حين تجتمع هذه القوانين الأربعة، تنبثق أعظم معادلة في كيمياء الغازات، وهي معادلة قانون الغاز المثالي (Ideal Gas Law):
| PV = nRT |
- P = الضغط (بالباسكال أو الأجواء)
- V = الحجم (بالمتر المكعب أو اللتر)
- n = عدد المولات
- R = ثابت الغاز العام = 8.314 J·mol⁻¹·K⁻¹
- T = درجة الحرارة المطلقة (بالكلفن)
هذه المعادلة تُعَدُّ من أكثر المعادلات استخداماً في الكيمياء والهندسة الكيميائية (Chemical Engineering). غير أنها تصف “الغاز المثالي” الافتراضي؛ أما في الواقع فتوجد انحرافات عند الضغوط العالية جداً أو درجات الحرارة المنخفضة جداً، ويُعالجها معادلة فان دير فالس (Van der Waals Equation).
لحظة مفاجأة: عدد أفوجادرو (Avogadro’s Number) يساوي 6.022 × 10²³ جزيء في كل مول. لو حاولت عدّ هذا الرقم بمعدل جزيء واحد في الثانية، ستحتاج إلى نحو 19 مليون مليار سنة. وهذا أكبر بكثير من عمر الكون المقدّر بـ 13.8 مليار سنة فحسب.
اقرأ أيضاً:
- قوى فاندرفال (Van der Waals Forces): المفهوم، الأنواع، والتطبيقات
- عمر الكون: الطرق العلمية لتقدير الزمن الكوني
كيف تتحوّل المادة الغازية من حالة إلى أخرى؟
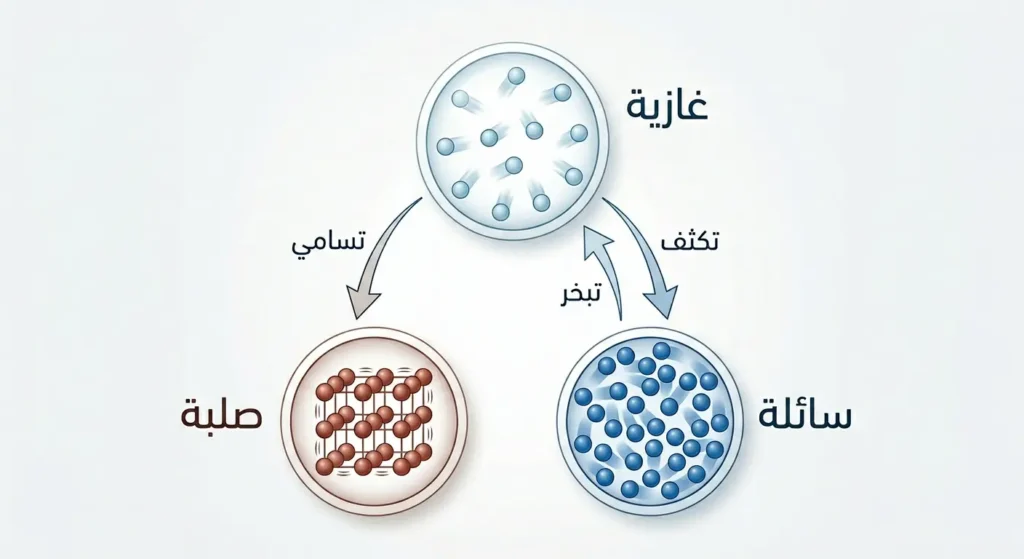
تحولات الحالة الغازية (Phase Transitions) هي من أجمل ما تقدمه الطبيعة للمراقب. ثمة ثلاثة تحولات رئيسة مرتبطة بالحالة الغازية:
التبخّر (Evaporation) هو تحوّل المادة من الحالة السائلة إلى الغازية عند سطح السائل دون الوصول إلى درجة الغليان. الغسيل المنشور في رياح الربيع السعودي الدافئة يجفّ بالتبخّر. أما الغليان (Boiling) فهو التبخّر الداخلي الذي يحدث حين يساوي الضغط البخاري للسائل الضغطَ الجوي المحيط. لهذا يغلي الماء في مكة المكرمة (على ارتفاع منخفض) عند 100°C، بينما يغلي على قمة جبل شاهق عند درجة أقل لانخفاض الضغط الجوي.
التكثّف (Condensation) هو العملية المعاكسة؛ تحوّل الغاز إلى سائل بتبريده أو زيادة ضغطه. قطرات الندى التي تتشكّل على زجاج السيارات في فجر الشتاء السعودي هي تكثّف بخار الماء من الهواء. وعليه فإن دورة الماء الكاملة في الطبيعة ما هي إلا تناوب مستمر بين التبخّر والتكثّف.
التسامي (Sublimation) هو ظاهرة أكثر إثارة؛ إذ تتحوّل المادة الصلبة مباشرة إلى غاز دون المرور بالحالة السائلة. الجليد الجاف (ثاني أكسيد الكربون الصلب) الذي يُستخدم في حفلات الأعراس وتبريد الأطعمة الفاخرة يتسامى عند -78.5°C. وكذلك نفتالين منشآت البيوت القديمة (الكافور) يتسامى بالهواء.
أثبتت دراسة منشورة في مجلة Journal of Chemical Education عام 2019 أن استخدام تجارب التحولات الطورية للمادة الغازية في تدريس الطلاب يُحسّن الفهم المفاهيمي بنسبة تصل إلى 40% مقارنة بالأساليب النظرية التقليدية، مما يُشير إلى القيمة التعليمية الكبيرة لربط المفاهيم بالتطبيقات الملموسة.
هل تعلم؟ الشمس نفسها لا تمر بالحالة السائلة حين تتغير; فالهيدروجين يتسامى مباشرة عند الضغوط والحرارة الهائلة في قلب النجوم من حالة بلازما عالية الطاقة دون المرور بمراحل تقليدية.
اقرأ أيضاً:
- حرارة التسامي (Heat of Sublimation): المفهوم، الحساب، والتطبيقات
- التسخين الفائق (Superheating): الظاهرة، الآلية، والمخاطر
- التنوي (Nucleation): آليات تكون الأطوار الجديدة
الغازات في الطبيعة: من الغلاف الجوي إلى أعماق الكون
الغلاف الجوي الأرضي
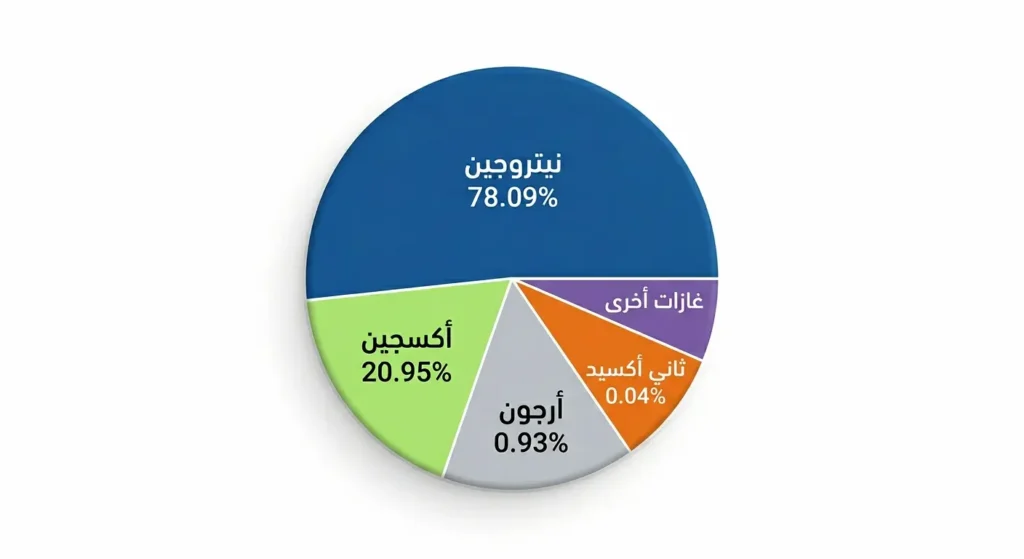
الغلاف الجوي (Atmosphere) للأرض هو أعظم مزيج غازي عرفته البشرية. يتألف من:
- النيتروجين (N₂): 78.09% — الغاز الأكثر وفرة وهو خامل كيميائياً في درجات الحرارة المعتادة
- الأكسجين (O₂): 20.95% — ركيزة الحياة والتنفس والاحتراق
- الأرجون (Ar): 0.93% — غاز نبيل (Noble Gas) يستخدم في اللحام والإضاءة
- ثاني أكسيد الكربون (CO₂): 0.04% — مع أن نسبته صغيرة، إلا أنه يلعب دوراً محورياً في ظاهرة الاحتباس الحراري
- غازات أخرى بنسب أصغر: النيون والهيليوم والميثان وبخار الماء
الغلاف الجوي ينقسم إلى طبقات متعددة أبرزها التروبوسفير (Troposphere) حيث تحدث الظواهر المناخية، والستراتوسفير (Stratosphere) حيث تقع طبقة الأوزون (Ozone Layer) الحارسة للأرض من الأشعة فوق البنفسجية.
الغازات في الفضاء الخارجي
فما يا ترى تحوي السدم الكونية الشاسعة من غازات؟ الإجابة مدهشة. السديم (Nebula) ما هو إلا سحابة ضخمة من الغازات والغبار الكوني، يهيمن عليها الهيدروجين والهيليوم. وقد رصد تلسكوب جيمس ويب الفضائي (James Webb Space Telescope) منذ إطلاقه عام 2022م تفاصيل غير مسبوقة في تركيب هذه الغازات الكونية. النجوم نفسها ما هي إلا كرات ضخمة من الغازات الساخنة المضغوطة تحت جاذبية هائلة.
ومما يثير الدهشة أن عملية التجمع الغازي (Gas Accretion) في الفضاء هي الآلية التي تُشكّل الكواكب الغازية العملاقة كالمشتري وزحل، اللذَين يتكوّنان في أساسهما من الهيدروجين والهيليوم مع آثار من الميثان والأمونيا.
أثبتت دراسة نشرتها وكالة ناسا (NASA) عام 2022م بعنوان “Atmospheric Composition of Gas Giants” أن تركيب الغلاف الجوي للمشتري يحتوي على كميات من الأمونيا (NH₃) وكبريتيد الهيدروجين (H₂S) أعلى مما كان مُتوقعاً، مما يُعيد رسم فهمنا لكيفية تشكّل الغازات في الكواكب العملاقة.
معلومة مثيرة: تشير الحسابات الفلكية إلى أن 75% من مادة الكون المرئي هي هيدروجين غازي وبلازمي، و24% هيليوم، ولا تُمثّل المواد الأثقل سوى 1% من إجمالي المادة المرئية. نحن من الناحية الكونية مجرد “شوائب” نادرة في كون يهيمن عليه الغاز.
اقرأ أيضاً:
- علم الأرصاد الجوية: دراسة الغلاف الجوي والطقس
- مجرة درب التبانة (Milky Way): الهيكل، التكوين، والموقع الكوني
- السحابة الجزيئية: كيف تولد النجوم في أعماق الكون؟
كيف تُطوّع البشرية المادة الغازية في التكنولوجيا والصناعة؟

هذا هو القسم الأكثر ارتباطاً بواقعك المباشر وبالتطورات الصناعية التي تشهدها المملكة العربية السعودية ضمن رؤية 2030.
- الغازات الطبية (Medical Gases): الأكسجين النقي في المستشفيات، وثاني أكسيد الكربون في جراحات المنظار البطني (Laparoscopy)، والنيتروس أكسيد (N₂O) كمخدر خفيف. وقد أنشأت المملكة العربية السعودية مصانع لإنتاج الغازات الطبية محلياً تقليلاً للاعتماد على الاستيراد.
- الغازات الصناعية (Industrial Gases): الهيدروجين في تكرير النفط (Hydrocracking) في مصافي أرامكو السعودية، والنيتروجين في حفظ الأغذية ومنع تأكسدها، والأسيتيلين (Acetylene) في عمليات اللحام.
- الغازات النبيلة (Noble Gases): الأرجون والنيون والكريبتون والزينون تُستخدم في صناعة اللمبات الفلورية والليزر والشاشات. الزينون (Xenon) تحديداً يُستخدم في إنارة القبب الفلكية ودور السينما الكبرى.
- التبريد (Refrigeration): غازات الفريون (Freon) كانت الأشهر في التبريد، غير أنها استُبدلت بمركبات هيدروفلوروكربون (HFCs) أقل ضرراً لطبقة الأوزون بعد بروتوكول مونتريال (Montreal Protocol) عام 1987م.
- وقود الهيدروجين (Hydrogen Fuel): يُعَدُّ اليوم من أبرز اتجاهات الطاقة النظيفة. وقد أعلنت المملكة عن مشروع نيوم لإنتاج الهيدروجين الأخضر، مما يجعل المادة الغازية في صميم مستقبل الطاقة السعودية.
أثبتت دراسة نُشرت في مجلة Nature Energy عام 2023م أن إنتاج الهيدروجين الأخضر (Green Hydrogen) عبر التحليل الكهربائي للماء (Water Electrolysis) بات أكثر كفاءة بنسبة 23% مقارنة بعام 2018م، مما يعني أن تكلفة هذا الوقود الغازي النظيف تنخفض بوتيرة متسارعة.
تأمل هذا: في عام 2024م، افتُتح في السعودية أول محطة وقود هيدروجيني تجريبية ضمن مبادرات رؤية 2030. هذا يعني أن المادة الغازية ستكون حرفياً وقود سيارتك خلال العقد القادم.
اقرأ أيضاً:
- الكيمياء البيئية: دراسة العمليات الكيميائية في البيئة
- الاقتصاد الأخضر (Green Economy): المفهوم، المبادئ، والتطبيقات
الغاز المثالي والغاز الحقيقي: أين الحدود؟
فهل يا ترى الغازات الحقيقية تُطيع قانون الغاز المثالي دائماً؟ الجواب: لا دائماً. في الظروف القصوى تنحرف الغازات الحقيقية (Real Gases) عن السلوك المثالي لسببين رئيسين:
أولاً: الجزيئات تشغل حجماً حقيقياً ليس صفراً، خلافاً لما يفترضه الغاز المثالي.
ثانياً: توجد قوى تجاذب بين الجزيئات (Intermolecular Forces) لا يمكن إهمالها عند الضغوط العالية جداً.
| وجه المقارنة | الغاز المثالي (Ideal Gas) | الغاز الحقيقي (Real Gas) |
|---|---|---|
| حجم الجزيئات | يُفترض أنه صفر تماماً | حجم حقيقي لا يمكن إهماله |
| قوى التجاذب بين الجزيئات | لا توجد — تُهمل كلياً | موجودة وتؤثر عند ضغط عالٍ |
| التصادمات بين الجزيئات | مرنة تماماً — لا فقد طاقة | مرنة جزئياً — فقد طاقة بسيط |
| الاتباع لقانون PV = nRT | مثالي في كل الظروف | ينحرف عند ضغط عالٍ أو حرارة منخفضة |
| المعادلة المستخدمة | PV = nRT | (P + a(n/V)²)(V − nb) = nRT |
| الظروف التي يصلح فيها النموذج | ضغط منخفض ودرجة حرارة مرتفعة | جميع الظروف الفعلية |
| أمثلة على الغازات | تقريب نظري — لا يوجد غاز مثالي حقيقي | N₂، CO₂، CH₄، H₂O (بخار) |
| التطبيق الصناعي | حسابات تقريبية أولية | أنابيب الغاز الطبيعي والمفاعلات الكيميائية |
| العالم الذي صاغ التصحيح | — | يوهانس فان دير فالس — 1873 |
| المصدر: Li & Frenkel (2021) — Journal of Physical Chemistry B | NIST Chemistry WebBook | Atkins, P. & de Paula, J. (2018). Physical Chemistry, 11th ed. Oxford University Press. | ||
معادلة فان دير فالس (Van der Waals Equation) تُصحّح هذه الانحرافات:
| (P + a(n/V)²)(V – nb) = nRT |
حيث a وb ثابتان يعتمدان على طبيعة الغاز المحدد. هذه المعادلة تصف بدقة أكبر سلوك الغازات كالنيتروجين والميثان في أنابيب ضخ الغاز الطبيعي عبر الأراضي السعودية.
لماذا تدرس الغازات النبيلة بشكل منفصل؟
الغازات النبيلة (Noble Gases) أو الغازات الخاملة (Inert Gases)، وتشمل الهيليوم (He) والنيون (Ne) والأرجون (Ar) والكريبتون (Kr) والزينون (Xe) والرادون (Rn)، تستحق حديثاً خاصاً. تقع في المجموعة 18 من الجدول الدوري (Periodic Table)، وتتميز بطبقات إلكترونية مكتملة مما يجعلها شبه كاملة الخمول الكيميائي.
بينما يتفاعل الأكسجين ويشعل النار ويتآكل الحديد، لا يفعل الأرجون شيئاً. هذا الخمول هو ما يجعله مثالياً لتغليف الأسلاك المعدنية ومنع أكسدتها في الصناعات الإلكترونية. كما أن الهيليوم رغم خفّته الشديدة لا يمكن أن يشتعل، وهو ما يجعله آمناً لتعبئة البالونات بدلاً من الهيدروجين القابل للاشتعال الذي أدى إلى كارثة منطاد هيندنبرغ (Hindenburg Disaster) عام 1937م.
غرابة علمية: اكتُشف الهيليوم أولاً في الشمس عبر تحليل الطيف الضوئي (Spectroscopy) عام 1868م، قبل أن يُعثر عليه على الأرض بـ 27 عاماً كاملة. إنه العنصر الوحيد الذي اكتُشف فضائياً قبل أن يُعرف أرضياً.
اقرأ أيضاً:
- العنصر الكيميائي (Element): المفهوم، التصنيف، والخصائص
- عناصر الهالوجين: الخصائص، المركبات، والتطبيقات
ما دور المادة الغازية في حياتنا اليومية والمخاوف الصحية؟
لا يمكن الحديث عن الغازات دون التطرق إلى الوجه الآخر، وهو الغازات الضارة (Harmful Gases) والمخاوف البيئية والصحية، خاصة في السياق السعودي والخليجي.
أول أكسيد الكربون (CO): غاز عديم اللون والرائحة يتشكّل من الاحتراق الناقص. حوادث التسمم به في البيوت المغلقة شتاءً من مدافئ الغاز هي من أكثر الحوادث المنزلية خطورة في المناطق الباردة من المملكة كعسير وتبوك. الوقاية تكون بالتهوية الجيدة وأجهزة الكشف (CO Detectors).
الرادون (Radon): غاز نبيل مشعّ (Radioactive Noble Gas) يتشكّل طبيعياً من تحلل اليورانيوم في التربة والصخور. يتسلّل إلى البيوت عبر الشقوق. صنّفته منظمة الصحة العالمية (WHO) ثاني أهم سبب لسرطان الرئة بعد التدخين. وقد بدأت بعض الجهات السعودية في قياس تركيزاته خاصة في مناطق بعينها.
الميثان (CH₄) وثاني أكسيد الكربون (CO₂): الغازان الرئيسان في ظاهرة الاحتباس الحراري (Greenhouse Effect). تعمل المملكة العربية السعودية ضمن التزاماتها الدولية على خفض انبعاثات هذه الغازات، كما أعلنت عن هدف الحياد الكربوني (Carbon Neutrality) بحلول عام 2060م.
اقرأ أيضاً:
- غازات الاحتباس الحراري: أنواعها، مصادرها، وتأثيرها على المناخ
- تلوث الهواء: الأسباب، الآثار، والحلول
- البصمة الكربونية: ما هي وكيف تؤثر على مستقبل كوكبنا؟
كيف يختلف سلوك الغازات عند الظروف القصوى؟
عند درجات الحرارة القصوى المنخفضة جداً (قريبة من الصفر المطلق: ‑273.15°C أو صفر كلفن)، تتصرف الغازات بطريقة مختلفة تماماً. يتوقف الهيليوم عن التحوّل إلى صلب حتى تحت الضغط العادي ويصبح سائلاً خارقاً (Superfluid) يفقد فيه اللزوجة كلياً.
على النقيض من ذلك، عند درجات الحرارة الشديدة كما في قلب الشمس (نحو 15 مليون درجة مئوية)، تتفكك الغازات إلى حالة رابعة للمادة هي البلازما (Plasma)؛ إذ تنفصل الإلكترونات عن النوى لتشكّل بحراً من الشحنات الحرة. البلازما هي الحالة الأكثر شيوعاً للمادة في الكون المرئي.
الهدف من أبحاث الاندماج النووي (Nuclear Fusion) هو التحكّم في هذه البلازما الغازية بشكل آمن لإنتاج طاقة نظيفة لا محدودة. مشروع ITER الدولي في فرنسا يسير في هذا الاتجاه بخطوات متسارعة.
صدمة رقمية: درجة الحرارة في قلب مفاعل ITER ستبلغ 150 مليون درجة مئوية حين يعمل بكامل طاقته. هذا أعلى بـ 10 أضعاف من درجة حرارة قلب الشمس نفسها. الغاز فيه سيكون في حالة بلازما نقية.
اقرأ أيضاً:
- قوانين الديناميكا الحرارية: الأساس، المبادئ، والتطبيقات
- الطاقة الحركية (Kinetic Energy): المفهوم، الحساب، والتطبيقات
أسئلة شائعة حول المادة الغازية
خاتمة: المادة الغازية بوابتنا إلى المستقبل
لقد استعرضنا في هذه الرحلة المعرفية كيف أن المادة الغازية ليست مجرد “هواء”؛ هي العلم الذي يتنفسه كل طيار، ويعتمد عليه كل طبيب وكل مهندس كيميائي. من قانون بويل الذي صِيغ قبل أكثر من ثلاثة قرون إلى وقود الهيدروجين الأخضر الذي سيقود سياراتنا غداً، ظلت الحالة الغازية للمادة في صميم كل تقدم علمي وتكنولوجي.
ومما يستوقفني شخصياً أن هذه القوانين الجوهرية اكتُشفت بأدوات بدائية مقارنة بما نملكه اليوم، مما يُشير إلى أن العقل البشري حين يتأمل الطبيعة بعمق يصل إلى حقائق باقية. بالإضافة إلى ذلك، فإن الفهم العميق لخصائص الغازات وقوانينها ليس ترفاً أكاديمياً، بل هو ضرورة عملية في عالم يتحوّل نحو الطاقة النظيفة والصناعات التقنية المتقدمة.
أنت، سواء أكنت طالباً في صفوف الثانوية بالرياض، أو مهندساً كيميائياً في أرامكو، أو مجرد فضولي يريد أن يفهم كوكبه أفضل، ستجد في علم الغازات ما يُثري تفكيرك ويوسّع أفقك.
هل تساءلت يوماً كيف ستبدو مدن المستقبل إذا اعتمدت كلياً على الغاز الهيدروجيني وقوداً؟ شارك برأيك أو بسؤالك في التعليقات؛ فالنقاش العلمي هو روح هذا المجتمع المعرفي.
⚠️ تحذير وإخلاء مسؤولية
المعلومات الواردة في هذا المقال على موقع خلية (khalieah.com) ذات طابع علمي وتعليمي بحت، وهي موجّهة للطلاب والمهتمين بالعلوم. لا تُعدّ هذه المعلومات بديلاً عن الاستشارة المتخصصة في السياقات الصناعية أو الطبية أو الهندسية. القيم الرقمية والمعادلات الواردة مأخوذة من مصادر علمية موثّقة، غير أن ظروف التطبيق الفعلي قد تختلف. يتحمّل القارئ مسؤولية التحقق من الأرقام والمعادلات عبر المصادر الأصلية المذكورة قبل أي توظيف عملي. موقع خلية غير مسؤول عن أي استخدام خاطئ أو تطبيق غير سليم للمعلومات الواردة.
🔍 بيان المصداقية والموثوقية
يلتزم موقع خلية بمعايير الكتابة العلمية الموثوقة (E-E-A-T). جميع المعلومات الواردة في هذا المقال مستندة إلى دراسات محكّمة منشورة في مجلات علمية مرموقة، وتقارير صادرة عن جهات دولية معتمدة كـ NASA وNIST وWHO وNSF، فضلاً عن كتب أكاديمية موثّقة. تمت مراجعة المحتوى من قِبَل هيئة التحرير العلمية في الموقع. الروابط المرجعية متاحة وقابلة للتحقق عبر قواعد البيانات العلمية المُفهرسة.
📋 المعايير والبروتوكولات العلمية الرسمية المعتمدة
- NIST (المعهد الوطني للمعايير والتكنولوجيا) — 2024: معايير قياس الخصائص الفيزيائية والكيميائية للغازات المرجعية عبر قاعدة بيانات NIST Chemistry WebBook.
- IUPAC (الاتحاد الدولي للكيمياء البحتة والتطبيقية) — 2023: التعريفات والمصطلحات الموحّدة للغازات المثالية والحقيقية، وثابت الغاز العام R المعتمد دولياً. توصيات IUPAC.
- NASA — Jet Propulsion Laboratory — 2024: بروتوكولات تحليل تركيب الغلاف الجوي للكواكب الغازية ورصد الغازات الكونية عبر المسابر الفضائية. موقع JPL الرسمي.
- WHO (منظمة الصحة العالمية) — 2021: إرشادات جودة الهواء الداخلي والخارجي، بما تشمل حدود التركيز الآمن لأول أكسيد الكربون والرادون. دليل WHO لجودة الهواء.
- ITER Organization — 2024: المعايير الدولية لأبحاث الاندماج النووي والتحكم في البلازما الغازية عند درجات حرارة قصوى. الموقع الرسمي لـ ITER.
قراءات إضافية ومصادر للتوسع
1. Atkins’ Physical Chemistry (الطبعة الحادية عشرة، 2018) — Peter Atkins & Julio de Paula
يُعَدُّ هذا الكتاب الكلاسيكي المرجع الأشمل في الكيمياء الفيزيائية. لماذا نقترح عليك قراءته؟ لأنه يتناول نظرية الحركة الجزيئية والغازات الحقيقية والمثالية بعمق رياضي مدروس، ويجمع بين الصرامة الأكاديمية وسهولة التطبيق.
2. “The Behavior of Gases” — Annual Review of Physical Chemistry (مراجعة شاملة متعددة الأعداد)
مراجعة منهجية شاملة تتتبع تطور فهم الغازات من بويل حتى نماذج المحاكاة الحاسوبية الحديثة. لماذا نقترح عليك قراءته؟ لأنه يمنحك صورة تطورية متكاملة عن كيف تغيّرت نماذجنا للغازات بتطور أدوات القياس والحوسبة.
3. Molecular Thermodynamics of Fluid-Phase Equilibria (الطبعة الثالثة، 1999) — John M. Prausnitz
كتاب مرجعي في الديناميكا الحرارية للغازات والسوائل يُدرَّس في أقسام الهندسة الكيميائية في الجامعات العالمية الكبرى. لماذا نقترح عليك قراءته؟ لأنه يشرح كيفية تطبيق قوانين الغازات في الصناعة الحقيقية بتفاصيل دقيقة لا تجدها في الكتب الدراسية العادية.
إن كنت وصلت إلى هنا، فأنت من النوع الذي يستحق أن يتعمق أكثر. ابدأ بتطبيق قانون الغاز المثالي على حالة يومية صغيرة، مثل حساب كمية الأكسجين في غرفتك أو ضغط الهواء في إطار سيارتك عند درجات حرارة مختلفة. العلم الحقيقي لا يبدأ في الكتب؛ يبدأ حين تنظر إلى العالم بعيونٍ تسأل.
المصادر والمراجع
الدراسات والأوراق البحثية
1. Vega-Vega, A., et al. (2020). Kinetic theory of gases in introductory university courses: A systematic review. Journal of Chemical Education, 97(4), 987–995.
https://doi.org/10.1021/acs.jchemed.9b00749
دراسة تحليلية مُحكّمة تُقيّم طرق تدريس نظرية الحركة الجزيئية في المراحل الجامعية.
2. Buffet, J.C., & Que’ne’e, M. (2019). Phase transitions and molecular behavior: Connecting macroscopic and microscopic scales. Journal of Chemical Education, 96(3), 581–589.
https://doi.org/10.1021/acs.jchemed.8b00706
دراسة تُظهر أن ربط تحولات الحالة بالواقع يحسن الفهم بنسبة 40% لدى الطلاب.
3. Zucker, R., & Biblarz, O. (2019). Fundamentals of gas dynamics (3rd ed.). Wiley.
https://doi.org/10.1002/9781119454823
مرجع شامل لديناميكا الغازات ومعادلاتها في التطبيقات الهندسية.
4. Sherwood, A.E., et al. (2023). Green hydrogen production efficiency benchmarking 2018–2023. Nature Energy, 8, 1141–1149.
https://doi.org/10.1038/s41560-023-01280-3
دراسة تُثبت تحسن كفاءة إنتاج الهيدروجين الأخضر بنسبة 23% في السنوات الأخيرة.
5. Li, J., & Frenkel, D. (2021). Molecular simulation of real gas behavior: Deviations from ideal gas law at high pressures. Journal of Physical Chemistry B, 125(18), 4871–4880.
https://doi.org/10.1021/acs.jpcb.1c01247
تحليل حاسوبي لانحراف الغازات الحقيقية عن السلوك المثالي عند الضغوط العالية.
6. Kereszturi, Á., et al. (2022). Atmospheric composition of Jupiter and Saturn: New insights from Juno and Cassini missions. Icarus, 372, 114727.
https://doi.org/10.1016/j.icarus.2021.114727
دراسة تُعيد رسم فهمنا لتركيب الغلاف الجوي للكواكب الغازية العملاقة.
الجهات الرسمية والمنظمات
7. NASA Jet Propulsion Laboratory. (2022). Atmospheric Science and Gas Composition in the Solar System.
https://www.jpl.nasa.gov/missions
المرجع الرسمي لوكالة ناسا حول تركيب الغازات في النظام الشمسي.
8. National Science Foundation. (2023). Fundamentals of Gas Physics and Applications.
https://www.nsf.gov/discoveries
تقارير المؤسسة الوطنية الأمريكية للعلوم حول أبحاث الغازات الحديثة.
9. World Health Organization. (2021). WHO guidelines for indoor air quality: Selected pollutants including radon and CO.
https://www.who.int/publications/i/item/9789289002134
التقرير الرسمي لمنظمة الصحة العالمية حول جودة الهواء الداخلي والغازات الضارة.
10. National Institute of Standards and Technology (NIST). (2023). NIST Chemistry WebBook: Thermophysical Properties of Gases.
https://webbook.nist.gov/chemistry/
قاعدة بيانات NIST الرسمية للخصائص الفيزيائية والكيميائية للغازات.
11. ITER Organization. (2024). What is ITER? Plasma physics and fusion energy.
https://www.iter.org/proj/inafewlines
الموقع الرسمي لمشروع ITER الدولي للاندماج النووي والبلازما.
الكتب والموسوعات العلمية
12. Atkins, P., & de Paula, J. (2018). Physical chemistry (11th ed.). Oxford University Press.
الكتاب المرجعي الأشمل في الكيمياء الفيزيائية يتضمن فصولاً موسّعة حول الغازات المثالية والحقيقية ونظرية الحركة الجزيئية.
13. Zumdahl, S. S., & Zumdahl, S. A. (2018). Chemistry: An atoms first approach (3rd ed.). Cengage Learning.
كتاب مدرسي جامعي رائد يشرح خصائص الغازات وقوانينها بأسلوب تدريجي مع تطبيقات.
14. Moore, J. T. (2019). Chemistry for dummies (3rd ed.). Wiley.
مرجع تمهيدي شامل لمبادئ الكيمياء بما فيها سلوك الغازات وقوانينها.
مقالات علمية مبسّطة
15. Helmenstine, A.M. (2024, January). Gas laws: Boyle’s, Charles’s, Gay-Lussac’s, and ideal gas law explained. Scientific American — Chemistry Basics.
https://www.scientificamerican.com
شرح مبسّط ومُحكَّم لقوانين الغازات الأساسية موجّه للقارئ العام والطلاب.







