ما هي الديناميكا الحرارية: وكيف تتحكم الحرارة والطاقة في كل شيء حولنا؟
ما العلاقة بين كوب الشاي الساخن ومحرك سيارتك والكون بأسره؟

تعريف مختصر
الديناميكا الحرارية فرعٌ أساسي من فروع الفيزياء يدرس العلاقات بين الحرارة والشغل والطاقة. تُعنى هذه العلوم بتحولات الطاقة في الأنظمة الفيزيائية والكيميائية. تحكمها أربعة قوانين أساسية تصف سلوك المادة والطاقة. نشأت في القرن التاسع عشر مع الثورة الصناعية. تُطبَّق اليوم في الهندسة والكيمياء والأحياء وعلوم المواد.
هل تساءلت يوماً لماذا يبرد كوب الشاي الذي تركته على مكتبك؟ أو كيف تستطيع ثلاجتك أن تُبقي طعامك بارداً رغم حرارة الصيف القائظ؟ ربما وقفت حائراً أمام سؤال بسيط: لماذا لا يمكن لمحرك سيارتك أن يعمل بكفاءة كاملة مهما تطورت التقنية؟
أنت لست وحدك في هذه الحيرة. لقد شغلت هذه الأسئلة عقول العلماء لقرون، ومن رحم البحث عن إجاباتها وُلد علم الديناميكا الحرارية. في هذا المقال، ستكتشف أن الإجابات ليست معقدة كما تتخيل؛ إذ إن فهمك لهذا العلم سيغير نظرتك للعالم من حولك. ستدرك أن القوانين التي تحكم محركات الطائرات هي ذاتها التي تفسر برودة قدميك في ليالي الشتاء.
كيف نشأت الديناميكا الحرارية وما قصتها التاريخية؟
لم تولد الديناميكا الحرارية في المختبرات الأكاديمية الهادئة، بل وُلدت في قلب المصانع الصاخبة إبان الثورة الصناعية. كان المهندسون في بريطانيا وفرنسا يسعون جاهدين لتحسين كفاءة المحركات البخارية التي كانت تُدير المصانع والقطارات. من هذه الحاجة العملية الملحة، انطلق البحث النظري الذي أسس لهذا العلم العظيم.
في عام 1824، نشر المهندس الفرنسي الشاب سادي كارنو (Sadi Carnot) كتابه الشهير “تأملات في القوة المحركة للنار”. كان عمره آنذاك 28 عاماً فقط. وضع كارنو في هذا الكتاب أسس فهمنا للمحركات الحرارية؛ إذ أثبت أن هناك حداً أقصى للكفاءة لا يمكن لأي محرك تجاوزه مهما بلغت براعة تصميمه. لقد كانت هذه الفكرة ثورية في وقتها، ولا تزال صامدة حتى اليوم.
معلومة سريعة: توفي سادي كارنو بمرض الكوليرا عن عمر يناهز 36 عاماً، ولم يشهد التقدير الكبير الذي ناله عمله لاحقاً. أُحرقت معظم أوراقه ومخطوطاته خوفاً من انتشار العدوى، وضاعت بذلك أفكار كثيرة ربما كانت ستسرّع تطور الفيزياء.
جاء بعد كارنو علماء عظام أكملوا البناء. الألماني رودولف كلاوزيوس (Rudolf Clausius) صاغ القانون الثاني للديناميكا الحرارية بصورته الرياضية الدقيقة في خمسينيات القرن التاسع عشر. كذلك قدّم مفهوم الإنتروبيا (Entropy) الذي أصبح حجر الزاوية في فهمنا لاتجاه العمليات الطبيعية. وفي الجانب الآخر من الأطلسي، طوّر الأمريكي جوزايا ويلارد جيبس (Josiah Willard Gibbs) الأسس الرياضية للديناميكا الحرارية الكيميائية في سبعينيات القرن ذاته.
أما اللورد كلفن، واسمه الحقيقي وليام طومسون (William Thomson)، فقد صاغ مصطلح “الديناميكا الحرارية” عام 1854. ساهم أيضاً في تطوير مقياس الحرارة المطلق الذي يحمل اسمه حتى اليوم (الكلفن). من ناحية أخرى، ربط العالم النمساوي لودفيغ بولتزمان (Ludwig Boltzmann) بين العالم الميكروسكوبي للذرات والجزيئات والخصائص الحرارية الكبرى التي نرصدها، مؤسساً بذلك الميكانيكا الإحصائية (Statistical Mechanics).
ما المفاهيم الأساسية التي يجب أن تفهمها أولاً؟
قبل أن نغوص في قوانين الديناميكا الحرارية، نحتاج إلى فهم بعض المفاهيم التأسيسية. هذه المفاهيم ستكون أدواتك لفهم كل ما يأتي لاحقاً، فخذ وقتك في استيعابها جيداً.
المفهوم الأول هو “النظام الحراري” (Thermodynamic System). النظام هو ببساطة الجزء من الكون الذي نريد دراسته. قد يكون هذا النظام غازاً داخل أسطوانة، أو ماءً في قدر، أو حتى جسم الإنسان. كل ما عدا النظام نسميه “المحيط” (Surroundings)، والحدود التي تفصل بينهما تُسمى “جدران النظام” (System Boundaries).
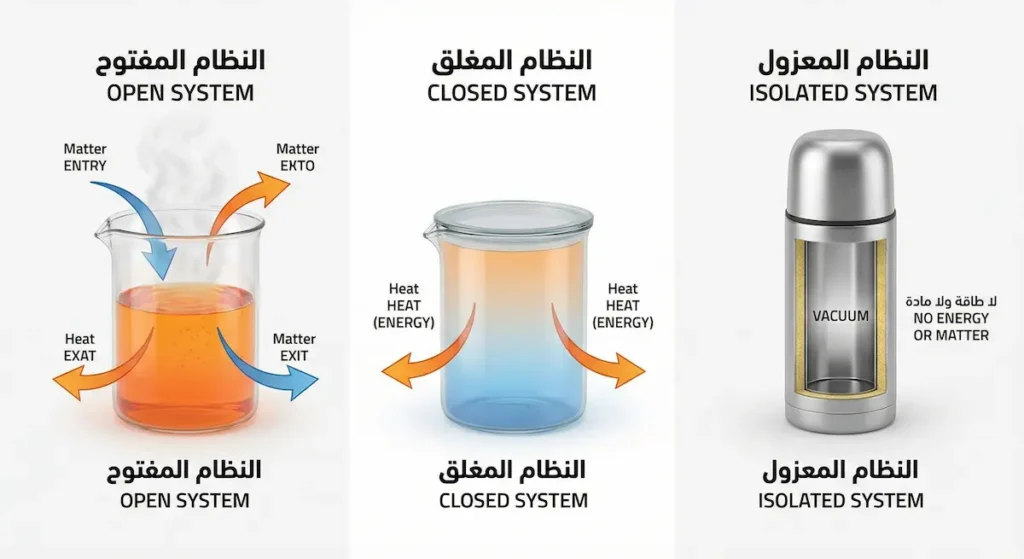
تنقسم الأنظمة الحرارية إلى ثلاثة أنواع رئيسة. النظام المفتوح (Open System) يسمح بتبادل كل من المادة والطاقة مع محيطه؛ مثل قدر الطبخ المكشوف. النظام المغلق (Closed System) يسمح بتبادل الطاقة فقط دون المادة؛ كالقدر المغطى بإحكام. أما النظام المعزول (Isolated System) فلا يتبادل شيئاً مع محيطه إطلاقاً، لا مادة ولا طاقة. الكون بأكمله يُعدُّ النظام المعزول الوحيد الحقيقي.
المفهوم الثاني مهم جداً: “الحالة الحرارية” (Thermodynamic State). نصف حالة أي نظام بمجموعة من المتغيرات مثل الضغط (Pressure) ودرجة الحرارة (Temperature) والحجم (Volume). عندما تتغير هذه المتغيرات، نقول إن النظام انتقل من حالة إلى أخرى. هذا الانتقال هو ما ندرسه في الديناميكا الحرارية.
حقيقة علمية: يمكن وصف حالة غاز مثالي بثلاثة متغيرات فقط: الضغط والحجم ودرجة الحرارة. لكن في الواقع، نحتاج غالباً إلى متغيرين فقط لأن المعادلة الشهيرة PV = nRT تربط بينها جميعاً.
ثمة مفاهيم أخرى ستصادفها كثيراً. “الشغل” (Work) في الديناميكا الحرارية هو الطاقة المنقولة عندما تتحرك حدود النظام تحت تأثير قوة. تخيّل مكبساً يضغط غازاً داخل أسطوانة: القوة المبذولة مضروبة في المسافة تُعطينا الشغل المبذول. “الحرارة” (Heat) بالمقابل هي الطاقة المنتقلة بسبب فرق درجات الحرارة. كلاهما طريقتان لنقل الطاقة، لكنهما مختلفتان جوهرياً.
أخيراً، هناك “دوال الحالة” (State Functions) و”دوال المسار” (Path Functions). دوال الحالة تعتمد فقط على الحالة الحالية للنظام، بغض النظر عن كيفية وصوله إليها؛ مثل الطاقة الداخلية والإنتروبيا. بينما دوال المسار تعتمد على المسار الذي سلكه النظام؛ مثل الحرارة والشغل. هذا التمييز دقيق لكنه جوهري.
ما القانون الصفري وكيف يُعرّف التوازن الحراري؟
قد يبدو غريباً أن نبدأ بقانون يحمل الرقم “صفر”، لكن هذا القانون سُمي هكذا لأنه اكتُشف بعد القانونين الأول والثاني، رغم أنه أكثر أساسية منهما. فقد أدرك العلماء لاحقاً أنه يجب أن يسبقهما منطقياً.
ينص القانون الصفري للديناميكا الحرارية (Zeroth Law of Thermodynamics) على ما يلي: إذا كان جسمان (أ) و(ب) في توازن حراري مع جسم ثالث (ج)، فإن الجسمين (أ) و(ب) في توازن حراري مع بعضهما. يبدو هذا بديهياً، أليس كذلك؟ لكنه في الحقيقة يُؤسس لمفهوم درجة الحرارة ذاته.
لنوضح الأمر بمثال عملي. تخيل أن لديك كوب ماء ساخن (أ) وكوب ماء بارد (ب)، ووضعت ميزان حرارة (ج) في الكوب الأول حتى استقرت قراءته، ثم نقلته إلى الكوب الثاني. إذا أعطى الميزان القراءة نفسها في الكوبين، فهذا يعني أن الكوبين لهما درجة الحرارة ذاتها؛ إذ كلاهما في توازن حراري مع الميزان. هذا هو جوهر القانون الصفري.
بفضل هذا القانون، نستطيع قياس درجة الحرارة ومقارنتها بين أجسام مختلفة. دون هذا القانون، لن يكون لموازين الحرارة أي معنى. إنه الأساس الذي يُبنى عليه كل شيء آخر في الديناميكا الحرارية.
لمحة تاريخية: صاغ العالم البريطاني رالف فاولر (Ralph Fowler) القانون الصفري رسمياً عام 1931، أي بعد أكثر من قرن من صياغة القانونين الأول والثاني. أدرك فاولر أن هذا المبدأ كان مفترضاً ضمنياً طوال تلك الفترة دون أن يُصاغ صراحةً.
التوازن الحراري (Thermal Equilibrium) حالة مهمة جداً. عندما يكون نظامان في توازن حراري، لا تنتقل حرارة صافية بينهما. هذا لا يعني أن الجزيئات تتوقف عن الحركة، بل يعني أن معدل انتقال الطاقة في الاتجاهين متساوٍ. درجة الحرارة المتساوية هي شرط التوازن الحراري وعلامته في آن معاً.
كيف ينص القانون الأول على حفظ الطاقة؟
القانون الأول للديناميكا الحرارية (First Law of Thermodynamics) هو في جوهره تطبيق لمبدأ حفظ الطاقة على الأنظمة الحرارية. ينص على أن الطاقة لا تُخلق من عدم ولا تُفنى، إنما تتحول من شكل إلى آخر. الطاقة الكلية للكون ثابتة دائماً.
رياضياً، يمكن التعبير عن هذا القانون بالمعادلة: ΔU=Q−W
حيث ΔU هو التغير في الطاقة الداخلية للنظام، وQ هي الحرارة المضافة إلى النظام، وW هو الشغل الذي يبذله النظام. هذه المعادلة البسيطة تختصر قانوناً كونياً عظيماً.
لنفهم هذا بمثال ملموس. تخيل أنك تضخ هواءً في إطار دراجة. أنت تبذل شغلاً على الهواء داخل المضخة، وستلاحظ أن المضخة تسخن. هذا لأن الشغل الذي بذلته تحول إلى طاقة داخلية في الغاز، مما رفع درجة حرارته. لم تُخلق طاقة من عدم؛ إنما تحولت طاقة عضلاتك إلى طاقة حرارية.
القانون الأول يمنعنا من بناء ما يُسمى “آلة الحركة الدائمة من النوع الأول” (Perpetual Motion Machine of the First Kind). هذه آلة خيالية تُنتج شغلاً دون أن تستهلك أي طاقة. لقد حاول كثيرون عبر التاريخ بناء مثل هذه الآلة، لكنهم فشلوا جميعاً. القانون الأول يُخبرنا أن فشلهم لم يكن صدفة، بل ضرورة فيزيائية.
من جهة ثانية، يُقدم القانون الأول مفهوم “الطاقة الداخلية” (Internal Energy) الذي يرمز له بـ U. هذه هي الطاقة الكلية المخزنة في النظام على المستوى الميكروسكوبي: طاقة حركة الجزيئات وطاقة التفاعلات بينها. لا نستطيع قياس الطاقة الداخلية مباشرة، لكننا نستطيع قياس التغير فيها بدقة.
رقم مدهش: تُقدر الطاقة الداخلية في لتر واحد من الماء عند درجة حرارة الغرفة بنحو 300 كيلوجول. هذه طاقة هائلة لو استطعنا تحريرها كلها، لكن معظمها مقيد في حركة الجزيئات العشوائية.
هناك دالة حرارية أخرى مرتبطة بالقانون الأول تُسمى “الإنثالبي” (Enthalpy) ويُرمز لها بـ H. تُعرَّف بالعلاقة: H=U+PV
الإنثالبي مفيدة جداً في دراسة التفاعلات الكيميائية التي تحدث عند ضغط ثابت، وهي الحالة الأكثر شيوعاً في المختبرات والصناعة.
اقرأ أيضاً: الطاقة في الفيزياء: ما هي أشكالها وكيف تتحول بين الأنظمة؟
لماذا يُعدُّ القانون الثاني أهم قوانين الفيزياء؟
إذا كان القانون الأول يُخبرنا بكمية الطاقة التي يمكن تحويلها، فإن القانون الثاني للديناميكا الحرارية (Second Law of Thermodynamics) يُخبرنا بالاتجاه الذي تسير فيه العمليات الطبيعية. إنه القانون الذي يُميز الماضي من المستقبل، ويشرح لماذا لا يعود الزمن إلى الوراء.
للقانون الثاني صياغات متعددة، كلها متكافئة رياضياً رغم اختلاف ظاهرها. صياغة كلاوزيوس تقول: لا يمكن للحرارة أن تنتقل تلقائياً من جسم بارد إلى جسم أسخن. صياغة كلفن-بلانك تقول: لا يمكن بناء محرك حراري يحول الحرارة بالكامل إلى شغل دون أي أثر آخر.
لكن الصياغة الأكثر عمومية تستخدم مفهوم الإنتروبيا (Entropy): في أي عملية طبيعية، تميل الإنتروبيا الكلية للكون إلى الازدياد أو البقاء ثابتة، ولا تنقص أبداً. رياضياً: ΔSuniverse≥0
فما هي الإنتروبيا يا ترى؟ يمكن فهمها على أنها مقياس “الفوضى” أو “العشوائية” في النظام. لكن التعريف الأدق هو أنها مقياس لعدد الطرق الميكروسكوبية التي يمكن أن يتحقق بها وضع ماكروسكوبي معين. كلما زادت هذه الطرق، زادت الإنتروبيا.
لنأخذ مثالاً بسيطاً. إذا وضعت قطرة حبر في كوب ماء، ستنتشر تدريجياً حتى يتوزع الحبر بالتساوي. هذا الانتشار يزيد الإنتروبيا. على النقيض من ذلك، لن تشاهد أبداً الحبر يتجمع تلقائياً في قطرة واحدة مرة أخرى. ليس لأن هذا مستحيل فيزيائياً، بل لأن احتماله صغير بشكل لا يمكن تصوره.
القانون الثاني يفسر أيضاً لماذا لا يمكن لأي محرك حراري أن يعمل بكفاءة 100%. جزء من الطاقة يجب أن “يُهدر” كحرارة تُطرح إلى المحيط. هذا ليس عيباً هندسياً يمكن إصلاحه؛ إنه قانون كوني لا مفر منه. أفضل المحركات الحرارية في محطات توليد الكهرباء الحديثة تصل كفاءتها إلى نحو 60% فقط.
معلومة سريعة: حسب القانون الثاني، يتجه الكون ككل نحو ما يُسمى “الموت الحراري” (Heat Death)، حالة من التوازن الكامل لا تحدث فيها أي عمليات مفيدة. لكن لا تقلق، هذا لن يحدث قبل تريليونات السنين!
العالم النمساوي لودفيغ بولتزمان ربط الإنتروبيا بالعالم الميكروسكوبي بمعادلته الشهيرة: S=kBlnΩ
حيث kB هو ثابت بولتزمان، وΩ هو عدد الحالات الميكروسكوبية الممكنة. هذه المعادلة محفورة على شاهد قبره في فيينا، وهي تُعدُّ من أجمل المعادلات في تاريخ الفيزياء.
ماذا يقول القانون الثالث عن الصفر المطلق؟
القانون الثالث للديناميكا الحرارية (Third Law of Thermodynamics) يتعلق بما يحدث عند درجات الحرارة المنخفضة للغاية. ينص على أن إنتروبيا نظام بلوري مثالي تقترب من الصفر كلما اقتربت درجة حرارته من الصفر المطلق.
الصفر المطلق (Absolute Zero) هو أدنى درجة حرارة ممكنة نظرياً، ويساوي صفر كلفن أو -273.15 درجة مئوية. عند هذه الدرجة، تتوقف الحركة الحرارية للجزيئات تماماً (باستثناء اهتزازات نقطة الصفر الكمومية). لا يوجد في الجزيئات طاقة حرارية يمكن استخلاصها.
نتيجة مهمة للقانون الثالث: من المستحيل الوصول إلى الصفر المطلق بعدد محدود من الخطوات. يمكننا الاقتراب منه أكثر فأكثر، لكننا لن نصل إليه أبداً. هذا يُسمى أحياناً “صيغة نرنست” للقانون الثالث، نسبةً إلى العالم الألماني فالتر نرنست (Walther Nernst) الذي صاغه عام 1906.
لقد نجح العلماء في تبريد المواد إلى درجات قريبة جداً من الصفر المطلق. في عام 2021، وصل فريق في معهد ماساتشوستس للتقنية (MIT) إلى درجة حرارة تبلغ 38 تريليون جزء من الكلفن فوق الصفر المطلق. عند هذه الدرجات، تظهر ظواهر كمومية غريبة مثل الميوعة الفائقة (Superfluidity) والموصلية الفائقة (Superconductivity).
ما أنواع العمليات الحرارية وكيف تختلف عن بعضها؟
عندما ينتقل نظام حراري من حالة إلى أخرى، فإنه يمر بما نسميه “عملية حرارية” (Thermodynamic Process). هناك عدة أنواع مثالية من هذه العمليات، كل منها يتميز بثبات متغير معين:
- العملية الأيزوثرمية (Isothermal Process): تحدث عند درجة حرارة ثابتة. مثال: ضغط غاز ببطء شديد بحيث تتسرب الحرارة الناتجة إلى المحيط. في هذه العملية، تبقى الطاقة الداخلية ثابتة للغاز المثالي.
- العملية الأديباتية (Adiabatic Process): لا يحدث فيها تبادل حراري مع المحيط. مثال: الضغط السريع للغاز في أسطوانة معزولة. هنا ترتفع درجة حرارة الغاز لأن كل الشغل يتحول إلى طاقة داخلية.
- العملية الأيزوبارية (Isobaric Process): تحدث عند ضغط ثابت. مثال: تسخين غاز في أسطوانة ذات مكبس حر الحركة. الغاز يتمدد ليحافظ على الضغط ثابتاً.
- العملية الأيزوكورية (Isochoric Process): تحدث عند حجم ثابت. مثال: تسخين غاز في وعاء صلب مغلق. الضغط يرتفع لأن الغاز لا يستطيع التمدد.
فهم هذه العمليات ضروري لتحليل الدورات الحرارية في المحركات والثلاجات. كل محرك حقيقي هو مزيج من هذه العمليات بدرجات متفاوتة من المثالية.
حقيقة علمية: العملية الأديباتية هي سبب ارتفاع درجة حرارة الهواء عند ضغطه في محرك الديزل إلى نحو 550 درجة مئوية، مما يكفي لإشعال الوقود تلقائياً دون الحاجة إلى شمعات إشعال.
هناك أيضاً “العمليات العكوسة” (Reversible Processes) و”العمليات اللاعكوسة” (Irreversible Processes). العملية العكوسة هي عملية مثالية يمكن عكس اتجاهها دون ترك أي أثر في النظام أو محيطه. في الواقع، كل العمليات الطبيعية لاعكوسة بدرجة ما بسبب الاحتكاك وانتقال الحرارة عبر فروق محدودة في درجات الحرارة.
اقرأ أيضاً: قانون الغاز المثالي: المفهوم، الصيغة، والتطبيقات
كيف تعمل دورة كارنو ولماذا هي مهمة؟
دورة كارنو (Carnot Cycle) هي دورة حرارية مثالية اقترحها سادي كارنو عام 1824. رغم أنها نظرية بحتة ولا يمكن تحقيقها عملياً، إلا أنها تضع الحد الأعلى للكفاءة التي يمكن أن يحققها أي محرك حراري يعمل بين مستودعين حراريين.
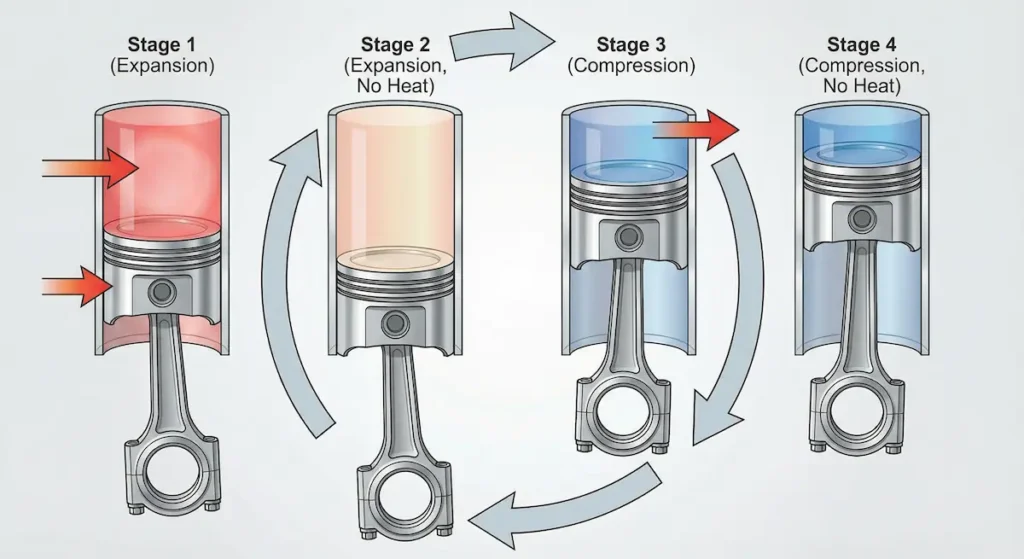
تتكون دورة كارنو من أربع عمليات متتالية تُعيد النظام إلى حالته الأولى:
- تمدد أيزوثرمي: الغاز يتمدد ويمتص حرارة من المستودع الساخن عند درجة حرارة TH.
- تمدد أديباتي: الغاز يستمر بالتمدد دون تبادل حراري، فتنخفض درجة حرارته.
- انضغاط أيزوثرمي: الغاز يُضغط ويطرد حرارة إلى المستودع البارد عند درجة حرارة TC.
- انضغاط أديباتي: الغاز يستمر بالانضغاط دون تبادل حراري، فترتفع درجة حرارته إلى قيمتها الأولى.
كفاءة محرك كارنو المثالي تُعطى بالمعادلة: ηCarnot=1−THTC
حيث درجات الحرارة مُقاسة بالكلفن. هذه المعادلة تُخبرنا بشيء عميق: كلما زاد الفرق بين درجتي حرارة المستودعين، زادت الكفاءة القصوى الممكنة.
لنحسب مثالاً. محطة توليد كهرباء تعمل بالبخار، المستودع الساخن (البخار) عند 600 كلفن والمستودع البارد (ماء التبريد) عند 300 كلفن. الكفاءة القصوى النظرية: ηmax=1−600300=0.5=50%
هذا يعني أنه حتى في أفضل الظروف المثالية، نصف الطاقة الحرارية يجب أن يُطرح إلى المحيط. في الواقع، الكفاءة الفعلية أقل من ذلك بسبب اللاعكوسية.
معلومة سريعة: محطات توليد الكهرباء ذات الدورة المركبة (Combined Cycle) الحديثة تصل كفاءتها إلى نحو 62%، وهي من أعلى الكفاءات المحققة في تحويل الحرارة إلى كهرباء. تُستخدم هذه التقنية بشكل متزايد في الدول العربية، خاصة في الإمارات والسعودية.
كيف تعمل المحركات الحرارية في حياتنا اليومية؟
المحركات الحرارية (Heat Engines) هي أجهزة تحول الطاقة الحرارية إلى شغل ميكانيكي. إنها القلب النابض للحضارة الصناعية، من السيارات إلى محطات توليد الكهرباء.
دورة أوتو (Otto Cycle) هي الدورة المثالية لمحركات البنزين. سُميت باسم المهندس الألماني نيكولاس أوتو الذي طور أول محرك احتراق داخلي ناجح تجارياً عام 1876. تتكون من أربعة أشواط: السحب، الانضغاط، القدرة (الاحتراق والتمدد)، والعادم. نسبة الانضغاط (Compression Ratio) هي العامل الرئيس في تحديد كفاءة المحرك.
دورة ديزل (Diesel Cycle) تختلف في أن الاشتعال يحدث تلقائياً بسبب ارتفاع درجة حرارة الهواء المضغوط، دون الحاجة إلى شرارة. نسب الانضغاط في محركات الديزل أعلى (حوالي 20:1 مقارنة بـ 10:1 للبنزين)، مما يعطيها كفاءة أعلى. لهذا تُفضل محركات الديزل في الشاحنات والمعدات الثقيلة.
دورة رانكين (Rankine Cycle) هي الأساس لمحطات توليد الكهرباء البخارية. الماء يُسخن في غلاية ليصبح بخاراً عالي الضغط، ثم يتمدد في توربينة لتوليد الكهرباء، ثم يُكثف ويُعاد إلى الغلاية. هذه الدورة تُنتج نحو 80% من الكهرباء في العالم.
مثال تطبيقي من الواقع العربي: محطة “نور” للطاقة الشمسية المركزة في المغرب تستخدم مبادئ الديناميكا الحرارية ذاتها. المرايا تُركز أشعة الشمس لتسخين ملح مصهور إلى نحو 400 درجة مئوية، ثم تُستخدم هذه الحرارة لتوليد بخار يُدير توربينات. الكفاءة تصل إلى نحو 40%، وهي منافسة للوقود الأحفوري.
اقرأ أيضاً: المحرك البخاري (Steam Engine): الاختراع، المبدأ، والتأثير الصناعي
كيف تعمل الثلاجات والمكيفات؟
الثلاجات والمكيفات هي “محركات حرارية معكوسة” أو ما يُسمى “المضخات الحرارية” (Heat Pumps). بدلاً من تحويل الحرارة إلى شغل، تستخدم الشغل لنقل الحرارة من مكان بارد إلى مكان أسخن.
هل هذا يتعارض مع القانون الثاني؟ لا، لأن العملية ليست تلقائية. نحن نبذل شغلاً (الكهرباء التي تُشغل الضاغط) لنقل الحرارة في الاتجاه “غير الطبيعي”. القانون الثاني يمنع الانتقال التلقائي فقط.
المبدأ بسيط: سائل التبريد (مثل الفريون) يمر بدورة من الضغط والتمدد. عندما يتمدد (في المبخر داخل الثلاجة)، يمتص حرارة من محيطه فيبرّده. عندما يُضغط (في المكثف خارج الثلاجة)، يطرد هذه الحرارة إلى الهواء الخارجي. لهذا تشعر بالحرارة خلف الثلاجة.
حقيقة علمية: مكيف الهواء الذي تستخدمه في الصيف يمكنه نظرياً نقل حرارة أكثر مما يستهلك من كهرباء. معامل الأداء (COP) للمكيفات الحديثة يصل إلى 4 أو أكثر، أي أن كل كيلوواط كهرباء ينقل 4 كيلوواط من الحرارة. هذا ليس خرقاً للديناميكا الحرارية؛ إذ نحن ننقل الحرارة ولا نُنتجها.
في المنطقة العربية، يستهلك التكييف نسبة هائلة من الكهرباء. في السعودية مثلاً، يُقدر أن التكييف يستهلك نحو 70% من الكهرباء السكنية صيفاً. فهم مبادئ الديناميكا الحرارية يساعد في تصميم أنظمة تكييف أكثر كفاءة واختيار الأجهزة المناسبة.
ما علاقة الديناميكا الحرارية بالكيمياء؟
الديناميكا الحرارية الكيميائية (Chemical Thermodynamics) تدرس التغيرات الطاقوية المصاحبة للتفاعلات الكيميائية. هل التفاعل يُطلق حرارة أم يمتصها؟ هل يحدث تلقائياً أم يحتاج إلى طاقة؟ هذه الأسئلة تُجيب عنها الديناميكا الحرارية.
التفاعلات الطاردة للحرارة (Exothermic Reactions) تُطلق طاقة إلى المحيط. الاحتراق مثال كلاسيكي: حرق الخشب أو البنزين يُطلق حرارة وضوءاً. في المقابل، التفاعلات الماصة للحرارة (Endothermic Reactions) تمتص طاقة من المحيط. إذابة الثلج مثال بسيط: الجليد يمتص حرارة من محيطه ليتحول إلى ماء.
طاقة جيبس الحرة (Gibbs Free Energy) هي الدالة السحرية التي تُخبرنا هل التفاعل تلقائي أم لا. تُعرَّف بالعلاقة: G=H−TS
إذا كان التغير في طاقة جيبس سالباً (ΔG<0)، فالتفاعل تلقائي. إذا كان موجباً، فالتفاعل غير تلقائي ويحتاج إلى إمداد بالطاقة. وإذا كان صفراً، فالنظام في حالة توازن.
هذا له تطبيقات عملية هائلة. الصناعات الكيميائية تستخدم حسابات الديناميكا الحرارية لتحديد ظروف التفاعل المثلى. مصافي النفط في الخليج العربي تعتمد على هذه الحسابات لتحسين عمليات التكرير والبتروكيماويات.
اقرأ أيضاً: علم الكيمياء (Chemistry): دراسة المادة وتفاعلاتها
كيف تؤثر الديناميكا الحرارية في حياتنا اليومية؟
ربما تظن أن الديناميكا الحرارية علم أكاديمي بعيد عن حياتك اليومية. الحقيقة أنك تتعامل مع مبادئها كل يوم، وإن لم تدرك ذلك.
لنأخذ مثالاً تطبيقياً مفصلاً: قدر الضغط (Pressure Cooker) في مطبخك. عندما تُغلق القدر بإحكام وتُسخنه، يرتفع الضغط داخله لأن البخار لا يستطيع الهروب. هذا الضغط المرتفع يرفع درجة غليان الماء من 100 إلى نحو 120 درجة مئوية. عند هذه الدرجة الأعلى، يطهى الطعام أسرع. العلاقة بين الضغط ودرجة الغليان تحكمها معادلة كلابيرون-كلاوزيوس (Clausius-Clapeyron Equation) في الديناميكا الحرارية.
تخيل أنك تُعد وليمة لعائلتك. قررت طهي اللحم في قدر الضغط. تضع الماء واللحم، تُغلق القدر، وتُشعل النار. بعد دقائق، يبدأ صمام الأمان بإصدار صوت الفحيح المميز. هذا الصوت إشارة إلى أن الضغط وصل القيمة المطلوبة والبخار الزائد يُطرد. داخل القدر، الماء يغلي عند درجة حرارة أعلى من المعتاد، مما يُسرّع التفاعلات الكيميائية في الطعام. بعد 30 دقيقة بدلاً من ساعتين، اللحم جاهز وطري. وفّرت الوقت والغاز، بفضل الديناميكا الحرارية.
أمثلة أخرى من حياتك اليومية:
التعرق نظام تبريد طبيعي للجسم. عندما يتبخر العرق من جلدك، يمتص حرارة كامنة للتبخر (Latent Heat of Vaporization) ويُبردك. لهذا تشعر بالبرودة عند خروجك من المسبح.
سيارتك الأوتوماتيكية تستخدم ناقل حركة يعتمد على سائل هيدروليكي يسخن أثناء القيادة. إذا ارتفعت حرارته كثيراً، تتغير لزوجته ويتدهور أداؤه. نظام التبريد مصمم وفق مبادئ انتقال الحرارة.
حتى هاتفك المحمول يُولّد حرارة من المعالج، ومهندسوه استخدموا مبادئ التبديد الحراري لمنعه من الاحتراق.

ما التطورات الحديثة في هذا المجال؟
الديناميكا الحرارية ليست علماً جامداً انتهى في القرن التاسع عشر. ثمة تطورات مثيرة في السنوات الأخيرة، خاصة في المجالات التالية:
الديناميكا الحرارية الكمومية (Quantum Thermodynamics) تدرس سلوك الأنظمة الصغيرة جداً حيث تصبح التأثيرات الكمومية مهمة. في عام 2024، نجح باحثون في إثبات أن القانون الثاني يبقى صالحاً على المستوى الكمومي، لكن بصياغة معدلة. هذا المجال يعد بتطبيقات في الحوسبة الكمومية وتقنية النانو.
الديناميكا الحرارية النانوية (Nanothermodynamics) تتعامل مع أنظمة صغيرة لدرجة أن التقلبات الإحصائية تصبح ملحوظة. المحركات الجزيئية (Molecular Motors) في الخلايا الحية مثال على ذلك. هذه المحركات البيولوجية تعمل بكفاءات قريبة من الحد النظري، مما يُلهم المهندسين لتصميم آلات نانوية.
في مجال الطاقة المتجددة، تُستخدم مبادئ الديناميكا الحرارية لتحسين كفاءة الخلايا الشمسية. الحد النظري الأقصى لكفاءة خلية شمسية أحادية الوصلة هو نحو 33% (حد شوكلي-كويسر). باستخدام خلايا متعددة الوصلات، وصلت الكفاءة في المختبرات إلى أكثر من 47% عام 2023.
رقم مدهش: تُشير تقديرات وكالة الطاقة الدولية (IEA) لعام 2024 إلى أن تحسين الكفاءة الحرارية بنسبة 1% فقط في محطات توليد الكهرباء عالمياً يمكن أن يوفر نحو 1000 مليار كيلوواط ساعة سنوياً، ما يعادل استهلاك الكهرباء في جميع الدول العربية مجتمعة.
ما واقع أبحاث الديناميكا الحرارية في العالم العربي؟
المنطقة العربية تواجه تحديات فريدة تجعل فهم الديناميكا الحرارية أمراً حيوياً. المناخ الصحراوي الحار يعني استهلاكاً هائلاً للطاقة في التبريد. وفرة الطاقة الشمسية تفتح آفاقاً واعدة للاستغلال الحراري.
في المملكة العربية السعودية، يُجري مركز الملك عبدالله للدراسات والبحوث البترولية (KAPSARC) أبحاثاً متقدمة في كفاءة استخدام الطاقة. جامعة الملك عبدالله للعلوم والتقنية (KAUST) تضم مختبرات متخصصة في الديناميكا الحرارية التطبيقية، مع تركيز على تحلية المياه وتوليد الطاقة الشمسية.
في الإمارات، محطة “شمس” للطاقة الشمسية المركزة في أبوظبي كانت عند افتتاحها عام 2013 أكبر محطة من نوعها في العالم. تستخدم مبادئ الديناميكا الحرارية لتركيز أشعة الشمس وتسخين زيت حراري يُنتج بخاراً لتشغيل التوربينات.
مصر تستضيف مشروع “بنبان” للطاقة الشمسية، أحد أكبر مجمعات الطاقة الشمسية في العالم. رغم أنه يعتمد على الألواح الكهروضوئية بشكل رئيس، إلا أن الفهم الحراري ضروري لإدارة درجات حرارة الألواح التي تؤثر في كفاءتها.
من جهة ثانية، تحلية المياه في الخليج العربي تعتمد بشكل كبير على التقطير متعدد المراحل (Multi-Stage Flash Distillation) الذي هو تطبيق مباشر لمبادئ الديناميكا الحرارية. السعودية وحدها تُنتج نحو 22% من المياه المحلاة عالمياً.
معلومة سريعة: تستهلك تحلية متر مكعب من مياه البحر نحو 3-4 كيلوواط ساعة في أفضل التقنيات الحديثة. هذا الرقم انخفض من نحو 20 كيلوواط ساعة قبل عقود، بفضل التطورات في فهم الديناميكا الحرارية وتطبيقاتها.
اقرأ أيضاً: الحفاظ على البيئة: المبادئ، الاستراتيجيات، والحلول
ما الأخطاء الشائعة في فهم الديناميكا الحرارية؟
حتى طلاب الفيزياء يقعون أحياناً في سوء فهم لبعض المفاهيم. دعني أُصحح بعض الأخطاء الشائعة:
الخطأ الأول: الخلط بين الحرارة ودرجة الحرارة. الحرارة طاقة منتقلة، بينما درجة الحرارة مقياس لمتوسط الطاقة الحركية للجزيئات. يمكن لجسمين بالدرجة نفسها أن يحتويا كميات مختلفة جداً من الطاقة الحرارية.
الخطأ الثاني: الاعتقاد بأن القانون الثاني يمنع النظام من الانتظام. ما يمنعه القانون هو انخفاض الإنتروبيا الكلية للكون، لا إنتروبيا نظام محدد. الكائنات الحية مثلاً تبني هياكل معقدة منتظمة، لكنها تزيد إنتروبيا محيطها بأكثر مما تُنقصها في نفسها.
الخطأ الثالث: الظن بأن الصفر المطلق يعني غياب كل الطاقة. في الواقع، تبقى “طاقة نقطة الصفر” الكمومية حتى عند الصفر المطلق. الذرات لا تتوقف عن الاهتزاز تماماً؛ إذ يمنع ذلك مبدأ الريبة لهايزنبرغ.
الخطأ الرابع: الاعتقاد بأن الكفاءة يمكن أن تتجاوز حد كارنو بتصميم أذكى. هذا الحد نتيجة حتمية للقانون الثاني، ولا يعتمد على التقنية المستخدمة. أي ادعاء بتجاوزه يجب التعامل معه بشك كبير.
نصائح عملية لفهم الديناميكا الحرارية
إذا كنت طالباً تدرس هذا المجال، أو مهتماً يريد توسيع معرفته، إليك بعض النصائح من خبرتي:
ابدأ بفهم المفاهيم قبل المعادلات. كثير من الطلاب يحفظون الصيغ الرياضية دون فهم معناها الفيزيائي، ثم يجدون صعوبة في تطبيقها. اسأل نفسك دائماً: ماذا تعني هذه المعادلة فيزيائياً؟
استخدم الأمثلة اليومية. عندما تفتح ثلاجتك، فكر في دورة التبريد. عندما تركب سيارتك، تخيل الدورة الحرارية في المحرك. هذا الربط يُرسخ الفهم.
لا تخف من الرياضيات، لكن لا تغرق فيها. الديناميكا الحرارية تستخدم حساب التفاضل والتكامل بكثافة. أتقن الأساسيات الرياضية، لكن لا تنسَ الصورة الفيزيائية الكبرى.
حل المسائل بكثرة. كل مسألة تكشف جانباً جديداً من المفاهيم. ابدأ بالسهلة وتدرج نحو الأصعب.
اقرأ تاريخ العلم. معرفة كيف تطورت الأفكار تُعمق الفهم. قصص كارنو وكلاوزيوس وبولتزمان ملهمة وتعليمية في آن.
اقرأ أيضاً: تعلم الرياضيات: التحديات، الاستراتيجيات، والموارد
الخاتمة
لقد رأينا كيف أن الديناميكا الحرارية ليست مجرد فرع جاف من فروع الفيزياء، بل هي مفتاح فهم العالم من حولنا. من كوب الشاي على مكتبك إلى محطات توليد الكهرباء، ومن ثلاجة مطبخك إلى النجوم في السماء، قوانين الديناميكا الحرارية تحكم كل تحول للطاقة.
القوانين الأربعة التي استعرضناها تُشكل إطاراً متكاملاً لفهم سلوك المادة والطاقة. القانون الصفري يُؤسس لمفهوم درجة الحرارة. القانون الأول يُخبرنا أن الطاقة محفوظة. القانون الثاني يُحدد اتجاه العمليات الطبيعية. والقانون الثالث يضع حدوداً عند درجات الحرارة المنخفضة جداً.
في عالمنا العربي، فهم هذا العلم ليس ترفاً أكاديمياً. إنه ضرورة لمواجهة تحديات الطاقة والمياه والمناخ. المشاريع الضخمة في الطاقة الشمسية وتحلية المياه تعتمد جوهرياً على تطبيقات الديناميكا الحرارية.
هل ستنظر إلى محرك سيارتك أو ثلاجتك بعين مختلفة بعد الآن؟
الأسئلة الشائعة
ما الفرق بين الديناميكا الحرارية الكلاسيكية والإحصائية؟
الديناميكا الحرارية الكلاسيكية تتعامل مع الخصائص الماكروسكوبية للأنظمة مثل الضغط والحرارة والحجم دون النظر إلى البنية الجزيئية، بينما الديناميكا الحرارية الإحصائية تربط هذه الخصائص بسلوك الذرات والجزيئات الفردية باستخدام الاحتمالات والإحصاء. الأولى ظاهرية وصفية، والثانية تفسيرية تشرح الأسباب الميكروسكوبية للظواهر الحرارية.
لماذا لا يمكن تحويل الحرارة بالكامل إلى شغل بينما يمكن تحويل الشغل بالكامل إلى حرارة؟
الشغل طاقة منظمة تتحرك فيها الجسيمات باتجاه واحد، بينما الحرارة طاقة عشوائية موزعة في كل الاتجاهات. تحويل النظام من العشوائي يتطلب حتماً طرح جزء من الطاقة كحرارة مهدورة وفقاً للقانون الثاني، أما العكس فالعشوائية تزداد تلقائياً دون قيود.
كيف تختلف السعة الحرارية عند ضغط ثابت عن السعة الحرارية عند حجم ثابت؟
السعة الحرارية عند ضغط ثابت Cp أكبر دائماً من السعة الحرارية عند حجم ثابت Cv للغازات. السبب أن التسخين عند ضغط ثابت يسمح للغاز بالتمدد وبذل شغل على المحيط، فتحتاج كمية حرارة إضافية لتعويض هذا الشغل فوق رفع درجة الحرارة.
ما معنى العملية شبه الساكنة في الديناميكا الحرارية؟
العملية شبه الساكنة هي عملية تحدث ببطء شديد بحيث يظل النظام في حالة توازن حراري تقريبي في كل لحظة. هذا الافتراض ضروري لتطبيق معادلات الديناميكا الحرارية الكلاسيكية لأنها تصف حالات التوازن فقط.
ما الفرق بين المستودع الحراري ومصدر الحرارة؟
المستودع الحراري جسم ضخم جداً بحيث لا تتغير درجة حرارته مهما امتص أو أعطى من حرارة، مثل المحيط أو الغلاف الجوي. أما مصدر الحرارة فمصطلح عام يشمل أي جسم يُزود النظام بالطاقة الحرارية بغض النظر عن حجمه.
لماذا تُقاس درجات الحرارة في الديناميكا الحرارية بالكلفن وليس بالمئوية؟
مقياس كلفن مقياس مطلق يبدأ من الصفر المطلق حيث تنعدم الطاقة الحرارية نظرياً. المعادلات الحرارية مثل كفاءة كارنو ومعادلة الغاز المثالي تتطلب قيماً موجبة دائماً ونسباً ذات معنى فيزيائي، وهذا يتحقق فقط بالمقياس المطلق.
ما العلاقة بين الإنتروبيا ونظرية المعلومات؟
أثبت كلود شانون عام 1948 أن صيغة الإنتروبيا في نظرية المعلومات مطابقة رياضياً لصيغة بولتزمان في الديناميكا الحرارية. كلتاهما تقيسان درجة عدم اليقين أو نقص المعلومات عن حالة النظام، مما يوحد المفهوم الفيزيائي والمفهوم المعلوماتي.
كيف تعمل المضخة الحرارية الأرضية وما علاقتها بالديناميكا الحرارية؟
تستغل المضخة الحرارية الأرضية ثبات درجة حرارة باطن الأرض على عمق أمتار قليلة عند نحو 15 درجة مئوية طوال العام. في الشتاء تنقل حرارة من الأرض إلى المبنى، وفي الصيف تعكس الاتجاه. كفاءتها تفوق أنظمة التدفئة التقليدية لأنها تنقل حرارة موجودة بدلاً من توليدها.
ما مبدأ عمل أنابيب الحرارة المستخدمة في تبريد الحواسيب؟
أنبوب الحرارة يحتوي سائلاً يتبخر عند الطرف الساخن ممتصاً الحرارة الكامنة للتبخر، ثم ينتقل البخار إلى الطرف البارد حيث يتكثف مُطلقاً هذه الحرارة، ثم يعود السائل بالخاصية الشعرية. هذه الدورة تنقل حرارة بكفاءة تفوق التوصيل المعدني بمئات المرات.
هل يمكن أن تنخفض إنتروبيا الكون في المستقبل البعيد؟
وفقاً للفيزياء الكلاسيكية لا يمكن ذلك إطلاقاً. لكن بعض النظريات الكمومية تطرح احتمالات ضئيلة جداً لتقلبات عشوائية تُنتج انخفاضاً محلياً في الإنتروبيا على مقاييس زمنية تتجاوز عمر الكون الحالي بأضعاف لا تُحصى.
إذا وجدت هذا المقال مفيداً، شاركه مع أصدقائك وزملائك المهتمين بالعلوم. ولا تتردد في طرح أسئلتك في التعليقات. اشترك في نشرتنا البريدية لتصلك مقالات علمية جديدة كل أسبوع. وإذا كنت طالباً أو باحثاً، نرحب بمساهماتك وملاحظاتك التي تُثري محتوانا.
المراجع
- Cengel, Y. A., & Boles, M. A. (2019). Thermodynamics: An engineering approach (9th ed.). McGraw-Hill Education. — مرجع أساسي شامل يُستخدم في معظم كليات الهندسة عالمياً، يغطي الأسس النظرية والتطبيقات الهندسية.
- Fermi, E. (1956). Thermodynamics. Dover Publications. — كتاب كلاسيكي من أحد عمالقة الفيزياء، يُقدم الموضوع بوضوح وعمق نادرين.
- Demirel, Y. (2014). Nonequilibrium thermodynamics: Transport and rate processes in physical, chemical and biological systems (3rd ed.). Elsevier. DOI: 10.1016/C2012-0-00459-0 — يغطي التطورات الحديثة في الديناميكا الحرارية اللاتوازنية.
- Seifert, U. (2012). Stochastic thermodynamics, fluctuation theorems and molecular machines. Reports on Progress in Physics, 75(12), 126001. DOI: 10.1088/0034-4885/75/12/126001 — ورقة مرجعية مهمة في الديناميكا الحرارية على المستوى الجزيئي.
- International Energy Agency. (2024). World Energy Outlook 2024. IEA Publications. https://www.iea.org/reports/world-energy-outlook-2024 — تقرير رسمي يُقدم إحصائيات محدثة عن استهلاك الطاقة وكفاءتها عالمياً.
- Lienhard IV, J. H., & Lienhard V, J. H. (2020). A heat transfer textbook (5th ed.). Phlogiston Press. https://ahtt.mit.edu — كتاب متاح مجاناً من MIT، يربط بين الديناميكا الحرارية وانتقال الحرارة بتطبيقات عملية.
إخلاء المسؤولية: هذا المقال لأغراض تعليمية وتثقيفية. للتطبيقات الهندسية الدقيقة، يُنصح بالرجوع إلى المراجع الأكاديمية المتخصصة واستشارة الخبراء.
جرت مراجعة هذا المقال من قبل فريق التحرير في موقعنا لضمان الدقة والمعلومة الصحيحة.





