الهالوجين: الخصائص الكيميائية، والتفاعلات لعناصر المجموعة السابعة عشر
تحليل عميق لأكثر المجموعات الكيميائية تفاعلية في الجدول الدوري ودورها المحوري في العلوم والحياة
تعتبر عناصر الهالوجين من أكثر المجموعات الكيميائية تفاعلية وأهمية في الجدول الدوري. تمتد تطبيقاتها من الصناعات الثقيلة إلى الاستخدامات اليومية في حياتنا.
المقدمة: تعريف بمجموعة الهالوجين
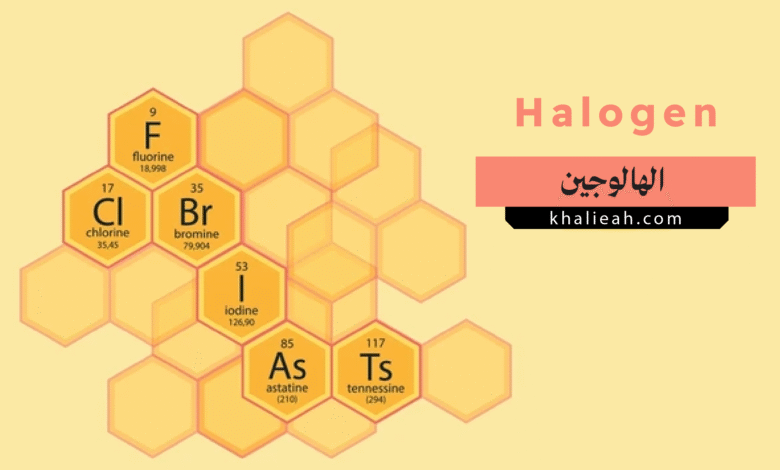
تشكل مجموعة الهالوجين العمود السابع عشر (المجموعة VIIA وفقاً للتسمية القديمة) في الجدول الدوري للعناصر، وتضم مجموعة من العناصر اللافلزية ذات الخصائص الكيميائية المتشابهة والمتميزة. تتكون هذه المجموعة من خمسة عناصر أساسية هي الفلور (Fluorine, F)، والكلور (Chlorine, Cl)، والبروم (Bromine, Br)، واليود (Iodine, I)، والأستاتين (Astatine, At)، بالإضافة إلى العنصر المُصنّع حديثاً وهو التينيسين (Tennessine, Ts). يشتق اسم الهالوجين من الكلمات اليونانية “halos” (بمعنى ملح) و “gennan” (بمعنى يُنتج أو يُكوّن)، أي “مُكوِّنات الأملاح”، وهو وصف دقيق لطبيعتها، حيث تتفاعل هذه العناصر بسهولة مع الفلزات لتكوين طيف واسع من الأملاح، أشهرها كلوريد الصوديوم (ملح الطعام).
إن السمة الأساسية التي توحد مجموعة الهالوجين هي تركيبها الإلكتروني، فكل ذرة من ذرات هذه العناصر تمتلك سبعة إلكترونات في غلاف تكافئها الخارجي (ns²np⁵)، مما يجعلها على بعد إلكترون واحد فقط من الوصول إلى التوزيع الإلكتروني المستقر المشابه للغازات النبيلة. هذه الحاجة الشديدة لاكتساب إلكترون إضافي هي السبب الرئيسي وراء نشاطها الكيميائي العالي وكهروسلبيتها المرتفعة، مما يجعل كل الهالوجين من أقوى العوامل المؤكسدة المعروفة في الكيمياء. تتدرج خصائص عناصر الهالوجين بشكل منتظم عند الانتقال من أعلى إلى أسفل المجموعة، مما يتيح للعلماء التنبؤ بسلوكها وفهم تفاعلاتها المعقدة.
يمثل كل عنصر في مجموعة الهالوجين حالة فريدة من التنوع الكيميائي والفيزيائي. الفلور، على سبيل المثال، هو أكثر العناصر كهروسلبية على الإطلاق، ونشاطه الكيميائي شديد لدرجة أنه يتفاعل مع معظم العناصر الأخرى، حتى الغازات النبيلة في ظروف معينة. يليه الكلور، وهو غاز سام ذو أهمية صناعية هائلة، ثم البروم، السائل الوحيد من بين اللافلزات في درجة حرارة الغرفة، واليود، وهو مادة صلبة لامعة تتسامى بسهولة عند تسخينها. أما الأستاتين، فهو عنصر مشع ونادر للغاية، وتُستنتج معظم خصائصه من خلال دراسة سلوك نظائره المشعة قصيرة العمر.
إن دراسة مجموعة الهالوجين لا تقتصر فقط على فهم الكيمياء الأساسية، بل تمتد لتشمل تطبيقاتها الحيوية في الطب، ودورها المحوري في الصناعات الكيميائية، وتأثيراتها البيئية التي تتطلب فهماً عميقاً ومسؤولية في التعامل مع مركباتها. تُعد هذه المجموعة مثالاً نموذجياً على كيفية تأثير التركيب الذري بشكل مباشر على الخصائص الكلية للعنصر، مما يجعل الهالوجين حقلاً غنياً بالدراسة والبحث العلمي المستمر.
الخصائص الفيزيائية لعناصر الهالوجين
تُظهر عناصر مجموعة الهالوجين تدرجاً واضحاً ومثالياً في خصائصها الفيزيائية عند الانتقال من الفلور إلى اليود، مما يعكس الزيادة المنتظمة في العدد الذري والكتلة الذرية. هذا التدرج يجعل من دراسة مجموعة الهالوجين نموذجاً تعليمياً ممتازاً في الكيمياء الدورية. أحد أبرز هذه التدرجات هو الحالة الفيزيائية للعناصر في الظروف القياسية من الضغط ودرجة الحرارة. فبينما يوجد الفلور والكلور في الحالة الغازية، يكون البروم سائلاً متطايراً، أما اليود فيوجد في الحالة الصلبة.
هذا التغير في الحالة يعود مباشرة إلى زيادة قوة قوى التشتت (London dispersion forces) بين جزيئات الهالوجين ثنائية الذرة (X₂). مع زيادة حجم الذرة وعدد الإلكترونات فيها من الفلور إلى اليود، تزداد هذه القوى بين الجزيئية، مما يتطلب طاقة أكبر للتغلب عليها، وبالتالي ترتفع درجات الانصهار والغليان بشكل ملحوظ عبر المجموعة.
تتميز عناصر الهالوجين أيضاً بألوانها المميزة والزاهية، والتي تزداد قتامة كلما اتجهنا لأسفل المجموعة. هذا اللون ناتج عن امتصاص الجزيئات للضوء في الطيف المرئي، مما يؤدي إلى إثارة إلكترون من المدار الجزيئي المشغول الأعلى (HOMO) إلى المدار الجزيئي غير المشغول الأدنى (LUMO). تختلف فجوة الطاقة بين هذين المدارين لكل الهالوجين، مما يؤدي إلى امتصاص أطوال موجية مختلفة من الضوء.
- الفلور (F₂): هو غاز أصفر باهت جداً، وشديد التآكل والسمية. فجوة الطاقة لديه هي الأكبر، مما يجعله يمتص الضوء في المنطقة البنفسجية من الطيف، ويظهر باللون المكمل وهو الأصفر الشاحب.
- الكلور (Cl₂): هو غاز أصفر مخضر، وهو أيضاً سام وله رائحة نفاذة مميزة. فجوة الطاقة لديه أصغر من الفلور، مما يزيح الامتصاص نحو المنطقة الزرقاء، فيظهر باللون الأصفر المخضر.
- البروم (Br₂): هو سائل بني محمر داكن، كثيف ومتطاير، يُنتج أبخرة خانقة ذات لون مماثل. امتصاصه للضوء يقع في نطاق أوسع من الطيف المرئي مقارنة بالكلور.
- اليود (I₂): هو مادة صلبة بلورية ذات لون رمادي مسود ولمعان معدني خفيف. عند تسخينه، يتسامى اليود بسهولة (يتحول مباشرة من الحالة الصلبة إلى الغازية) مُكوناً بخاراً بنفسجياً زاهياً وجميلاً.
بالإضافة إلى ذلك، فإن قابلية ذوبان الهالوجين في الماء تتناقص بشكل عام بالانتقال من الكلور إلى اليود، على الرغم من أن تفاعل الفلور مع الماء عنيف ويؤدي إلى تحلله. ومع ذلك، تذوب عناصر الهالوجين بشكل أفضل في المذيبات العضوية غير القطبية مثل رابع كلوريد الكربون (CCl₄) أو الهكسان، حيث تكون قوى التجاذب بين جزيئات المذيب والمذاب متشابهة (قوى تشتت)، مما ينتج عنه محاليل ملونة مميزة. على سبيل المثال، يذوب اليود في رابع كلوريد الكربون ليعطي محلولاً بنفسجياً، بينما يذوب في مذيبات أخرى مثل الإيثانول ليعطي محلولاً بنياً بسبب تكوين معقدات تناسقية. هذا السلوك الفيزيائي المتدرج والفريد يجعل من الهالوجين موضوعاً غنياً للدراسة والتحليل.
التركيب الإلكتروني والخصائص الكيميائية لمجموعة الهالوجين
يكمن مفتاح فهم السلوك الكيميائي الفريد لمجموعة الهالوجين في تركيبها الإلكتروني. تمتلك جميع عناصر الهالوجين سبعة إلكترونات في غلافها الخارجي (غلاف التكافؤ)، موزعة في المدارات s و p وفق التوزيع الإلكتروني العام ns²np⁵. هذا التكوين يجعلها على بعد إلكترون واحد فقط من تحقيق التوزيع الإلكتروني الثماني المستقر الذي يميز الغازات النبيلة. هذه الرغبة القوية في اكتساب إلكترون إضافي هي القوة الدافعة وراء معظم خصائصها الكيميائية، وأبرزها نشاطها الكيميائي العالي وكهروسلبيتها المرتفعة.
تُعرّف الكهروسلبية (Electronegativity) بأنها مقياس لمقدرة الذرة على جذب إلكترونات الرابطة الكيميائية نحوها. يعتبر الفلور، أول عنصر في مجموعة الهالوجين، هو العنصر الأعلى كهروسلبية في الجدول الدوري بأكمله (قيمة 4.0 على مقياس باولنج)، مما يجعله أقوى عامل مؤكسد. تتناقص الكهروسلبية بشكل منتظم عند النزول في المجموعة، حيث يصبح الكلور (3.16)، ثم البروم (2.96)، واليود (2.66) أقل قدرة على جذب الإلكترونات بسبب زيادة الحجم الذري وزيادة حجب الإلكترونات الداخلية لنواة الذرة.
يترتب على هذه الكهروسلبية العالية أن الهالوجين يميل بشدة إلى تكوين أيونات سالبة أحادية الشحنة (X⁻)، تُعرف بأيونات الهاليد (Halide ions)، وذلك عند تفاعلها مع الفلزات أو العناصر الأقل كهروسلبية. في هذه الحالة، تكون حالة الأكسدة الأكثر شيوعاً واستقراراً لعناصر الهالوجين هي (-1). ومع ذلك، فإن عناصر الهالوجين (باستثناء الفلور) قادرة أيضاً على إظهار حالات أكسدة موجبة متعددة (+1, +3, +5, +7) عندما ترتبط بعناصر أكثر كهروسلبية منها، مثل الأكسجين أو حتى الهالوجين الذي يسبقها في المجموعة.
على سبيل المثال، في مركب ثلاثي فلوريد الكلور (ClF₃)، يكون للكلور حالة أكسدة (+3)، بينما في أيون فوق الكلورات (⁻ClO₄)، يصل الكلور إلى أعلى حالة أكسدة له وهي (+7). يعود سبب عدم قدرة الفلور على تكوين حالات أكسدة موجبة إلى كونه العنصر الأكثر كهروسلبية، فلا يوجد عنصر آخر قادر على سحب إلكترونات الرابطة منه. كما أن طاقة التأين (Ionization Energy) لمجموعة الهالوجين مرتفعة جداً، مما يعني أن فقدان إلكترون لتكوين أيون موجب يتطلب طاقة كبيرة، وهذا يفسر طبيعتها اللافلزية السائدة. ومع ذلك، تتناقص طاقة التأين بالانتقال إلى أسفل المجموعة، مما يمنح اليود بعض الخصائص شبه المعدنية الطفيفة.
تفاعلات الهالوجين مع العناصر الأخرى
يُترجم النشاط الكيميائي المرتفع لمجموعة الهالوجين إلى قدرتها على التفاعل مع طيف واسع جداً من العناصر والمركبات، بما في ذلك الفلزات واللافلزات والمركبات العضوية. تتفاوت شدة هذه التفاعلات بشكل كبير، حيث يكون الفلور هو الأكثر عنفاً وتفاعلية، وتقل هذه التفاعلية تدريجياً عبر المجموعة وصولاً إلى اليود. عند تفاعل الهالوجين مع الفلزات، تتكون مركبات أيونية تُعرف بالهاليدات الفلزية. على سبيل المثال، يتفاعل الصوديوم بشدة مع الكلور لينتج كلوريد الصوديوم (2Na + Cl₂ → 2NaCl). يكون التفاعل مع الفلور أكثر عنفاً وانفجارية، حيث يتفاعل مع جميع الفلزات تقريباً، بما في ذلك الفلزات الخاملة مثل الذهب والبلاتين. تتفاعل عناصر الهالوجين أيضاً مع الهيدروجين لتكوين مركبات تساهمية قطبية تُعرف بهاليدات الهيدروجين (HX). هذا التفاعل يُظهر بوضوح تدرج النشاط الكيميائي: تفاعل الفلور مع الهيدروجين انفجاري حتى في الظلام وفي درجات حرارة منخفضة جداً، بينما يتطلب تفاعل الكلور مع الهيدروجين وجود ضوء أو حرارة، ويتطلب تفاعل البروم حرارة أعلى، أما تفاعل اليود فهو تفاعل بطيء وتوازني ولا يكتمل حتى مع التسخين.
أحد أهم أنواع التفاعلات التي تميز مجموعة الهالوجين هو تفاعلات الإزاحة أو الإحلال. في هذه التفاعلات، يمكن للهالوجين الأكثر نشاطاً (الأعلى في المجموعة) أن يحل محل الهالوجين الأقل نشاطاً في محاليل أملاحه. على سبيل المثال، عند تمرير غاز الكلور في محلول بروميد البوتاسيوم (KBr)، يقوم الكلور بأكسدة أيونات البروميد (⁻Br) إلى البروم (Br₂)، بينما يُختزل هو إلى أيونات الكلوريد (⁻Cl)، وفقاً للمعادلة: Cl₂(g) + 2KBr(aq) → 2KCl(aq) + Br₂(aq). هذا التفاعل يحدث لأن الكلور عامل مؤكسد أقوى من البروم. بالمثل، يمكن للكلور والبروم إزاحة اليود من محاليل اليوديد، ولكن لا يمكن لليود أو البروم إزاحة الكلور.
هذا المبدأ له أهمية صناعية كبيرة، حيث يُستخدم في استخلاص البروم واليود من مصادرهما الطبيعية. علاوة على ذلك، يتفاعل الهالوجين مع العديد من اللافلزات الأخرى مثل الكبريت والفوسفور، مكوناً مجموعة متنوعة من الهاليدات اللافلزية مثل سداسي فلوريد الكبريت (SF₆) وخماسي كلوريد الفوسفور (PCl₅). كما تدخل عناصر الهالوجين في تفاعلات إضافة واستبدال مع المركبات العضوية، مما يفتح الباب لتصنيع آلاف المركبات العضوية المهلجنة ذات التطبيقات الواسعة في صناعة البوليمرات، الأدوية، والمبيدات. إن فهم تفاعلات الهالوجين يعد ركيزة أساسية في الكيمياء غير العضوية والعضوية على حد سواء.
مركبات الهالوجين: الهاليدات والأحماض الهالوجينية
تُكوّن عناصر الهالوجين مجموعة هائلة ومتنوعة من المركبات الكيميائية التي تلعب أدواراً حيوية في الطبيعة والصناعة. يمكن تصنيف هذه المركبات بشكل أساسي إلى الهاليدات، والأحماض الهالوجينية، والأكاسيد، والمركبات بين الهالوجينية. الهاليدات (Halides) هي مركبات ثنائية تحتوي على الهالوجين في حالة أكسدة (-1). عندما يتحد الهالوجين مع فلز نشط (مثل عناصر المجموعتين الأولى والثانية)، تتكون هاليدات أيونية تتميز بدرجات انصهار وغليان مرتفعة، وهي غالباً ما تكون مواد صلبة بلورية قابلة للذوبان في الماء، مثل كلوريد الصوديوم (NaCl) وفلوريد الكالسيوم (CaF₂). أما عند اتحاد الهالوجين مع الفلزات الانتقالية أو اللافلزات، فإن طبيعة الرابطة تصبح أكثر تساهمية. على سبيل المثال، رابع كلوريد الكربون (CCl₄) هو سائل متطاير ذو رابطة تساهمية غير قطبية، بينما كلوريد الألومنيوم (AlCl₃) له طابع يقع بين الأيوني والتساهمي. هذه المركبات لها تطبيقات لا حصر لها، بدءاً من المذيبات الصناعية وحتى المواد الأولية في التخليق الكيميائي.
أما هاليدات الهيدروجين (HX) فهي فئة أخرى بالغة الأهمة من مركبات الهالوجين. وهي عبارة عن غازات في حالتها النقية، ولكن محاليلها المائية تُعرف بالأحماض الهالوجينية (Hydrohalic acids). يُعد حمض الهيدروكلوريك (HCl)، وهو محلول مائي لغاز كلوريد الهيدروجين، أحد أقوى الأحماض المعدنية وأكثرها استخداماً في الصناعة والمختبرات. تزداد قوة هذه الأحماض عند النزول في المجموعة من HF إلى HI. على الرغم من الكهروسلبية العالية للفلور، فإن حمض الهيدروفلوريك (HF) يعتبر حمضاً ضعيفاً نسبياً في المحاليل المائية، وذلك بسبب قوة الرابطة H-F العالية.
بينما تكون الروابط H-Cl، و H-Br، و H-I أضعف، مما يسهل تفككها وإطلاق أيون الهيدروجين (⁺H) في المحلول، وبالتالي فإن أحماض HCl و HBr و HI هي أحماض قوية جداً. بالإضافة إلى ذلك، تُكوّن عناصر الهالوجين (باستثناء الفلور) سلسلة من الأحماض الأكسجينية (Oxoacids)، حيث يرتبط الهالوجين بذرة أكسجين واحدة أو أكثر. من أشهر الأمثلة أحماض الكلور الأكسجينية: حمض هيبوكلوروز (HClO)، وحمض كلوروز (HClO₂)، وحمض كلوريك (HClO₃)، وحمض بيركلوريك (HClO₄). تزداد قوة هذه الأحماض واستقرارها مع زيادة عدد ذرات الأكسجين المرتبطة بذرة الهالوجين المركزية، مما يجعل حمض البيركلوريك واحداً من أقوى الأحماض المعروفة. هذه الأحماض وأملاحها لها استخدامات هامة كعوامل مؤكسدة ومطهرات ومكونات في صناعة المتفجرات والألعاب النارية.
استخلاص وإنتاج عناصر الهالوجين
نظراً للنشاط الكيميائي الشديد لعناصر الهالوجين، فإنها لا توجد أبداً في الطبيعة في حالتها العنصرية الحرة (X₂)، بل توجد دائماً على شكل مركبات، غالباً كأملاح هاليدات منتشرة في مياه البحار والمحيطات أو مترسبة في القشرة الأرضية. يتطلب استخلاص كل الهالوجين من مركباته عمليات أكسدة لأيونات الهاليد (⁻X)، وتختلف طرق الإنتاج الصناعي لكل عنصر بناءً على مدى صعوبة أكسدته وتوافر مصادره الطبيعية.
- الفلور (F₂): يعتبر الفلور أقوى عامل مؤكسد، وبالتالي لا يمكن أكسدة أيون الفلوريد (⁻F) باستخدام أي عامل كيميائي آخر. الطريقة الوحيدة لإنتاج الفلور هي من خلال التحليل الكهربائي. تاريخياً، كانت هذه العملية صعبة وخطيرة للغاية بسبب تفاعلية الفلور الشديدة. الطريقة الحديثة، المعروفة بعملية مواسان (Moissan’s process) المُحسّنة، تتضمن التحليل الكهربائي لمزيج منصهر من فلوريد الهيدروجين (HF) وفلوريد البوتاسيوم (KHF₂). يتم استخدام مصعد (anode) من الكربون ومهبط (cathode) من الفولاذ، وتُجرى العملية في خلية تحليل كهربائي مصممة خصيصاً لمقاومة التآكل الشديد الذي يسببه الفلور.
- الكلور (Cl₂): يُنتج الكلور على نطاق صناعي هائل، بشكل أساسي عبر عملية الكلور القلوي (Chlor-alkali process)، والتي تتضمن التحليل الكهربائي لمحلول ملحي مركز من كلوريد الصوديوم (NaCl)، المعروف باسم “brine”. عند تطبيق تيار كهربائي، تتأكسد أيونات الكلوريد عند المصعد لإنتاج غاز الكلور، بينما يتم اختزال الماء عند المهبط لإنتاج غاز الهيدروجين وأيونات الهيدروكسيد (⁻OH)، التي تتحد مع أيونات الصوديوم لتكوين هيدروكسيد الصوديوم (NaOH)، وهو منتج ثانوي ذو قيمة اقتصادية كبيرة.
- البروم (Br₂): المصدر الرئيسي للبروم هو أيونات البروميد الموجودة بتركيزات منخفضة في مياه البحر والآبار المالحة. تعتمد عملية الاستخلاص على مبدأ تفاعلات الإزاحة. يتم ضخ مياه البحر في أبراج خاصة، ويُمرر من خلالها غاز الكلور (وهو الهالوجين الأكثر نشاطاً). يقوم الكلور بأكسدة أيونات البروميد إلى البروم، والذي يتم بعد ذلك فصله وتنقيته. هذه العملية تُظهر التطبيق الصناعي المباشر لتدرج النشاط الكيميائي داخل مجموعة الهالوجين.
- اليود (I₂): يُستخلص اليود من مصادر مختلفة، بما في ذلك الآبار المالحة التي تحتوي على أيونات اليوديد، ورماد بعض أنواع الأعشاب البحرية (kelp). على غرار استخلاص البروم، يمكن استخدام الكلور لأكسدة أيونات اليوديد إلى اليود. طريقة أخرى شائعة تتضمن معالجة المحاليل التي تحتوي على اليوديد بعامل مؤكسد مثل ثاني أكسيد المنجنيز (MnO₂) في وسط حمضي. إن التحكم الدقيق في ظروف التفاعل ضروري لضمان كفاءة إنتاج كل الهالوجين.
التطبيقات الصناعية والتكنولوجية لمجموعة الهالوجين
تتخلل تطبيقات عناصر الهالوجين ومركباتها تقريباً كل جانب من جوانب الحياة الحديثة والصناعة، مما يجعلها من أكثر المواد الكيميائية قيمة على المستوى الاقتصادي. يلعب الكلور، وهو الهالوجين الأكثر إنتاجاً، دوراً محورياً في الصحة العامة والصناعات الكيميائية. يُستخدم الكلور على نطاق واسع لتعقيم مياه الشرب وحمامات السباحة، حيث يقضي على الكائنات الدقيقة المسببة للأمراض. كما أنه مادة خام أساسية في إنتاج كلوريد متعدد الفينيل (PVC)، وهو أحد أكثر أنواع البلاستيك استخداماً في العالم، ويدخل في صناعة الأنابيب، وإطارات النوافذ، والأرضيات، والعوازل الكهربائية. بالإضافة إلى ذلك، يُستخدم الكلور في صناعة المذيبات المكلورة (مثل ثلاثي كلورو الإيثيلين)، والمبيدات الحشرية، وكمادة تبييض في صناعة الورق والمنسوجات. إن تعدد استخدامات هذا الهالوجين يجعله عصب العديد من الصناعات.
الفلور، على الرغم من صعوبة التعامل معه، إلا أن مركباته لها تطبيقات تكنولوجية فريدة ومتقدمة. يُعرف مركب بولي تترا فلورو إيثيلين (PTFE)، الذي يحمل الاسم التجاري “تفلون”، بخصائصه المانعة للالتصاق ومقاومته الكيميائية والحرارية العالية، مما يجعله مثالياً لأواني الطهي غير اللاصقة، والعوازل الكهربائية، والطلاءات الصناعية. تُستخدم مركبات الفلوروكربون (التي حلت محل الكلوروفلوروكربون الضار بالبيئة) في أنظمة التبريد وتكييف الهواء. كما أن إضافة كميات ضئيلة من أيونات الفلوريد (على شكل فلوريد الصوديوم أو فلوريد القصدير) إلى معاجين الأسنان ومياه الشرب أثبتت فعاليتها العالية في تقوية مينا الأسنان والوقاية من التسوس. أما البروم، فيجد تطبيقاته الرئيسية في صناعة مثبطات اللهب المبرومة، وهي مركبات تُضاف إلى المواد البلاستيكية والمنسوجات والإلكترونيات لتقليل قابليتها للاشتعال وزيادة السلامة من الحرائق. كما تدخل مركبات البروم في صناعة بعض الأدوية، والأصباغ، والمواد الكيميائية المستخدمة في التصوير الفوتوغرافي (تاريخياً). وأخيراً، يشتهر اليود بخصائصه المطهرة؛ فمحلول اليود في الكحول (صبغة اليود) هو مطهر فعال للجروح. كما يُستخدم اليود كعامل حفاز في بعض التفاعلات الصناعية، وفي إنتاج مرشحات الاستقطاب لشاشات الكريستال السائل (LCD). هذا التنوع الهائل في التطبيقات يؤكد على الأهمية الاستراتيجية لمجموعة الهالوجين في الاقتصاد العالمي.
الدور الحيوي والأثر البيئي لعناصر الهالوجين
على الرغم من أن عناصر الهالوجين في حالتها الجزيئية (X₂) سامة بشكل عام، إلا أن أيوناتها تلعب أدواراً حيوية أساسية في فسيولوجيا الكائنات الحية، بما في ذلك الإنسان. أيون الكلوريد (⁻Cl) هو الأنيون (الأيون السالب) الأكثر وفرة في السوائل خارج الخلوية في الجسم، مثل بلازما الدم. يلعب دوراً حاسماً في الحفاظ على التوازن الأسموزي، وتوازن الحمض والقاعدة، ونقل الأكسجين وثاني أكسيد الكربون في الدم. كما أنه مكون أساسي لحمض الهيدروكلوريك الذي تفرزه المعدة لهضم الطعام. أما اليود، فهو عنصر ضروري بكميات نزرة لتخليق هرمونات الغدة الدرقية (الثيروكسين وثلاثي يودوثيرونين)، التي تنظم عمليات الأيض والنمو والتطور في الجسم. يؤدي نقص اليود إلى تضخم الغدة الدرقية (goiter) ومشاكل صحية خطيرة أخرى، وهذا هو السبب وراء إضافة يوديد البوتاسيوم إلى ملح الطعام في العديد من البلدان. أيون الفلوريد (⁻F) أيضاً له دور في تقوية العظام والأسنان، مما يجعله مقاوماً للتسوس. إن فهم الدور الحيوي لهذه الأيونات أمر بالغ الأهمية في مجالات الطب والتغذية. إن الطبيعة المزدوجة لعناصر الهالوجين، كونها سامة في شكل ومفيدة في شكل آخر، تُظهر تعقيد الكيمياء الحيوية.
في المقابل، كان لبعض مركبات الهالوجين المُصنّعة تأثيرات بيئية سلبية كبيرة. أبرز مثال على ذلك هو مركبات الكلوروفلوروكربون (CFCs)، التي كانت تستخدم على نطاق واسع في الماضي كمواد دافعة في علب الرش ومواد تبريد. اكتُشف لاحقاً أن هذه المركبات مستقرة جداً في طبقات الجو السفلى، ولكن عند وصولها إلى طبقة الستراتوسفير، تتحلل بفعل الأشعة فوق البنفسجية مطلقةً ذرات الكلور الحرة. تعمل ذرة كلور واحدة كعامل حفاز قادر على تدمير آلاف جزيئات الأوزون (O₃)، مما أدى إلى ترقق طبقة الأوزون التي تحمي الأرض من الأشعة فوق البنفسجية الضارة. أدى هذا الاكتشاف إلى بروتوكول مونتريال، وهو اتفاق دولي ناجح حظر إنتاج واستخدام مركبات الكلوروفلوروكربون. وبالمثل، تثير بعض مثبطات اللهب المبرومة القلق بسبب ثباتها في البيئة وقدرتها على التراكم الأحيائي في السلسلة الغذائية، مما قد يسبب مشاكل صحية. كما أن الاستخدام المفرط للمبيدات الحشرية المكلورة مثل الـ دي.دي.تي (DDT) أظهر آثاراً ضارة طويلة الأمد على النظم البيئية. هذه الأمثلة تؤكد على ضرورة إجراء تقييم دقيق للأثر البيئي لمركبات الهالوجين الجديدة قبل استخدامها على نطاق واسع، وتبرز أهمية تطوير “الكيمياء الخضراء” التي تهدف إلى تصميم منتجات وعمليات كيميائية تقلل من استخدام وتوليد المواد الخطرة. إن إدارة استخدام الهالوجين ومركباته تتطلب توازناً دقيقاً بين فوائدها الهائلة ومخاطرها المحتملة.
العناصر الأثقل في مجموعة الهالوجين: الأستاتين والتينيسين
تقع العناصر الأثقل في مجموعة الهالوجين، وهما الأستاتين (Astatine, At) والتينيسين (Tennessine, Ts)، في قاع الجدول الدوري، وتتميز بخصائص فريدة تجعل دراستها تحدياً علمياً كبيراً. الأستاتين، الذي يقع مباشرة تحت اليود، هو أندر عنصر طبيعي في القشرة الأرضية. جميع نظائره مشعة وذات أعمار نصف قصيرة جداً، حيث أن أكثر نظائره استقراراً (أستاتين-210) له عمر نصف يبلغ حوالي 8.1 ساعة فقط. بسبب ندرته الشديدة وعدم استقراره، لم يتمكن العلماء من تجميع كمية مرئية منه، وتُستنتج معظم خصائصه الكيميائية والفيزيائية من خلال تجارب على كميات ضئيلة جداً (تجارب التتبع) ومقارنتها بسلوك الهالوجين الآخر، وخاصة اليود. من المتوقع أن يكون الأستاتين مادة صلبة سوداء ذات لمعان معدني أكثر من اليود، وأن يكون أقل تفاعلية من اليود، ويظهر خصائص معدنية أو شبه فلزية أكثر وضوحاً. تشير الدراسات إلى أنه يمكن أن يُظهر حالة أكسدة موجبة (+1) أكثر استقراراً في بعض مركباته، مما يعكس الاتجاه العام لزيادة الطابع الفلزي عند النزول في المجموعة. على الرغم من صعوبة دراسته، يجري البحث حالياً حول الاستخدامات المحتملة لنظائر الأستاتين في الطب النووي، وتحديداً في العلاج الإشعاعي الموجه للخلايا السرطانية. إن هذا الهالوجين يمثل حدود المعرفة في الكيمياء العملية.
أما التينيسين (Ts)، الذي يحمل العدد الذري 117، فهو أحدث إضافة إلى مجموعة الهالوجين وتم تصنيعه لأول مرة في عام 2010 في المعهد المشترك للبحوث النووية في دوبنا، روسيا. هو عنصر اصطناعي فائق الثقل، يتم إنتاجه عن طريق قذف أهداف من البركليوم-249 بأيونات الكالسيوم-48. وكما هو الحال مع الأستاتين، فإن التينيسين مشع للغاية وله عمر نصف قصير جداً (في حدود أجزاء من الثانية)، مما يجعل دراسة كيميائيته بشكل مباشر أمراً مستحيلاً حالياً. تعتمد خصائصه المتوقعة بالكامل على الحسابات النظرية التي تأخذ في الاعتبار التأثيرات النسبية (Relativistic effects)، والتي تصبح مهمة جداً للذرات فائقة الثقل. تتنبأ النماذج بأن التينيسين سيتبع اتجاهات مجموعة الهالوجين، ولكنه سيكون الأكثر شبهاً بالفلزات بين جميع عناصر المجموعة. قد لا يكون قادراً على تكوين أيون (-1) مستقر، وقد تكون حالة الأكسدة (+3) هي الأكثر استقراراً له. من المرجح أن يكون مادة صلبة ذات درجة غليان عالية جداً. تمثل دراسة هذه العناصر الفائقة الثقل، مثل هذا الهالوجين النادر، تحدياً مثيراً للفيزيائيين والكيميائيين، حيث تدفع حدود فهمنا للجدول الدوري وتأثيرات ميكانيكا الكم على المادة.
الخاتمة: الأهمية المستمرة لمجموعة الهالوجين
في الختام، لا يمكن المبالغة في تقدير أهمية مجموعة الهالوجين في عالم الكيمياء والعلوم التطبيقية. من الفلور، العنصر الأكثر نشاطاً وتفاعلية، إلى اليود ذي الدور الحيوي الأساسي، وصولاً إلى العناصر المشعة الغامضة في قاع المجموعة، يقدم كل الهالوجين قصة فريدة من الخصائص والتطبيقات. إن التدرج المنتظم والمثالي في خصائصها الفيزيائية والكيميائية يجعلها نموذجاً محورياً في تدريس مبادئ الجدول الدوري. لقد أدت قدرة الهالوجين على تكوين روابط قوية مع الكربون وعناصر أخرى إلى ثورة في الكيمياء العضوية، مما مكن من تصنيع مجموعة لا حصر لها من المواد، من البلاستيك المتين والأدوية المنقذة للحياة إلى المواد المتقدمة ذات الخصائص الفريدة.
ومع ذلك، فإن قصة الهالوجين هي أيضاً قصة توازن ومسؤولية. فكما أن مركباتها يمكن أن تكون مفيدة للغاية، يمكن لبعضها الآخر أن يشكل تهديداً للبيئة والصحة العامة إذا لم يتم التعامل معها بحكمة. إن التحديات التي فرضتها مركبات مثل الكلوروفلوروكربون والمبيدات الحشرية المستمرة قد علمت المجتمع العلمي والصناعي دروساً قيمة حول أهمية الاستدامة والتفكير طويل الأمد. يستمر البحث اليوم في استكشاف طرق جديدة ومبتكرة لتسخير القوة الكيميائية لمجموعة الهالوجين بطرق أكثر أماناً وكفاءة، سواء في تطوير مواد جديدة، أو تحسين العمليات الصناعية، أو ابتكار علاجات طبية متقدمة. وبذلك، تظل مجموعة الهالوجين، “مُكوِّنات الأملاح”، مصدراً لا ينضب للاكتشاف العلمي والتقدم التكنولوجي، مؤكدة على مكانتها الراسخة كواحدة من أهم مجموعات العناصر في الكيمياء. إن فهم كيمياء الهالوجين سيظل دائماً جزءاً لا يتجزأ من تطور العلوم.
الأسئلة الشائعة
1. لماذا سُميت عناصر المجموعة السابعة عشر باسم “الهالوجين”؟
يرجع أصل تسمية الهالوجين إلى اللغة اليونانية، وهو مصطلح مركب من كلمتين: “halos” وتعني “ملح”، و “gennan” وتعني “يُكوّن” أو “يُنتج”. وبالتالي، فإن المعنى الحرفي لكلمة الهالوجين هو “مُكوِّن الملح”. أُطلقت هذه التسمية الدقيقة على عناصر المجموعة السابعة عشر بسبب ميلها الشديد للتفاعل المباشر مع طيف واسع من الفلزات، خاصة الفلزات القلوية والقلوية الترابية، لتكوين مركبات أيونية مستقرة تُعرف بالأملاح. المثال الأكثر شهرة وبساطة على هذه الخاصية هو تفاعل الصوديوم مع الكلور لإنتاج كلوريد الصوديوم (NaCl)، وهو ملح الطعام الشائع. هذه القدرة على تكوين الأملاح بسهولة هي السمة الكيميائية الأساسية والمميزة التي تجمع كل عناصر الهالوجين، وتُعد انعكاساً مباشراً لتركيبها الإلكتروني وحاجتها لاكتساب إلكترون واحد للوصول إلى حالة الاستقرار.
2. ما هو السبب الرئيسي للنشاط الكيميائي العالي الذي تتميز به عناصر الهالوجين؟
يكمن السبب الجوهري وراء النشاط الكيميائي الفائق لمجموعة الهالوجين في تركيبها الإلكتروني الذري. تحتوي كل ذرة من ذرات الهالوجين على سبعة إلكترونات في غلاف التكافؤ الخارجي (التوزيع الإلكتروني ns²np⁵). هذا التوزيع يجعلها على بعد إلكترون واحد فقط من تحقيق التوزيع الإلكتروني الثماني المستقر والمشابه لأقرب غاز نبيل في الجدول الدوري. هذه الرغبة الشديدة في اكتساب إلكترون إضافي تُترجم إلى خصائص كيميائية محددة: أولاً، تمتلك عناصر الهالوجين ألفة إلكترونية (Electron Affinity) عالية جداً، وهي الطاقة المنطلقة عند إضافة إلكترون إلى ذرة متعادلة. ثانياً، تتميز بكهروسلبية (Electronegativity) هي الأعلى ضمن كل دورة في الجدول الدوري، مما يعني أن لديها قدرة هائلة على جذب إلكترونات الرابطة الكيميائية نحوها. هذا الدافع القوي لاكتساب الإلكترونات يجعل كل الهالوجين عوامل مؤكسدة قوية، قادرة على انتزاع الإلكترونات من العديد من العناصر والمركبات الأخرى، مما يؤدي إلى تفاعلات كيميائية سريعة وعنيفة في كثير من الأحيان.
3. كيف يتدرج النشاط الكيميائي والخصائص الفيزيائية عبر مجموعة الهالوجين؟
تُظهر مجموعة الهالوجين تدرجاً نموذجياً ومنتظماً في خصائصها عند الانتقال من أعلى إلى أسفل المجموعة (من الفلور إلى اليود). كيميائياً، تقل الفعالية والنشاط الكيميائي (القدرة كعامل مؤكسد). الفلور هو الهالوجين الأكثر نشاطاً والأقوى كعامل مؤكسد بسبب صغر حجمه الذري وكهروسلبيته الأعلى، بينما اليود هو الأقل نشاطاً. هذا التدرج يفسر تفاعلات الإحلال، حيث يمكن للكلور أن يحل محل البروم واليود في أملاحهما، ولكن العكس غير صحيح. فيزيائياً، يزداد الحجم الذري ونصف القطر الأيوني، مما يؤدي إلى زيادة درجات الانصهار والغليان بشكل ملحوظ. هذا بسبب زيادة قوة قوى التشتت (London dispersion forces) بين الجزيئات ثنائية الذرة (X₂) مع زيادة عدد الإلكترونات. هذا التدرج هو المسؤول المباشر عن تغير الحالة الفيزيائية للعناصر في الظروف القياسية: فالفلور والكلور غازات، والبروم سائل، واليود مادة صلبة.
4. ما هو الفرق الأساسي بين مصطلحي “هالوجين” و “هاليد”؟
على الرغم من ارتباط المصطلحين، إلا أنهما يشيران إلى حالتين كيميائيتين مختلفتين تماماً. مصطلح “الهالوجين” (Halogen) يشير إلى العنصر في حالته الطبيعية المتعادلة، والتي تكون عادةً على شكل جزيء ثنائي الذرة (X₂) مثل F₂, Cl₂, Br₂, I₂. في هذه الحالة، تكون حالة الأكسدة للعنصر صفراً، ويكون الهالوجين نشطاً كيميائياً وعاملاً مؤكسداً. أما مصطلح “هاليد” (Halide)، فيشير إلى الأيون السالب أحادي الشحنة (⁻X) الذي يتكون عندما تكتسب ذرة الهالوجين إلكتروناً واحداً، مثل أيون الفلوريد (⁻F)، أو الكلوريد (⁻Cl)، أو البروميد (⁻Br)، أو اليوديد (⁻I). تكون حالة الأكسدة هنا (-1). أيونات الهاليد مستقرة كيميائياً بشكل عام وتشكل الجزء الأنيوني (السالب) في الأملاح الأيونية، وهي الصورة التي يوجد عليها الهالوجين عادةً في الطبيعة.
5. هل يمكن لعناصر الهالوجين أن تكوّن روابط مع بعضها البعض؟
نعم، يمكن لعناصر الهالوجين المختلفة أن تتفاعل مع بعضها البعض لتكوين فئة من المركبات التساهمية تُعرف بالمركبات بين الهالوجينية (Interhalogen Compounds). في هذه المركبات، يكون أحد أنواع الهالوجين هو الذرة المركزية، ويرتبط بذرة هالوجين واحدة أو أكثر من نوع آخر. القاعدة العامة هي أن الذرة المركزية تكون دائماً الهالوجين الأكبر حجماً والأقل كهروسلبية، بينما تكون الذرات الطرفية هي الهالوجين الأصغر حجماً والأكثر كهروسلبية. تتخذ هذه المركبات صيغاً مختلفة مثل XY, XY₃, XY₅, و XY₇ (على سبيل المثال، ثلاثي فلوريد الكلور ClF₃، خماسي فلوريد البروم BrF₅، سباعي فلوريد اليود IF₇). تتميز المركبات بين الهالوجينية بأنها شديدة التفاعلية، وغالباً ما يكون نشاطها الكيميائي أكبر من نشاط الهالوجينات المكونة لها، وتُستخدم كعوامل فلورة أو هلجنة قوية في التفاعلات الكيميائية.
6. هل كل عناصر الهالوجين سامة وخطرة على الكائنات الحية؟
في حالتها العنصرية الجزيئية (X₂)، تعتبر جميع عناصر الهالوجين سامة ومسببة للتآكل بدرجات متفاوتة، ويجب التعامل معها بحذر شديد في المختبرات والصناعة. الفلور هو الأخطر على الإطلاق، فهو شديد السمية والتآكل. غاز الكلور أيضاً سام جداً ويسبب أضراراً بالغة للجهاز التنفسي. أبخرة البروم أكالة وسامة، واليود، على الرغم من أنه أقل خطورة، إلا أن أبخرته مهيجة ويمكن أن يكون ساماً بتركيزات عالية. ومع ذلك، فإن هذه الخطورة تتناقض تماماً مع الدور الحيوي الذي تلعبه أيونات الهاليد (⁻X) في أجسام الكائنات الحية. فأيون الكلوريد ضروري للحفاظ على توازن السوائل في الجسم، واليود مكون أساسي لهرمونات الغدة الدرقية، والفلوريد يساعد في تقوية الأسنان والعظام. هذا يوضح المبدأ الكيميائي الهام بأن الخصائص الكيميائية والبيولوجية للمادة تعتمد بشكل كامل على شكلها الكيميائي وحالة الأكسدة الخاصة بها.
7. لماذا يعتبر حمض الهيدروفلوريك (HF) حمضاً ضعيفاً بينما الأحماض الهالوجينية الأخرى (HCl, HBr, HI) قوية جداً؟
على الرغم من أن الفلور هو الهالوجين الأعلى كهروسلبية، مما يوحي بأن الرابطة H-F يجب أن تكون الأكثر قطبية، إلا أن حمض الهيدروفلوريك (HF) يُصنف كحمض ضعيف في المحاليل المائية. يعود السبب الرئيسي في ذلك إلى القوة الاستثنائية للرابطة التساهمية بين الهيدروجين والفلور (H-F). طاقة تفكك هذه الرابطة عالية جداً (565 كيلوجول/مول)، مما يجعل من الصعب كسرها وتأين الجزيء لإطلاق أيون الهيدروجين (⁺H). بالإضافة إلى ذلك، فإن أيونات الفلوريد الصغيرة الناتجة تتفاعل بقوة مع جزيئات HF غير المتأينة لتكوين روابط هيدروجينية قوية (أيون ⁻FHF). في المقابل، كلما اتجهنا لأسفل في مجموعة الهالوجين، يزداد طول الرابطة H-X وتضعف قوتها، مما يسهل عملية التفكك في الماء. لهذا السبب، تعتبر أحماض الهيدروكلوريك (HCl)، والهيدروبروميك (HBr)، والهيدرويوديك (HI) أحماضاً قوية تتأين بشكل كامل تقريباً في المحاليل المائية.
8. ما هي الأهمية الصناعية الرئيسية للكلور مقارنة ببقية عناصر الهالوجين؟
يحتل الكلور مكانة فريدة كأكثر عنصر الهالوجين أهمية من الناحية الصناعية والإنتاجية بفارق كبير. تعود هذه الأهمية إلى تعدد استخداماته وتكلفة إنتاجه المنخفضة نسبياً عبر عملية الكلور القلوي. يُستخدم الكلور على نطاق هائل في تعقيم مياه الشرب ومعالجة مياه الصرف الصحي، وهو تطبيق حيوي للصحة العامة العالمية. كما أنه مادة خام لا غنى عنها في الصناعات الكيميائية، حيث يُستخدم في إنتاج كلوريد متعدد الفينيل (PVC)، وهو ثالث أكثر أنواع البلاستيك إنتاجاً في العالم. بالإضافة إلى ذلك، يدخل الكلور في تصنيع مجموعة واسعة من المنتجات الأخرى، بما في ذلك المذيبات، والمبيدات، والمستحضرات الصيدلانية، وكمادة تبييض فعالة في صناعات الورق والنسيج. بينما تمتلك عناصر الهالوجين الأخرى تطبيقات متخصصة وهامة (مثل الفلور في صناعة التفلون والبروم في مثبطات اللهب)، إلا أن حجم وتنوع تطبيقات الكلور يجعله حجر الزاوية في العديد من القطاعات الصناعية.
9. لماذا يصعب دراسة الخصائص الكيميائية لعنصر الأستاتين؟
تنشأ الصعوبة البالغة في دراسة كيمياء الأستاتين (At) من عاملين رئيسيين متلازمين: ندرته الشديدة وعدم استقراره النووي. الأستاتين هو أندر عنصر طبيعي في القشرة الأرضية، وجميع نظائره مشعة وتتحلل بسرعة كبيرة، حيث يبلغ عمر النصف لأكثر نظائره استقراراً (²¹⁰At) حوالي 8.1 ساعة فقط. هذا يعني أنه من المستحيل عملياً تجميع كمية مرئية أو قابلة للوزن من العنصر لإجراء التجارب الكيميائية التقليدية. لذلك، يتم استنتاج معظم ما هو معروف عن كيمياء هذا الهالوجين من خلال نوعين من الدراسات: أولاً، التجارب على نطاق التتبع (Tracer-scale experiments) التي تستخدم كميات ضئيلة جداً من الذرات المشعة لمراقبة سلوكها في التفاعلات. ثانياً، الاستقراء النظري والحسابي بناءً على الاتجاهات الدورية الملحوظة في مجموعة الهالوجين وسلوك جاره الأثقل، اليود.
10. ما هو الأثر البيئي لمركبات الكلوروفلوروكربون (CFCs)، وكيف يرتبط ذلك بكيمياء الهالوجين؟
مركبات الكلوروفلوروكربون (CFCs) هي مركبات عضوية تحتوي على ذرات الكربون والكلور والفلور. كانت تُستخدم على نطاق واسع في الماضي كمواد تبريد ومواد دافعة. يكمن أثرها البيئي المدمر في استقرارها الكيميائي العالي، الذي يسمح لها بالبقاء في الغلاف الجوي لعقود دون أن تتحلل. عند وصولها إلى طبقة الستراتوسفير العليا، تقوم الأشعة فوق البنفسجية القوية القادمة من الشمس بتكسير الروابط الضعيفة نسبياً بين الكربون والكلور (C-Cl)، مما يؤدي إلى إطلاق ذرات كلور حرة (•Cl)، وهي جذور حرة شديدة التفاعلية. تعمل ذرة الكلور الواحدة كعامل حفاز في سلسلة من التفاعلات التي تدمر جزيئات الأوزون (O₃)، حيث يمكن لذرة كلور واحدة أن تدمر ما يصل إلى 100,000 جزيء أوزون قبل أن يتم إزالتها من الدورة. هذا التدمير الحفزي هو السبب الرئيسي لترقق طبقة الأوزون، مما يزيد من كمية الأشعة فوق البنفسجية الضارة التي تصل إلى سطح الأرض. هذه الظاهرة هي مثال صارخ على كيف يمكن لمركب هالوجين مُصنّع أن يؤثر بشكل كبير على كيمياء الغلاف الجوي العالمي.