متلازمة الأجسام المضادة للفوسفولبيد (APS): الدليل الطبي الشامل
لماذا تتكرر الجلطات والإجهاض دون سبب واضح؟ وهل يمكن السيطرة على هذه المتلازمة المناعية؟
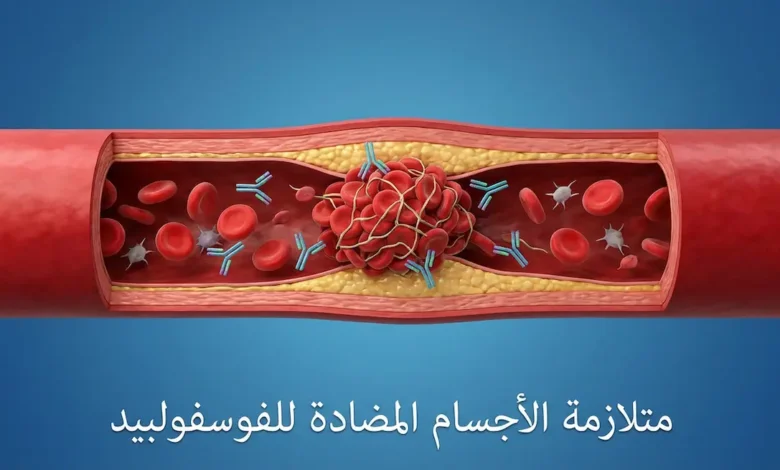
متلازمة الأجسام المضادة للفوسفولبيد هي اضطراب مناعي ذاتي يُنتج فيه الجسم أجساماً مضادة تستهدف بروتينات مرتبطة بالفوسفوليبيدات في أغشية الخلايا. يؤدي ذلك إلى فرط تخثر الدم، مما يُسبب جلطات وريدية وشريانية متكررة ومضاعفات حمل خطِرة كالإجهاض المتكرر. تُعرف أيضاً بمتلازمة هيوز، وتُشخَّص بتحاليل مخبرية محددة تُعاد بعد 12 أسبوعاً للتأكيد.
هيئة التحرير العلمية · تواصل معنا
هل عانيتِ من إجهاض متكرر دون أن يجد أحد السبب؟ أو ربما أُصبتَ بجلطة في ساقك وأنت في الثلاثينيات، فأخبرك الأطباء أن الأمر “غير طبيعي” لعمرك؟ تخيّل أن جهازك المناعي — الذي صُمم لحمايتك — يقرر فجأة مهاجمة مكونات دمك الطبيعية، فيجعل دمك أكثر لزوجة وقابلية للتخثر. هذا ليس سيناريو نظرياً بعيداً عنك. إن متلازمة الأجسام المضادة للفوسفولبيد تصيب شخصاً واحداً من كل ألفَي شخص تقريباً حول العالم. في هذا المقال ستجد كل ما تحتاج معرفته: من الآلية المرضية الدقيقة إلى أحدث بروتوكولات العلاج لعام 2025، بأسلوب يفهمه المريض والطالب والطبيب على حدٍّ سواء.
- اضطراب مناعي ذاتي يُسبب جلطات متكررة وإجهاض غير مفسر.
- اشتبه بها عند حدوث جلطة قبل سن 50 أو إجهاضين متتاليين بلا سبب واضح.
- التشخيص يتطلب تحاليل إيجابية مرتين يفصل بينهما 12 أسبوعاً.
- الوارفارين هو العلاج الأول بعد الجلطة — تجنب مضادات التخثر الحديثة (DOACs).
- الحوامل: أسبرين + هيبارين منخفض الوزن الجزيئي يرفع نسبة نجاح الحمل إلى 80%.
- حافظ على كمية ثابتة يومياً من الأطعمة الغنية بفيتامين K.
- متلازمة APS الكارثية (CAPS) نادرة لكن معدل وفاتها يتجاوز 30% — طوارئ فورية.
- لا تُوقف الوارفارين من تلقاء نفسك حتى لو أصبحت التحاليل سلبية.
- أوقفي حبوب منع الحمل الهرمونية فوراً إذا كانت تحاليلك إيجابية.
كيف تبدو الحياة الحقيقية مع هذا المرض؟ (مثال تطبيقي)
لنأخذ قصة سارة — سيدة سعودية في الثامنة والعشرين من عمرها. حملت ثلاث مرات، وفي كل مرة فقدت جنينها قبل الأسبوع العاشر. أخبرها أطباء النساء والتوليد أن كل شيء “يبدو طبيعياً” في فحوصاتها الروتينية. لكن طبيبة ذكية طلبت منها تحليل الأجسام المضادة للفوسفولبيد، وبعد 12 أسبوعاً أعادت التحليل. جاءت النتيجة إيجابية في المرتين.
بدأت سارة بتلقي جرعة يومية من الأسبرين منخفض الجرعة (Low-dose Aspirin) مع حقن الهيبارين منخفض الوزن الجزيئي (Low Molecular Weight Heparin – LMWH) منذ بداية حملها الرابع. النتيجة؟ أنجبت طفلة سليمة في الأسبوع السابع والثلاثين. هذا المثال ليس خيالياً؛ بل يتكرر يومياً في عيادات أمراض الدم والروماتيزم في المملكة العربية السعودية وغيرها. الفارق الوحيد بين نتيجة مأساوية ونتيجة سعيدة هو التشخيص المبكر والعلاج الصحيح.
ما هي متلازمة الأجسام المضادة للفوسفولبيد (APS)؟ وكيف تحدث؟
لكي نفهم هذه المتلازمة، علينا أن نبدأ من الأساس. الفوسفوليبيدات (Phospholipids) هي جزيئات دهنية تُشكّل الطبقة الخارجية لكل خلية في جسمك. في الوضع الطبيعي، ترتبط بروتينات معينة بهذه الفوسفوليبيدات لتنظيم عملية تخثر الدم. لكن في متلازمة APS، يُنتج جهاز المناعة أجساماً مضادة تُهاجم هذه البروتينات عن طريق الخطأ.
وما النتيجة؟ يفقد الجسم التوازن الدقيق بين التخثر والسيولة. يُصبح الدم ميّالاً للتجلط بشكل مفرط، فتتشكل جلطات في الأوردة والشرايين في أي مكان من الجسم تقريباً.
📖 اقرأ أيضاً: غشاء البلازما (Plasma Membrane): التركيب، الوظيفة، والنقل
كيف يهاجم جهاز المناعة بروتينات الدم بالخطأ؟
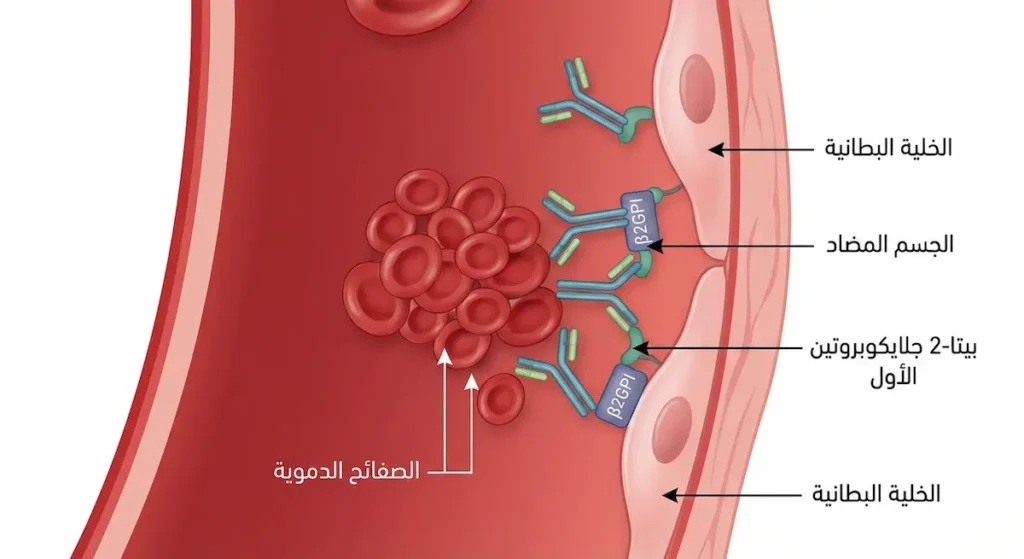
الآلية المرضية (Pathophysiology) معقدة، لكنني سأبسطها قدر الإمكان. تستهدف أضداد الفوسفوليبيد بروتيناً يُسمى بيتا-2 جلايكوبروتين الأول (Beta-2 Glycoprotein I – β2GPI). هذا البروتين يرتبط بسطح الخلايا البطانية (Endothelial cells) التي تُبطّن الأوعية الدموية من الداخل.
عندما ترتبط الأجسام المضادة بهذا البروتين، تحدث سلسلة من الأحداث الكارثية:
أولاً، تتنشط الخلايا البطانية وتبدأ بإفراز مواد تُحفّز التخثر مثل عامل النسيج (Tissue Factor). ثانياً، تتنشط الصفائح الدموية (Platelets) بشكل مفرط فتتكتل وتُسهم في تكوين الجلطات. ثالثاً، يتعطل نظام مضاد التخثر الطبيعي في الجسم، وخصوصاً مسار البروتين C (Protein C Pathway). رابعاً، يتأثر نظام المتممة المناعي (Complement System) ويُسهم في تلف الأنسجة.
فقد أثبتت دراسة منشورة في مجلة The New England Journal of Medicine عام 2020 أن تفعيل نظام المتممة يلعب دوراً محورياً في إحداث مضاعفات الحمل لدى مريضات متلازمة الأجسام المضادة للفوسفولبيد، وليس فقط آلية التخثر المباشرة.
ما الفرق بين متلازمة الأجسام المضادة للفوسفولبيد الأولية والثانوية؟

هنا نقطة مهمة جداً يخلط فيها كثيرون. متلازمة APS الأولية (Primary APS) تعني أن المتلازمة تظهر وحدها دون وجود مرض مناعي آخر مصاحب. تُشكّل هذه الفئة نحو 50% من الحالات.
بالمقابل، متلازمة الأجسام المضادة للفوسفولبيد الثانوية (Secondary APS) تظهر كمضاعفة لمرض مناعي آخر. وفي الغالبية الساحقة من الحالات الثانوية، يكون المرض المرافق هو الذئبة الحمراء الجهازية (Systemic Lupus Erythematosus – SLE). تُظهر الإحصائيات أن 30-40% من مرضى الذئبة الحمراء يحملون أضداد الفوسفوليبيد، لكن ليس جميعهم يُطوّرون أعراض المتلازمة. هذا التمييز ليس أكاديمياً فحسب؛ بل يؤثر على خطة العلاج والمتابعة طويلة الأمد.
| وجه المقارنة | APS الأولية (Primary) | APS الثانوية (Secondary) |
|---|---|---|
| التعريف | تظهر وحدها دون مرض مناعي مرافق | تظهر مصاحبة لمرض مناعي آخر (غالباً الذئبة الحمراء) |
| نسبة الحالات | ~50% من إجمالي الحالات | ~50% — الغالبية مع SLE |
| المرض المرافق | لا يوجد | الذئبة الحمراء، التهاب المفاصل الروماتويدي، شوغرن |
| الأعراض السريرية | جلطات ومضاعفات حمل بشكل رئيس | أعراض المتلازمة + أعراض المرض المناعي الأساسي |
| الفحوصات الإضافية | تحاليل APS فقط + فحوصات التخثر | تحاليل APS + ANA + Anti-dsDNA + C3/C4 |
| خطة العلاج | مميعات الدم + وقاية من الجلطات | مميعات الدم + علاج المرض المناعي الأساسي (مثبطات مناعة) |
| المتابعة | طبيب أمراض الدم | طبيب أمراض الدم + طبيب الروماتيزم |
| المصدر: EULAR Recommendations for APS Management, 2019 | ||
ما أسباب الإصابة بمتلازمة الأجسام المضادة للفوسفولبيد؟ ومن هم الأكثر عرضة؟
لا يزال السبب الدقيق وراء إنتاج الجسم لهذه الأجسام المضادة غامضاً إلى حدٍّ ما. لكن الباحثين يتفقون على أن التفاعل بين عوامل جينية وبيئية هو المحرك الأساس. دعنا نستعرض هذه العوامل واحدة تلو الأخرى.
الأمراض المناعية المرافقة: متلازمة الأجسام المضادة للفوسفولبيد والذئبة الحمراء
كما ذكرنا، تُعَدُّ الذئبة الحمراء الجهازية الشريك الأكثر شيوعاً. لكنها ليست وحدها. فقد تترافق المتلازمة أيضاً مع التهاب المفاصل الروماتويدي (Rheumatoid Arthritis)، ومتلازمة شوغرن (Sjögren’s Syndrome)، والتهاب الأوعية الدموية (Vasculitis). وجود أي من هذه الأمراض يرفع احتمال ظهور أضداد الفوسفوليبيد بشكل ملحوظ.
في السعودية تحديداً، تُشير بيانات مستشفى الملك فيصل التخصصي إلى أن نسبة لا يُستهان بها من مريضات الذئبة الحمراء السعوديات يحملن هذه الأضداد. وهذا يستوجب فحصاً دورياً لكل مريض ذئبة — حتى لو لم تظهر أعراض تخثرية بعد.
📖 اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
العوامل الوراثية والجينية
هل المتلازمة وراثية؟ الإجابة ليست بسيطة. لا يوجد جين واحد يُسبب المرض مباشرة. لكن الدراسات الجينية كشفت عن ارتباط بين بعض أنماط مستضدات الكريات البيضاء البشرية (HLA Types) وبين زيادة خطر الإصابة. تحديداً، الأنماط HLA-DR7 و HLA-DR4 ظهرت بشكل متكرر لدى المرضى. بمعنى آخر: الاستعداد الجيني يُهيّئ الأرض، لكنه لا يُشعل النار وحده.
📖 اقرأ أيضاً: علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
المحفزات البيئية: العدوى الفيروسية وبعض الأدوية
هنا يأتي دور المحفز. عدوى فيروسية عابرة — مثل فيروس إبشتاين-بار (EBV)، أو الفيروس المضخم للخلايا (CMV)، أو حتى كوفيد-19 (COVID-19) — قد تُنشّط الجهاز المناعي بطريقة خاطئة عبر ما يُسمى التقليد الجزيئي (Molecular Mimicry). يتعرف الجهاز المناعي على بروتينات الفيروس التي تُشبه بروتينات الجسم، فيبدأ بمهاجمة الاثنين معاً.
كذلك، بعض الأدوية قد تُحفّز ظهور الأضداد مؤقتاً، مثل الهيدرالازين (Hydralazine) والبروكيناميد (Procainamide). لقد نشرت مجلة Journal of Autoimmunity عام 2021 دراسة مراجعة أكدت أن العدوى بفيروس SARS-CoV-2 قد تُحفّز ظهور أضداد الفوسفوليبيد بشكل عابر لدى ما يصل إلى 50% من مرضى كوفيد الحاد، لكن معظمها يختفي تلقائياً خلال أشهر.
ما أعراض متلازمة الأجسام المضادة للفوسفولبيد بالتفصيل؟
أعراض هذه المتلازمة متنوعة ومراوغة. قد يظن المريض أنه يعاني من مشكلة في الساق فقط، بينما المتلازمة تؤثر على أعضاء متعددة. دعني أفصّلها لك عضواً بعضو.
الجلطات الدموية: العلامة الكبرى التي لا يمكن تجاهلها

الجلطات هي السمة المميزة لمتلازمة APS. يمكن أن تحدث في أي وعاء دموي — وريدي أو شرياني — وفي أي مكان من الجسم. لكن الأكثر شيوعاً هو تجلط الأوردة العميقة (Deep Vein Thrombosis – DVT)، وخصوصاً في الساقين. يشعر المريض بتورم مفاجئ في ربلة الساق مع ألم وسخونة موضعية واحمرار.
إذا انفصل جزء من الجلطة وانتقل عبر مجرى الدم إلى الرئة، تحدث الصمة الرئوية (Pulmonary Embolism – PE) — وهي حالة مهددة للحياة تتظاهر بضيق تنفس مفاجئ وألم صدري حاد وتسارع في ضربات القلب. من ناحية أخرى، الجلطات الشريانية تُسبب سكتات دماغية (Stroke) أو نوبات قلبية (Myocardial Infarction)، وخصوصاً عند شباب لا يحملون عوامل الخطر التقليدية لأمراض القلب كالتدخين أو السكري.
مضاعفات الحمل: متلازمة الأجسام المضادة للفوسفولبيد والإجهاض المتكرر

هل متلازمة الأجسام المضادة للفوسفولبيد تمنع الحمل؟ لا، هي لا تمنع الحمل بذاته، لكنها قد تمنع استمراره. تُسبب الأضداد تكوّن جلطات دقيقة في أوعية المشيمة (Placenta)، فتحرم الجنين من الأكسجين والغذاء. النتائج تتراوح بين:
- إجهاض متكرر (Recurrent Miscarriage)، وخصوصاً بعد الأسبوع العاشر من الحمل.
- تسمم الحمل المبكر (Preeclampsia) الذي يظهر قبل الأسبوع 34.
- تأخر نمو الجنين داخل الرحم (Intrauterine Growth Restriction – IUGR).
- الولادة المبكرة (Preterm Birth).
- ولادة جنين ميت (Stillbirth).
📖 اقرأ أيضاً: الخصوبة (Fertility): العوامل المؤثرة والتحديات
العلامات الجلدية: التزرق الشبكي وعلامات أخرى
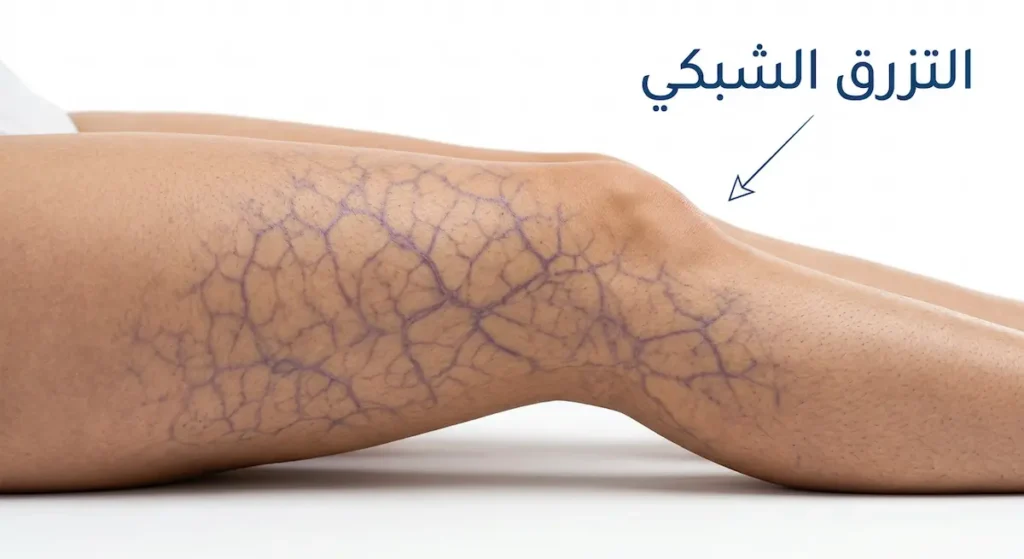
التزرق الشبكي (Livedo Reticularis) هو من أكثر العلامات الجلدية ارتباطاً بالمتلازمة. يظهر كنمط شبكي بنفسجي أو أزرق على الجلد — يُشبه شبكة الصيد — ويبرز أكثر في البرد. لا يُسبب ألماً عادة، لكنه إشارة تحذيرية لا ينبغي تجاهلها.
بالإضافة إلى ذلك، قد تظهر تقرحات جلدية (Skin Ulcers) مزمنة يصعب شفاؤها، وعُقيدات تحت الجلد، ونخر في أصابع اليدين أو القدمين في الحالات الشديدة. كما أن بعض المرضى يُصابون بما يُشبه متلازمة رينو (Raynaud’s Phenomenon) مع تغيّر لون الأصابع عند التعرض للبرد.
الأعراض العصبية: أكثر من مجرد صداع
الصداع النصفي (Migraine) المتكرر والشديد قد يكون العرض الأول لمتلازمة هيوز — وأحياناً الوحيد لسنوات. لقد لفت غراهام هيوز نفسه الانتباه إلى أن كثيراً من مرضاه تحسّن صداعهم بشكل ملحوظ بعد بدء العلاج المميع.
على النقيض من ذلك، الأعراض العصبية الأخطر تشمل النوبات الإقفارية العابرة (Transient Ischemic Attacks – TIAs) التي تُعَدُّ سكتات دماغية مصغرة، واضطرابات الذاكرة والتركيز، والرقص (Chorea)، وفي حالات نادرة التهاب النخاع المستعرض (Transverse Myelitis). فمن المنظور العصبي، قد تُشبه المتلازمة التصلب المتعدد (Multiple Sclerosis – MS) في بعض تظاهراتها، مما يجعل التشخيص التفريقي تحدياً حقيقياً.
كيف تؤثر المتلازمة على القلب والكلى والصفائح الدموية؟
القلب يتأثر بطرق متعددة. أشهرها التهاب صمامات القلب غير الجرثومي (Libman-Sacks Endocarditis)، الذي يُسبب ثخانة الصمامات — وخصوصاً الصمام التاجي (Mitral Valve) — مع ارتجاع دموي. هذا وقد تُسبب المتلازمة أيضاً تضيقاً في الشرايين التاجية وزيادة خطر أمراض القلب المبكرة.
أما الكلى، فتتأثر بما يُسمى اعتلال الكلى بأضداد الفوسفوليبيد (APS Nephropathy)، حيث تتكون جلطات دقيقة في الأوعية الكلوية الصغيرة. هذا يؤدي إلى ارتفاع ضغط الدم وتراجع وظائف الكلى تدريجياً.
الجدير بالذكر أن نقص الصفائح الدموية (Thrombocytopenia) يظهر لدى 20-30% من المرضى. قد يبدو هذا متناقضاً — كيف ينخفض عدد الصفائح بينما يزداد التخثر؟ السر أن الأجسام المضادة تُنشّط الصفائح وتستهلكها في تكوين الجلطات، فينخفض عددها في الدم.
📖 اقرأ أيضاً: تصلب الشرايين (Arteriosclerosis): الأسباب، الأعراض، والوقاية
كيف يتم تشخيص متلازمة الأجسام المضادة للفوسفولبيد؟ معايير سيدني الدولية
التشخيص لا يعتمد على التحاليل المخبرية وحدها، ولا على الأعراض السريرية وحدها. بل يتطلب الأمرين معاً وفق معايير صارمة تُعرف بمعايير سيدني المُعدَّلة (Revised Sydney Classification Criteria) الصادرة عام 2006 والمُحدَّثة في إرشادات 2023.
لكي يُشخَّص المريض بمتلازمة APS، يجب أن يستوفي:
معياراً سريرياً واحداً على الأقل:
- جلطة دموية مؤكدة — وريدية أو شريانية — في أي عضو.
- مضاعفة حمل مؤكدة: إما وفاة جنين طبيعي بعد الأسبوع 10، أو ولادة مبكرة قبل الأسبوع 34 بسبب تسمم الحمل أو قصور المشيمة، أو ثلاث حالات إجهاض عفوي متتالية أو أكثر قبل الأسبوع 10.
ومعياراً مخبرياً واحداً على الأقل:
أي من التحاليل الثلاثة التالية يجب أن يكون إيجابياً في مناسبتين مختلفتين يفصل بينهما 12 أسبوعاً على الأقل.
متى يطلب الطبيب إجراء تحليل الأجسام المضادة للفوسفولبيد؟
يطلبه في عدة سيناريوهات: جلطة وريدية أو شريانية غير مبررة خصوصاً في عمر أقل من 50 سنة، إجهاض متكرر، سكتة دماغية في شاب، نقص صفائح دموية غير مفسر، أو وجود تزرق شبكي على الجلد مع أي مما سبق. كذلك يُطلب التحليل لكل مريض ذئبة حمراء كفحص روتيني.
كيف تقرأ نتيجة تحليل الأجسام المضادة للفوسفولبيد؟ (التحاليل الثلاثة الأساسية)

1. مضاد التخثر الذئبي (Lupus Anticoagulant – LA):
اسمه مضلل! فهو لا يُسبب نقص تخثر بل فرط تخثر. يُكشف عنه بسلسلة من اختبارات التخثر الوظيفية وليس بفحص واحد. يُعَدُّ أقوى مؤشر تنبؤي للجلطات بين التحاليل الثلاثة.
2. أضداد الكارديوليبين (Anticardiolipin Antibodies – aCL):
تُقاس بتقنية الإليزا (ELISA). يُعتَدُّ بالنتائج المتوسطة إلى العالية فقط (أعلى من 40 GPL أو MPL، أو أعلى من المئين 99). النتائج الإيجابية المنخفضة قد تكون عابرة وغير ذات أهمية سريرية.
3. أضداد بيتا-2 جلايكوبروتين الأول (Anti-β2GPI Antibodies):
تُقاس أيضاً بالإليزا. وجودها يدعم التشخيص ويرفع خطر التخثر، خصوصاً من النوع IgG.
| التحليل | طريقة القياس | القيمة الإيجابية المعتبرة | القوة التنبؤية |
|---|---|---|---|
| مضاد التخثر الذئبي (LA) | اختبارات تخثر وظيفية متسلسلة (dRVVT + aPTT) | إيجابي / سلبي (لا يُقاس بالأرقام) | الأقوى — أعلى ارتباط بالجلطات |
| أضداد الكارديوليبين (aCL) | تقنية الإليزا (ELISA) — IgG و IgM | أعلى من 40 GPL/MPL أو أعلى من المئين 99 | قوية — خصوصاً IgG بالمستويات المرتفعة |
| أضداد β2GPI | تقنية الإليزا (ELISA) — IgG و IgM | أعلى من المئين 99 وفقاً للمختبر | قوية — داعمة للتشخيص ومرتبطة بالتخثر |
| المصدر: ACR/EULAR 2023 Classification Criteria for APS | |||
قراءة تحليل متلازمة الأجسام المضادة للفوسفولبيد ليست بسيطة كقراءة تحليل السكر. يجب أن يُفسرها طبيب متخصص في سياق الصورة السريرية الكاملة. المريض الذي تكون لديه التحاليل الثلاثة إيجابية (يُسمى Triple Positive) يحمل أعلى خطر للجلطات والمضاعفات.
لماذا يجب إعادة التحليل بعد 12 أسبوعاً؟
لأن أضداد الفوسفوليبيد قد تظهر بشكل عابر بعد العدوى أو تناول أدوية معينة. التأكيد بعد 12 أسبوعاً يضمن أن هذه الأضداد مستمرة (Persistent) وليست مجرد ظاهرة مؤقتة. بدون هذا التأكيد، لا يُمكن وضع التشخيص النهائي. وإن وجدت تحليلاً إيجابياً واحداً لم يُعاد تأكيده، فلا تقل إنك مريض بمتلازمة APS.
لقد أصدرت الكلية الأمريكية لأمراض الروماتيزم (ACR) والرابطة الأوروبية لمكافحة الروماتيزم (EULAR) في عام 2023 معايير تصنيف جديدة مُحدَّثة تعتمد نظام النقاط (Scoring System) لتشخيص متلازمة الأجسام المضادة للفوسفولبيد. هذه المعايير الجديدة تأخذ بعين الاعتبار شدة التحاليل المخبرية ونوع المظهر السريري، مما يرفع دقة التشخيص بشكل كبير مقارنة بمعايير سيدني القديمة.
ما هي الخطة العلاجية لمتلازمة الأجسام المضادة للفوسفولبيد وفق أحدث البروتوكولات؟
العلاج يعتمد على حالة المريض: هل هو حامل للأضداد فقط؟ أم حدثت لديه جلطة؟ أم حامل ويحتاج حماية خاصة؟ كل سيناريو له بروتوكول مختلف.
كيف نعالج الحالات الإيجابية للتحليل بدون جلطات سابقة؟ (الوقاية الأولية)
هذا سؤال يطرحه كثير من المرضى: “تحاليلي إيجابية لكنني لم أتعرض لجلطة — هل أحتاج دواء؟” الجواب يعتمد على ملف الخطر الشخصي. إذا كان المريض يحمل الأضداد الثلاثة (Triple Positive) أو لديه عوامل خطر إضافية مثل التدخين أو السمنة أو استخدام أقراص منع الحمل الهرمونية، فإن الأسبرين منخفض الجرعة (75-100 mg يومياً) يُستخدم كوقاية أولية.
من ناحية أخرى، إذا كان لدى المريض ضد واحد فقط بمستوى منخفض ولا عوامل خطر مرافقة، فقد يكتفي الطبيب بالمراقبة وتعديل نمط الحياة. الأهم من الأدوية في هذه المرحلة هو تجنب المحفزات: إيقاف التدخين، تجنب حبوب منع الحمل الحاوية على إستروجين (Estrogen)، التحكم بالوزن وضغط الدم، وتجنب فترات الجلوس الطويلة.
ما هو علاج المرضى بعد التعرض لجلطة؟
بعد الجلطة الأولى، يُصبح العلاج المميع إلزامياً وطويل الأمد — غالباً مدى الحياة. الوارفارين (Warfarin) يبقى حجر الزاوية في علاج متلازمة أضداد الفوسفوليبيد بعد الجلطة. يُضبط بتحليل INR الذي يجب أن يبقى بين 2.0 و 3.0 في حالة الجلطات الوريدية.
إذاً كيف يختلف هذا عن علاج الجلطات العادية؟ الفرق الجوهري أن مضادات التخثر الفموية الحديثة المباشرة (Direct Oral Anticoagulants – DOACs) مثل الريفاروكسابان (Rivaroxaban) والأبيكسابان (Apixaban) ليست بديلاً مناسباً لمرضى متلازمة APS. فقد أثبتت دراسة TRAPS المنشورة في مجلة Blood عام 2018 أن الريفاروكسابان ارتبط بمعدل أعلى من الجلطات المتكررة مقارنة بالوارفارين لدى مرضى متلازمة الأجسام المضادة للفوسفولبيد الثلاثي الإيجابية، مما أدى إلى إيقاف الدراسة مبكراً لأسباب تتعلق بسلامة المرضى.
📖 اقرأ أيضاً: مميعات الدم: ما هي وكيف تعمل في جسمك؟
ما بروتوكول علاج متلازمة الأجسام المضادة للفوسفولبيد للحوامل؟
هذا هو القسم الذي تبحث عنه آلاف السيدات في العالم العربي. بداية، الوارفارين ممنوع أثناء الحمل لأنه يعبر المشيمة ويُسبب تشوهات جنينية خطِرة (Warfarin Embryopathy). البديل هو:
- الأسبرين منخفض الجرعة (81 mg يومياً) يبدأ قبل الحمل أو فور اكتشافه.
- الهيبارين منخفض الوزن الجزيئي (LMWH) مثل الإنوكسابارين (Enoxaparin) بجرعة وقائية أو علاجية حسب التاريخ المرضي.
هذا البروتوكول يرفع معدل نجاح الحمل من أقل من 20% بدون علاج إلى أكثر من 70-80% مع العلاج — وهو رقم يُحدث فارقاً هائلاً.
يجب إيقاف الهيبارين قبل الولادة بـ 24 ساعة لتجنب النزيف أثناء الوضع. بعد الولادة، يُعاد الوارفارين أو الهيبارين حسب الحاجة. الجدير بالذكر أن الوارفارين آمن أثناء الرضاعة الطبيعية.
📖 اقرأ أيضاً: صيام الحامل في رمضان: الدليل العلمي الكامل لسلامتكِ وسلامة جنينكِ
متلازمة الأجسام المضادة للفوسفولبيد الكارثية (CAPS): حالة الطوارئ النادرة
| الحالة السريرية | العلاج الموصى به | المدة | ملاحظات مهمة |
|---|---|---|---|
| أضداد إيجابية بدون أعراض (Asymptomatic) | أسبرين 75-100 mg يومياً (خصوصاً Triple Positive) | طويلة الأمد | تعديل نمط الحياة + إيقاف حبوب منع الحمل الهرمونية |
| جلطة وريدية أولى | وارفارين (INR 2.0-3.0) | مدى الحياة غالباً | تجنب DOACs — أقل فعالية في APS |
| جلطة شريانية (سكتة دماغية) | وارفارين (INR 2.0-3.0) أو (INR 3.0-4.0 في بعض الحالات) | مدى الحياة | بعض الخبراء يضيفون الأسبرين |
| حمل مع تاريخ إجهاض فقط | أسبرين 81 mg + هيبارين LMWH بجرعة وقائية | طوال الحمل + 6 أسابيع بعد الولادة | إيقاف الوارفارين قبل الحمل — خطر تشوهات جنينية |
| حمل مع تاريخ جلطة سابقة | أسبرين 81 mg + هيبارين LMWH بجرعة علاجية كاملة | طوال الحمل + 6 أسابيع بعد الولادة | متابعة مشتركة: أمراض الدم + أمراض النساء |
| CAPS (الكارثية) | هيبارين وريدي + كورتيكوستيرويدات + تبديل بلازما أو IVIG | حاد — عناية مركزة | إيكوليزوماب في الحالات المقاومة — معدل الوفاة > 30% |
| المصادر: EULAR 2019 · ACR/EULAR 2023 | |||
- 🔹 ACR/EULAR 2023: معايير تصنيف محدثة لمتلازمة أضداد الفوسفوليبيد — نظام النقاط الجديد. [الرابط]
- 🔹 EULAR 2019: التوصيات الأوروبية لإدارة وعلاج متلازمة APS عند البالغين. [الرابط]
- 🔹 British Society for Haematology (BSH) 2022: إرشادات التعامل مع أضداد الفوسفوليبيد في سياق الجلطات والحمل. [الرابط]
- 🔹 الهيئة السعودية للتخصصات الصحية (SCFHS): البرنامج التدريبي في أمراض الدم يتضمن بروتوكولات تشخيص وعلاج APS ضمن المنهج المعتمد. [الرابط]
هذا هو أخطر أشكال المتلازمة على الإطلاق. متلازمة APS الكارثية (Catastrophic Antiphospholipid Syndrome – CAPS) تُصيب أقل من 1% من مرضى المتلازمة، لكن معدل الوفاة فيها يتجاوز 30% حتى مع العلاج المكثف.
ما يحدث هو عاصفة تخثرية (Thrombotic Storm) تضرب ثلاثة أعضاء أو أكثر خلال أقل من أسبوع. الكلى والرئتان والدماغ والقلب تتأثر في آنٍ واحد. المريض يدخل في فشل أعضاء متعدد (Multi-organ Failure) ويحتاج عناية مركزة فورية.
العلاج يشمل ثلاثة محاور متزامنة: مضادات التخثر بجرعات عالية (الهيبارين الوريدي)، والكورتيكوستيرويدات بجرعات نبضية (Pulse Steroids)، وتبديل البلازما العلاجي (Therapeutic Plasma Exchange – TPE) أو الغلوبيولين المناعي الوريدي (IVIG). في الحالات المقاومة، يُستخدم دواء إيكوليزوماب (Eculizumab) الذي يُثبط نظام المتممة. وعليه فإن كل ساعة تأخير في العلاج تُقلل فرص النجاة.
📖 اقرأ أيضاً: الإنتان (Sepsis): الأسباب، الأعراض، والعلاج
كيف يتعايش المريض مع المتلازمة؟ نمط الحياة والنظام الغذائي
هل يوجد نظام غذائي لمرضى متلازمة الأجسام المضادة للفوسفولبيد؟
لا يوجد “حمية خاصة” للمتلازمة بحد ذاتها. لكن النظام الغذائي لمرضى متلازمة الأجسام المضادة للفوسفولبيد يتأثر بشكل مباشر بنوع الدواء المستخدم. إذا كنت تتناول الوارفارين، فإن فيتامين K (Vitamin K) هو محور اهتمامك الغذائي.
فيتامين K ضروري لتصنيع عوامل التخثر في الكبد. الوارفارين يعمل بتثبيط فيتامين K. لذلك، أي تغيير مفاجئ في استهلاك الأطعمة الغنية بفيتامين K — مثل السبانخ والبروكلي والملفوف واللفت — يُربك جرعة الوارفارين. القاعدة الذهبية ليست تجنب هذه الأطعمة، بل تناول كمية ثابتة ومتسقة يومياً.
بالإضافة إلى ذلك، يُنصح بتجنب الإفراط في شرب عصير التوت البري (Cranberry Juice) والكحول، وتجنب المكملات العشبية بدون استشارة — فالجنكو بيلوبا (Ginkgo Biloba) والثوم المركز والزنجبيل بجرعات عالية قد تزيد سيولة الدم بشكل خطِر.
نظام غذائي مضاد للالتهاب (Anti-inflammatory Diet) غني بأوميغا-3 من الأسماك، والفواكه والخضراوات الملونة، وزيت الزيتون البكر — قد يُسهم في تقليل الالتهاب المزمن المرتبط بالمتلازمة، وإن لم تُثبت دراسات كبيرة فائدته المباشرة في منع الجلطات.
| الطعام | محتوى فيتامين K لكل 100g (تقريباً) | مستوى التأثير على الوارفارين | التوصية |
|---|---|---|---|
| اللفت (Kale) | ~817 μg | مرتفع جداً | حافظ على كمية ثابتة يومياً |
| السبانخ | ~483 μg | مرتفع جداً | حافظ على كمية ثابتة يومياً |
| البروكلي | ~101 μg | متوسط | تناوُل معتدل ومنتظم |
| البقدونس | ~1,640 μg | مرتفع جداً | كميات صغيرة ثابتة كالتزيين فقط |
| الخيار | ~16 μg | منخفض | آمن — تناوله بحرية |
| الطماطم | ~8 μg | منخفض | آمن — تناوله بحرية |
| المصدر: National Institutes of Health (NIH) — Office of Dietary Supplements | |||
📖 اقرأ أيضاً: الطعام: ما هي أسس التغذية السليمة وكيف يؤثر على صحتنا؟
ما النصائح العملية لتجنب النزيف والجلطات أثناء السفر الطويل؟
السفر الطويل — وخصوصاً الرحلات الجوية التي تتجاوز أربع ساعات — يُعَدُّ عامل خطر مستقل للجلطات الوريدية حتى عند الأصحاء. فكيف بمريض متلازمة APS؟ إليك نصائح عملية مباشرة:
تحرّك كل ساعة واحدة على الأقل — قف وامشِ في الممر. ارتدِ جوارب ضاغطة طبية (Compression Stockings) تبدأ قوتها من 15-20 mmHg. أكثر من شرب الماء وتجنب الجفاف. لا تثنِ ساقيك لفترات طويلة. واستشر طبيبك قبل السفر — فقد يحتاج بعض المرضى جرعة إضافية من الهيبارين قبل الرحلة.
بالنسبة لتجنب النزيف — وهو الوجه الآخر لعملة العلاج المميع — استخدم فرشاة أسنان ناعمة، تجنب الرياضات العنيفة والتي قد تُسبب إصابات، واحمل معك بطاقة تعريفية طبية (Medical Alert Card) تُوضّح أنك تتناول مميعات الدم.
📖 اقرأ أيضاً: النزيف المسيطر عليه: الإسعافات الأولية وخطوات التعامل معه
هل يمكن الشفاء التام من متلازمة الأجسام المضادة للفوسفولبيد؟
نسبة الشفاء من متلازمة الأجسام المضادة للفوسفولبيد بالمعنى الكامل — أي اختفاء الأضداد نهائياً — هي موضوع بحثي نشط. في بعض الحالات، تختفي الأضداد تلقائياً بعد سنوات. دراسات حديثة تُشير إلى أن 10-20% من المرضى قد تصبح تحاليلهم سلبية بعد فترة طويلة من المتابعة.
لكن هل يعني ذلك إيقاف العلاج؟ هذا قرار معقد يتخذه الطبيب المتخصص بناءً على عدة عوامل: نوع المظهر السريري الأولي (جلطة أم مضاعفة حمل؟)، شدة الأضداد، وعدد التحاليل السلبية المتتالية. بشكل عام، إذا كان المريض قد تعرض لجلطة سابقة، فإن معظم الإرشادات تنصح بالاستمرار في العلاج المميع حتى لو أصبحت التحاليل سلبية — لأن خطر التكرار يبقى قائماً.
من جهة ثانية، العلاجات المستقبلية تُبشّر بآفاق جديدة. الأدوية التي تستهدف الخلايا اللمفاوية البائية (B-cell Targeted Therapies) مثل الريتوكسيماب (Rituximab) أظهرت نتائج واعدة في دراسات صغيرة لمرضى متلازمة APS المقاومة للعلاج التقليدي. كما أن مثبطات نظام المتممة تفتح باباً جديداً لعلاج الحالات الكارثية والمقاومة.
📖 اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
الأسئلة الشائعة
اضغط على السؤال لتعرف الإجابة
الخلاصة
متلازمة الأجسام المضادة للفوسفولبيد ليست مرضاً نادراً كما يظن كثيرون. إنها سبب خفي وراء آلاف حالات الإجهاض المتكرر والجلطات غير المفسرة في العالم العربي. ثلاث نقاط يجب أن تبقى في ذهنك:
أولاً، أي جلطة في عمر مبكر أو إجهاض متكرر يستوجب فحص أضداد الفوسفوليبيد. ثانياً، التشخيص يتطلب تأكيداً بتحليلين يفصل بينهما 12 أسبوعاً — لا تقبل تشخيصاً من تحليل واحد. ثالثاً، العلاج متاح وفعال ويُغيّر حياة المرضى بشكل جذري، لكنه يتطلب التزاماً طويل الأمد ومتابعة دورية مع طبيب أمراض الدم أو الروماتيزم.
فهل أجريت تحليل الأجسام المضادة للفوسفولبيد من قبل، أو هل تعرف شخصاً يحتاج معرفة هذه المعلومات؟
المصادر والمراجع
- Miyakis, S., Lockshin, M. D., Atsumi, T., et al. (2006). International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS). Journal of Thrombosis and Haemostasis, 4(2), 295–306. DOI: 10.1111/j.1538-7836.2006.01753.x
- الورقة المرجعية لمعايير سيدني المُعدَّلة لتشخيص متلازمة APS.
- Pengo, V., Denas, G., Zoppellaro, G., et al. (2018). Rivaroxaban vs warfarin in high-risk patients with antiphospholipid syndrome (TRAPS trial). Blood, 132(13), 1365–1371. DOI: 10.1182/blood-2018-04-848333
- الدراسة التي أثبتت عدم تفوق الريفاروكسابان على الوارفارين في مرضى APS.
- Barbhaiya, M., Zuily, S., Naden, R., et al. (2023). 2023 ACR/EULAR antiphospholipid syndrome classification criteria. Annals of the Rheumatic Diseases, 82(10), 1258–1270. DOI: 10.1136/ard-2023-224609
- معايير التصنيف الجديدة لعام 2023 المعتمدة على نظام النقاط.
- Zuo, Y., Estes, S. K., Ali, R. A., et al. (2020). Prothrombotic autoantibodies in serum from patients hospitalized with COVID-19. Science Translational Medicine, 12(570), eabd3876. DOI: 10.1126/scitranslmed.abd3876
- دراسة الارتباط بين كوفيد-19 وظهور أضداد الفوسفوليبيد العابرة.
- Tektonidou, M. G., Andreoli, L., Limper, M., et al. (2019). EULAR recommendations for the management of antiphospholipid syndrome in adults. Annals of the Rheumatic Diseases, 78(10), 1296–1304. DOI: 10.1136/annrheumdis-2019-215213
- توصيات EULAR لإدارة متلازمة APS عند البالغين.
- Cervera, R., Rodríguez-Pintó, I., Espinosa, G. (2018). The diagnosis and clinical management of the catastrophic antiphospholipid syndrome: A comprehensive review. Journal of Autoimmunity, 92, 1–11. DOI: 10.1016/j.jaut.2018.05.007
- مراجعة شاملة لتشخيص وعلاج متلازمة APS الكارثية.
- National Institutes of Health (NIH). Antiphospholipid Syndrome. MedlinePlus. https://medlineplus.gov/antiphospholipidsyndrome.html
- صفحة المعاهد الوطنية للصحة عن المتلازمة بمعلومات محدثة للمرضى.
- Centers for Disease Control and Prevention (CDC). Venous Thromboembolism (Blood Clots). https://www.cdc.gov/blood-clots/
- معلومات CDC عن الجلطات الوريدية وعوامل الخطر.
- World Health Organization (WHO). Cardiovascular diseases (CVDs). https://www.who.int/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds)
- حقائق منظمة الصحة العالمية عن أمراض القلب والأوعية الدموية.
- American College of Rheumatology (ACR). Antiphospholipid Syndrome. https://rheumatology.org/patients/antiphospholipid-syndrome
- صفحة ACR التثقيفية للمرضى عن متلازمة APS.
- Lupus Foundation of America. Antiphospholipid Antibodies. https://www.lupus.org/resources/what-are-antiphospholipid-antibodies
- شرح مبسط للعلاقة بين الذئبة الحمراء وأضداد الفوسفوليبيد.
- Levine, J. S., Branch, D. W., Rauch, J. (2002). The antiphospholipid syndrome. New England Journal of Medicine, 346(10), 752–763. DOI: 10.1056/NEJMra002974
- مرجع كلاسيكي في NEJM عن الآلية المرضية للمتلازمة.
- Ruiz-Irastorza, G., Crowther, M., Branch, W., Khamashta, M. A. (2010). Antiphospholipid syndrome. The Lancet, 376(9751), 1498–1509. DOI: 10.1016/S0140-6736(10)60709-X
- مراجعة شاملة في The Lancet عن المتلازمة.
- Hughes, G. R. V. (2014).Hughes Syndrome: A Patient’s Guide (2nd ed.). Springer. ISBN: 978-1-4471-5415-1.
- كتاب مرجعي من مكتشف المتلازمة نفسه، مكتوب للمرضى والأطباء.
- Knight, J. S., Branch, D. W., Engel, J. A. (2023). Antiphospholipid syndrome: advances in diagnosis, pathogenesis, and management. Scientific American Medicine. https://www.scientificamerican.com/
- مقالة مبسطة تعرض أحدث التطورات في فهم وعلاج المتلازمة.
قراءات إضافية ومصادر للتوسع
- Asherson, R. A., Cervera, R., Piette, J.-C., Shoenfeld, Y. (Eds.). (2002).The Antiphospholipid Syndrome II: Autoimmune Thrombosis. Elsevier. ISBN: 978-0444509871.
- لماذا نقترح عليك قراءته؟ هذا الكتاب يُعَدُّ من “أمهات المصادر” في دراسة متلازمة أضداد الفوسفوليبيد. يغطي التاريخ الكامل للمتلازمة والآليات المرضية بعمق لا تجده في المراجعات القصيرة.
- Garcia, D., Erkan, D. (2018). Diagnosis and management of the antiphospholipid syndrome. New England Journal of Medicine, 378(21), 2010–2021. DOI: 10.1056/NEJMra1700891
- لماذا نقترح عليك قراءته؟ مراجعة حديثة من NEJM تُلخّص كل ما يحتاجه الطبيب المقيم أو طالب الطب المتقدم لفهم التشخيص والعلاج وفق أحدث الأدلة.
- Cervera, R. (2017). Antiphospholipid syndrome. Thrombosis Research, 151(Suppl 1), S43–S47. DOI: 10.1016/S0049-3848(17)30066-X
- لماذا نقترح عليك قراءته؟ ورقة مراجعة موجزة لكنها شاملة من أبرز الباحثين في هذا المجال، مناسبة لمن يريد مدخلاً سريعاً قبل التعمق في المصادر الأكبر.
إذا وجدت هذا المقال مفيداً ومعلوماته غيّرت فهمك لهذه المتلازمة، فشاركه مع طبيبك أو مع أي شخص في عائلتك يعاني من جلطات غير مفسرة أو إجهاض متكرر. التشخيص المبكر قد يُنقذ حياة أو يُحقق حلم أمومة. تابعنا على موسوعة خلية للمزيد من المقالات الطبية المبنية على أحدث الأدلة العلمية.
إخلاء مسؤولية طبية: المعلومات الواردة في هذا المقال لأغراض تثقيفية فقط ولا تُغني عن استشارة طبيب مختص. لا تبدأ أو توقف أي علاج دوائي بناءً على هذا المقال دون مراجعة طبيبك المعالج.
جرت مراجعة هذا المقال من قبل هيئة التحرير العلمية في موقعنا لضمان الدقة والمعلومة الصحيحة.