سرطان المعدة: ما أعراضه المبكرة وكيف يُعالج بأحدث الطرق؟
كيف تتحول خلايا المعدة الطبيعية إلى ورم خبيث وما فرص النجاة منه؟
سرطان المعدة هو نمو غير طبيعي ومتسارع لخلايا خبيثة تنشأ في البطانة الداخلية للمعدة. يحتل المرتبة الخامسة عالمياً بين أكثر السرطانات شيوعاً، ويُسبب نحو 800,000 وفاة سنوياً. تتراوح أنواعه بين السرطان الغدي والأورام اللمفاوية وأورام اللحمة المعدية المعوية. يعتمد التشخيص على التنظير والخزعة، بينما يشمل العلاج الجراحة والعلاج الكيميائي والمناعي.
تمت المراجعة والتدقيق بواسطة الهيئة الطبية:

اختصاصية الأورام والطب النووي

اختصاصية أمراض الجهاز الهضمي

اختصاصية تغذية علاجية

خبير الرقابة الدوائية
هل شعرت يوماً بحرقة مزمنة في رأس معدتك أو فقدان غير مبرر في شهيتك، ثم أقنعت نفسك بأنها مجرد “قرحة عابرة” أو “توتر نفسي”؟ أنت لست وحدك. الآلاف من المرضى في العالم العربي يؤجلون زيارة طبيب الجهاز الهضمي حتى يصل المرض إلى مرحلة متقدمة، وهذا بالضبط ما يجعل سرطان المعدة من أخطر الأورام الصامتة. في هذا المقال من موقع خلية، ستجد كل ما تحتاج معرفته — من أول عَرَض خفي إلى أحدث بروتوكولات العلاج المناعي لعام 2025 — بلغة واضحة ومعلومات دقيقة راجعها أطباء متخصصون. لن تغادر هذه الصفحة إلا وأنت تملك وعياً حقيقياً قد ينقذ حياتك أو حياة شخص تحبه.
🔑 خلاصة المقال في دقيقة واحدة
⚡ حقائق جوهرية
- سرطان المعدة خامس أكثر السرطانات شيوعاً عالمياً بنحو 968,000 حالة سنوياً، والسرطان الغدي يشكل 90–95% منها.
- جرثومة المعدة (H. pylori) مسرطن مؤكد من المجموعة الأولى — وعلاجها يُقلل خطر الإصابة بشكل كبير.
- نسبة الشفاء في المراحل المبكرة تتجاوز 90%، لكنها تنخفض إلى أقل من 5% في المرحلة الرابعة.
🛡️ خطوات وقائية فورية
- اطلب فحص جرثومة المعدة إن كنت تعاني من أعراض هضمية مزمنة أو لديك تاريخ عائلي.
- أقلع عن التدخين — يُقلل الخطر بنسبة 30–40% خلال 10 سنوات.
- قلّل اللحوم المعالجة والمملحة وأكثِر من الخضروات والفواكه الطازجة.
🚨 تحذيرات لا تتجاهلها
- حرقة المعدة المزمنة + فقدان وزن + فقر دم = زيارة طبيب فوراً وليس مضادات حموضة فقط.
- العلاجات المناعية والموجهة الحديثة (2025) ضاعفت فرص البقاء في المراحل المتقدمة — اسأل طبيبك عن الاختبارات الجزيئية.
ما هو سرطان المعدة (Gastric Cancer) وكيف يبدأ في “الخلية”؟
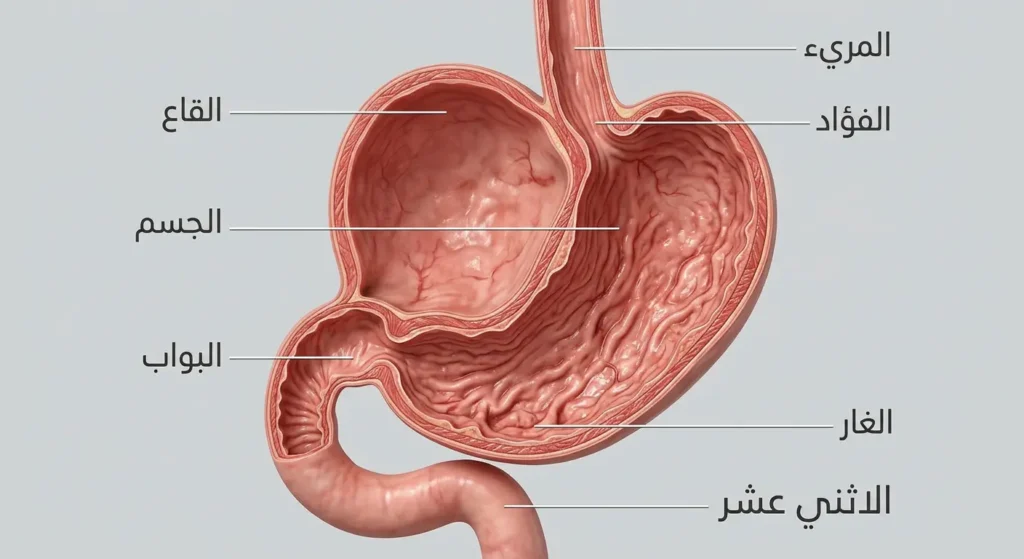
لفهم كيف ينشأ سرطان المعدة، من الضروري أولاً أن تعرف تشريح هذا العضو. المعدة ليست كيساً بسيطاً كما يتخيل كثيرون. إنها عضو عضلي مجوف يتكون من خمسة أجزاء تشريحية: الفؤاد (Cardia) وهو الموضع الذي يلتقي فيه المريء بالمعدة، ثم القاع (Fundus) في الأعلى، يليه الجسم (Body) وهو الجزء الأكبر، ثم الغار (Antrum) بالقرب من المخرج، وأخيراً البواب (Pylorus) الذي يتحكم في مرور الطعام نحو الاثني عشر. لكل جزء من هذه الأجزاء خصائص نسيجية مختلفة؛ إذ إن السرطان الذي ينشأ في الفؤاد يختلف سلوكياً وعلاجياً عن ذلك الذي يظهر في الغار.
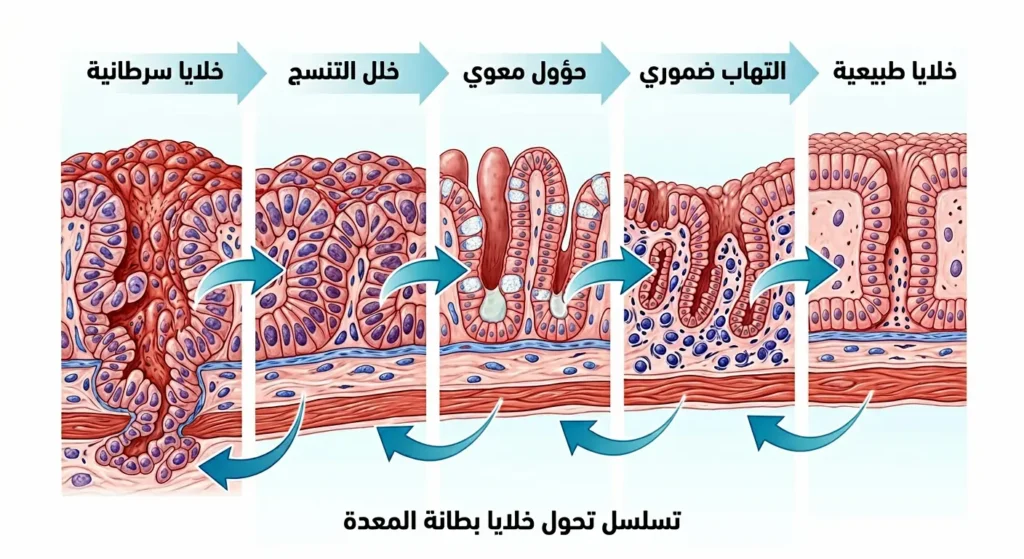
فكيف تتحول خلية سليمة في بطانة المعدة إلى خلية سرطانية؟ تبدأ القصة عادة بتعرض الغشاء المخاطي المبطن للمعدة لعوامل ضارة مزمنة — كالتهاب مستمر ناتج عن جرثومة المعدة (Helicobacter pylori) أو تناول كميات كبيرة من الأطعمة المملحة والمدخنة لسنوات طويلة. هذا الضرر المتكرر يُحدث تغيرات تدريجية في الخلايا، تبدأ بما يُعرف بالتهاب المعدة الضموري (Atrophic Gastritis)، ثم تتطور إلى حؤول معوي (Intestinal Metaplasia)، وصولاً إلى خلل التنسج (Dysplasia). في مرحلة خلل التنسج، تكون الخلية قد فقدت آليات التحكم الطبيعية في انقسامها. وعندما تتراكم طفرات جينية كافية — مثل تعطل جينات كابتة للورم كـ TP53 أو تفعيل جينات مسرطنة — تنفلت الخلية من كل قيود النمو الطبيعي وتبدأ بالتكاثر دون توقف. هنا بالضبط تولد الخلية السرطانية الأولى.
معلومة سريعة: وفقاً لبيانات الوكالة الدولية لأبحاث السرطان (IARC) الصادرة عام 2024، سُجِّل نحو 968,000 حالة جديدة من سرطان المعدة حول العالم خلال عام 2022 وحده، مما يجعله خامس أكثر السرطانات تشخيصاً على مستوى الكوكب.
اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
ما أنواع أورام المعدة الخبيثة؟
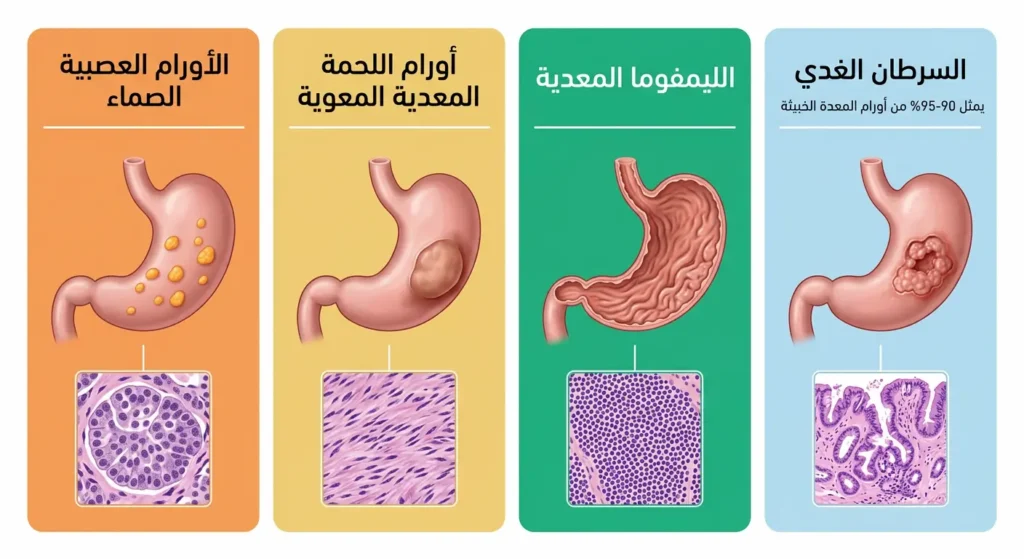
ليست كل أورام المعدة متشابهة. التصنيف الدقيق لنوع الورم يحدد كل شيء — من خطة العلاج إلى التوقعات طويلة الأمد. إليك الأنواع الأربعة الرئيسة:
السرطان الغدي (Adenocarcinoma): الأكثر شيوعاً
يشكل السرطان الغدي ما بين 90% و95% من جميع حالات سرطان المعدة. ينشأ من الخلايا الغدية المنتجة للمخاط في البطانة الداخلية. وينقسم وفق تصنيف لورين (Lauren Classification) إلى نمطين: النمط المعوي (Intestinal type) الذي يرتبط غالباً بعدوى جرثومة المعدة والعوامل البيئية ويميل للظهور في الأعمار المتقدمة، والنمط المنتشر (Diffuse type) الذي يصيب فئات عمرية أصغر ويتميز بعدوانية أعلى وصعوبة في التشخيص المبكر. من الأشكال الفرعية الخطيرة ما يُعرف بسرطان الخلايا الخاتمية (Signet ring cell carcinoma) الذي ينتمي للنمط المنتشر ويتسلل بين طبقات جدار المعدة بصمت.
أورام الليمفوما المعدية (Gastric Lymphoma)
تمثل نحو 3-5% من أورام المعدة. تنشأ من خلايا الجهاز اللمفاوي الموجودة في جدار المعدة، وأشهر أنواعها ليمفوما مالت (MALT Lymphoma) المرتبطة ارتباطاً وثيقاً بعدوى H. pylori المزمنة. والمفاجأة أن بعض حالات ليمفوما مالت تستجيب تماماً للعلاج بالمضادات الحيوية فقط — دون حاجة لجراحة أو كيماوي — إذا شُخِّصت مبكراً وعولجت العدوى البكتيرية.
أورام اللحمة المعدية المعوية (Gastrointestinal Stromal Tumors – GIST)
تنشأ من خلايا كاخال البينية (Interstitial Cells of Cajal) المسؤولة عن تنظيم حركة الجهاز الهضمي. لقد أحدث اكتشاف دور طفرة جين KIT (أو CD117) ثورة في علاج هذا النوع؛ إذ أصبح دواء إيماتينيب (Imatinib) علاجاً موجهاً فعالاً بشكل مذهل. هذه الأورام نادرة نسبياً لكنها تختلف جذرياً عن السرطان الغدي في سلوكها البيولوجي واستجابتها العلاجية.
الأورام العصبية الصماء (Neuroendocrine Tumors – NETs)
تنشأ من خلايا الغدد الصماء العصبية المنتشرة في جدار المعدة. تُعَدُّ نادرة، وتتفاوت بين أورام بطيئة النمو وأخرى شديدة العدوانية. بعضها يفرز هرمونات تسبب أعراضاً مميزة كاحمرار الوجه والإسهال الشديد.
حقيقة طبية مهمة: ليس كل ورم في المعدة خبيثاً. توجد أورام حميدة (Benign) مثل البوليبات المعدية (Gastric Polyps) التي لا تتحول جميعها إلى سرطان. لكن بعض أنواع البوليبات — كالبوليبات الغدية (Adenomatous Polyps) — تحمل خطراً حقيقياً للتحول الخبيث وتحتاج متابعة دورية بالتنظير.
اقرأ أيضاً: الورم الخبيث: دليلك الطبي الشامل لفهم المرض ومواجهته
ما هي أعراض سرطان المعدة المبكرة والغازات — وكيف تفرق بينها وبين مشكلات الهضم العادية؟
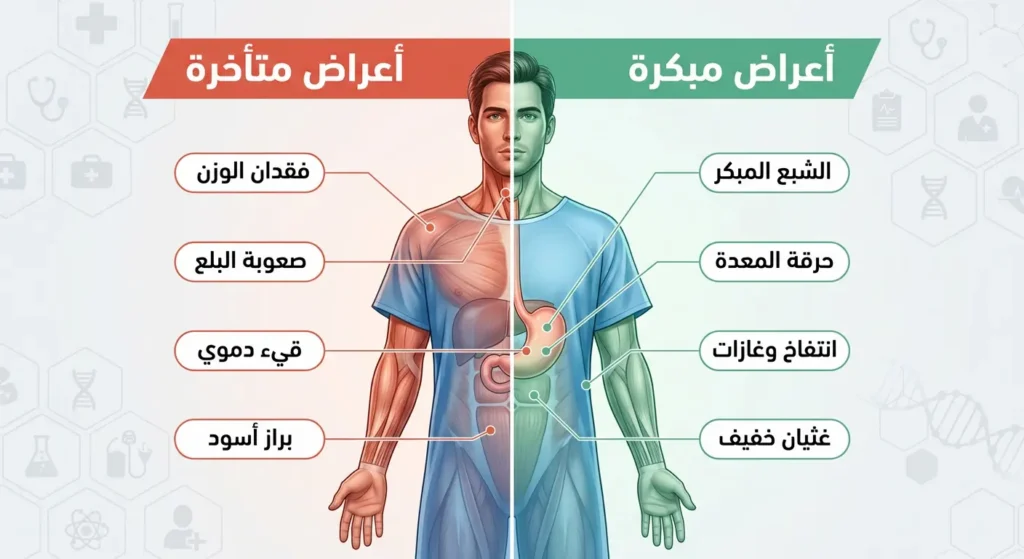
الأعراض المبكرة التي كثيراً ما تُهمَل
هنا تكمن المأساة الحقيقية. أعراض سرطان المعدة في مراحله الأولى تتشابه بشكل محبط مع أعراض عسر الهضم (Dyspepsia) والقرحة المعدية والارتجاع الحمضي. لهذا السبب، يتجاهل كثير من المرضى — خاصة في السعودية والخليج العربي — هذه العلامات لأشهر أو حتى سنوات. ومن أبرز هذه الأعراض المبكرة: شعور بالامتلاء المفرط بعد تناول كمية قليلة من الطعام (الشبع المبكر)، وحرقة معدة متكررة لا تستجيب بشكل كامل لمضادات الحموضة، وانتفاخ وغازات مزمنة بعد الوجبات، وغثيان خفيف متقطع. الفرق بين قرحة المعدة وسرطان المعدة في هذه المرحلة قد لا يتضح إلا بالتنظير.
فقد أثبتت دراسة منشورة في مجلة Gastric Cancer عام 2021 أن أكثر من 40% من مرضى سرطان المعدة في مراحله المبكرة أُخطِئ في تشخيصهم مبدئياً على أنهم يعانون من التهاب معدة مزمن أو ارتجاع مريئي فقط.
الأعراض المتقدمة
عندما يكبر الورم ويتسلل إلى طبقات أعمق من جدار المعدة أو ينتشر إلى أعضاء مجاورة، تظهر أعراض أكثر وضوحاً وإثارة للقلق:
- فقدان وزن غير مبرر وسريع (أكثر من 5% من وزن الجسم خلال 6 أشهر).
- صعوبة في البلع (Dysphagia) خاصة إذا كان الورم في الجزء العلوي من المعدة أو قرب الفؤاد.
- قيء دموي أو قيء يشبه “ثفل القهوة”.
- براز أسود قاتم (Melena) يدل على نزيف هضمي.
- ألم شرسوفي شديد ومتواصل.
- تضخم محسوس في البطن أو استسقاء (Ascites) في الحالات المتقدمة.
متى يجب عليك زيارة طبيب الجهاز الهضمي فوراً؟
تقول الدكتورة تمارا محمدوف، اختصاصية الجهاز الهضمي: “أنصح كل شخص تجاوز الخامسة والأربعين ويعاني من عسر هضم مستمر لأكثر من ثلاثة أسابيع، أو فقدان شهية غير مبرر، أو فقر دم بنقص الحديد دون سبب واضح — بالخضوع لتنظير معدي علوي دون تأخير. الاكتشاف المبكر يصنع فرقاً هائلاً في نسبة الشفاء من سرطان المعدة.”
علامات الخطر الحمراء (Red Flags) التي تستدعي زيارة فورية تشمل: فقدان وزن مفاجئ، نزيف هضمي بأي شكل، صعوبة بلع متصاعدة، كتلة محسوسة في البطن، أو تاريخ عائلي لسرطان المعدة.
اقرأ أيضاً: الدليل الشامل لألم البطن: الأسباب والأعراض وطرق العلاج
صندوق اقتباس طبي — منظمة الصحة العالمية (WHO):
صنفت منظمة الصحة العالمية بكتيريا هيليكوباكتر بيلوري (H. pylori) كمسرطن من المجموعة الأولى (Group 1 Carcinogen) منذ عام 1994، مؤكدةً وجود علاقة سببية مباشرة بينها وبين سرطان المعدة. وتوصي المنظمة بعلاج هذه العدوى في المناطق عالية الانتشار كإستراتيجية للوقاية من سرطان المعدة.
من هو الأكثر عُرضة للإصابة — وما أسباب سرطان المعدة الحقيقية؟
دور جرثومة المعدة (H. pylori) الحاسم
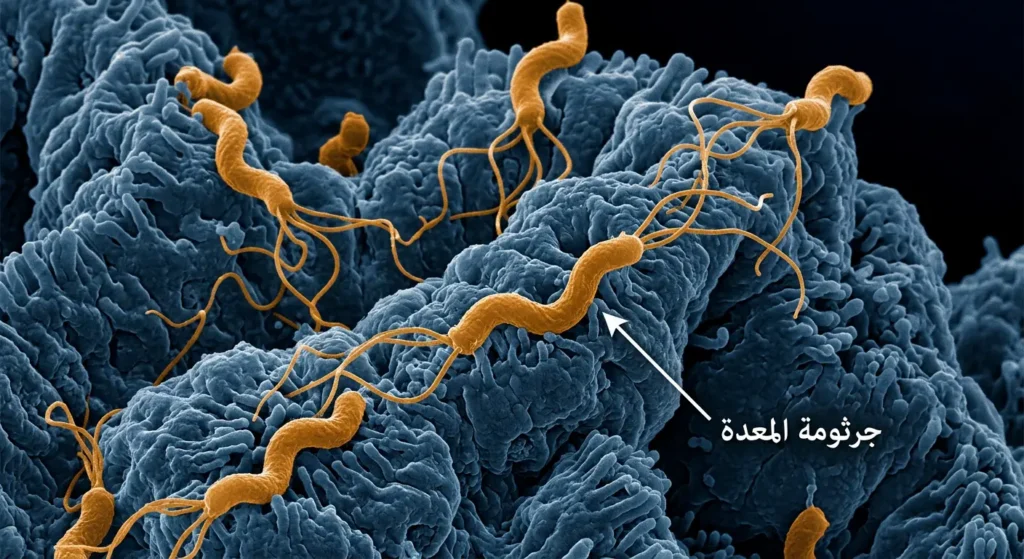
إذا كان لسرطان المعدة “عدو رقم واحد” يمكن مواجهته مبكراً، فهو بلا شك جرثومة المعدة. هذه البكتيريا الحلزونية تستعمر بطانة المعدة لدى نحو نصف سكان الأرض، لكنها لا تسبب السرطان عند الجميع. ما يحدث هو أن الالتهاب المزمن الذي تسببه على مدار سنوات طويلة يُحدث سلسلة من التغيرات النسيجية (الالتهاب الضموري ← الحؤول المعوي ← خلل التنسج ← السرطان). هذا التسلسل يُعرف بـ “شلال كوريا” (Correa Cascade) نسبة إلى العالم الكولومبي بيلايو كوريا الذي وصفه.
في السعودية، تُشير دراسات محلية إلى أن نسبة الإصابة بجرثومة المعدة قد تصل إلى 40-50% في بعض المناطق. وعليه فإن علاج هذه العدوى يُعَدُّ من أهم خطوات الوقاية.
العادات الغذائية: ما تأكله يهم
اللحوم المدخنة والمملحة والمعالجة (كاللانشون والنقانق) تحتوي على مركبات نيتروزامينية (N-nitroso compounds) مسرطنة. كما أن المخللات المحضرة بطرق غير صحية والأطعمة شديدة الملوحة ترتبط بزيادة خطر الإصابة. على النقيض من ذلك، أظهرت الأبحاث أن النظام الغذائي الغني بالخضروات والفواكه الطازجة — وخاصة الحمضيات والخضروات الصليبية كالبروكلي — يوفر حماية ملحوظة.
تقول الدكتورة علا الأحمد، اختصاصية التغذية العلاجية: “النظام الغذائي لمرضى سرطان المعدة أو المعرضين للإصابة يجب أن يركز على تقليل الملح إلى أقل من 5 غرامات يومياً، وزيادة الألياف والخضروات الملونة، وتجنب الأطعمة المشوية على الفحم بشكل متكرر. هذه ليست مجرد نصائح عامة — بل توصيات مبنية على أدلة وبائية قوية.”
اقرأ أيضاً: الأطعمة المسببة للسرطان: ما الذي يختبئ في مطبخك ويهدد صحتك؟
العوامل الوراثية والجينية
بعض الحالات لا تتعلق بالبيئة أو الطعام، بل بالجينات الموروثة. من أبرز هذه المتلازمات الوراثية:
- سرطان المعدة الوراثي المنتشر (Hereditary Diffuse Gastric Cancer – HDGC): يرتبط بطفرة في جين CDH1 الذي يُرمّز بروتين E-cadherin المسؤول عن التصاق الخلايا ببعضها. حاملو هذه الطفرة يواجهون خطراً تراكمياً يصل إلى 70% للإصابة بسرطان المعدة المنتشر خلال حياتهم. لذلك تُقدَّم لهم خيارات جذرية كاستئصال المعدة الوقائي (Prophylactic Gastrectomy).
- متلازمة لينش (Lynch Syndrome): المعروفة أيضاً بسرطان القولون والمستقيم الوراثي غير السليلي (HNPCC)، تزيد خطر سرطانات متعددة بما فيها سرطان المعدة.
- داء البوليبات الغدي العائلي (Familial Adenomatous Polyposis – FAP).
عوامل خطر أخرى لا تتجاهلها
التدخين يُضاعف خطر الإصابة تقريباً مقارنة بغير المدخنين. كذلك السمنة — وخاصة السمنة المركزية (حول البطن) — ترتبط بسرطان الفؤاد تحديداً. ومن الملاحظ أن أصحاب فصيلة الدم A يحملون خطراً أعلى بنسبة 20% تقريباً مقارنة بفصائل الدم الأخرى، وهذه علاقة وبائية لم تُفهم آليتها بالكامل بعد.
لقد أثبتت دراسة واسعة النطاق منشورة في مجلة The Lancet Oncology عام 2020 شملت أكثر من 12 مليون شخص أن الإقلاع عن التدخين يُقلل خطر الإصابة بسرطان المعدة بنسبة تتراوح بين 30-40% خلال عشر سنوات من الإقلاع.
هل تعلم؟ اليابان وكوريا الجنوبية — رغم كونهما من أعلى الدول إصابةً بسرطان المعدة عالمياً — تسجلان أعلى نسب شفاء أيضاً. السبب؟ برامج الفحص الشامل (Mass Screening) التي تُلزم المواطنين فوق سن الأربعين بإجراء تنظير معدي دوري كل عامين. هذا يكتشف الأورام في مراحل مبكرة جداً حيث نسبة الشفاء تتجاوز 90%.
كيف يُشخَّص سرطان المعدة بدقة؟
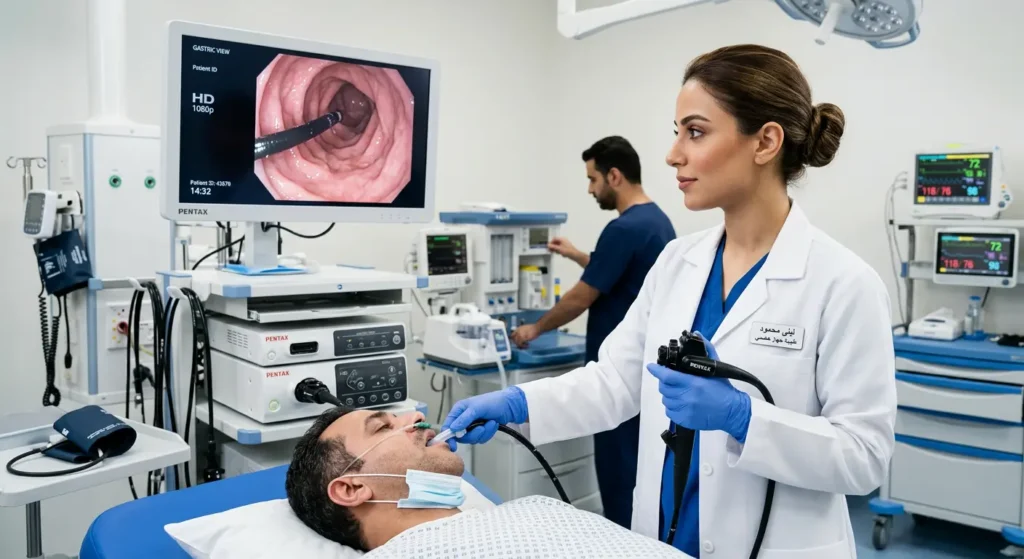
التنظير العلوي (Upper Endoscopy) وأخذ الخزعة
يُعَدُّ التنظير العلوي للجهاز الهضمي (Esophagogastroduodenoscopy – EGD) المعيار الذهبي (Gold Standard) لتشخيص سرطان المعدة. يُدخل الطبيب أنبوباً مرناً مزوداً بكاميرا عبر الفم ليفحص بطانة المريء والمعدة والاثني عشر مباشرة. عند رؤية أي نسيج مشبوه — سواء كان كتلة بارزة أو قرحة غير طبيعية أو تغيراً في لون الغشاء المخاطي — يأخذ الطبيب عينات نسيجية (خزعات) لفحصها تحت المجهر.
التقنيات الحديثة رفعت دقة التنظير بشكل كبير. التنظير بالتكبير (Magnifying Endoscopy) والتصوير ضيق النطاق (Narrow Band Imaging – NBI) يسمحان برؤية التفاصيل الدقيقة لسطح الغشاء المخاطي وأنماط الأوعية الدموية، مما يساعد في تحديد المناطق المشبوهة بدقة أعلى حتى قبل أخذ الخزعة.
الفحوصات التصويرية لتحديد مدى الانتشار
بعد تأكيد التشخيص بالخزعة، يأتي السؤال الحاسم: هل انتشر الورم؟ وإلى أين؟ هنا تدخل عدة فحوصات:
التصوير المقطعي المحوسب (CT Scan) للصدر والبطن والحوض هو الفحص الأول لتقييم مدى الانتشار الموضعي والبعيد. أما التصوير المقطعي بالإصدار البوزيتروني (PET-CT) فيكشف عن بؤر سرطانية نشطة استقلابياً في أنحاء الجسم. كما أن التنظير بالموجات فوق الصوتية (Endoscopic Ultrasound – EUS) يتيح تحديد عمق اختراق الورم لجدار المعدة وتقييم العقد الليمفاوية المجاورة بدقة عالية. بالمقابل، يُجرى تنظير البطن التشخيصي (Diagnostic Laparoscopy) أحياناً قبل الجراحة الكبرى للتأكد من عدم وجود انتشار بريتوني (Peritoneal Carcinomatosis) لا تكشفه الصور الشعاعية.
اقرأ أيضاً: التصوير بالرنين المغناطيسي: ما الذي يحدث داخل الجهاز وكيف تستعد له؟
الاختبارات الجزيئية (Biomarker Testing): مفتاح العلاج الشخصي
هذا القسم تحديداً يميز الطب الحديث عن الطب التقليدي. لم يعد يكفي أن نعرف أن المريض مصاب بسرطان غدي في المعدة؛ بل نحتاج لمعرفة “البصمة الجزيئية” للورم. من أبرز الاختبارات:
اختبار مستقبل HER2 (Human Epidermal Growth Factor Receptor 2): نحو 15-20% من سرطانات المعدة تُفرط في التعبير عن هذا المستقبل. هؤلاء المرضى يستفيدون من العلاج الموجه بعقار تراستوزوماب (Trastuzumab).
اختبار PD-L1 (Programmed Death-Ligand 1): يحدد ما إذا كان المريض مرشحاً للعلاج المناعي بعقاقير مثل بيمبروليزوماب (Pembrolizumab) أو نيفولوماب (Nivolumab).
اختبار عدم استقرار الساتل المجهري (Microsatellite Instability – MSI): الأورام ذات MSI-High تستجيب بشكل ممتاز للعلاج المناعي. كما أن هذا الاختبار قد يكشف عن متلازمة لينش الوراثية.
اختبار Claudin 18.2: هدف علاجي جديد واعد؛ إذ وافقت إدارة الغذاء والدواء الأمريكية (FDA) في عام 2024 على عقار زولبيراكتين (Zolbetuximab) كأول علاج موجه يستهدف هذا البروتين في سرطان المعدة المتقدم إيجابي Claudin 18.2.
صندوق اقتباس طبي — إدارة الغذاء والدواء الأمريكية (FDA):
في يناير 2025، أعلنت إدارة الغذاء والدواء الأمريكية (FDA) عن موافقتها على استخدام عقار زولبيراكتين (Zolbetuximab) بالتزامن مع العلاج الكيميائي لعلاج سرطان المعدة الغدي المتقدم غير القابل للاستئصال أو المنتشر الإيجابي لبروتين Claudin 18.2 والسلبي لـ HER2، مما يمثل نقلة نوعية في العلاج الموجه لهذا المرض.
تقول الدكتورة مها منصور، اختصاصية الأورام والطب النووي: “الاختبارات الجزيئية لم تعد ترفاً إضافياً، بل أصبحت ركيزة أساسية في كل قرار علاجي لسرطان المعدة المتقدم. مريض واحد إيجابي لـ HER2 يحصل على تراستوزوماب قد يعيش أشهراً أطول مقارنة بمريض مماثل لم يُجرَ له الاختبار أصلاً.”
اقرأ أيضاً: البيولوجيا الجزيئية: ما الذي يجعلها أساس فهم الحياة؟
ما مراحل سرطان المعدة وما نسب الشفاء الحقيقية؟
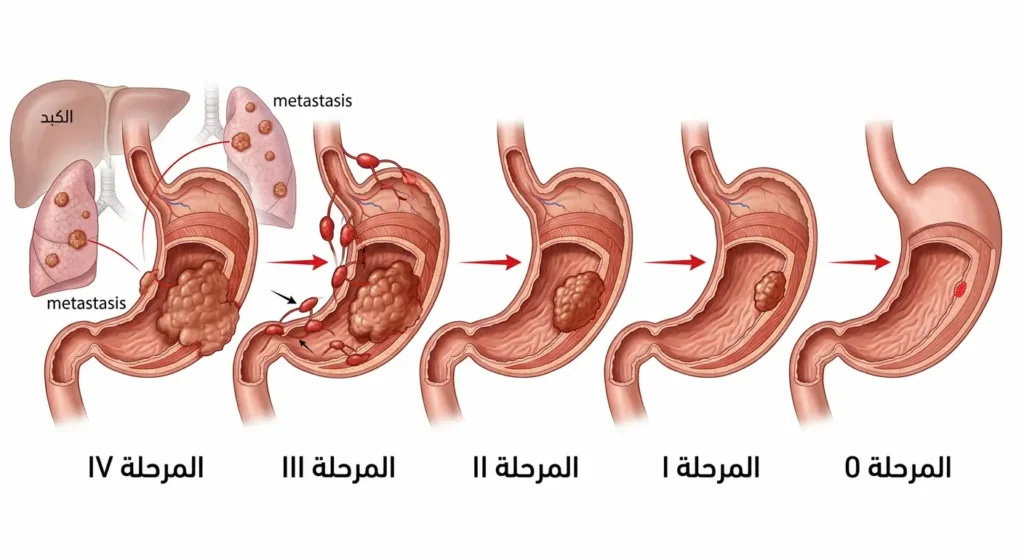
يعتمد أطباء الأورام حول العالم على نظام TNM العالمي الذي وضعته اللجنة الأمريكية المشتركة للسرطان (AJCC) لتصنيف مراحل سرطان المعدة. يرمز الحرف T لحجم الورم وعمق اختراقه لجدار المعدة، وN لمدى إصابة العقد الليمفاوية القريبة، وM لوجود أو غياب انتشار بعيد (Metastasis).
المرحلة صفر (Stage 0): يُعرف بالسرطان الموضعي (Carcinoma in situ). الخلايا السرطانية محصورة في الطبقة السطحية فقط ولم تخترق الغشاء القاعدي. نسبة البقاء على قيد الحياة لمدة 5 سنوات تتجاوز 95%. هذه المرحلة نادراً ما تُشخَّص في العالم العربي لغياب برامج الفحص الدوري.
المرحلة الأولى (Stage I): الورم اخترق الطبقة المخاطية أو تحت المخاطية مع إصابة محدودة (أو بدون إصابة) للعقد الليمفاوية. نسبة البقاء 5 سنوات تتراوح بين 60-80%.
المرحلة الثانية (Stage II): اختراق أعمق لجدار المعدة مع إصابة عدد أكبر من العقد الليمفاوية. نسبة البقاء 5 سنوات نحو 30-50%.
المرحلة الثالثة (Stage III): الورم اخترق كامل جدار المعدة أو انتشر إلى أعضاء مجاورة مع إصابة واسعة للعقد الليمفاوية. نسبة البقاء 5 سنوات تهبط إلى 10-20%.
المرحلة الرابعة (Stage IV): انتشار بعيد إلى أعضاء كالكبد أو الرئتين أو الغشاء البريتوني. نسبة البقاء 5 سنوات لا تتجاوز 5%. لكن هذا الرقم يتحسن تدريجياً مع العلاجات المناعية والموجهة الحديثة.
من المهم جداً التأكيد أن هذه الأرقام إحصائية وتعكس متوسطات عامة. كل مريض فريد، وعوامل كثيرة تؤثر في النتيجة — منها عمر المريض، حالته الصحية العامة، نوع الورم الجزيئي، واستجابته للعلاج.
رقم صادم: وفقاً لبيانات المعهد الوطني للسرطان الأمريكي (NCI)، لا يُشخَّص سوى 30% تقريباً من حالات سرطان المعدة في الولايات المتحدة في مراحل موضعية مبكرة. الأغلبية تُكتشف بعد انتشار المرض إلى العقد الليمفاوية أو أعضاء بعيدة. وفي العالم العربي، النسبة أسوأ.
ما أحدث طرق علاج سرطان المعدة؟

التدخل الجراحي: الأمل الأول في الشفاء
الجراحة تظل الركيزة الأساسية لعلاج سرطان المعدة القابل للاستئصال. ويعتمد نوع الجراحة على موقع الورم وحجمه ومرحلته:
الاستئصال بالتنظير (Endoscopic Resection): للأورام المبكرة جداً (المحصورة في الطبقة المخاطية) يمكن إزالتها عبر التنظير دون فتح البطن. تقنية التسليخ تحت المخاطي بالتنظير (Endoscopic Submucosal Dissection – ESD) أصبحت معياراً علاجياً في اليابان وكوريا الجنوبية وبدأت تنتشر في مراكز متخصصة حول العالم.
الاستئصال الجزئي للمعدة (Subtotal/Distal Gastrectomy): يُجرى عندما يقع الورم في الجزء السفلي من المعدة (الغار أو البواب). يُستأصل الجزء المصاب مع هامش أمان من النسيج السليم.
الاستئصال الكلي للمعدة (Total Gastrectomy): ضروري عندما يقع الورم في الجسم أو القاع أو عندما يكون منتشراً. يُوصل المريء مباشرة بـالأمعاء الدقيقة. ورغم قسوة هذا الإجراء، يمكن للمريض أن يعيش حياة طبيعية نسبياً مع تعديلات غذائية مهمة.
في جميع أنواع الجراحة، يُجرى استئصال العقد الليمفاوية (Lymphadenectomy). المعيار الحالي هو استئصال D2 — أي إزالة مجموعتين من العقد الليمفاوية المحيطة بالمعدة — وهو ما أثبتت الدراسات أنه يحسن نسب البقاء بشكل ملحوظ مقارنة بالاستئصال المحدود D1.
العلاج الكيميائي: قبل الجراحة وبعدها
العلاج الكيميائي المحيط بالجراحة (Perioperative Chemotherapy) أصبح النهج المعياري في أوروبا وأمريكا. بروتوكول FLOT (يتضمن أدوية Fluorouracil, Leucovorin, Oxaliplatin, Docetaxel) هو البروتوكول الأكثر استخداماً حالياً. يُعطى 4 دورات قبل الجراحة لتقليص الورم وزيادة فرص الاستئصال الكامل، ثم 4 دورات بعدها للقضاء على أي خلايا متبقية.
لقد أثبتت دراسة FLOT4 الألمانية المنشورة في مجلة The Lancet عام 2019 أن هذا البروتوكول رفع معدل البقاء الإجمالي إلى 50 شهراً مقارنة بـ 35 شهراً للبروتوكول القديم ECF/ECX.
العلاج الإشعاعي: متى يُستخدم؟
العلاج الإشعاعي ليس خط العلاج الأول في سرطان المعدة كما هو الحال في بعض السرطانات الأخرى. لكنه يُستخدم في سياقات محددة: بعد الجراحة بالتزامن مع الكيماوي (العلاج الكيميائي الإشعاعي المساعد – Adjuvant Chemoradiation) خاصة عند عدم استئصال عقد ليمفاوية كافية، أو كعلاج تلطيفي (Palliative) لتخفيف الألم أو وقف النزيف في الحالات المتقدمة.
العلاجات الموجهة (Targeted Therapy): ضربات دقيقة
على عكس العلاج الكيميائي الذي يستهدف جميع الخلايا سريعة الانقسام، تعمل العلاجات الموجهة على أهداف جزيئية محددة في الخلية السرطانية:
تراستوزوماب (Trastuzumab): يستهدف مستقبل HER2 على سطح الخلية السرطانية. يُعطى بالتزامن مع الكيماوي في المرحلة الأولى من علاج سرطان المعدة المتقدم إيجابي HER2. دراسة ToGA الشهيرة أثبتت أنه يزيد البقاء الإجمالي بنحو 2.7 شهر.
تراستوزوماب ديروكستيكان (Trastuzumab Deruxtecan – T-DXd): جيل جديد من الأجسام المضادة المقترنة بالدواء (Antibody-Drug Conjugates – ADC). أحدث ثورة لأنه فعال حتى في الأورام ذات التعبير المنخفض عن HER2 (HER2-low). دراسة DESTINY-Gastric02 أكدت فعاليته كخط علاجي ثانٍ.
زولبيراكتين (Zolbetuximab): يستهدف بروتين Claudin 18.2 الموجود على سطح نحو 38% من سرطانات المعدة الغدية. حصل على موافقة FDA عام 2025 بعد نتائج دراستي SPOTLIGHT وGLOW الإيجابية.
راموسيروماب (Ramucirumab): يستهدف مستقبل عامل نمو بطانة الأوعية الدموية (VEGFR2)، فيقطع إمدادات الدم عن الورم.
العلاج المناعي (Immunotherapy): تسليح خلايا الجسم لمحاربة السرطان
فكرة العلاج المناعي بسيطة وعبقرية في آن واحد: الخلايا السرطانية تملك “أقنعة” تخدع بها الجهاز المناعي لكي لا يهاجمها. العلاج المناعي ينزع هذه الأقنعة ويُطلق يد الخلايا المناعية لتفعل ما خُلقت لأجله.
بيمبروليزوماب (Pembrolizumab – Keytruda): مثبط لنقطة التفتيش المناعية PD-1. أصبح جزءاً من العلاج الأولي لسرطان المعدة المتقدم إيجابي PD-L1 بالتزامن مع الكيماوي. دراسة KEYNOTE-859 المنشورة عام 2023 أثبتت تحسناً ملحوظاً في البقاء الإجمالي.
نيفولوماب (Nivolumab – Opdivo): حصل على موافقات متعددة لعلاج سرطان المعدة المتقدم. دراسة CheckMate 649 الضخمة — التي شملت أكثر من 2,000 مريض — أظهرت أن إضافة نيفولوماب للكيماوي في الخط الأول حسّنت البقاء الإجمالي بشكل ذي دلالة إحصائية، خاصة في المرضى ذوي CPS ≥ 5.
كما أن نيفولوماب أظهر نتائج واعدة في الإعداد المساعد (Adjuvant) بعد الجراحة. دراسة CheckMate 577 (وإن كانت أُجريت على سرطان المريء والموصل المعدي المريئي) فتحت الباب لدراسات مماثلة في سرطان المعدة.
تصريح متخصص:
البروفيسور تشارلز فوكس (Charles S. Fuchs)، مدير مركز ييل للسرطان (Yale Cancer Center) وأستاذ الطب الباطني في كلية الطب بجامعة ييل، والباحث الرئيس في عدة دراسات محورية حول سرطان المعدة:“العلاج المناعي غيّر قواعد اللعبة في سرطان المعدة المتقدم. للمرة الأولى، نرى مرضى في المرحلة الرابعة يحققون استجابات مستمرة تتجاوز السنتين — وهو أمر كان مستحيلاً قبل عقد واحد فقط. لكن التحدي الأكبر يظل في تحديد المرضى الذين سيستفيدون فعلاً من هذا العلاج عبر مؤشرات حيوية أكثر دقة.”
معلومة قد تفاجئك: علاج سرطان المعدة المتقدم تطور بشكل مذهل خلال خمس سنوات فقط. في عام 2019، كان الخيار العلاجي للخط الأول هو الكيماوي وحده. اليوم في 2025، أصبح الخط الأول يشمل الكيماوي + العلاج المناعي + العلاج الموجه (في حالة HER2+ أو Claudin 18.2+) — مما ضاعف معدلات الاستجابة تقريباً.
اقرأ أيضاً: علاج السرطان: التقنيات الحديثة والابتكارات المستقبلية
كيف تبدو الحياة بعد تشخيص وعلاج سرطان المعدة؟

النظام الغذائي بعد استئصال المعدة: التأقلم مع واقع جديد
بعد استئصال المعدة الجزئي أو الكلي، يواجه المريض تحديات غذائية حقيقية. أبرزها ما يُعرف بمتلازمة الإغراق (Dumping Syndrome) التي تحدث عندما يمر الطعام — وخاصة السكريات — بسرعة كبيرة من المعدة (أو ما تبقى منها) إلى الأمعاء الدقيقة. تظهر بعد 15-30 دقيقة من الأكل على شكل غثيان، تعرق، دوار، إسهال، وتسارع في ضربات القلب.
النصائح الغذائية الأساسية تشمل: تناول 6-8 وجبات صغيرة يومياً بدلاً من 3 وجبات كبيرة، ومضغ الطعام ببطء شديد، وتجنب السوائل أثناء الأكل (شربها قبل أو بعد الوجبة بـ 30 دقيقة)، وتقليل السكريات البسيطة، وزيادة البروتين. كما يحتاج المريض بعد الاستئصال الكلي إلى حقن فيتامين B12 مدى الحياة لأن المعدة هي المصدر الوحيد للعامل الداخلي (Intrinsic Factor) الضروري لامتصاص هذا الفيتامين. ومتابعة مستويات الحديد والكالسيوم ضرورية أيضاً.
اقرأ أيضاً: تغذية مريض السرطان: الدليل الطبي الشامل للمسموح والممنوع
الدعم النفسي: الجانب المنسي في رحلة العلاج
لا أبالغ حين أقول إن التشخيص بسرطان المعدة يُحدث زلزالاً نفسياً لا يقل قسوة عن المرض ذاته. القلق من المستقبل، الاكتئاب، اضطرابات النوم، صعوبة التكيف مع تغيرات الجسم والنظام الغذائي — كلها تحديات حقيقية يعيشها المريض يومياً.
في الواقع العربي، لا يزال كثيرون يتحرجون من طلب الدعم النفسي. لكن الدراسات أثبتت أن المرضى الذين يتلقون دعماً نفسياً متخصصاً بالتوازي مع العلاج الطبي يحققون نتائج أفضل في نوعية الحياة وربما في الاستجابة العلاجية أيضاً. مجموعات الدعم — سواء الحضورية أو عبر الإنترنت — توفر مساحة آمنة لتبادل الخبرات بين المرضى وذويهم.
مثال تطبيقي من الواقع:
أبو خالد، رجل سعودي في الثانية والخمسين من عمره، راجع طبيب الباطنية يشكو من حرقة معدة مستمرة لستة أشهر وفقدان في الشهية. وصف له الطبيب مضادات حموضة لمدة شهرين. لم تتحسن الأعراض، فأُحيل لأخصائي جهاز هضمي أجرى تنظيراً علوياً كشف عن قرحة مشبوهة في غار المعدة. الخزعة أكدت وجود سرطان غدي في المرحلة الثانية. تلقى أبو خالد 4 دورات كيماوي (بروتوكول FLOT) قبل الجراحة، ثم أُجري له استئصال جزئي للمعدة مع تنظيف العقد الليمفاوية D2، تلتها 4 دورات كيماوي إضافية. اليوم، بعد ثلاث سنوات، أبو خالد بصحة جيدة ويتابع بانتظام كل 6 أشهر. قصته تؤكد أن الإصرار على التشخيص الدقيق وعدم الاكتفاء بمضادات الحموضة قد يصنع الفارق بين الحياة والموت.
تصريح متخصص:
البروفيسور إريك فان كوتسم (Eric Van Cutsem)، أستاذ أمراض الجهاز الهضمي والأورام في جامعة لوفان الكاثوليكية (KU Leuven) في بلجيكا، وأحد أبرز الباحثين الأوروبيين في سرطان الجهاز الهضمي:“نحن ندخل عصراً جديداً في علاج سرطان المعدة. الجمع بين العلاج المناعي والموجه والكيميائي — ما نسميه العلاج الثلاثي المركب — أعطى نتائج لم نكن نحلم بها قبل عقد. لكنني أؤكد دائماً أن أفضل علاج هو الاكتشاف المبكر؛ فلا يوجد دواء في العالم يضاهي قوة التشخيص في المرحلة الأولى.”
هل يمكن الوقاية من سرطان المعدة فعلاً؟

السؤال الأهم الذي يطرحه كل قارئ بعد كل هذه المعلومات: هل أستطيع حماية نفسي؟ الجواب: نعم، جزئياً. لا يمكن القضاء على الخطر بالكامل، لكن يمكن تقليله بشكل كبير.
الخطوة الأولى والأهم هي اختبار وعلاج جرثومة المعدة (H. pylori). إذا كنت تعاني من أعراض هضمية مزمنة أو لديك تاريخ عائلي لسرطان المعدة، فاطلب من طبيبك إجراء اختبار التنفس أو اختبار مستضد البراز. العلاج الثلاثي أو الرباعي بالمضادات الحيوية فعال في القضاء على البكتيريا في أكثر من 80% من الحالات.
من ناحية أخرى، الإقلاع عن التدخين أمر محوري. فقد أكدت جمعية السرطان الأمريكية (ACS) أن المدخنين يواجهون ضعف خطر الإصابة بسرطان المعدة مقارنة بغير المدخنين.
تعديل النظام الغذائي يُحدث فرقاً حقيقياً: قلّل من اللحوم المعالجة والمملحة، أكثِر من الخضروات والفواكه الطازجة، واستبدل الشواء على الفحم بطرق طهي أقل ضرراً. كذلك الحفاظ على وزن صحي ومؤشر كتلة جسم طبيعي يقلل خطر سرطان الفؤاد تحديداً.
بالنسبة لأصحاب التاريخ العائلي القوي أو حاملي الطفرات الجينية (مثل CDH1)، فإن المتابعة المكثفة بالتنظير الدوري أو حتى الاستئصال الوقائي للمعدة قد يكون الخيار الأنسب — وهذا قرار يُتخذ بالتشاور مع فريق متعدد التخصصات يشمل طبيب أورام، جراح، مستشار جيني، واختصاصي تغذية.
المستشار الدوائي جاسم محمد مراد يضيف: “أنصح كل من يتناول مثبطات مضخة البروتون (PPIs) كالأوميبرازول لفترات طويلة تتجاوز 8 أسابيع بمراجعة طبيبه، ليس فقط لتقييم الحاجة لاستمرار الدواء، بل أيضاً لمناقشة ضرورة إجراء تنظير تشخيصي، خاصة عند وجود أعراض مقلقة كفقدان الوزن أو فقر الدم.”
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
تصريح متخصص:
البروفيسور بيتر كورنيليوس ثيس (Peter C. Thuss-Patience)، رئيس قسم أمراض الدم والأورام في مستشفى شاريتيه الجامعي (Charité – Universitätsmedizin Berlin) في برلين، ألمانيا، والباحث الرئيس في عدة تجارب سريرية متعلقة بسرطان المعدة:“الوقاية من سرطان المعدة تبدأ من الوعي. في ألمانيا، ندعو لفحص جرثومة المعدة وعلاجها كإستراتيجية سكانية شاملة. كل يورو يُنفق على برنامج استئصال H. pylori يوفر عشرات اليورويات من تكاليف علاج السرطان المتقدم لاحقاً.”
حقيقة ختامية: في السعودية، يحتل سرطان المعدة المرتبة السابعة تقريباً بين أكثر السرطانات شيوعاً وفقاً للسجل الوطني السعودي للأورام (SCR). ورغم أن معدلات الإصابة أقل مقارنة بدول شرق آسيا، فإن أغلب الحالات تُشخَّص في مراحل متقدمة — وهذا ما يجب أن يتغير.
اقرأ أيضاً: سرطان الثدي: دليلك الشامل من التشخيص إلى التعافي
📑 بروتوكولات طبية رسمية حديثة
- إرشادات NCCN (النسخة 2.2024): توصي بإضافة العلاج المناعي (نيفولوماب أو بيمبروليزوماب) إلى الكيماوي كخط أول في سرطان المعدة المتقدم إيجابي PD-L1. — المصدر
- إرشادات ESMO (الجمعية الأوروبية لطب الأورام – 2024): توصي ببروتوكول FLOT كمعيار للكيماوي المحيط بالجراحة في سرطان المعدة القابل للاستئصال. — المصدر
- إرشادات وزارة الصحة السعودية: تنصح بإجراء فحص جرثومة المعدة وعلاجها لدى الأفراد ذوي التاريخ العائلي لسرطان المعدة أو الأعراض الهضمية المزمنة. — المصدر
- توصيات الهيئة الوطنية للصحة والرعاية في الإمارات (MOHAP): تدعو إلى رفع الوعي بأعراض سرطان المعدة المبكرة وإدراج التنظير المعدي ضمن برامج الكشف للمجموعات عالية الخطورة. — المصدر
أسئلة شائعة حول سرطان المعدة
الخاتمة
سرطان المعدة عدو صامت لكنه ليس لا يُقهر. لقد استعرضنا في هذا المقال كيف تبدأ الخلية السرطانية رحلتها في بطانة المعدة، وما الأنواع المختلفة لهذا المرض، وكيف تتدرج أعراضه من إشارات خفية قد تُهمل إلى علامات صريحة تستدعي تدخلاً فورياً. تعرفنا على أسباب سرطان المعدة وعوامل الخطر — من جرثومة المعدة إلى العوامل الوراثية والغذائية — وعلى أدوات التشخيص الدقيقة التي تشمل التنظير والاختبارات الجزيئية. واستعرضنا الترسانة العلاجية الحديثة التي تتضمن الجراحة والكيماوي والعلاج الموجه والمناعي. كما ناقشنا تحديات الحياة بعد العلاج وخطوات الوقاية العملية.
الرسالة الأهم التي أريدك أن تحملها من هذا المقال: لا تتجاهل أعراضك الهضمية المزمنة. حرقة المعدة التي لا تستجيب للعلاج، فقدان الشهية غير المبرر، نقصان الوزن — كلها إشارات تستحق تنظيراً معدياً وليس مجرد وصفة مضادات حموضة.
شارك هذا المقال مع من تحب — فربما كلمة واعية تصل في الوقت المناسب تنقذ حياة.
هل أجريت فحصاً لجرثومة المعدة من قبل؟ إن لم تكن فعلت، فربما حان الوقت لتطلب من طبيبك هذا الاختبار البسيط الذي قد يقيك من مرض خطير.
اقرأ أيضاً: سرطان البروستاتا — هل كل تضخم يعني الإصابة وما أحدث طرق العلاج؟
اقرأ أيضاً: سرطان المريء (Esophageal Cancer): ما أعراضه المبكرة وكيف يُعالَج؟
⚠️ تحذير وإخلاء مسؤولية
جميع المعلومات الواردة في هذا المقال على موقع خلية مُعَدّة لأغراض التثقيف الصحي والتوعية العامة فقط، ولا تُغني بأي شكل من الأشكال عن استشارة الطبيب المختص أو أخصائي الرعاية الصحية المؤهل. لا يجوز استخدام محتوى هذا المقال لتشخيص أي حالة مرضية أو اتخاذ قرارات علاجية دون إشراف طبي مباشر. كل حالة صحية فريدة وتتطلب تقييماً سريرياً فردياً. موقع خلية وكتّابه لا يتحملون أي مسؤولية عن أي ضرر ناتج عن سوء استخدام المعلومات المنشورة.
إذا كنت تعاني من أعراض صحية مقلقة، يُرجى التوجه إلى أقرب مرفق صحي أو الاتصال بخط الطوارئ فوراً.
هذا المقال أُعِدّ بواسطة فريق المحتوى الطبي في موقع خلية، وراجعته الدكتورة مها منصور (اختصاصية الأورام والطب النووي) والدكتورة تمارا محمدوف (اختصاصية الجهاز الهضمي). جرت مراجعة نهائية من قبل هيئة التحرير العلمية في الموقع.
المصادر المعتمدة: استندت المعلومات إلى دراسات وأوراق بحثية مُحكّمة منشورة في مجلات طبية مرموقة (The Lancet, NEJM, Annals of Oncology)، وإرشادات رسمية من NCCN وESMO وFDA وWHO، وكتب طبية مرجعية معتمدة.
آخر تحديث: يوليو 2025 | جميع الروابط الخارجية تم التحقق منها وقت النشر.
المصادر والمراجع
الدراسات والأوراق البحثية
- Janjigian, Y. Y., et al. (2021). First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649). The Lancet, 398(10294), 27-40.
doi:10.1016/S0140-6736(21)00797-2
دراسة محورية أثبتت تفوق إضافة نيفولوماب للكيماوي كخط أول في سرطان المعدة المتقدم. - Al-Batran, S. E., et al. (2019). Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4). The Lancet, 393(10184), 1948-1957.
doi:10.1016/S0140-6736(19)30952-8
أسست لبروتوكول FLOT كمعيار علاجي في الكيماوي المحيط بالجراحة. - Shitara, K., et al. (2023). Pembrolizumab plus chemotherapy versus chemotherapy as first-line therapy for HER2-negative advanced gastric or gastro-oesophageal junction cancer: Phase 3 KEYNOTE-859 study. Annals of Oncology, 34(Suppl 2), S1316.
doi:10.1016/j.annonc.2023.10.064
دراسة أثبتت فعالية بيمبروليزوماب مع الكيماوي في الخط الأول. - Shitara, K., et al. (2023). Zolbetuximab plus mFOLFOX6 in patients with CLDN18.2-positive, HER2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (SPOTLIGHT). The Lancet, 401(10389), 1655-1668.
doi:10.1016/S0140-6736(23)00620-7
دراسة أسست لزولبيراكتين كعلاج موجه جديد يستهدف Claudin 18.2. - Ford, A. C., et al. (2020). Helicobacter pylori eradication therapy to prevent gastric cancer: systematic review and meta-analysis. Gut, 69(12), 2113-2121.
doi:10.1136/gutjnl-2020-320839
مراجعة منهجية أكدت أن استئصال جرثومة المعدة يقلل خطر سرطان المعدة. - Shitara, K., et al. (2020). Trastuzumab deruxtecan in previously treated HER2-positive gastric cancer. New England Journal of Medicine, 382(25), 2419-2430.
doi:10.1056/NEJMoa2004413
دراسة DESTINY-Gastric01 التي أثبتت فعالية T-DXd في سرطان المعدة إيجابي HER2.
الجهات الرسمية والمنظمات
- World Health Organization (WHO). (2024). Helicobacter pylori Fact Sheet.
https://www.who.int/news-room/fact-sheets/detail/helicobacter-pylori
معلومات رسمية عن تصنيف جرثومة المعدة كمسرطن. - International Agency for Research on Cancer (IARC/WHO). (2024). Global Cancer Observatory: Stomach Cancer Factsheet.
https://gco.iarc.who.int/today/data/factsheets/cancers/7-Stomach-fact-sheet.pdf
إحصائيات عالمية محدثة عن سرطان المعدة. - National Cancer Institute (NCI/NIH). (2024). Gastric Cancer Treatment (PDQ).
https://www.cancer.gov/types/stomach/hp/stomach-treatment-pdq
بروتوكولات العلاج المعتمدة من المعهد الوطني للسرطان. - U.S. Food and Drug Administration (FDA). (2024). FDA Approves Zolbetuximab.
https://www.fda.gov/drugs/resources-information-approved-drugs
إعلان الموافقة على زولبيراكتين لعلاج سرطان المعدة. - National Comprehensive Cancer Network (NCCN). (2024). NCCN Clinical Practice Guidelines in Oncology: Gastric Cancer (Version 2.2024).
https://www.nccn.org/professionals/physician_gls/pdf/gastric.pdf
الإرشادات السريرية الأكثر استخداماً عالمياً في علاج سرطان المعدة.
الكتب والموسوعات العلمية
- DeVita, V. T., Lawrence, T. S., & Rosenberg, S. A. (2023). DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (12th ed.). Wolters Kluwer.
المرجع الأشمل في طب الأورام، يتضمن فصولاً مفصلة عن سرطان المعدة. - Feldman, M., Friedman, L. S., & Brandt, L. J. (2021). Sleisenger and Fordtran’s Gastrointestinal and Liver Disease (11th ed.). Elsevier.
الكتاب المرجعي الأول في أمراض الجهاز الهضمي، يغطي سرطان المعدة من منظور تشخيصي وعلاجي. - Ajani, J. A., et al. (2022). Gastric Cancer (MD Anderson Cancer Care Series). Springer.
كتاب متخصص حصرياً في سرطان المعدة صادر عن مركز MD Anderson العريق.
مقالات علمية مبسطة
- Thrift, A. P., & El-Serag, H. B. (2020). Burden of Gastric Cancer. Clinical Gastroenterology and Hepatology, 18(3), 534-542.
doi:10.1016/j.cgh.2019.07.045
مقالة مراجعة شاملة عن عبء سرطان المعدة عالمياً، مكتوبة بأسلوب مبسط نسبياً.
قراءات إضافية ومصادر للتوسع
- Smyth, E. C., et al. (2020). Gastric cancer. The Lancet, 396(10251), 635-648.
doi:10.1016/S0140-6736(20)31288-5
لماذا نقترح عليك قراءته؟ هذه مراجعة شاملة (Seminar) من مجلة The Lancet تغطي سرطان المعدة من الألف إلى الياء — من الوبائيات إلى أحدث العلاجات — وتُعَدُّ من أكثر المراجعات استشهاداً في المجال. - Lauren, P. (1965). The two histological main types of gastric carcinoma. Acta Pathologica et Microbiologica Scandinavica, 64, 31-49.
لماذا نقترح عليك قراءته؟ هذه الورقة الكلاسيكية هي أساس تصنيف لورين لسرطان المعدة الغدي (النمط المعوي مقابل المنتشر) الذي لا يزال مستخدماً حتى اليوم. فهم هذا التصنيف أساسي لأي طالب أو باحث في المجال. - Cancer Genome Atlas Research Network. (2014). Comprehensive molecular characterization of gastric adenocarcinoma. Nature, 513(7517), 202-209.
doi:10.1038/nature13480
لماذا نقترح عليك قراءته؟ هذه الدراسة الجينومية الضخمة صنّفت سرطان المعدة إلى أربعة أنماط جزيئية فرعية (EBV, MSI, GS, CIN)، مما أحدث ثورة في فهم البيولوجيا الجزيئية للمرض ومهّد لعصر العلاج الشخصي.
إذا وجدت هذا المقال مفيداً، ندعوك لمشاركته مع أصدقائك وعائلتك عبر وسائل التواصل الاجتماعي. المعرفة الطبية الصحيحة هي خط الدفاع الأول ضد السرطان. وإن كنت تعاني من أي أعراض هضمية مزعجة ومستمرة، لا تتردد في حجز موعد مع طبيب جهاز هضمي متخصص — فالفحص المبكر قد يصنع كل الفارق.
إخلاء مسؤولية: هذا المقال مُعَد لأغراض تثقيفية وتوعوية فقط ولا يُغني عن الاستشارة الطبية المتخصصة. جميع المعلومات الواردة مبنية على مصادر علمية موثقة ومراجعة من قبل متخصصين، لكن كل حالة طبية فريدة وتتطلب تقييماً فردياً من الطبيب المعالج.
جرت مراجعة هذا المقال من قبل هيئة التحرير العلمية في موقعنا لضمان الدقة والمعلومة الصحيحة.







