سرطان البروستاتا — هل كل تضخم يعني الإصابة وما أحدث طرق العلاج؟
كيف تكتشفه مبكراً وما فرص الشفاء الحقيقية؟

سرطان البروستاتا هو نمو خبيث يبدأ في خلايا غدة البروستاتا (Prostate Gland) لدى الرجال. يُعَدُّ ثاني أكثر السرطانات شيوعاً بين الذكور عالمياً. يتميز ببطء نموه في أغلب الحالات، وترتفع نسب الشفاء منه إلى 99% عند اكتشافه في مراحله الأولى. يعتمد التشخيص على تحليل PSA والخزعة، بينما تتنوع خيارات العلاج بين المراقبة والجراحة والعلاج الإشعاعي والهرموني.
تمت المراجعة والتدقيق بواسطة الهيئة الطبية:

اختصاصية الأورام والطب النووي

اختصاصي جراحة مسالك بولية

اختصاصية تغذية علاجية

خبير الرقابة الدوائية
MEDICAL REVIEW
خلية — 2026
- نسبة البقاء لـ 5 سنوات تتجاوز 99% في المراحل المبكرة.
- أغلب الأورام المكتشفة مبكراً بطيئة النمو وقد لا تحتاج علاجاً فورياً.
- حتى المرحلة الرابعة أصبحت قابلة للسيطرة لسنوات طويلة.
- ابدأ فحص PSA السنوي عند سن 50 (أو 45 إن وُجد تاريخ عائلي).
- ركّز على نظام غذائي غني بالطماطم المطبوخة والخضراوات الصليبية.
- لا تتجاهل أعراض: الدم في البول، ألم العظام المزمن، ضعف التبول.
- سرطان البروستاتا لا يعطي أعراضاً مبكرة — الفحص الدوري هو طوق النجاة.
- ارتفاع PSA لا يعني بالضرورة سرطاناً — لكنه يستدعي تقييماً طبياً.
- تضخم البروستاتا الحميد ليس سرطاناً ولا يتحول إليه بالضرورة.
هل لاحظت يوماً أنك تستيقظ مرتين أو ثلاثاً في الليل للتبول؟ هل شعرت بضعف في تدفق البول وتجاهلت الأمر ظناً منك أنه “شيء طبيعي مع التقدم في العمر”؟ أنت لست وحدك. آلاف الرجال في المنطقة العربية يؤجلون زيارة الطبيب خجلاً أو خوفاً من سماع كلمة “سرطان”. لكن الحقيقة التي ستطمئنك هي أن سرطان البروستاتا — رغم انتشاره — يُعَدُّ من أكثر السرطانات قابلية للعلاج والشفاء التام إذا اكتُشف مبكراً. هذا المقال يضع بين يديك كل ما تحتاج معرفته: من التشخيص إلى العلاج، بلغة واضحة وأرقام حقيقية ونصائح عملية من أطباء مختصين.
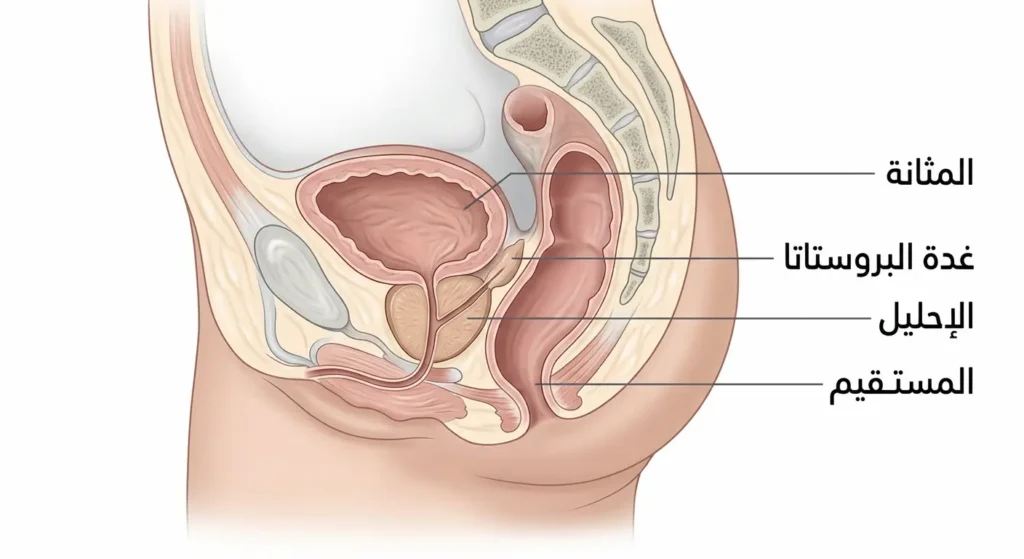
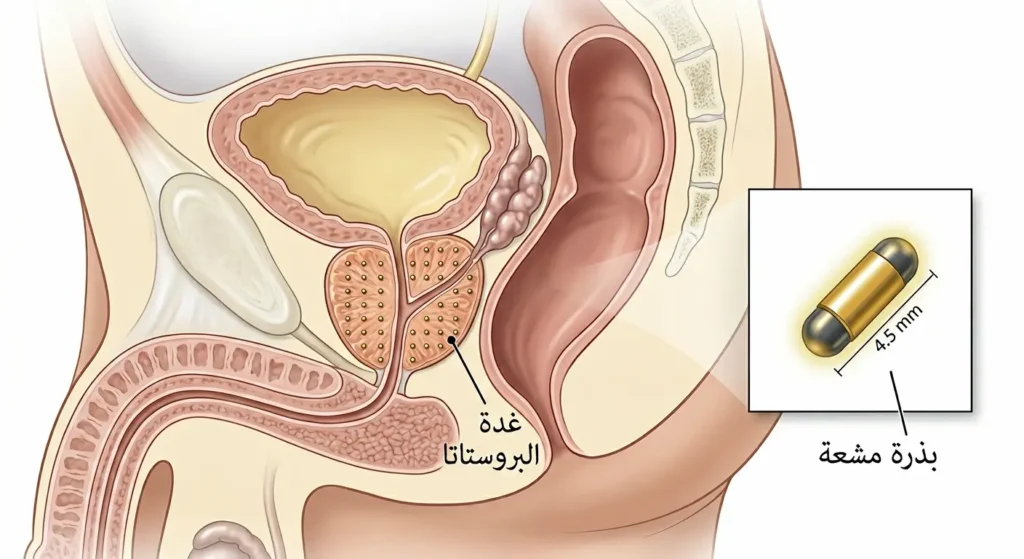
لنبدأ بنبذة تشريحية سريعة. غدة البروستاتا هي غدة صغيرة بحجم حبة الجوز تقع أسفل المثانة مباشرة وأمام المستقيم. تحيط بالإحليل (Urethra) — وهو الأنبوب الذي ينقل البول من المثانة إلى خارج الجسم. وظيفتها الرئيسة هي إنتاج جزء من السائل المنوي الذي يغذي الحيوانات المنوية ويحميها. ولأنها تحيط بالإحليل، فإن أي تضخم أو ورم فيها قد يؤثر مباشرة على التبول والوظيفة الجنسية.
هل كل تضخم في البروستاتا يعني السرطان؟
الفرق بين تضخم البروستاتا الحميد (BPH) وسرطان البروستاتا
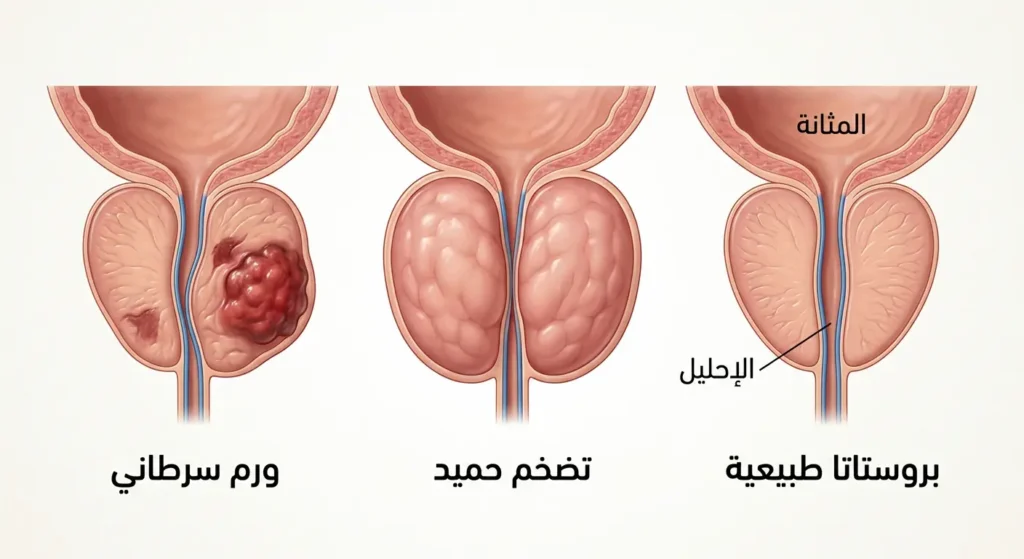
هذا السؤال يطرحه تقريباً كل رجل تجاوز الخمسين. والإجابة المطمئنة هي: لا، بالتأكيد لا. تضخم البروستاتا الحميد (Benign Prostatic Hyperplasia – BPH) حالة شائعة جداً تصيب نحو 50% من الرجال فوق سن الستين، وهي ببساطة زيادة في حجم الغدة دون وجود خلايا سرطانية. على النقيض من ذلك، سرطان البروستاتا ينشأ عندما تبدأ خلايا الغدة بالانقسام بشكل غير طبيعي وخارج عن السيطرة.
الفرق الجوهري يكمن في طبيعة الخلايا ذاتها. في التضخم الحميد، الخلايا طبيعية لكنها تتكاثر أكثر من اللازم فتضغط على الإحليل. أما في سرطان البروستاتا، فالخلايا تكون متحولة وقادرة على غزو الأنسجة المجاورة والانتشار إلى أعضاء أخرى. ومن المهم التأكيد أن وجود تضخم حميد لا يزيد بالضرورة من خطر الإصابة بسرطان البروستاتا، لكنهما قد يتواجدان معاً في الوقت ذاته.
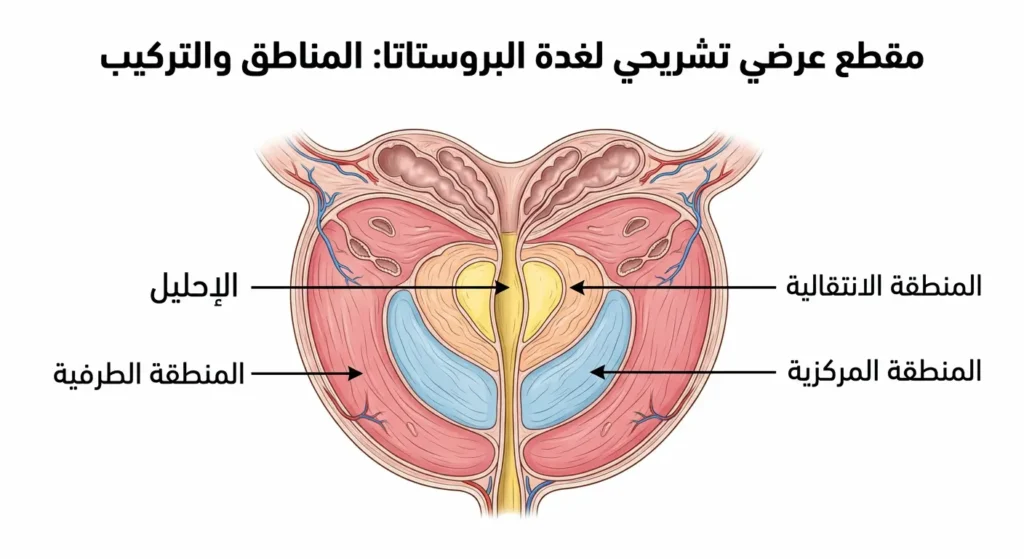
أثبتت دراسة منشورة في مجلة European Urology عام 2019 أن تضخم البروستاتا الحميد وسرطان البروستاتا ينشآن عادة في مناطق مختلفة من الغدة؛ إذ يبدأ التضخم الحميد غالباً في المنطقة الانتقالية (Transitional Zone)، بينما ينشأ السرطان في أغلب الحالات في المنطقة الطرفية (Peripheral Zone).
متى يجب أن تقلق وتزور الطبيب فوراً؟
لا تنتظر حتى تظهر أعراض شديدة. إذا كنت فوق سن الخمسين — أو فوق الخامسة والأربعين إن كان لديك تاريخ عائلي — فإن الفحص الدوري السنوي ضروري حتى في غياب أي شكوى. لكن هناك علامات تستوجب زيارة فورية لطبيب المسالك البولية: وجود دم في البول أو السائل المنوي، ألم مستمر في الحوض أو أسفل الظهر دون سبب واضح، أو فقدان مفاجئ للوزن. هذه الأعراض لا تعني بالضرورة وجود سرطان، لكنها تستدعي تقييماً طبياً عاجلاً.
“كثير من المرضى يأتون إلى العيادة وهم مرعوبون لأن طبيباً آخر أخبرهم أن البروستاتا ‘متضخمة’. أول ما أقوله لهم: التضخم وحده ليس سرطاناً. لكنني أنصح كل رجل تجاوز الخمسين بإجراء تحليل PSA سنوياً، لأن الاكتشاف المبكر يصنع فرقاً هائلاً في نتائج العلاج.”
اقرأ أيضاً: الورم الحميد: دليلك الطبي الشامل للفهم والعلاج (علامات الاطمئنان والخطر)
ما أعراض سرطان البروستاتا — القاتل الصامت؟
هل توجد أعراض مبكرة؟
هنا تكمن المفارقة الخطيرة. سرطان البروستاتا في مراحله الأولى لا يُعطي أي إنذار تقريباً. لا ألم، لا تغير في البول، لا أي شيء يلفت الانتباه. وهذا بالضبط ما يجعله “القاتل الصامت”. كثير من الرجال يعيشون سنوات وهم مصابون دون أن يدركوا ذلك، ولا يُكتشف المرض إلا صدفة أثناء فحص روتيني أو عند إجراء تحليل PSA لسبب آخر.
هذا الغياب للأعراض المبكرة هو السبب الذي يجعل الأطباء يصرون على أهمية الفحص الدوري. فالاعتماد على ظهور الأعراض يعني في كثير من الأحيان أن المرض قد تجاوز مرحلة البداية. لقد أظهرت بيانات السجل السعودي للأورام أن نسبة ملحوظة من حالات سرطان البروستاتا في المملكة تُشخَّص في مراحل متقدمة، ويُرجع الخبراء ذلك جزئياً إلى تأخر الرجال في إجراء الفحوصات الدورية.
الأعراض المتقدمة
عندما يكبر الورم أو ينتشر، تبدأ الأعراض بالظهور تدريجياً. وأبرز أعراض سرطان البروستاتا المتقدمة تشمل:
- صعوبة في بدء التبول أو ضعف ملحوظ في تدفق البول.
- الحاجة المتكررة للتبول، خاصة أثناء الليل (Nocturia).
- وجود دم في البول (Hematuria) أو في السائل المنوي.
- ألم أو حرقة أثناء التبول أو القذف.
- ألم مزمن في أسفل الظهر أو الحوض أو الوركين.
- ضعف الانتصاب (Erectile Dysfunction).
- ألم في العظام — وخاصة العمود الفقري والحوض — وهو غالباً علامة على انتشار المرض إلى الهيكل العظمي.
من المهم التنبيه إلى أن هذه الأعراض ليست حصرية لسرطان البروستاتا؛ إذ قد تنتج عن التهاب البروستاتا (Prostatitis) أو التضخم الحميد. لكن ظهورها يستوجب تقييماً طبياً دقيقاً لاستبعاد الأسوأ.
ألم العظام المرتبط بسرطان البروستاتا المنتشر يختلف عن آلام العظام العادية — فهو ألم عميق ومستمر لا يتحسن بالراحة، وغالباً ما يكون أسوأ في الليل. إذا كنت تعاني من ألم عظمي مزمن غير مبرر ولديك عوامل خطر، فلا تتردد في مراجعة الطبيب.
اقرأ أيضاً: ألم أسفل الظهر: الأسباب الحقيقية وطرق العلاج الفعالة
ما أسباب سرطان البروستاتا ومن هو الأكثر عُرضة؟
العمر والتاريخ العائلي والجينات
لا يوجد سبب واحد محدد يُعرف بأنه “المسبب” لسرطان البروستاتا. لكن الأبحاث حددت عدة عوامل خطر ترفع احتمالية الإصابة بشكل واضح. العمر يأتي في المقدمة؛ إذ إن أكثر من 60% من الحالات تُشخَّص عند رجال تجاوزوا الخامسة والستين. يندر حدوث هذا السرطان قبل سن الأربعين.
التاريخ العائلي عامل محوري أيضاً. إذا كان والدك أو أخوك قد أصيب بسرطان البروستاتا، فإن خطر إصابتك يتضاعف مقارنة بالرجل العادي. فقد ربطت الأبحاث بعض الطفرات الجينية بزيادة خطر الإصابة، أبرزها طفرات جينَي BRCA1 وBRCA2 — وهي الجينات ذاتها المرتبطة بسرطان الثدي والمبيض عند النساء. كما أن متلازمة لينش (Lynch Syndrome) ترفع الخطر بشكل ملحوظ.
أثبتت دراسة منشورة في مجلة The New England Journal of Medicine عام 2019 أن الرجال الحاملين لطفرة BRCA2 يواجهون خطراً أعلى بنحو 3 إلى 5 أضعاف للإصابة بسرطان البروستاتا العدواني مقارنة بالرجال غير الحاملين لهذه الطفرة. وعليه فإن الفحص الجيني أصبح أداة مهمة في تحديد الفئات الأعلى خطراً.
العرق والنظام الغذائي
يختلف معدل الإصابة بسرطان البروستاتا بين الأعراق. الرجال من أصول إفريقية يسجلون أعلى معدلات الإصابة والوفاة عالمياً، بينما تكون المعدلات أقل في شرق آسيا. في المملكة العربية السعودية، تشير إحصائيات الهيئة العامة للإحصاء والسجل السعودي للأورام إلى ارتفاع تدريجي في معدلات الإصابة خلال العقدين الأخيرين، وهو ما يربطه بعض الباحثين بتغير أنماط الحياة والتغذية.
من ناحية أخرى، أظهرت دراسات وبائية أن الأنظمة الغذائية الغنية بالدهون الحيوانية واللحوم الحمراء المصنّعة ومنتجات الألبان عالية الدسم قد ترتبط بارتفاع طفيف في خطر الإصابة. بالمقابل، الأطعمة الغنية بمادة اللايكوبين (Lycopene) — الموجودة بوفرة في الطماطم المطبوخة — والخضراوات الصليبية مثل البروكلي والقرنبيط أظهرت تأثيراً وقائياً محتملاً في عدة دراسات.
“أنصح الرجال فوق الخمسين بالتركيز على نظام غذائي متوسطي غني بزيت الزيتون والطماطم المطبوخة والأسماك الدهنية، مع تقليل اللحوم الحمراء المصنّعة والدهون المشبعة. الطعام وحده لا يمنع السرطان، لكنه جزء مهم من منظومة الوقاية الشاملة.”
اقرأ أيضاً: حمية البحر الأبيض المتوسط — كيف تبدأ وتستمر بنظام غذائي يحمي قلبك وعقلك؟
دراسة واسعة أجراها فريق بحثي في جامعة هارفارد عام 2020 ونُشرت في Journal of the National Cancer Institute أظهرت أن الرجال الذين يتناولون 10 حصص أو أكثر أسبوعياً من منتجات الطماطم المطبوخة (صلصة، معجون) انخفض لديهم خطر الإصابة بسرطان البروستاتا بنسبة تقارب 18% مقارنة بمن لا يتناولونها بانتظام.
كيف يتم تشخيص سرطان البروستاتا — رحلة المريض خطوة بخطوة؟
الفحص السريري — فحص المستقيم الرقمي (DRE)
يبدأ التشخيص عادة في عيادة طبيب المسالك البولية. الفحص السريري الأول هو فحص المستقيم الرقمي (Digital Rectal Examination – DRE)، حيث يُدخل الطبيب إصبعه — مرتدياً قفازاً مشحماً — عبر فتحة الشرج ليتحسس سطح البروستاتا الخلفي. يبحث الطبيب عن أي كتل صلبة أو عدم انتظام في ملمس الغدة. هذا الفحص سريع ولا يستغرق أكثر من دقيقة، وقد يسبب إزعاجاً بسيطاً لكنه نادراً ما يكون مؤلماً.
كثير من الرجال — خاصة في مجتمعاتنا العربية — يتجنبون هذا الفحص بسبب الحرج. لكن تأجيله قد يكلفك اكتشافاً متأخراً. الفحص بحد ذاته لا يؤكد التشخيص، لكنه يعطي الطبيب مؤشراً أولياً مهماً.
تحليل مستضد البروستاتا النوعي (PSA)

تحليل PSA (Prostate-Specific Antigen) هو فحص دم بسيط يقيس مستوى بروتين تفرزه خلايا البروستاتا. في الوضع الطبيعي، تكون نسبة PSA أقل من 4 نانوغرام/مل (ng/mL). ارتفاع النسبة فوق هذا الحد لا يعني بالضرورة وجود سرطان — فالتضخم الحميد والتهاب البروستاتا وحتى ركوب الدراجة قبل الفحص قد ترفعه مؤقتاً.
لكن ارتفاع PSA فوق 10 ng/mL يرفع احتمالية وجود سرطان البروستاتا إلى نحو 50%. أما المنطقة “الرمادية” بين 4 و10 فتحتاج إلى مزيد من التقييم. هنا يلجأ الطبيب إلى حساب نسبة PSA الحر إلى الكلي (Free/Total PSA Ratio)، وسرعة ارتفاع PSA مع الوقت (PSA Velocity). كلما كانت النسبة الحرة أقل، زاد الشك في وجود خباثة.
توصي إدارة الغذاء والدواء الأمريكية (FDA) بأن تحليل PSA وحده لا ينبغي أن يكون الأساس الوحيد لتشخيص سرطان البروستاتا أو استبعاده، بل يجب تفسيره ضمن السياق السريري الكامل — بما يشمل الفحص السريري والتصوير والخزعة عند الحاجة.
التصوير بالرنين المغناطيسي والموجات فوق الصوتية
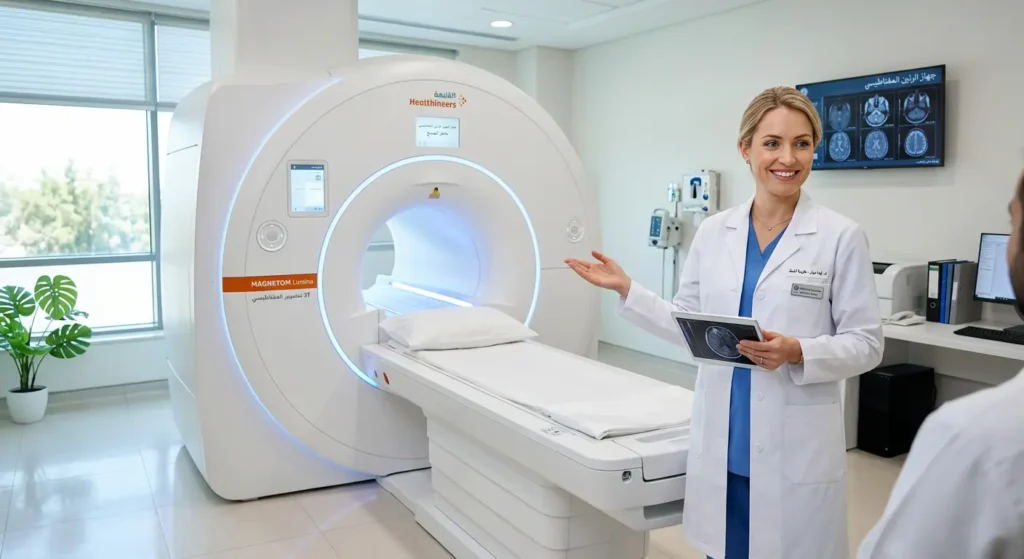
إذا أشارت نتائج PSA والفحص السريري إلى احتمال وجود ورم، ينتقل الطبيب إلى التصوير. التصوير بالرنين المغناطيسي متعدد المعلمات (Multiparametric MRI – mpMRI) أصبح الأداة الذهبية اليوم لتقييم البروستاتا قبل الخزعة. هذا التصوير يستطيع تحديد مواقع الأورام المحتملة داخل الغدة بدقة عالية، ويساعد الطبيب في توجيه الخزعة نحو المناطق المشبوهة بدلاً من أخذ عينات عشوائية.
الموجات فوق الصوتية عبر المستقيم (Transrectal Ultrasound – TRUS) لا تزال تُستخدم أيضاً، خاصة لتوجيه إبرة الخزعة. لكن دقتها في اكتشاف الأورام الصغيرة أقل من الرنين المغناطيسي.
خزعة البروستاتا (Prostate Biopsy) — كيف تتم وهل هي مؤلمة؟
خزعة البروستاتا هي الخطوة الحاسمة لتأكيد التشخيص. يأخذ الطبيب — تحت تخدير موضعي غالباً — من 10 إلى 12 عينة نسيجية دقيقة من مناطق مختلفة في الغدة باستخدام إبرة رفيعة موجهة بالموجات فوق الصوتية أو الرنين المغناطيسي. العملية تستغرق عادة من 15 إلى 20 دقيقة.
هل هي مؤلمة؟ أغلب المرضى يصفونها بأنها “مزعجة” أكثر من كونها مؤلمة فعلاً، خاصة مع التخدير الموضعي الجيد. قد يشعر المريض بوخز بسيط أو ضغط عند أخذ كل عينة. بعد الخزعة، من الطبيعي ملاحظة بعض الدم في البول أو السائل المنوي لعدة أيام. تُرسل العينات إلى مختبر الأنسجة (Histopathology) لتحليلها تحت المجهر وتحديد ما إذا كانت تحتوي على خلايا سرطانية.
اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
🔔 مثال تطبيقي من الواقع:
تخيل أن أبو محمد — رجل سعودي في الثانية والستين من عمره — ذهب لفحصه السنوي الروتيني. لا يعاني من أي شكوى. طبيب المسالك طلب تحليل PSA وكانت النتيجة 7.5 ng/mL. الطبيب لم يقل “عندك سرطان”، بل قال: “النسبة في المنطقة الرمادية، ونحتاج رنيناً مغناطيسياً للاطمئنان”. أظهر الرنين بقعة مشبوهة صغيرة. أُجريت خزعة موجهة، وتبين وجود سرطان موضعي في مرحلته الأولى بدرجة غليسون 6. تم وضع أبو محمد على بروتوكول مراقبة نشطة، وهو اليوم — بعد ثلاث سنوات — بصحة ممتازة دون أي تدخل جراحي. هذا السيناريو يتكرر يومياً، والرسالة واضحة: الفحص المبكر أنقذه.
كيف تقرأ نتائج الخزعة — ما هو مقياس غليسون (Gleason Score)؟
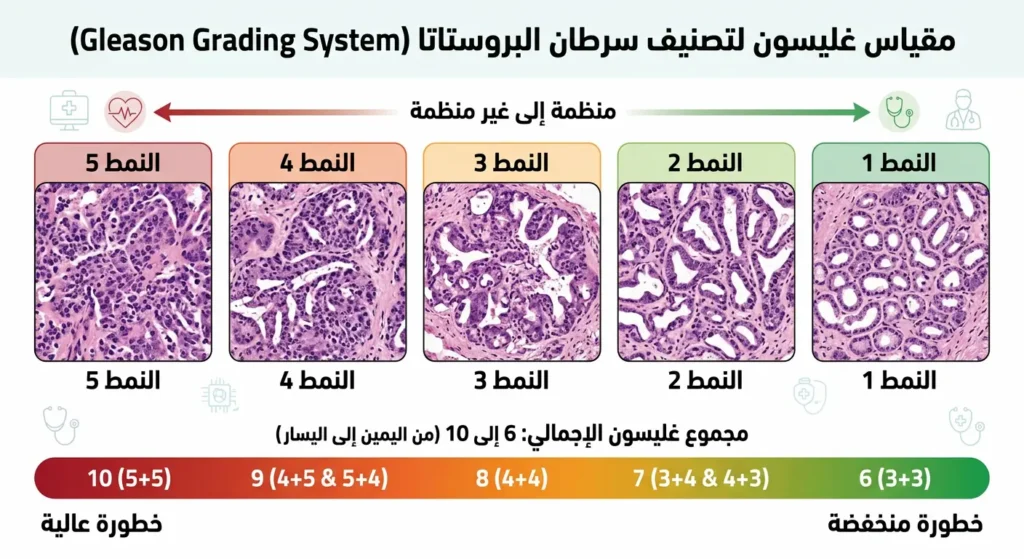
عندما يفحص طبيب الأنسجة (Pathologist) عينات الخزعة تحت المجهر، يستخدم نظاماً يُسمى مقياس غليسون لتحديد مدى “شراسة” الخلايا السرطانية. الفكرة بسيطة: كلما كانت الخلايا أقرب شكلاً للخلايا الطبيعية، كان السرطان أبطأ نمواً وأقل خطورة. وكلما ابتعدت عن الشكل الطبيعي، كان أكثر عدوانية.
يمنح الطبيب درجتين — كل منهما من 1 إلى 5 — للنمطين الأكثر شيوعاً في العينة، ثم يجمعهما. الناتج هو درجة غليسون الكلية التي تتراوح من 6 إلى 10 (الدرجات أقل من 6 لم تعد تُصنف كسرطان وفق التصنيفات الحديثة). غليسون 6 يعني سرطاناً بطيئاً جداً وقليل الخطورة. غليسون 7 يُقسم إلى (3+4) وهو متوسط الخطورة، و(4+3) وهو أعلى خطورة قليلاً. غليسون 8 إلى 10 يشير إلى سرطان عدواني يحتاج تدخلاً فورياً.
في عام 2014، طُوِّر نظام تصنيف جديد يُسمى مجموعات الدرجات (Grade Groups) من 1 إلى 5 لتبسيط الأمر على المرضى. المجموعة 1 تقابل غليسون 6، والمجموعة 5 تقابل غليسون 9-10. هذا النظام أصبح معتمداً من منظمة الصحة العالمية (WHO) ويُستخدم بشكل متزايد عالمياً.
وفقاً لبيانات الجمعية الأمريكية للسرطان (ACS)، فإن نحو 40-50% من حالات سرطان البروستاتا المُشخصة حديثاً تكون بدرجة غليسون 6 (المجموعة 1) — أي سرطانات بطيئة جداً قد لا تحتاج علاجاً فورياً على الإطلاق.
ما مراحل سرطان البروستاتا (Staging)؟
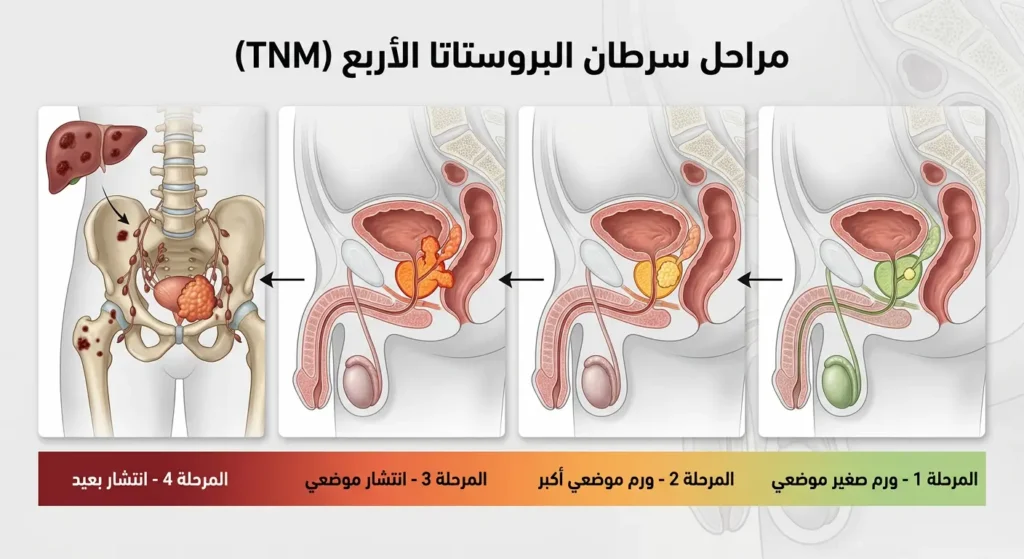
المرحلة الأولى والثانية — سرطان موضعي داخل الغدة
في المرحلتين الأولى والثانية (Stage I & II)، يكون الورم محصوراً بالكامل داخل غدة البروستاتا ولم يخترق كبسولتها الخارجية. في المرحلة الأولى، يكون الورم صغيراً جداً ولا يمكن تحسسه بالفحص السريري، ويُكتشف فقط عبر تحليل PSA أو صدفة أثناء جراحة لتضخم حميد. في المرحلة الثانية، يكون الورم أكبر وقد يُتحسس بالفحص، لكنه لا يزال داخل الغدة.
النبأ السار هو أن نسبة الشفاء من سرطان البروستاتا في هاتين المرحلتين تقارب 99% خلال خمس سنوات.
المرحلة الثالثة — الانتشار الموضعي
في المرحلة الثالثة (Stage III)، يكون الورم قد اخترق كبسولة البروستاتا وامتد إلى الأنسجة المجاورة مثل الحويصلات المنوية (Seminal Vesicles). لم ينتشر بعد إلى الغدد الليمفاوية أو الأعضاء البعيدة، لكنه لم يعد محصوراً داخل الغدة. خيارات العلاج هنا تتطلب عادة مزيجاً من العلاجات.
المرحلة الرابعة — الانتشار إلى الأعضاء الأخرى والعظام
المرحلة الرابعة (Stage IV) تعني أن السرطان قد انتشر (Metastasis) إلى أعضاء بعيدة. العظام هي الموقع الأكثر شيوعاً لانتقالات سرطان البروستاتا، وخاصة العمود الفقري والحوض والأضلاع. قد ينتشر أيضاً إلى الغدد الليمفاوية البعيدة أو الكبد أو الرئتين.
هل سرطان البروستاتا مميت في هذه المرحلة؟ ليس بالضرورة. حتى المرحلة الرابعة أصبحت قابلة للسيطرة لسنوات طويلة بفضل العلاجات الحديثة، وإن كان الشفاء التام يصبح أصعب. نسبة البقاء على قيد الحياة لخمس سنوات في حالة الانتشار البعيد تبلغ نحو 31% وفق بيانات SEER الأمريكية، لكنها في تحسن مستمر مع تطور العلاجات.
صنّفت منظمة الصحة العالمية (WHO) سرطان البروستاتا في تقريرها الصادر عام 2022 بوصفه رابع أكثر السرطانات تسبباً بالوفيات بين الذكور عالمياً، مع تسجيل أكثر من 1.4 مليون حالة جديدة سنوياً. لكنها أكدت أن معدلات البقاء على قيد الحياة تتحسن بشكل مضطرد بفضل التشخيص المبكر والعلاجات الحديثة.
اقرأ أيضاً: الورم الخبيث: دليلك الطبي الشامل لفهم المرض ومواجهته
ما أحدث طرق علاج سرطان البروستاتا؟
هذا القسم هو الأهم في هذا المقال، لأن فهم خيارات العلاج يمنح المريض وأسرته القدرة على المشاركة الفعالة في القرار العلاجي مع الفريق الطبي. خطة علاج سرطان البروستاتا ليست موحدة لكل المرضى؛ إذ تعتمد على مرحلة المرض ودرجة غليسون ومستوى PSA وعمر المريض وصحته العامة ورغباته الشخصية.
لماذا قد يقرر الطبيب عدم التدخل — المراقبة النشطة (Active Surveillance)؟
قد يبدو غريباً أن يقول لك الطبيب: “نعم، لديك سرطان، لكننا لن نعالجه الآن.” لكن هذا بالفعل أحد أهم أحدث علاجات سرطان البروستاتا المعتمدة في الخطوط الإرشادية العالمية. المراقبة النشطة تعني مراقبة الورم عن كثب — عبر فحوصات PSA دورية وخزعات متكررة ورنين مغناطيسي — دون تقديم أي علاج ما لم يُظهر السرطان علامات تقدم.
هذا الخيار مناسب تحديداً للأورام بطيئة النمو (غليسون 6 أو المجموعة 1) المحصورة داخل الغدة. الفكرة أن كثيراً من هذه الأورام لن تسبب أي ضرر خلال حياة المريض، بينما العلاج الجراحي أو الإشعاعي قد يسبب آثاراً جانبية تؤثر على جودة الحياة دون داعٍ.
أثبتت دراسة ProtecT الشهيرة المنشورة في The New England Journal of Medicine عام 2023 (متابعة 15 عاماً) أن معدلات الوفاة بسرطان البروستاتا كانت منخفضة جداً ومتقاربة بين المرضى الذين خضعوا للمراقبة النشطة وأولئك الذين خضعوا للجراحة أو الإشعاع في حالات السرطان الموضعي منخفض الخطورة.
“نتائج دراسة ProtecT بعد 15 عاماً من المتابعة أكدت أن المراقبة النشطة خيار آمن وفعال للرجال المصابين بسرطان بروستاتا موضعي منخفض الخطورة. معدلات الوفاة بسبب السرطان كانت منخفضة جداً بغض النظر عن العلاج المختار، مما يعني أن كثيراً من الرجال يمكنهم تأجيل العلاج دون تعريض حياتهم للخطر.”
الجراحة — استئصال البروستاتا الجذري
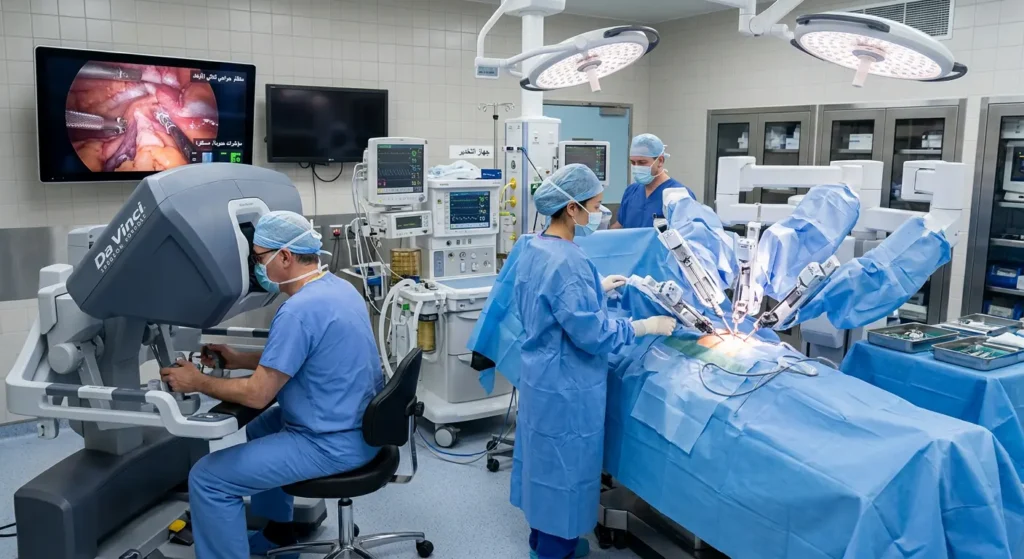
استئصال البروستاتا الجذري (Radical Prostatectomy) يعني إزالة غدة البروستاتا بالكامل مع الحويصلات المنوية والأنسجة المحيطة. هناك عدة طرق:
- الجراحة المفتوحة: شق جراحي كبير في أسفل البطن أو بين الفخذين.
- جراحة المنظار (Laparoscopic): شقوق صغيرة باستخدام أدوات دقيقة وكاميرا.
- الجراحة الروبوتية (Robot-Assisted) — روبوت دافنشي (Da Vinci System): وهي الأكثر انتشاراً اليوم في المراكز المتقدمة. يتحكم الجراح بأذرع روبوتية دقيقة جداً عبر وحدة تحكم. تتميز بدقة عالية، فقدان دم أقل، وفترة تعافٍ أقصر. عدة مراكز في السعودية — مثل مستشفى الملك فيصل التخصصي ومركز الأبحاث — تقدم هذه الجراحة الآن.
مضاعفات عملية استئصال البروستاتا تشمل خطر سلس البول وضعف الانتصاب. لكن الجراحين المهرة يحرصون على تقنية “حفظ الأعصاب” (Nerve-Sparing Technique) للحفاظ على الأعصاب المسؤولة عن الانتصاب قدر الإمكان.
العلاج الإشعاعي — الخارجي والداخلي
العلاج الإشعاعي يستخدم أشعة عالية الطاقة لقتل الخلايا السرطانية. ينقسم إلى نوعين رئيسين:
العلاج الإشعاعي الخارجي (External Beam Radiation Therapy – EBRT): يُوجَّه شعاع إشعاعي مركز من خارج الجسم نحو البروستاتا. التقنية الأحدث هي IMRT (Intensity-Modulated Radiation Therapy) التي تُشكِّل الشعاع ليتطابق مع شكل الورم، مما يقلل الضرر للأنسجة المجاورة. الجلسات تمتد عادة من 5 إلى 9 أسابيع، بمعدل 5 جلسات أسبوعياً.
العلاج الإشعاعي الداخلي (Brachytherapy): تُزرع بذور مشعة صغيرة (بحجم حبة الأرز) داخل نسيج البروستاتا مباشرة تحت التخدير. تبقى هذه البذور في مكانها وتبث إشعاعاً منخفض الجرعة بشكل مستمر لأسابيع أو أشهر. هذا الخيار مناسب للأورام الموضعية منخفضة إلى متوسطة الخطورة.
هل تعلم أن تقنية العلاج الإشعاعي بالبروتونات (Proton Beam Therapy) — وهي أحدث من الأشعة التقليدية — تستطيع إيصال الإشعاع بدقة أكبر وتقليل الأضرار الجانبية للأنسجة المحيطة؟ هذه التقنية بدأت تتوفر في عدد محدود من المراكز في المنطقة العربية.
اقرأ أيضاً: علاج السرطان: التقنيات الحديثة والابتكارات المستقبلية
العلاج الهرموني — كيف يعمل على تجويع الخلايا السرطانية؟
سرطان البروستاتا يعتمد في نموه بشكل كبير على هرمون التستوستيرون (Testosterone) والأندروجينات الأخرى. العلاج الهرموني (Androgen Deprivation Therapy – ADT) يهدف إلى خفض مستوى هذه الهرمونات إلى أدنى حد ممكن، مما “يُجوِّع” الخلايا السرطانية ويبطئ نموها بشكل كبير.
يتم ذلك إما بأدوية تمنع الخصيتين من إنتاج التستوستيرون (ناهضات أو مناهضات GnRH مثل ليوبروليد Leuprolide ودي غاريليكس Degarelix)، أو بأدوية تمنع التستوستيرون من العمل على الخلايا السرطانية (مضادات الأندروجين مثل بيكالوتاميد Bicalutamide وإنزالوتاميد Enzalutamide). في بعض الحالات، قد يُلجأ إلى استئصال الخصيتين الجراحي (Orchiectomy) كحل دائم.
العلاج الهرموني لا يُشفي من سرطان البروستاتا وحده عادةً، لكنه فعال جداً في إبطاء المرض وتصغير الأورام قبل الإشعاع أو في حالات الانتشار.
“العلاج الهرموني فعال للغاية في السيطرة على سرطان البروستاتا المنتشر، لكن له آثار جانبية يجب أن يعرفها المريض مسبقاً: هبّات حرارة، زيادة في الوزن، فقدان الكتلة العضلية، هشاشة العظام، وتغيرات مزاجية. التواصل المستمر بين المريض وفريقه الطبي ضروري لإدارة هذه الآثار وتعديل الخطة العلاجية عند الحاجة.”
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
العلاجات المتقدمة — العلاج الكيميائي والموجه والمناعي
العلاج الكيميائي (Chemotherapy): يُستخدم عادة عندما لا يستجيب سرطان البروستاتا للعلاج الهرموني (ما يُسمى سرطان البروستاتا المقاوم للإخصاء – Castration-Resistant Prostate Cancer أو CRPC). أبرز الأدوية المستخدمة هي دوسيتاكسيل (Docetaxel) وكابازيتاكسيل (Cabazitaxel). هذه الأدوية لا تشفي المرض لكنها تُطيل فترة البقاء وتُحسّن الأعراض.
العلاج الموجه (Targeted Therapy): أحدث الإضافات تشمل مثبطات إنزيم PARP مثل أولاباريب (Olaparib) الذي حصل على موافقة FDA في 2020 لعلاج سرطان البروستاتا المنتشر المقاوم للإخصاء لدى المرضى الحاملين لطفرات في جينات إصلاح الحمض النووي مثل BRCA1/2.
“دراسة PROfound أثبتت أن أولاباريب يمكن أن يُطيل فترة البقاء بشكل ملحوظ لدى مرضى سرطان البروستاتا المتقدم الذين يحملون طفرات في جينات إصلاح الحمض النووي. هذا يفتح باباً جديداً للطب الشخصي في علاج سرطان البروستاتا، حيث يتم اختيار العلاج بناءً على البصمة الجينية للورم.”
العلاج المناعي (Immunotherapy): سيبوليوسيل-تي (Sipuleucel-T) هو لقاح علاجي يُعَدُّ أول علاج مناعي مُعتمد لسرطان البروستاتا. يعمل بتحفيز جهاز المناعة لمهاجمة خلايا سرطان البروستاتا تحديداً. كما أن مثبطات نقاط التفتيش المناعية (Checkpoint Inhibitors) مثل بيمبروليزوماب (Pembrolizumab) أظهرت فعالية في حالات محددة تحمل طفرات MSI-H.
العلاج بالنظائر المشعة (Radiopharmaceuticals): لوتيتيوم-177 PSMA (Lu-177 PSMA) هو من أحدث العلاجات لسرطان البروستاتا المنتشر المقاوم للعلاج الهرموني. يرتبط بمستقبل PSMA على سطح خلايا سرطان البروستاتا ويوصل الإشعاع مباشرة إلى الورم. دراسة VISION المنشورة في The New England Journal of Medicine عام 2021 أظهرت أنه يُطيل فترة البقاء بشكل ملحوظ.
“العلاج بـ Lu-177 PSMA يُمثل ثورة حقيقية في علاج سرطان البروستاتا المتقدم. لقد رأيت مرضى كانت خياراتهم العلاجية محدودة جداً واستجابوا بشكل لافت لهذا العلاج. المستقبل واعد جداً في هذا المجال، ونحن في المنطقة العربية بدأنا نواكب هذه التطورات في مراكز متخصصة.”
في عام 2024، بدأت تجارب سريرية واعدة على جيل جديد من مثبطات PARP المدمجة مع العلاج المناعي لعلاج سرطان البروستاتا المقاوم. النتائج الأولية المنشورة في The Lancet Oncology تُشير إلى تحسن ملحوظ في معدلات الاستجابة مقارنة بالعلاج المنفرد.
كيف يتعامل المريض مع مضاعفات العلاج؟
التعامل مع سلس البول بعد الجراحة
سلس البول (Urinary Incontinence) هو أحد أكثر المضاعفات شيوعاً بعد استئصال البروستاتا الجذري. قد يعاني المريض من تسرب لا إرادي للبول — خاصة عند السعال أو الضحك أو رفع أشياء ثقيلة — في الأسابيع والأشهر الأولى بعد العملية.
الخبر المطمئن أن معظم الرجال يستعيدون السيطرة على المثانة خلال 6 إلى 12 شهراً. تمارين كيغل (Kegel Exercises) لتقوية عضلات قاع الحوض تُعَدُّ الخط الأول في التأهيل بعد العملية. في الحالات التي يستمر فيها السلس، تتوفر خيارات مثل الحقن حول الإحليل أو زراعة عاصرة بولية صناعية (Artificial Urinary Sphincter).
ضعف الانتصاب والصحة الجنسية بعد علاج البروستاتا
ضعف الانتصاب بعد العلاج — سواء كان جراحياً أو إشعاعياً — هو القلق الأكبر لدى كثير من الرجال. الأعصاب المسؤولة عن الانتصاب تمر على جانبَي البروستاتا مباشرة، وقد تتضرر أثناء العلاج حتى مع تقنيات حفظ الأعصاب.
التعافي يحتاج صبراً. قد يستغرق استعادة الانتصاب الكامل من 6 أشهر إلى سنتين. خلال هذه الفترة، يمكن استخدام أدوية مثل سيلدينافيل (Sildenafil) أو تادالافيل (Tadalafil)، أجهزة الشفط الفراغي (Vacuum Erection Device)، حقن داخل القضيب، أو في بعض الحالات زراعة دعامة قضيبية (Penile Implant). المهم أن يعرف المريض أن هذه المشكلة قابلة للعلاج ولا ينبغي أن تمنعه من طلب المساعدة.
إذا كنت مقبلاً على جراحة استئصال البروستاتا، ناقش مع جراحك خيار حفظ الأعصاب مسبقاً، واسأل عن خطة “التأهيل الجنسي المبكر” (Early Penile Rehabilitation) — فالبدء ببرنامج تأهيلي بعد العملية مباشرة يُحسّن فرص استعادة الوظيفة الجنسية بشكل كبير.
اقرأ أيضاً: الدليل الطبي الشامل لفهم وعلاج سرعة القذف نهائياً
ما نسبة الشفاء من سرطان البروستاتا بلغة الأرقام؟
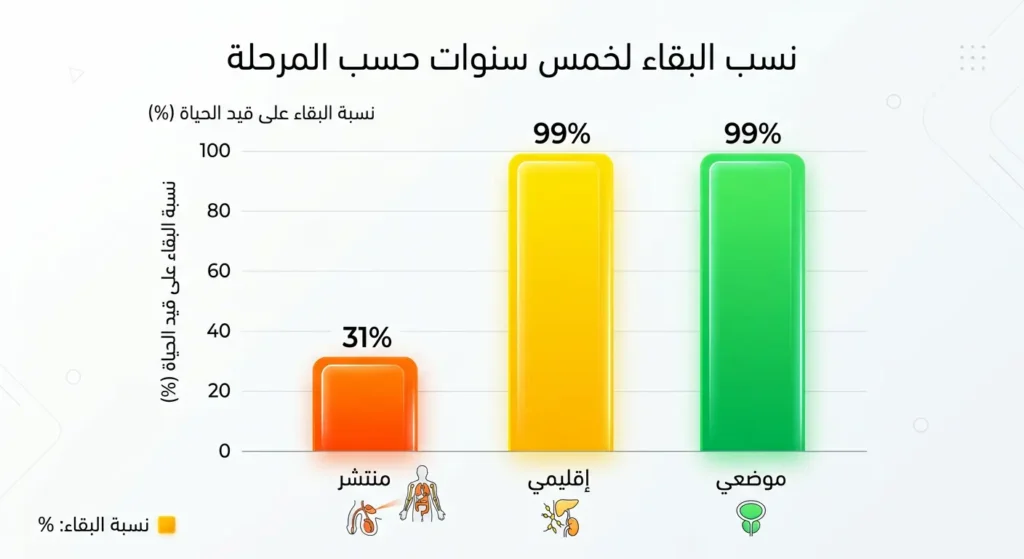
الأرقام هنا مبشّرة بحق. وفقاً لبيانات برنامج SEER التابع للمعهد الوطني الأمريكي للسرطان (NCI) المحدثة حتى 2024:
- المرحلة الموضعية (محصور داخل الغدة): نسبة البقاء لخمس سنوات تتجاوز 99%.
- المرحلة الإقليمية (انتشار للأنسجة القريبة أو الغدد الليمفاوية): نسبة البقاء لخمس سنوات تتجاوز 99% أيضاً.
- المرحلة المنتشرة (Distant Metastasis): نسبة البقاء لخمس سنوات حوالي 31-34% — وهي في تحسن مستمر.
- نسبة البقاء لعشر سنوات للمراحل المبكرة تتجاوز 98%.
هذه الأرقام تجعل سرطان البروستاتا واحداً من أكثر السرطانات “قابلية للشفاء” عند اكتشافه مبكراً. الجدير بالذكر أن كثيراً من الرجال المصابين بسرطان بروستاتا بطيء النمو يعيشون حياتهم الطبيعية كاملة ويموتون بأسباب أخرى لا علاقة لها بالسرطان.
“سرطان البروستاتا شهد تحولاً جذرياً في العقد الأخير. لم تعد الإصابة به تعني نهاية الحياة — بل أصبح لدينا ترسانة من العلاجات التي تمكننا من تحويل حتى الحالات المتقدمة إلى مرض مزمن يمكن السيطرة عليه لسنوات طويلة. المفتاح يبقى في التشخيص المبكر والعلاج المخصص.”
من بين كل 100 رجل يُشخَّص لديهم سرطان البروستاتا الموضعي اليوم ويتلقون العلاج المناسب، 99 منهم سيكونون على قيد الحياة بعد 5 سنوات. هذا يعني أن فرصة الشفاء أعلى من فرصة النجاح في كثير من العمليات الجراحية الروتينية الأخرى.
اقرأ أيضاً: الإحصاءات الحيوية (Vital Statistics): المفهوم، الأهمية، والتطبيقات
هل يمكن الوقاية من سرطان البروستاتا؟
لا توجد طريقة مضمونة 100% لمنع الإصابة بسرطان البروستاتا. لكن هناك خطوات مبنية على الأدلة العلمية يمكنها خفض الخطر أو على الأقل ضمان الاكتشاف المبكر.
من أهم هذه الخطوات الحفاظ على وزن صحي وممارسة النشاط البدني المنتظم. أظهرت دراسات عدة أن السمنة ترتبط بزيادة خطر الإصابة بسرطان بروستاتا عدواني. كذلك فإن تبني نظام غذائي غني بالخضراوات والفواكه والأسماك وفقير بالدهون المشبعة واللحوم المصنعة يُعَدُّ عاملاً وقائياً محتملاً.
بالنسبة للأدوية الوقائية، فقد أظهرت دراسة REDUCE المنشورة في The New England Journal of Medicine أن عقار دوتاستيرايد (Dutasteride) يقلل خطر الإصابة بسرطان البروستاتا بنحو 23% — لكنه لا يُوصف روتينياً لهذا الغرض بسبب آثاره الجانبية، ويُترك القرار للطبيب بعد تقييم المخاطر والفوائد.
لكن الركيزة الأهم تبقى الفحص الدوري المبكر. متى يجب فحص البروستاتا؟ توصي الجمعية الأمريكية للسرطان بأن يبدأ النقاش مع الطبيب حول الفحص في:
- سن 50 لمعظم الرجال.
- سن 45 للرجال ذوي الخطر المرتفع (تاريخ عائلي أو أصل إفريقي).
- سن 40 للرجال ذوي الخطر المرتفع جداً (أكثر من قريب من الدرجة الأولى أصيب مبكراً).
في المملكة العربية السعودية، بدأت عدة مبادرات حكومية وأهلية للتوعية بأهمية الكشف المبكر عن سرطان البروستاتا، لكن الوعي المجتمعي لا يزال يحتاج إلى تعزيز كبير. الحاجز الثقافي — الحرج من الفحص — لا يزال عقبة حقيقية يجب تجاوزها.
مادة الإبيغالوكاتشين غالات (EGCG) الموجودة في الشاي الأخضر أظهرت في دراسات مخبرية قدرة على إبطاء نمو خلايا سرطان البروستاتا. لكن الأدلة السريرية على البشر لا تزال غير كافية للتوصية به كعلاج وقائي. احرص فقط على نمط حياة صحي شامل بدلاً من الاعتماد على مكمل واحد.
اقرأ أيضاً:
- تغذية مريض السرطان: الدليل الطبي الشامل للمسموح والممنوع
- الأطعمة المسببة للسرطان: ما الذي يختبئ في مطبخك ويهدد صحتك؟
-
NCCN 2024: توصي الشبكة الوطنية الشاملة للسرطان بالمراقبة النشطة كخيار أول للمرضى ذوي الخطورة المنخفضة جداً (غليسون 6) بدلاً من العلاج الفوري.
المصدر: NCCN Clinical Practice Guidelines — Prostate Cancer 2024 -
EAU 2024: تؤكد الجمعية الأوروبية لجراحة المسالك البولية على ضرورة إجراء رنين مغناطيسي متعدد المعلمات (mpMRI) قبل أي خزعة أولية لتقليل الخزعات غير الضرورية.
المصدر: EAU Guidelines on Prostate Cancer 2024 -
AUA 2023: توصي الجمعية الأمريكية لجراحة المسالك البولية ببدء مناقشة فحص PSA مع الرجال في سن 55-69 وترك القرار مشتركاً بين الطبيب والمريض.
المصدر: AUA Early Detection of Prostate Cancer Guideline 2023 -
وزارة الصحة السعودية 2024: أطلقت حملة “افحص لتطمئن” لتشجيع الرجال فوق الخمسين على إجراء الفحص الدوري لسرطان البروستاتا ضمن برامج الكشف المبكر.
المصدر: وزارة الصحة — المملكة العربية السعودية
أسئلة شائعة حول سرطان البروستاتا
الخاتمة
سرطان البروستاتا ليس حكماً بالإعدام. هذه الرسالة يجب أن تصل إلى كل رجل عربي يقرأ هذا المقال. لقد رأينا أن نسبة الشفاء من سرطان البروستاتا عند اكتشافه في مراحله الأولى تقارب 99%، وأن خيارات العلاج تتطور بوتيرة متسارعة — من المراقبة النشطة إلى الجراحة الروبوتية إلى العلاجات المناعية والنظائر المشعة. المفتاح الحقيقي يكمن في كسر حاجز الخوف والحرج وإجراء الفحص الدوري في الوقت المناسب. غدة صغيرة بحجم حبة الجوز لا ينبغي أن تكون سبباً في قلق يمنعك من عيش حياة كاملة وصحية.
فهل أجريت فحصك الدوري هذا العام؟
اقرأ أيضاً: سرطان الثدي: دليلك الشامل من التشخيص إلى التعافي
اقرأ أيضاً: سرطان الخلايا الحرشوفية (SCC): الدليل الشامل للأعراض والتشخيص والعلاج
المعلومات الواردة في هذا المقال على موقع خلية ذات طابع تثقيفي عام ولا تُغني عن استشارة طبيب مختص. لا ينبغي استخدام هذا المحتوى لتشخيص أي حالة مرضية أو وصف علاج بديل عن الرعاية الطبية المتخصصة. القرارات العلاجية يجب أن تُتخذ دائماً بالتنسيق مع الفريق الطبي المعالج بناءً على الحالة الفردية لكل مريض. إذا كنت تعاني من أي أعراض مقلقة، فتوجه فوراً إلى أقرب مرفق صحي أو اتصل بخدمات الطوارئ.
يلتزم موقع خلية بأعلى معايير الدقة الطبية. تستند جميع المعلومات الواردة في هذا المقال إلى دراسات منشورة في مجلات طبية مُحكَّمة وتقارير جهات رسمية عالمية (WHO، FDA، NCI، ACS، EAU، NCCN). جرت مراجعة هذا المحتوى من قبل أطباء ومتخصصين ضمن هيئة التحرير العلمية لضمان تقديم معلومات موثوقة ومحدثة. المصادر والمراجع مُدرجة بالكامل في نهاية المقال مع معرّفات DOI وروابط مباشرة قابلة للتحقق.
المصادر والمراجع
- Hamdy, F. C., et al. (2023). Fifteen-Year Outcomes after Monitoring, Surgery, or Radiotherapy for Prostate Cancer. The New England Journal of Medicine, 388(17), 1547-1558.
https://doi.org/10.1056/NEJMoa2214122
دراسة ProtecT: متابعة 15 عاماً تقارن بين المراقبة والجراحة والإشعاع لسرطان البروستاتا الموضعي. - Sartor, O., et al. (2021). Lutetium-177–PSMA-617 for Metastatic Castration-Resistant Prostate Cancer. The New England Journal of Medicine, 385(12), 1091-1103.
https://doi.org/10.1056/NEJMoa2107322
دراسة VISION: أثبتت فعالية Lu-177 PSMA في إطالة البقاء لدى مرضى سرطان البروستاتا المنتشر المقاوم. - Rawla, P. (2019). Epidemiology of Prostate Cancer. World Journal of Oncology, 10(2), 63-89.
https://doi.org/10.14740/wjon1191
مراجعة وبائية شاملة لسرطان البروستاتا عالمياً. - Castro, E., et al. (2019). PROREPAIR-B: A Prospective Cohort Study of the Impact of Germline DNA Repair Mutations on the Outcomes of Patients With Metastatic Castration-Resistant Prostate Cancer. Journal of Clinical Oncology, 37(6), 490-503.
https://doi.org/10.1200/JCO.18.00358
دراسة حول تأثير طفرات BRCA على نتائج علاج سرطان البروستاتا المتقدم. - de Bono, J., et al. (2020). Olaparib for Metastatic Castration-Resistant Prostate Cancer. The New England Journal of Medicine, 382(22), 2091-2102.
https://doi.org/10.1056/NEJMoa1911440
دراسة PROfound: أثبتت فعالية أولاباريب في سرطان البروستاتا مع طفرات إصلاح الحمض النووي. - Andriole, G. L., et al. (2010). Effect of Dutasteride on the Risk of Prostate Cancer. The New England Journal of Medicine, 362(13), 1192-1202.
https://doi.org/10.1056/NEJMoa0908127
دراسة REDUCE: تأثير دوتاستيرايد على خفض خطر الإصابة بسرطان البروستاتا. - American Cancer Society (2024). Prostate Cancer: Key Statistics.
https://www.cancer.org/cancer/prostate-cancer/about/key-statistics.html
إحصائيات محدثة حول معدلات الإصابة والبقاء لسرطان البروستاتا. - National Cancer Institute – SEER Program (2024). Cancer Stat Facts: Prostate Cancer.
https://seer.cancer.gov/statfacts/html/prost.html
قاعدة بيانات SEER لنسب البقاء على قيد الحياة حسب مرحلة سرطان البروستاتا. - World Health Organization – IARC (2022). GLOBOCAN 2022: Prostate Cancer Fact Sheet.
https://gco.iarc.fr/today/data/factsheets/cancers/27-Prostate-fact-sheet.pdf
إحصائيات عالمية لمنظمة الصحة العالمية حول سرطان البروستاتا. - U.S. Food and Drug Administration – FDA (2023). Prostate-Specific Antigen (PSA).
https://www.fda.gov/medical-devices/in-vitro-diagnostics/prostate-specific-antigen-psa
توصيات FDA حول استخدام تحليل PSA في الكشف المبكر. - National Comprehensive Cancer Network – NCCN (2024). NCCN Clinical Practice Guidelines in Oncology: Prostate Cancer.
https://www.nccn.org/professionals/physician_gls/pdf/prostate.pdf
الخطوط الإرشادية السريرية الأحدث لعلاج سرطان البروستاتا. - Campbell, M. F., Walsh, P. C., & Wein, A. J. (2020). Campbell-Walsh-Wein Urology (12th ed.). Elsevier.
المرجع الأكاديمي الأشهر عالمياً في جراحة المسالك البولية. - DeVita, V. T., Lawrence, T. S., & Rosenberg, S. A. (2019). DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (11th ed.). Wolters Kluwer.
الموسوعة المرجعية الأهم في طب الأورام. - Epstein, J. I. (2018). Biopsy Interpretation of the Prostate (5th ed.). Wolters Kluwer.
مرجع متخصص في تفسير خزعات البروستاتا ونظام غليسون. - Pernar, C. H., et al. (2018). The Epidemiology of Prostate Cancer. Cold Spring Harbor Perspectives in Medicine, 8(12), a030361.
https://doi.org/10.1101/cshperspect.a030361
مقالة مراجعة علمية مبسطة وشاملة حول وبائيات سرطان البروستاتا.
قراءات إضافية ومصادر للتوسع
- Mottet, N., et al. (2024). EAU Guidelines on Prostate Cancer. European Association of Urology.
https://uroweb.org/guidelines/prostate-cancer
لماذا نقترح عليك قراءته؟ هذه الخطوط الإرشادية الأوروبية تُعَدُّ المرجع الأشمل والأحدث لتشخيص وعلاج سرطان البروستاتا، وتُحدَّث سنوياً بناءً على أحدث الأدلة العلمية. ضرورية لأي طالب أو باحث يريد فهم القرارات العلاجية المبنية على الأدلة. - Bray, F., et al. (2024). Global Cancer Statistics 2022: GLOBOCAN Estimates of Incidence and Mortality Worldwide. CA: A Cancer Journal for Clinicians, 74(3).
https://doi.org/10.3322/caac.21834
لماذا نقترح عليك قراءته؟ هذا التقرير يعطيك صورة بانورامية عن وبائيات السرطان عالمياً، بما في ذلك سرطان البروستاتا، مع مقارنات بين مناطق العالم المختلفة. لا غنى عنه لأي بحث أكاديمي في هذا المجال. - Schaeffer, E. M., et al. (2023). Prostate Cancer, Version 4.2023. NCCN Evidence Blocks™, Journal of the National Comprehensive Cancer Network, 21(10), 1067-1096.
https://doi.org/10.6004/jnccn.2023.0050
لماذا نقترح عليك قراءته؟ يقدم تقييماً فريداً لكل خيار علاجي باستخدام “كتل الأدلة” (Evidence Blocks) التي تقيّم الفعالية والأمان والجودة والاتساق والقدرة على تحمل التكاليف — أداة تعليمية ممتازة لفهم عملية صنع القرار العلاجي.
إذا وجدت في هذا المقال ما أجاب عن تساؤلاتك أو خفف من مخاوفك، فشاركه مع رجل آخر في عائلتك أو دائرتك — فربما تكون أنت السبب في دفعه لإجراء فحصه الدوري الأول الذي قد ينقذ حياته. ولا تتردد في حجز موعد مع طبيب مسالك بولية إذا كنت قد تجاوزت الخمسين ولم تبدأ بعد رحلة الفحص الدوري.