الورم الخبيث: دليلك الطبي الشامل لفهم المرض ومواجهته
كيف يتشكّل وما فرص الشفاء منه في ضوء أحدث البروتوكولات العلاجية؟
الورم الخبيث هو كتلة من الخلايا غير الطبيعية التي تنقسم دون ضوابط، وتمتلك القدرة على غزو الأنسجة المحيطة والانتقال إلى أعضاء بعيدة عبر الدم أو الجهاز اللمفاوي. يُشكّل تهديداً مباشراً للحياة إذا لم يُكتشف مبكراً، لكن التقدم الطبي رفع نسب الشفاء في كثير من أنواعه بشكل ملحوظ خلال العقد الأخير.
جرت مراجعة هذه المقالة طبياً
المراجعة الطبية: د. زيد مراد – اختصاصي طب عام |
مراجعة التغذية: د. علا الأحمد – اختصاصية تغذية علاجية |
المراجعة الدوائية: جاسم محمد مراد – مستشار دوائي
هيئة التحرير العلمية | آخر تحديث: مارس 2026 | تواصل معنا
هل لاحظت يوماً كتلة صغيرة تحت جلدك فأصابك القلق؟ أو سمعت أحد أقاربك يتحدث عن تشخيص مفاجئ بورم لم يكن يتوقعه أحد؟ ذلك الشعور بالخوف والحيرة طبيعي تماماً. لكن المعرفة الدقيقة تُبدّد كثيراً من هذا الرعب. في هذا المقال ستجد كل ما تحتاج معرفته عن طبيعة هذا المرض، بدءاً من آليات تشكّله البيولوجية، مروراً بطرق التشخيص الحديثة، وانتهاءً بأحدث البروتوكولات العلاجية المعتمدة عالمياً. المعلومات هنا ليست نظرية فقط؛ بل هي أدوات عملية تساعدك على اتخاذ قرارات صحية واعية لنفسك ولعائلتك.
📌 خلاصة المقال في دقيقة واحدة
🔬 حقائق علمية جوهرية
- الورم الخبيث ينشأ من طفرات جينية متراكمة (3–7 طفرات) تجعل الخلايا تنقسم دون رقابة وتنتشر لأعضاء بعيدة.
- ليس كل ورم سرطاناً: الأورام الحميدة لا تغزو الأنسجة ولا تنتشر، بينما الخبيثة تفعل ذلك.
- العدوى الفيروسية (مثل HPV وفيروسات الكبد) مسؤولة عن 13% من حالات السرطان عالمياً.
✅ خطوات وقائية وتطبيقية
- الكشف المبكر يرفع نسبة الشفاء إلى أكثر من 95% في كثير من الأنواع.
- الإقلاع عن التدخين وتجنب السمنة يُقلّلان خطر الإصابة بما لا يقل عن 13 نوعاً من السرطان.
- ممارسة المشي 150 دقيقة أسبوعياً أثناء العلاج تُقلّل التعب بنسبة تصل إلى 40%.
⚠️ تحذيرات طبية
- استمرار أي عَرَض (كتلة، سعال مزمن، فقدان وزن مفاجئ) أكثر من أسبوعين يستوجب زيارة الطبيب فوراً.
- لا تشخّص نفسك بنفسك: الخزعة هي الوسيلة الوحيدة لتأكيد أو نفي التشخيص.
- العلاج المناعي والموجه أصبحا بديلاً حقيقياً عن الكيماوي في أنواع محددة — ناقش الخيارات مع طبيبك.
مثال تطبيقي من الواقع:
تخيّل أن رجلاً في الخمسين من عمره، يعيش في الرياض، لاحظ سعالاً مستمراً لأكثر من ثلاثة أسابيع مع نزول طفيف في وزنه. تجاهل الأمر ظناً منه أنه نزلة برد عنيدة. بعد شهرين، زار طبيبه بسبب ألم في الصدر. أجرى الطبيب أشعة مقطعية كشفت عن كتلة في الرئة اليمنى. أخذ الفريق الطبي خزعة (Biopsy) وأكد التشخيص: ورم خبيث في المرحلة الثانية. لأن الاكتشاف جاء قبل انتشار المرض إلى أعضاء أخرى، خضع المريض لبرنامج علاجي جمع بين الجراحة والعلاج الكيميائي. بعد تسعة أشهر، أظهرت الفحوصات اختفاء الورم. هذا السيناريو يتكرر يومياً في مستشفيات المملكة العربية السعودية، ويؤكد حقيقة واحدة: الكشف المبكر يصنع الفارق بين الحياة والموت.
ما هو الورم الخبيث؟ التعريف الطبي الدقيق
لفهم طبيعة هذا المرض، يجب أولاً إدراك كيف تعمل الخلايا السليمة. في الوضع الطبيعي، تنقسم خلايا الجسم بنظام محكم تتحكم فيه جينات محددة. هذه الجينات تعمل كإشارات مرور داخلية: تأمر الخلية بالانقسام عند الحاجة، وتأمرها بالتوقف والموت المبرمج (Apoptosis) عندما تُصبح قديمة أو تالفة.
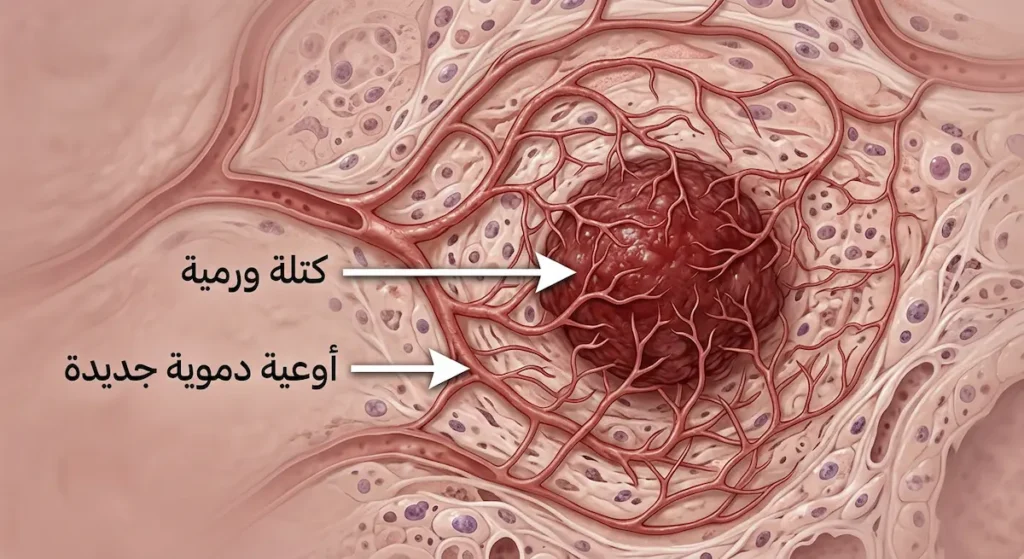
لكن حين تحدث طفرات في هذه الجينات المنظّمة، تفقد الخلية قدرتها على الاستجابة لأوامر التوقف. تبدأ بالانقسام بلا حدود، متجاهلةً كل الإشارات التنظيمية. هذا التمرد الخلوي هو جوهر ما يحدث في الورم الخبيث. لا يقتصر الأمر على الانقسام العشوائي فحسب؛ بل تكتسب هذه الخلايا المتمردة قدرات خطيرة إضافية، أبرزها تحفيز نمو أوعية دموية جديدة حولها فيما يُعرف طبياً بتكوين الأوعية الدموية الجديدة (Angiogenesis). هذه الأوعية تُغذّي الورم بالأكسجين والمواد الغذائية، مما يسمح له بالنمو المتسارع.
فهل كل سرطان (Cancer) هو بالضرورة ورم خبيث؟ من الناحية الطبية، نعم. مصطلح “السرطان” يُستخدم حصرياً للإشارة إلى الأورام الخبيثة. لكن ليس كل ورم سرطاناً؛ إذ توجد أورام حميدة (Benign Tumors) لا تغزو الأنسجة المجاورة ولا تنتشر. الخلط بين المصطلحين شائع جداً بين الناس، وفهم هذا الفرق يُزيل كثيراً من القلق غير المبرر.
💡 حقيقة طبية مهمة
لقد أثبتت الأبحاث أن الخلية الواحدة تحتاج عادةً إلى تراكم عدة طفرات جينية (بين 3 و 7 طفرات في المتوسط) قبل أن تتحول إلى خلية سرطانية كاملة القدرات. هذا يفسّر لماذا يزداد خطر الإصابة مع التقدم في العمر: الطفرات تتراكم ببطء على مدى عقود.
📖 اقرأ أيضاً: الورم الحميد: دليلك الطبي الشامل للفهم والعلاج (علامات الاطمئنان والخطر)
ما الفرق الجوهري بين الورم الخبيث والورم الحميد؟
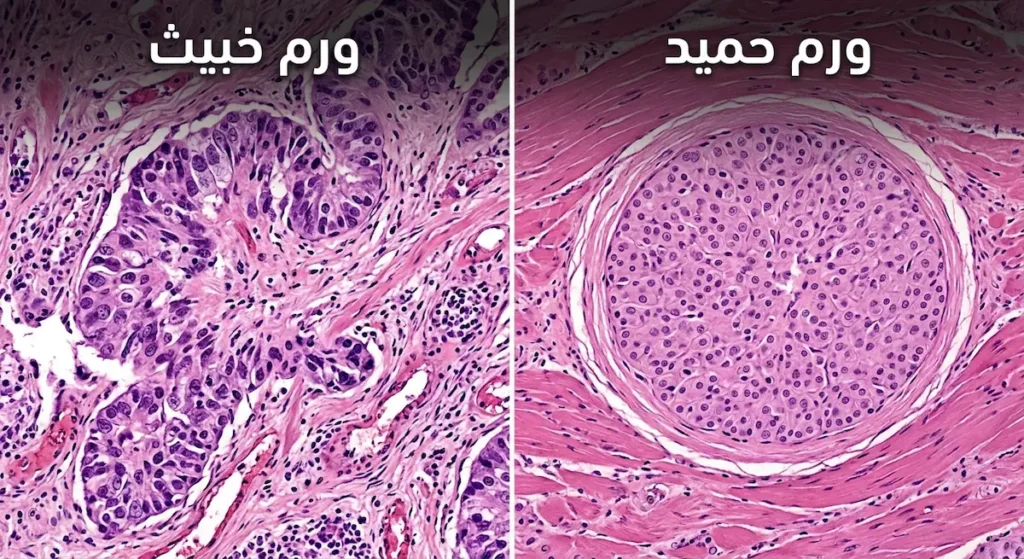
هذا السؤال من أكثر الأسئلة التي يطرحها المرضى عند سماعهم كلمة “ورم” لأول مرة. الفرق بين الورم الخبيث والحميد ليس مجرد تسمية؛ بل يتعلق بسلوك الخلايا ومصير المريض. الورم الحميد ينمو ببطء في معظم الحالات، ويبقى محصوراً في مكانه الأصلي محاطاً بغلاف ليفي يفصله عن الأنسجة السليمة. كأنه ضيف ثقيل يجلس في زاوية الغرفة دون أن يُزعج أحداً.
على النقيض من ذلك، يتميز الورم الخبيث بعدوانية واضحة. ينمو بسرعة أكبر في كثير من الأحيان، ويخترق الأنسجة المجاورة بلا احترام لأي حدود. وكذلك يمتلك قدرة فريدة على الانتقال (Metastasis) إلى أعضاء بعيدة تماماً عن مكانه الأصلي. تخيّل الفرق بين نبات ينمو في أصيصه بهدوء، وآخر يمدّ جذوره تحت الأرض ليخترق كل شيء حوله ويظهر في أماكن غير متوقعة.
من الفروق المهمة أيضاً أن احتمالية عودة الورم بعد الاستئصال الجراحي أعلى بكثير في الأورام الخبيثة. فحتى لو أزال الجرّاح الكتلة المرئية بالكامل، قد تكون خلايا مجهرية قد تسللت بالفعل إلى مناطق أخرى. لهذا السبب يلجأ الأطباء غالباً إلى العلاج الكيميائي أو الإشعاعي بعد الجراحة كإجراء احترازي. بالمقابل، نادراً ما يعود الورم الحميد بعد استئصاله الكامل.
❝
“أنصح كل شخص يكتشف كتلة غريبة في جسمه بعدم التسرع في الحكم عليها بأنها خبيثة أو حميدة. الفحص الطبي والخزعة هما الوسيلتان الوحيدتان للتفريق. كثير من الكتل التي تُسبب ذعراً كبيراً تتضح أنها حميدة تماماً، لكن التأخر في الفحص هو الخطر الحقيقي.”
— الدكتور زيد مراد، اختصاصي طب عام
جدول (1): مقارنة شاملة بين الورم الخبيث والورم الحميد
| وجه المقارنة | الورم الخبيث (Malignant) | الورم الحميد (Benign) |
|---|---|---|
| سرعة النمو | سريع وغير منتظم غالباً | بطيء ومنتظم في معظم الحالات |
| القدرة على الانتشار (Metastasis) | ينتشر إلى أعضاء بعيدة عبر الدم والجهاز اللمفاوي | لا ينتشر ويبقى محصوراً في مكانه |
| غزو الأنسجة المجاورة | يخترق ويغزو الأنسجة المحيطة | لا يغزو الأنسجة المجاورة (محاط بغلاف ليفي) |
| شكل الخلايا تحت المجهر | خلايا غير ناضجة وشاذة الشكل (Anaplastic) | خلايا ناضجة تشبه الخلايا الطبيعية |
| احتمالية العودة بعد الاستئصال | مرتفعة (خاصة في المراحل المتقدمة) | منخفضة جداً بعد الاستئصال الكامل |
| التأثير على الحالة العامة | يُسبب فقدان الوزن والتعب والهزال | نادراً ما يؤثر على الحالة العامة |
| العلاج المطلوب | جراحة + كيميائي + إشعاعي + علاج مناعي أو موجه | استئصال جراحي فقط في أغلب الحالات |
| الخطورة على الحياة | مهدد للحياة إذا لم يُعالج | غير مهدد للحياة عادةً (إلا في حالات الضغط على أعضاء حيوية) |
| المصدر: المعهد الوطني الأمريكي للسرطان (NCI) | منظمة الصحة العالمية (WHO) | ||
ما الأسباب وعوامل الخطر المسببة للأورام الخبيثة؟
لا يوجد سبب واحد يُفسّر ظهور جميع حالات الورم الخبيث. المسألة أشبه بلغز متعدد القطع، تتشابك فيه عوامل جينية وبيئية وسلوكية. فهم هذه العوامل لا يعني بالضرورة الوقاية المطلقة، لكنه يُقلّل المخاطر بشكل كبير.
العوامل الجينية والوراثية
بعض الأشخاص يرثون طفرات جينية تجعلهم أكثر عرضة لأنواع محددة من السرطان. مثلاً، طفرات جينَي BRCA1 وBRCA2 ترفع خطر الإصابة بسرطان الثدي والمبيض بشكل ملحوظ. هذا لا يعني أن الإصابة حتمية؛ بل يعني أن الخطر أعلى مقارنة بمن لا يحملون هذه الطفرات. في السعودية، بدأت مراكز طبية عديدة تُقدّم فحوصات جينية متقدمة للعائلات ذات التاريخ المرضي بالسرطان، وهو توجه إيجابي يستحق التشجيع.
📖 اقرأ أيضاً: علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
العوامل البيئية والمهنية
التعرض المزمن للإشعاع المؤيّن (Ionizing Radiation) يُعَدُّ من عوامل الخطر المؤكدة. وكذلك التعامل المستمر مع مواد كيميائية مسرطنة معروفة مثل الأسبستوس (Asbestos) والبنزين (Benzene). العاملون في بعض القطاعات الصناعية والتعدينية معرضون أكثر من غيرهم، مما يستوجب الالتزام الصارم بمعايير السلامة المهنية.
عوامل نمط الحياة
التدخين يأتي في مقدمة أسباب الورم الخبيث على مستوى العالم. وفقاً لمنظمة الصحة العالمية (WHO)، يتسبب التبغ في نحو 22% من وفيات السرطان عالمياً. السمنة المفرطة ترتبط بزيادة خطر الإصابة بما لا يقل عن 13 نوعاً من السرطان، بما فيها سرطانات القولون والكلى والبنكرياس. من جهة ثانية، يُسهم استهلاك الكحول المزمن في رفع خطر سرطانات الكبد والمريء والفم.
العدوى الفيروسية
ليس كل السرطانات ذاتية المنشأ. فيروس الورم الحليمي البشري (HPV) مسؤول عن الغالبية العظمى من حالات سرطان عنق الرحم. فيروسات التهاب الكبد B وC ترفع خطر سرطان الكبد بصورة كبيرة. فقد أثبتت دراسة منشورة في مجلة The Lancet Oncology عام 2019 أن العدوى الفيروسية والبكتيرية مسؤولة عن نحو 13% من حالات السرطان الجديدة حول العالم.
⚡ معلومة قد تُدهشك
بكتيريا هيليكوباكتر بيلوري (H. pylori) التي تُسبب قرحة المعدة صُنّفت من قِبل الوكالة الدولية لأبحاث السرطان (IARC) كمادة مسرطنة من الدرجة الأولى (Group 1 Carcinogen)، وترتبط بسرطان المعدة بشكل مباشر.
ما العلامات والأعراض التحذيرية للورم الخبيث؟
إن معرفة أعراض الورم الخبيث المبكرة قد تكون الفارق بين اكتشاف المرض في مرحلة قابلة للعلاج واكتشافه في مرحلة متأخرة. المشكلة أن كثيراً من هذه الأعراض تتشابه مع حالات صحية بسيطة، مما يدفع الناس لتجاهلها.
من الأعراض العامة المبكرة: التعب المستمر غير المبرر الذي لا يتحسن بالراحة. فقدان الوزن المفاجئ دون اتباع حمية أو تغيير في نمط الأكل. الحمى المستمرة أو المتكررة بلا سبب عدوائي واضح. التعرق الليلي الغزير الذي يبلّل الملابس. هذه كلها إشارات تستحق الانتباه.
بالإضافة إلى ذلك، توجد أعراض موضعية تختلف حسب مكان الورم. تغيرات مفاجئة في شامة على الجلد (تغير في اللون أو الحجم أو الشكل) قد تُشير إلى سرطان الجلد. كتلة صلبة غير مؤلمة في الثدي أو الرقبة أو تحت الإبط تستوجب فحصاً فورياً. سعال مزمن يستمر أكثر من ثلاثة أسابيع، خاصة إذا ترافق مع بصق دم، قد يُنذر بسرطان الرئة. تغيرات مستمرة في عادات الإخراج (إسهال أو إمساك مزمن أو دم في البراز) قد تكون علامة على سرطان القولون.
تنويه طبي مهم: لا تعني هذه الأعراض بالضرورة وجود ورم خبيث. لكن استمرارها لأكثر من أسبوعين دون تفسير واضح يستوجب زيارة الطبيب فوراً. إذا ترافقت الأعراض مع نزيف غير مبرر أو ألم شديد مفاجئ أو صعوبة في التنفس أو البلع، فالتوجه إلى الطوارئ ضرورة لا تحتمل التأجيل.
📖 اقرأ أيضاً: سرطان الثدي: دليلك الشامل من التشخيص إلى التعافي
ما أنواع الأورام الخبيثة وكيف تُصنَّف طبياً؟
التصنيف الطبي للأورام الخبيثة يعتمد على نوع النسيج الذي ينشأ منه الورم. هذا التصنيف ليس مجرد تسمية أكاديمية؛ بل يُحدد خطة العلاج والتوقعات المستقبلية (Prognosis) لكل حالة. إليك أبرز أنواع الأورام الخبيثة:
التصنيف الرئيس للأورام الخبيثة
- السرطانات (Carcinomas): تنشأ من الخلايا الظهارية (Epithelial Cells) التي تُبطّن الأعضاء الداخلية وسطح الجلد. تُمثّل النسبة الأكبر من جميع حالات السرطان (نحو 80-90%). تشمل سرطانات الرئة والثدي والقولون والبروستاتا والكلى.
- الساركوما (Sarcomas): تنشأ من الأنسجة الضامة كالعظام والعضلات والغضاريف والأنسجة الدهنية. نادرة نسبياً مقارنة بالسرطانات، لكنها قد تكون عدوانية جداً.
- اللوكيميا (Leukemias): سرطانات تصيب نخاع العظم والدم. لا تُشكّل كتلة صلبة عادةً، بل تظهر كاضطراب في إنتاج خلايا الدم. تُصنَّف إلى أنواع حادة ومزمنة.
- الليمفوما (Lymphomas): سرطانات تصيب الجهاز اللمفاوي. أشهرها ليمفوما هودجكين (Hodgkin Lymphoma) وليمفوما لاهودجكين (Non-Hodgkin Lymphoma).
- المايلوما المتعددة (Multiple Myeloma): تصيب خلايا البلازما في نخاع العظم.
- أورام الدماغ والنخاع الشوكي: مجموعة متنوعة من الأورام التي تنشأ في الجهاز العصبي المركزي. تتميز بصعوبة علاجها بسبب الحاجز الدموي الدماغي (Blood-Brain Barrier) الذي يمنع وصول كثير من الأدوية.
جدول (3): التصنيف الرئيس لأنواع الأورام الخبيثة
| نوع الورم | النسيج الأصلي | أمثلة شائعة | نسبة الشيوع التقريبية |
|---|---|---|---|
| السرطانات (Carcinomas) | الخلايا الظهارية (جلد، أعضاء) | سرطان الرئة، الثدي، القولون، البروستاتا | 80% – 90% |
| الساركوما (Sarcomas) | الأنسجة الضامة (عظام، عضلات، دهون) | ساركوما العظام، ساركوما الأنسجة الرخوة | أقل من 1% |
| اللوكيميا (Leukemias) | نخاع العظم والدم | اللوكيميا النخاعية الحادة (AML)، اللوكيميا اللمفاوية المزمنة (CLL) | حوالي 3.5% |
| الليمفوما (Lymphomas) | الجهاز اللمفاوي | ليمفوما هودجكين، ليمفوما لاهودجكين | حوالي 4% |
| المايلوما (Myeloma) | خلايا البلازما في نخاع العظم | المايلوما المتعددة (Multiple Myeloma) | حوالي 1.8% |
| أورام الجهاز العصبي المركزي | الدماغ والنخاع الشوكي | الورم الأرومي الدبقي (Glioblastoma)، الورم السحائي | حوالي 1.3% |
| المصدر: برنامج SEER – المعهد الوطني الأمريكي للسرطان | المرصد العالمي للسرطان (GLOBOCAN) – IARC/WHO | |||
في المملكة العربية السعودية، تُشير إحصائيات السجل السعودي للأورام إلى أن سرطان القولون والمستقيم وسرطان الثدي من أكثر الأنواع شيوعاً. هذا يُبرز أهمية برامج الفحص المبكر التي تُوسّعها وزارة الصحة باستمرار.
📊 رقم يستحق التأمل
وفقاً للوكالة الدولية لأبحاث السرطان (IARC/WHO)، سُجّلت نحو 20 مليون حالة سرطان جديدة حول العالم في عام 2022 وحده. وتُشير التوقعات إلى أن هذا الرقم قد يتجاوز 35 مليون حالة سنوياً بحلول عام 2050 إذا لم تُتخذ إجراءات وقائية أكثر فعالية.
📖 اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
كيف ينتشر الورم الخبيث في الجسم؟ (النقائل – Metastasis)
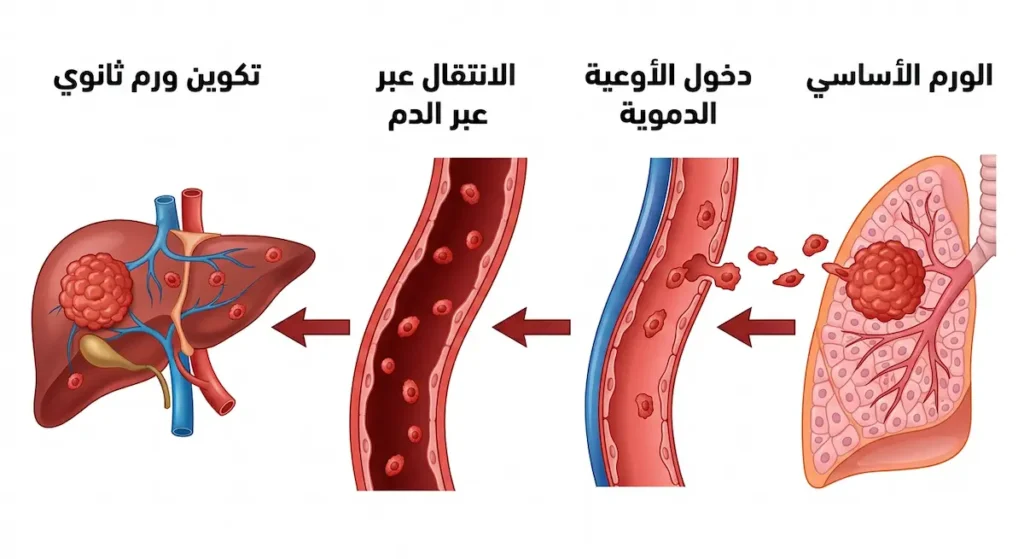
القدرة على الانتشار هي السمة الأخطر التي تُميّز الورم الخبيث عن الحميد. هذه العملية لا تحدث فجأة؛ بل تمر بمراحل معقدة يمكن تبسيطها كالتالي.
تبدأ العملية بمرحلة الغزو المحلي (Local Invasion)؛ إذ تُفرز الخلايا السرطانية إنزيمات خاصة تُذيب الأنسجة المحيطة بها حرفياً، مما يسمح لها بالتسلل إلى المناطق المجاورة. تخيّل جيشاً يحفر أنفاقاً تحت أسوار المدينة المحصنة.
بعد ذلك، تدخل بعض هذه الخلايا إلى الأوعية الدموية أو الأوعية اللمفاوية في ما يُعرف بمرحلة الانتقال (Intravasation). تنتقل الخلايا عبر مجرى الدم أو السائل اللمفاوي كأنها مسافرة في قطار سريع يجوب الجسم بأكمله.
إذاً كيف تستقر هذه الخلايا في أعضاء بعيدة؟ ليست كل خلية سرطانية تنجح في ذلك. الغالبية العظمى تموت في الطريق بسبب مهاجمة الجهاز المناعي لها أو بسبب ظروف ميكانيكية أخرى. لكن عدداً قليلاً منها ينجح في الخروج من الأوعية الدموية (Extravasation) والاستقرار في عضو جديد. الأعضاء الأكثر عرضة لاستقبال النقائل هي الكبد والرئتان والدماغ والعظام، ويعود ذلك جزئياً إلى طبيعة تدفق الدم فيها وخصائص بيئتها الخلوية.
لقد كشفت دراسة منشورة في مجلة Nature Reviews Cancer عام 2020 أن عملية الانتشار ليست عشوائية كما كان يُعتقد سابقاً. بل إن الخلايا السرطانية تُرسل إشارات كيميائية مسبقة إلى الأعضاء المستهدفة لتُهيّئ لها بيئة مناسبة قبل وصولها، في ما يُسمى “المنطقة ما قبل النقيلية” (Pre-metastatic Niche). هذا الاكتشاف فتح أبواباً جديدة لتطوير علاجات تمنع الانتشار قبل حدوثه.
❝
“فهمنا لآلية انتشار السرطان تغيّر جذرياً. لم تعد النقائل حدثاً عشوائياً؛ بل هي عملية منظمة تتطلب من الخلية السرطانية اكتساب برامج جينية محددة للغزو والبقاء في بيئات جديدة.”
— Prof. Robert A. Weinberg، أستاذ علم الأحياء – معهد ماساتشوستس للتكنولوجيا (MIT) ومعهد وايتهيد
ما مراحل الورم الخبيث وكيف تُحدَّد؟
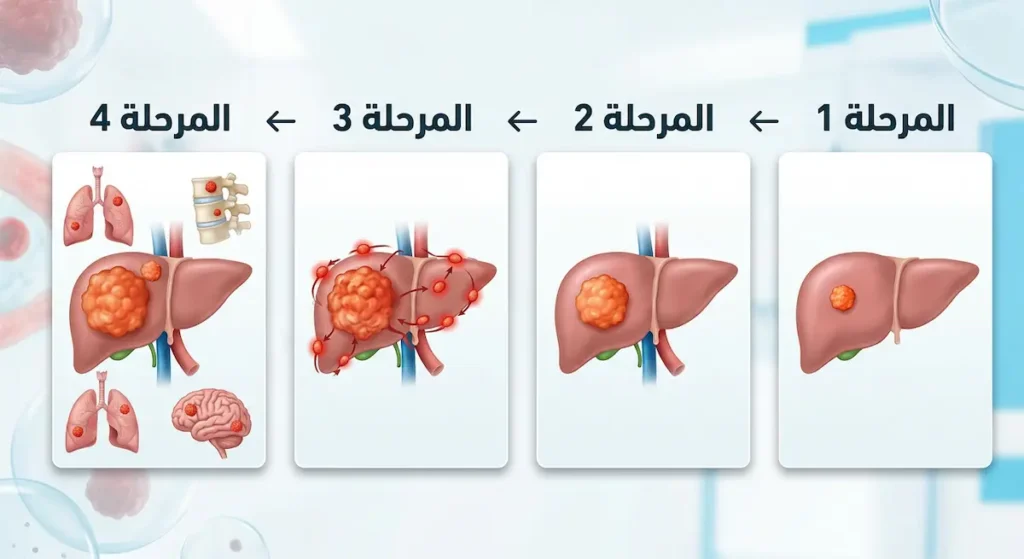
تحديد مرحلة الورم الخبيث (Staging) هو خطوة حاسمة تُحدد خطة العلاج والتوقعات. يعتمد الأطباء عالمياً على نظام TNM الذي وضعته اللجنة الأمريكية المشتركة للسرطان (AJCC).
الحرف T يُشير إلى حجم الورم الأساسي ومدى اختراقه للأنسجة المحيطة. يتدرج من T1 (ورم صغير ومحدود) إلى T4 (ورم كبير اخترق هياكل مجاورة). الحرف N يُشير إلى انتشار المرض في العقد اللمفاوية (Lymph Nodes) القريبة. N0 تعني عدم إصابة أي عقدة، بينما N3 تعني إصابة عدد كبير منها. أما الحرف M فيُشير إلى وجود نقائل بعيدة (Distant Metastasis): M0 تعني عدم وجود انتشار بعيد، وM1 تعني وجوده.
بناءً على هذا النظام، تُقسم مراحل الورم الخبيث بشكل مبسط:
المرحلة 0 (In Situ): خلايا غير طبيعية موجودة لكنها لم تغزُ الأنسجة المحيطة بعد. هذه مرحلة ما قبل السرطان الفعلي. نسبة الشفاء من الورم الخبيث في المرحلة الأولى وما قبلها تتجاوز 95% في كثير من الأنواع.
المرحلة الأولى: ورم صغير محصور في العضو الأصلي دون انتشار للعقد اللمفاوية. التوقعات ممتازة في معظم الحالات.
المرحلة الثانية والثالثة: الورم أكبر حجماً أو انتشر إلى عقد لمفاوية قريبة أو أنسجة مجاورة. العلاج يكون أكثر كثافة لكن الشفاء ممكن.
المرحلة الرابعة: انتشار المرض إلى أعضاء بعيدة. هذه المرحلة الأصعب علاجياً، لكنها ليست حكماً بالإعدام. العلاجات الحديثة مثل العلاج المناعي (Immunotherapy) حسّنت البقاء على قيد الحياة بشكل ملحوظ حتى في هذه المرحلة.
جدول (2): مراحل الورم الخبيث وفق نظام TNM العالمي
| المرحلة | وصف المرحلة | حالة العقد اللمفاوية | الانتشار البعيد | نسبة البقاء التقريبية (5 سنوات)* |
|---|---|---|---|---|
| المرحلة 0 (In Situ) | خلايا شاذة لم تغزُ النسيج المحيط | غير مصابة (N0) | لا يوجد (M0) | أعلى من 95% |
| المرحلة I | ورم صغير محصور في العضو الأصلي | غير مصابة (N0) | لا يوجد (M0) | 80% – 99% |
| المرحلة II | ورم أكبر حجماً أو اخترق أنسجة مجاورة محدودة | غير مصابة أو إصابة محدودة (N0-N1) | لا يوجد (M0) | 60% – 85% |
| المرحلة III | ورم كبير انتشر إلى عقد لمفاوية إقليمية | إصابة متعددة (N1-N3) | لا يوجد (M0) | 30% – 70% |
| المرحلة IV | انتشار المرض إلى أعضاء بعيدة (نقائل) | أي حالة (N0-N3) | موجود (M1) | 5% – 30% (تختلف حسب النوع) |
| * النسب تقريبية وتختلف بشكل كبير حسب نوع السرطان. المصدر: جمعية السرطان الأمريكية (ACS) | اللجنة الأمريكية المشتركة للسرطان (AJCC) | ||||
🔬 لفتة طبية
مصطلح “المرحلة الرابعة” يُثير رعباً شديداً لدى المرضى وذويهم. لكن الواقع الطبي أكثر تعقيداً من تصنيف رقمي بسيط. بعض أنواع السرطان في المرحلة الرابعة تستجيب بشكل ممتاز للعلاجات الحديثة، بينما بعض الأنواع الأخرى قد تكون صعبة حتى في المرحلة الثانية. النوع (Type) لا يقل أهمية عن المرحلة (Stage).
كيف تُشخَّص الأورام الخبيثة بالطرق الحديثة؟
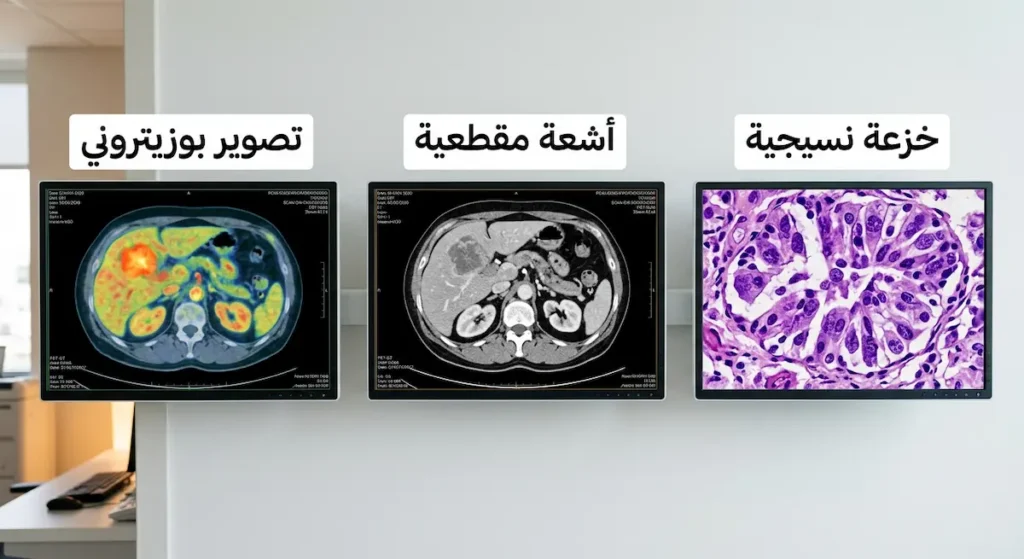
تشخيص الأورام الخبيثة تطور بشكل مذهل خلال العقدين الأخيرين. لم يعد الأمر يعتمد على الفحص السريري وحده؛ بل أصبح يجمع بين أدوات مخبرية وتصويرية ونسيجية متقدمة.
تبدأ الرحلة عادةً بالفحوصات المخبرية، بما فيها تحاليل الدم العامة ودلالات الأورام (Tumor Markers). هذه الدلالات هي مواد كيميائية تُفرزها بعض الأورام في الدم. مثلاً، مستضد البروستاتا النوعي (PSA) يُستخدم في الكشف عن سرطان البروستاتا، ومستضد السرطان 125 (CA-125) يرتبط بسرطان المبيض. لكن يجب التنويه إلى أن هذه الدلالات ليست دقيقة بنسبة 100%؛ فقد ترتفع لأسباب غير سرطانية أيضاً.
من ناحية أخرى، يلعب التصوير الطبي دوراً محورياً. التصوير بالرنين المغناطيسي (MRI) يُقدّم صوراً تفصيلية عالية الدقة للأنسجة الرخوة دون استخدام إشعاع. الأشعة المقطعية (CT Scan) تُوفّر مقاطع عرضية دقيقة وسريعة للجسم. أما التصوير المقطعي بالإصدار البوزيتروني (PET Scan) فيكشف عن النشاط الأيضي المرتفع في الخلايا السرطانية، مما يُساعد في تحديد مواقع الانتشار بدقة. في المراكز الطبية المتقدمة بالسعودية، مثل مستشفى الملك فيصل التخصصي ومركز الأبحاث، تتوفر جميع هذه التقنيات.
لكن الإجراء الفاصل والنهائي لتأكيد التشخيص يبقى الخزعة (Biopsy). يأخذ الطبيب عينة صغيرة من النسيج المشتبه به ويُرسلها لأخصائي الأنسجة المرضية (Histopathologist) الذي يفحصها تحت المجهر. هذا الفحص يُحدد بشكل قاطع ما إذا كانت الخلايا خبيثة أم لا، ويُحدد نوع السرطان ودرجة عدوانيته. وعليه فإن أي تشخيص سرطاني لا يُعتمد طبياً دون تأكيد من الخزعة.
الجدير بالذكر أن تقنية الخزعة السائلة (Liquid Biopsy) بدأت تكتسب زخماً كبيراً في السنوات الأخيرة (2023-2025). هذه التقنية تكشف عن الحمض النووي الورمي المنتشر في الدم (ctDNA) من خلال عينة دم بسيطة، مما قد يُغني في بعض الحالات عن الخزعة النسيجية التقليدية.
جدول (4): أبرز طرق تشخيص الأورام الخبيثة الحديثة
| طريقة التشخيص | آلية العمل | الاستخدام الأمثل | القيود الرئيسة |
|---|---|---|---|
| دلالات الأورام (Tumor Markers) | قياس مواد كيميائية تُفرزها الأورام في الدم | المتابعة وتقييم الاستجابة للعلاج | ليست نوعية 100%؛ قد ترتفع لأسباب غير سرطانية |
| الأشعة المقطعية (CT Scan) | أشعة سينية متعددة الزوايا تُنتج مقاطع عرضية | تحديد موقع الورم وحجمه وانتشاره | تعرض المريض للإشعاع |
| الرنين المغناطيسي (MRI) | مجالات مغناطيسية تُنتج صوراً عالية الدقة | أورام الدماغ والنخاع والأنسجة الرخوة | طويلة الوقت ومكلفة نسبياً |
| PET Scan (التصوير البوزيتروني) | يكشف النشاط الأيضي المرتفع للخلايا السرطانية | تحديد مواقع الانتشار (النقائل) | قد يُعطي نتائج إيجابية كاذبة في حالات الالتهاب |
| الخزعة النسيجية (Biopsy) | أخذ عينة من النسيج وفحصها مجهرياً | التأكيد النهائي للتشخيص وتحديد نوع الورم ودرجته | إجراء جراحي صغير قد يُسبب نزيفاً أو التهاباً محدوداً |
| الخزعة السائلة (Liquid Biopsy) | تحليل الحمض النووي الورمي في عينة دم | المتابعة والكشف المبكر عن عودة المرض | لا تزال قيد التطوير لبعض أنواع السرطان |
| المصدر: المعهد الوطني الأمريكي للسرطان (NCI) – قسم التشخيص | RadiologyInfo.org – الكلية الأمريكية للأشعة (ACR) | |||
🧬 هل تعلم أن
مشروع أبحاث الجينوم السرطاني (TCGA) الذي أنجزه المعهد الوطني الأمريكي للسرطان (NCI) حلّل الخرائط الجينومية لأكثر من 20,000 ورم أساسي و33 نوعاً من السرطان، مما أحدث ثورة في فهم التركيب الجيني للأورام الخبيثة وفتح الباب أمام العلاجات الموجهة جينياً.
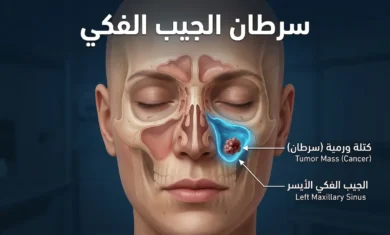
📖 اقرأ أيضاً: سرطان الجيب الفكي: كيف تميّزه عن التهاب الجيوب الأنفية العادي وما فرص الشفاء منه؟
ما الخيارات العلاجية المتاحة للأورام الخبيثة؟
علاج الورم الخبيث لم يعد محصوراً في الخيارات التقليدية الثلاثة (جراحة، كيماوي، إشعاعي). لقد شهد العقد الأخير ثورة حقيقية في البروتوكولات العلاجية المعتمدة، وباتت الخيارات أكثر تنوعاً ودقة.
العلاج الجراحي
يظل الاستئصال الجراحي الخطوة الأولى في كثير من حالات الأورام الصلبة. يمكن أن يكون الاستئصال جذرياً (إزالة العضو كاملاً مع الأنسجة المحيطة) أو جزئياً (إزالة الورم مع هامش أمان من الأنسجة السليمة). التطور في تقنيات الجراحة الروبوتية (Robotic Surgery) والجراحة طفيفة التدخل (Minimally Invasive Surgery) قلّل فترات التعافي بشكل كبير.
العلاج الكيميائي (Chemotherapy)
يعمل عن طريق استهداف الخلايا سريعة الانقسام في الجسم. المشكلة أنه لا يُفرّق بين الخلايا السرطانية والخلايا الطبيعية سريعة الانقسام (كخلايا الشعر والأمعاء ونخاع العظم)، مما يُسبب آثاراً جانبية معروفة كتساقط الشعر والغثيان وانخفاض المناعة. رغم ذلك، يبقى ركيزة أساسية في علاج كثير من أنواع السرطان، خاصة تلك المنتشرة.
العلاج الإشعاعي (Radiation Therapy)
يستخدم حزماً عالية الطاقة من الأشعة لتدمير الحمض النووي للخلايا السرطانية. يُستخدم أحياناً كعلاج وحيد، أو قبل الجراحة لتقليص حجم الورم (Neoadjuvant)، أو بعدها للقضاء على أي بقايا مجهرية (Adjuvant). التقنيات الحديثة مثل العلاج الإشعاعي التجسيمي (Stereotactic Radiation) تُركّز الأشعة بدقة متناهية على الورم مع تقليل الضرر للأنسجة المحيطة.
العلاجات الحديثة والمتقدمة
هنا يكمن التحول الحقيقي في عالم علاج الورم الخبيث:
العلاج الموجه (Targeted Therapy): أدوية تستهدف جزيئات محددة في الخلايا السرطانية دون الإضرار بالخلايا الطبيعية. مثلاً، عقار إيماتينيب (Imatinib) أحدث ثورة في علاج سرطان الدم النخاعي المزمن (CML) برفع نسبة البقاء على قيد الحياة لعشر سنوات من أقل من 30% إلى أكثر من 85%.
العلاج المناعي (Immunotherapy): بدلاً من مهاجمة السرطان مباشرة، يُعيد هذا العلاج تنشيط جهاز المناعة ليتعرف على الخلايا السرطانية ويقضي عليها. أدوية مثبطات نقاط التفتيش المناعية (Immune Checkpoint Inhibitors) مثل بيمبروليزوماب (Pembrolizumab) ونيفولوماب (Nivolumab) غيّرت قواعد اللعبة تماماً في علاج سرطان الرئة والميلانوما وغيرهما. فقد أثبتت دراسة منشورة في مجلة New England Journal of Medicine عام 2022 أن العلاج المناعي المساعد بعد الجراحة في سرطان الكلى قلّل خطر عودة المرض بنسبة 32%.
العلاج الهرموني (Hormonal Therapy): يُستخدم في السرطانات الحساسة للهرمونات مثل بعض أنواع سرطان الثدي وسرطان البروستاتا. يعمل على منع الهرمونات من تحفيز نمو الخلايا السرطانية.
العلاج بالخلايا التائية المُعدّلة (CAR-T Cell Therapy): تقنية ثورية تأخذ خلايا مناعية من المريض نفسه، تُعدّلها جينياً في المختبر لتتعرف على الخلايا السرطانية، ثم تُعاد إلى جسمه. أظهرت نتائج مبهرة في بعض أنواع اللوكيميا والليمفوما.
📋 بروتوكولات طبية رسمية معتمدة (2024–2025)
- الشبكة الوطنية الشاملة للسرطان (NCCN): تُصدر دلائل إرشادية محدّثة دورياً لكل نوع سرطان، وتُعَدُّ المرجع الأول لأطباء الأورام في أمريكا والعالم.
الدلائل الإرشادية – NCCN - الجمعية الأوروبية لطب الأورام (ESMO): تُقدم بروتوكولات أوروبية مُحدّثة لعلاج جميع أنواع الأورام الخبيثة بما فيها العلاج المناعي والموجه.
الدلائل الإرشادية – ESMO - وزارة الصحة السعودية: أطلقت البرنامج الوطني لمكافحة السرطان الذي يشمل بروتوكولات الكشف المبكر والإحالة العلاجية في جميع مناطق المملكة.
وزارة الصحة السعودية - هيئة الصحة بدبي – الإمارات: تتبنى بروتوكولات علاجية متوافقة مع NCCN وESMO في مراكز علاج الأورام الحكومية والخاصة.
هيئة الصحة بدبي (DHA)
الرعاية التلطيفية (Palliative Care)
في الحالات المتقدمة التي لا يكون الشفاء الكامل فيها ممكناً، تلعب الرعاية التلطيفية دوراً جوهرياً. هدفها تخفيف الألم والأعراض وتحسين جودة حياة المريض وأسرته. يجب التأكيد على أن الرعاية التلطيفية ليست مرادفة لـ “الاستسلام”؛ بل هي تخصص طبي متكامل يمكن تقديمه بالتوازي مع العلاجات الشفائية.
جدول (5): ملخص الخيارات العلاجية المعتمدة للأورام الخبيثة
| نوع العلاج | آلية العمل | متى يُستخدم | أبرز الآثار الجانبية |
|---|---|---|---|
| الجراحة (Surgery) | استئصال الورم جراحياً | الأورام الصلبة المحصورة (المراحل المبكرة) | ألم ما بعد العملية، نزيف، عدوى |
| العلاج الكيميائي (Chemotherapy) | أدوية تقتل الخلايا سريعة الانقسام | معظم الأنواع، خاصة المنتشرة | غثيان، تساقط الشعر، انخفاض المناعة |
| العلاج الإشعاعي (Radiation) | حزم طاقة عالية تدمر DNA الخلايا السرطانية | قبل أو بعد الجراحة أو كعلاج مستقل | احمرار الجلد، إرهاق، تليف نسيجي |
| العلاج الموجه (Targeted Therapy) | أدوية تستهدف جزيئات محددة في الخلايا السرطانية | سرطانات ذات طفرات جينية محددة | طفح جلدي، إسهال، مشاكل كبدية |
| العلاج المناعي (Immunotherapy) | تنشيط جهاز المناعة لمحاربة السرطان | سرطان الرئة، الميلانوما، الكلى وغيرها | التهاب المناعة الذاتية، تعب، طفح جلدي |
| العلاج الهرموني (Hormonal Therapy) | منع الهرمونات من تغذية نمو الورم | سرطان الثدي والبروستاتا الحساسين للهرمونات | هبّات حرارة، هشاشة العظام، تغيرات مزاجية |
| CAR-T Cell Therapy | تعديل الخلايا المناعية جينياً لمهاجمة السرطان | بعض أنواع اللوكيميا والليمفوما المقاومة | متلازمة إطلاق السيتوكينات (CRS)، سمية عصبية |
| المصدر: المعهد الوطني الأمريكي للسرطان (NCI) – قسم العلاج | الجمعية الأوروبية لطب الأورام (ESMO) – الدلائل الإرشادية | |||
❝
“أحدث طرق علاج الورم الخبيث بدون كيماوي لم تعد حلماً بعيداً. العلاج المناعي والموجه أصبحا بديلاً حقيقياً في أنواع محددة من السرطان. لكن اختيار البروتوكول المناسب يعتمد على نوع الورم ومرحلته وخصائصه الجزيئية. لذلك أنصح المرضى بمناقشة جميع الخيارات مع فريقهم الطبي قبل اتخاذ أي قرار.”
❝
“العلاج المناعي أعاد كتابة قواعد علاج الأورام. مرضى كانوا يُعتبرون في حالات ميؤوس منها أصبحوا يعيشون سنوات طويلة بفضل مثبطات نقاط التفتيش المناعية. نحن نعيش فعلاً عصراً ذهبياً في طب الأورام.”
— Prof. Alexander M.M. Eggermont، مدير سابق لمعهد غوستاف روسي (Gustave Roussy) – فرنسا
📖 اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
كيف تؤثر التغذية ونمط الحياة على مريض الورم الخبيث؟
لا يمكن الحديث عن رحلة علاج الورم الخبيث دون التطرق إلى الجانب التغذوي والنفسي. فالجسم الذي يخوض معركة ضد السرطان يحتاج إلى دعم شامل يتجاوز الأدوية والعمليات.
العلاج الكيميائي والإشعاعي يُرهقان الجسم ويُضعفان الشهية ويُسببان غثياناً وتقرحات في الفم. في هذه الظروف، يُصبح الحفاظ على تغذية كافية تحدياً حقيقياً. كثير من المرضى يفقدون كتلة عضلية كبيرة أثناء العلاج، مما يُؤثر سلباً على قدرتهم على تحمل الجرعات العلاجية. الهزال السرطاني (Cancer Cachexia) حالة خطيرة تصيب نسبة كبيرة من مرضى المراحل المتقدمة وتُؤثر بشكل مباشر على نتائج العلاج.
❝
“أنصح مرضى الأورام بالتركيز على البروتينات عالية الجودة مثل البيض والدجاج والسمك والبقوليات، لأن الجسم يحتاجها لإعادة بناء الأنسجة المتضررة من العلاج. كما أوصي بتناول وجبات صغيرة ومتكررة بدلاً من ثلاث وجبات كبيرة لتقليل الغثيان. ومن المهم الإكثار من الفواكه والخضروات الغنية بمضادات الأكسدة (Antioxidants) مع تجنب الأطعمة المصنّعة واللحوم المعالجة والسكريات المكررة قدر الإمكان.”
— الدكتورة علا الأحمد، اختصاصية تغذية علاجية
📖 اقرأ أيضاً: البروتين من منظور العلوم التطبيقية: دليلك الشامل لفهم الوظائف الحيوية والاحتياجات اليومية
كما أن الدعم النفسي والأسري يُعَدُّ ركيزة لا يمكن تجاهلها. تشخيص الورم الخبيث يُسبب صدمة نفسية عميقة للمريض وعائلته. الاكتئاب والقلق شائعان بين مرضى السرطان، وقد يُؤثران سلباً على التزامهم بالعلاج واستجابة أجسامهم له. الدعم النفسي المتخصص ومجموعات الدعم وحضور أفراد الأسرة في رحلة العلاج كلها عوامل ثبت علمياً أنها تُحسّن جودة الحياة وربما حتى نتائج العلاج.
في السعودية، تُقدم عدة جمعيات خيرية دعماً متكاملاً لمرضى السرطان، أبرزها جمعية “زهرة” لسرطان الثدي والجمعية السعودية الخيرية لمكافحة السرطان. هذه المبادرات تُسهم في سد فجوة مهمة في رعاية المرضى خارج أسوار المستشفيات.
🏃 معلومة عملية مفيدة
أثبتت دراسة منشورة في مجلة JAMA Oncology عام 2020 أن ممارسة النشاط البدني المعتدل (كالمشي 150 دقيقة أسبوعياً) أثناء علاج السرطان ترتبط بتقليل التعب المرتبط بالعلاج بنسبة تصل إلى 40%، وتحسين جودة النوم والحالة المزاجية بشكل ملحوظ.
📖 اقرأ أيضاً: مضادات الأكسدة (Antioxidants): الوظيفة، المصادر، والفوائد الصحية
هل يمكن الشفاء من الورم الخبيث تماماً؟ نسب الشفاء والإحصائيات الحديثة
هذا هو السؤال الذي يطرحه كل مريض وكل أسرة فور سماع التشخيص. الإجابة المختصرة: نعم، الشفاء الكامل ممكن في كثير من الحالات، لكنه يعتمد بشكل كبير على نوع السرطان ومرحلته عند الاكتشاف ومدى استجابته للعلاج.
لقد تطورت نسب الشفاء بشكل مذهل في العقد الأخير. سرطان الثدي المكتشف في المرحلة الأولى تتجاوز نسبة البقاء خمس سنوات فيه 99% في الولايات المتحدة وفقاً لجمعية السرطان الأمريكية (ACS). سرطان الخصية، حتى في مراحله المتقدمة، يُشفى بنسبة تزيد عن 95%. سرطان الغدة الدرقية تبلغ نسبة الشفاء منه أكثر من 98% في المراحل المبكرة. بالمقابل، تظل بعض الأنواع مثل سرطان البنكرياس المتقدم تُمثّل تحدياً كبيراً، رغم التحسن المستمر في الخيارات العلاجية.
الكشف المبكر هو المفتاح الذهبي. برامج الفحص الدوري مثل الماموغرام لسرطان الثدي، ومنظار القولون لسرطان القولون، ومسحة عنق الرحم (Pap Smear) لسرطان عنق الرحم، أنقذت ملايين الأرواح حول العالم. في السعودية، أطلقت وزارة الصحة مبادرات عديدة لرفع الوعي بأهمية الفحص المبكر، لكن الاستجابة المجتمعية لا تزال بحاجة إلى تعزيز.
الفرق بين الورم الخبيث والسرطان من حيث التسمية لا يُغيّر شيئاً من واقع أن الاكتشاف المبكر يرفع فرص النجاة بشكل هائل. ما هي أول علامات الورم الخبيث في الجسم؟ قد تكون بسيطة كتعب مستمر أو كتلة غير مؤلمة. لكن الانتباه لها مبكراً يصنع فارقاً حقيقياً بين نسب شفاء تتجاوز 90% ونسب أقل بكثير في المراحل المتأخرة.
هذا وقد بدأت تقنيات الذكاء الاصطناعي (AI) تُحدث فارقاً ملموساً في مجال التشخيص المبكر. خوارزميات تحليل صور الأشعة قادرة الآن على اكتشاف أورام دقيقة لا تلتقطها العين المجردة. في عام 2024، نُشرت دراسة في مجلة Nature Medicine أظهرت أن نظام ذكاء اصطناعي تفوّق على أطباء الأشعة في اكتشاف سرطان الرئة في مراحله الأولى بنسبة 11%.
📖 اقرأ أيضاً: الهندسة الوراثية: ما هي وكيف تُغيّر مستقبل البشرية؟
❝
“السرطان ليس مرضاً واحداً بل مئات الأمراض المختلفة. وكل تقدم نُحرزه في فهم البيولوجيا الجزيئية لكل نوع يُقرّبنا خطوة من تحويل هذا المرض القاتل إلى حالة مزمنة يمكن التعايش معها.”
— Prof. Siddhartha Mukherjee، أستاذ الطب – جامعة كولومبيا، حائز على جائزة بوليتزر
الأسئلة الشائعة
اضغط على رمز + لمعرفة الإجابة
❓ أسئلة شائعة حول الورم الخبيث
خاتمة: المعرفة سلاح والكشف المبكر إنقاذ
الورم الخبيث ليس نهاية الطريق. هو تشخيص مخيف بلا شك، لكن المعرفة الدقيقة والتصرف السريع يُحوّلانه من حكم مبهم إلى معركة يمكن كسبها. التقدم الطبي المتسارع يفتح أبواباً جديدة كل عام، والعلاجات التي كانت حلماً قبل عقد أصبحت واقعاً متاحاً اليوم.
لا تؤجّل فحصك الدوري. لا تتجاهل عرضاً مستمراً. لا تخجل من طلب رأي طبي ثانٍ. ولا تنسَ أن الوقاية بنمط حياة صحي، والابتعاد عن التدخين، والحفاظ على وزن متوازن، والنشاط البدني المنتظم، كلها تُقلّل المخاطر بشكل حقيقي ومثبت علمياً.
فهل أجريت فحصك الدوري هذا العام؟
المصادر والمراجع
- Hanahan, D. (2022). Hallmarks of Cancer: New Dimensions. Cancer Discovery, 12(1), 31–46. DOI: 10.1158/2159-8290.CD-21-1059
- تحديث شامل للسمات المميزة للسرطان بما فيها الآليات البيولوجية الحديثة.
- Peinado, H., et al. (2017). Pre-metastatic niches: organ-specific homes for metastases. Nature Reviews Cancer, 17(5), 302–317. DOI: 10.1038/nrc.2017.6
- دراسة مرجعية تشرح كيف تُهيئ الخلايا السرطانية بيئات مسبقة في الأعضاء البعيدة قبل انتقالها.
- Chowell, D., et al. (2022). Improved prediction of immune checkpoint blockade efficacy across multiple cancer types. Nature Biotechnology, 40, 499–506. DOI: 10.1038/s41587-021-01070-8
- بحث حديث حول التنبؤ بفعالية العلاج المناعي في أنواع متعددة من السرطان.
- Sung, H., et al. (2021). Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide. CA: A Cancer Journal for Clinicians, 71(3), 209–249. DOI: 10.3322/caac.21660
- الإحصائيات العالمية الأكثر استشهاداً لأعداد حالات السرطان والوفيات.
- Ardila, D., et al. (2019). End-to-end lung cancer screening with three-dimensional deep learning on low-dose chest computed tomography. Nature Medicine, 25, 954–961. DOI: 10.1038/s41591-019-0447-x
- دراسة رائدة حول استخدام الذكاء الاصطناعي في الكشف المبكر عن سرطان الرئة.
- Choueiri, T.K., et al. (2021). Adjuvant Pembrolizumab after Nephrectomy in Renal-Cell Carcinoma. New England Journal of Medicine, 385, 683–694. DOI: 10.1056/NEJMoa2106391
- دراسة سريرية أثبتت فعالية العلاج المناعي المساعد بعد جراحة سرطان الكلى.
- World Health Organization (WHO). (2024). Global Cancer Burden Growing. https://www.who.int/news/item/01-02-2024-global-cancer-burden-growing
- تقرير منظمة الصحة العالمية حول ارتفاع عبء السرطان عالمياً.
- National Cancer Institute (NCI). (2024). What Is Cancer? https://www.cancer.gov/about-cancer/understanding/what-is-cancer
- شرح مبسط وموثوق من المعهد الوطني الأمريكي للسرطان.
- American Cancer Society (ACS). (2024). Cancer Facts & Figures 2024. https://www.cancer.org/research/cancer-facts-statistics/all-cancer-facts-figures/2024-cancer-facts-figures.html
- التقرير السنوي لجمعية السرطان الأمريكية بالأرقام والإحصائيات المحدثة.
- Centers for Disease Control and Prevention (CDC). (2023). Cancer Screening Tests. https://www.cdc.gov/cancer/screening/index.html
- إرشادات مركز السيطرة على الأمراض حول فحوصات الكشف المبكر.
- Saudi Cancer Registry. (2023). Cancer Incidence Report Saudi Arabia 2019. https://nhic.gov.sa/
- بيانات السجل السعودي للأورام عن أكثر أنواع السرطان شيوعاً في المملكة.
- DeVita, V.T., Lawrence, T.S., & Rosenberg, S.A. (Eds.). (2019).DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (11th ed.). Wolters Kluwer.
- المرجع الأكاديمي الأشمل في طب الأورام، يُغطي التشخيص والعلاج لجميع أنواع السرطان.
- Weinberg, R.A. (2013).The Biology of Cancer (2nd ed.). Garland Science. ISBN: 978-0815342205.
- كتاب مرجعي رئيس في بيولوجيا السرطان على المستوى الجزيئي والخلوي.
- Pecorino, L. (2021).Molecular Biology of Cancer: Mechanisms, Targets, and Therapeutics (5th ed.). Oxford University Press. ISBN: 978-0198833024.
- مرجع أكاديمي يشرح الأسس الجزيئية للسرطان والعلاجات الموجهة الحديثة.
- Mukherjee, S. (2022). “Cancer’s Invasion Equation.” Scientific American. https://www.scientificamerican.com/
- مقال علمي مبسط يشرح آليات انتشار السرطان للقارئ غير المتخصص.
قراءات إضافية مقترحة ومصادر للتوسع
- Vogelstein, B., et al. (2013). Cancer Genome Landscapes. Science, 339(6127), 1546–1558. DOI: 10.1126/science.1235122
- لماذا نقترح عليك قراءته؟ هذه الورقة تُعَدُّ من أمهات المراجع في فهم المشهد الجينومي للسرطان. تشرح كيف أن عدداً محدوداً من الجينات المحركة (Driver Genes) مسؤول عن غالبية الأورام، وهي قراءة أساسية لأي طالب يرغب في فهم الأسس الجزيئية للمرض.
- Mukherjee, S. (2010).The Emperor of All Maladies: A Biography of Cancer. Scribner. ISBN: 978-1439170915.
- لماذا نقترح عليك قراءته؟ هذا الكتاب الحائز على جائزة بوليتزر يروي تاريخ الإنسانية مع السرطان بأسلوب أدبي مشوق. يجمع بين السرد القصصي والعلم الدقيق، وهو مثالي لمن يريد فهم السياق التاريخي والإنساني لهذا المرض.
- Balkwill, F.R., Capasso, M., & Hagemann, T. (2012). The tumor microenvironment at a glance. Journal of Cell Science, 125(23), 5591–5596. DOI: 10.1242/jcs.116392
- لماذا نقترح عليك قراءته؟ ورقة مراجعة مختصرة وعميقة تشرح البيئة المحيطة بالورم (Tumor Microenvironment) ودورها المحوري في نمو السرطان وانتشاره ومقاومته للعلاج. مفيدة جداً لطلاب البيولوجيا الجزيئية والمناعة.
إذا وجدت هذا المقال مفيداً، شاركه مع من تحب. المعلومة الصحيحة قد تُنقذ حياة شخص لا يعلم أن عرضاً بسيطاً يستحق الفحص. ساعدنا في نشر الوعي بأهمية الكشف المبكر في محيطك العائلي والمهني. ولا تتردد في ترك تعليقك أو سؤالك لفريقنا الطبي.
⚠️ إخلاء مسؤولية طبية
المعلومات المنشورة في هذا المقال على موقع موسوعة خلية ذات طابع تثقيفي وتوعوي عام، ولا تُغني بأي حال من الأحوال عن الاستشارة الطبية المتخصصة أو الفحص السريري المباشر. لا تتخذ أي قرار علاجي أو تُوقف أي دواء بناءً على ما قرأته هنا دون مراجعة طبيبك المعالج. كل حالة طبية فريدة وتحتاج إلى تقييم فردي من قبل مختص مؤهل. موسوعة خلية لا تتحمل أي مسؤولية عن سوء استخدام المعلومات الواردة في هذا المحتوى.
🔍 بيان المصداقية
يلتزم موقع موسوعة خلية بأعلى معايير الدقة العلمية والنزاهة التحريرية. يُبنى المحتوى الطبي على مراجع محكّمة منشورة في مجلات علمية مرموقة وتقارير صادرة عن جهات صحية رسمية (WHO، NCI، ACS). تخضع جميع المقالات لمراجعة طبية من قبل مختصين مؤهلين ضمن هيئة التحرير العلمية. لا يتأثر المحتوى بأي اعتبارات تجارية أو إعلانية. نسعى دائماً لتحديث المعلومات وفق أحدث الأدلة العلمية المتاحة.
Medical Review
تمت المراجعة الطبية بواسطة هيئة التحرير العلمية في موسوعة خلية