مرض الهيموفيليا (الناعور): الدليل الطبي الشامل للأسباب، الأنواع، وطرق العلاج الأحدث
لماذا يُسمّى بمرض الملوك وما علاقته بعوامل التخثر في الدم؟

مرض الهيموفيليا (Hemophilia) هو اضطراب وراثي نادر يصيب آلية تخثر الدم نتيجة نقص أو غياب أحد بروتينات التخثر الأساسية. ينتقل عبر الكروموسوم X ويصيب الذكور بصورة رئيسة. يؤدي إلى نزيف مطوّل بعد الإصابات أو نزيف تلقائي في المفاصل والعضلات. تتراوح شدته بين خفيف ومتوسط وشديد حسب مستوى عامل التخثر الناقص.
مراجعة التغذية: د. علا الأحمد — اختصاصية تغذية علاجية
المراجعة الدوائية: جاسم محمد مراد — مستشار دوائي
هيئة التحرير العلمية | آخر تحديث: مارس 2026 | تواصل معنا
هل شهدت يوماً طفلاً صغيراً يسقط أثناء لعبه فتظهر عليه كدمات مبالغ فيها لا تتناسب مع بساطة السقوط؟ أو ربما سمعت عن عائلة فقدت أحد أبنائها بسبب نزيف لم يتوقف بعد عملية بسيطة كخلع ضرس. هذا ليس سيناريو خيالياً بل واقع يعيشه آلاف المرضى حول العالم وفي منطقتنا العربية تحديداً. إن فهمك لهذا المرض قد ينقذ حياة شخص تعرفه، وهذا المقال يضع بين يديك كل ما تحتاجه من معلومات طبية دقيقة ومحدّثة حتى عام 2025.
- الهيموفيليا اضطراب وراثي يمنع تخثر الدم بسبب نقص العامل VIII (النوع A) أو IX (النوع B).
- يصيب الذكور بشكل رئيس وتكون الإناث حاملات للمرض غالباً.
- يوجد ~400,000 مصاب عالمياً و75% منهم لا يتلقون علاجاً كافياً.
- النوع A يُشكّل 80% من الحالات بمعدل إصابة 1 من كل 5,000 ذكر.
- العلاج الوقائي المنتظم يقلّل نزيف المفاصل بنسبة 85%.
- العلاج الجيني (Hemgenix وRoctavian) يُعطى بجرعة واحدة مدى الحياة.
- إيميسيزوماب (Hemlibra) يُحقن تحت الجلد ويصلح لحالات المثبّطات.
- صداع مفاجئ شديد + قيء + تشنجات = اشتباه نزيف دماغي → طوارئ فوراً.
- تجنّب الأسبرين والإيبوبروفين نهائياً — استخدم الباراسيتامول بديلاً آمناً.
- أي إصابة رأس حتى لو بدت بسيطة تستوجب تقييماً طبياً عاجلاً.
ما هو مرض الهيموفيليا وكيف يحدث خلل التخثر؟
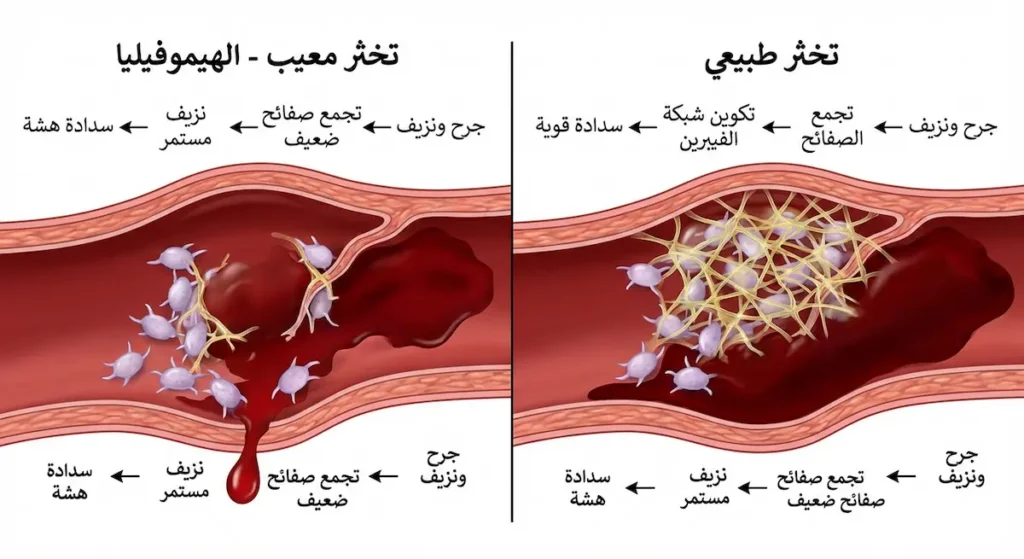
لكي نفهم مرض الهيموفيليا علينا أولاً أن نفهم كيف يوقف الجسم النزيف في الحالة الطبيعية. عندما تجرح إصبعك مثلاً يبدأ الجسم سلسلة معقدة تُسمّى “شلال التخثر” (Coagulation Cascade). تبدأ هذه السلسلة بانقباض الوعاء الدموي المصاب ثم تتجمع الصفائح الدموية (Platelets) في موقع الجرح لتشكّل سدادة مؤقتة. بعدها تتنشط بروتينات التخثر — وعددها ثلاثة عشر عاملاً — بتسلسل دقيق كقطع الدومينو حتى تتكون شبكة من الفيبرين (Fibrin) تُثبّت السدادة وتوقف النزيف نهائياً.
في حالة نزف الدم الوراثي يكون أحد هذه البروتينات ناقصاً أو غائباً تماماً. وعليه فإن شلال التخثر ينقطع عند نقطة محددة ولا يكتمل. النتيجة؟ سدادة الصفائح الدموية تتشكّل لكنها هشّة ولا تُثبَّت. فيستمر النزيف لفترة أطول بكثير من المعتاد. تسمية “مرض الملوك” جاءت لأن المرض انتشر في العائلات الملكية الأوروبية خلال القرنين التاسع عشر والعشرين؛ إذ حملت الملكة فيكتوريا ملكة بريطانيا الطفرة الجينية ونقلتها عبر المصاهرات إلى بيوت ملكية في إسبانيا وروسيا وألمانيا. كما يُعرف المرض باسم “الناعور” في بعض الدول العربية.
الملكة فيكتوريا كانت حاملة لطفرة الهيموفيليا B تحديداً وليس A كما يظن كثيرون. لقد أكّد تحليل جيني أُجري عام 2009 على عظام أفراد من العائلة القيصرية الروسية هذه الحقيقة ونُشر في مجلة Science.
كيف ينتقل مرض الهيموفيليا وراثياً من الآباء إلى الأبناء؟
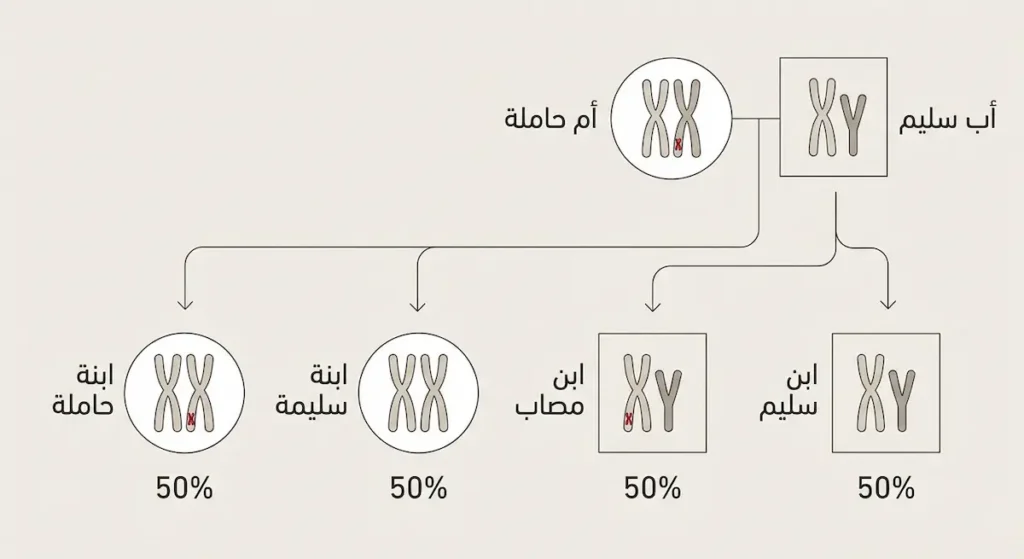
يرتبط مرض الناعور بالكروموسوم الجنسي X ارتباطاً وثيقاً. لدى الذكر كروموسوم جنسي واحد من نوع X وآخر من نوع Y (أي XY)، بينما تحمل الأنثى كروموسومين من نوع X (أي XX). الجين المسؤول عن إنتاج عاملي التخثر الثامن والتاسع يقع على الكروموسوم X. فإذا حمل كروموسوم X الوحيد لدى الذكر طفرة في هذا الجين فلن يوجد كروموسوم X سليم آخر للتعويض، وبالتالي يظهر المرض. أما الأنثى فتحتاج إلى طفرة في كِلا الكروموسومين X لكي تُصاب فعلياً.
لهذا السبب يُصاب الذكور بمرض الهيموفيليا بنسبة أعلى بكثير بينما تكون الإناث في الغالب حاملات للمرض (Carriers) دون أعراض واضحة. لكن هل يمكن للأنثى أن تُصاب حقاً؟ نعم، في حالات نادرة جداً: حين يكون الأب مصاباً والأم حاملة للطفرة، أو في حالة تعطّل أحد كروموسومي X (ظاهرة تُعرف بـ Skewed X-inactivation)، أو في متلازمة تيرنر (Turner Syndrome) حين تملك الأنثى كروموسوم X واحداً فقط.
اقرأ أيضاً: علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
الهيموفيليا المكتسبة: حين يهاجم الجسم نفسه
ثمة شكل آخر من المرض لا علاقة له بالوراثة يُسمّى الهيموفيليا المكتسبة (Acquired Hemophilia). يحدث هذا الشكل حين ينتج الجهاز المناعي أجساماً مضادة تهاجم عوامل التخثر — غالباً العامل الثامن — وتُبطل عملها. يظهر عادةً عند كبار السن أو بعد الولادة أو مع أمراض المناعة الذاتية وبعض أنواع السرطان. إنه نادر جداً بمعدل حالة واحدة لكل مليون شخص سنوياً، لكن خطورته تكمن في أنه يُفاجئ المريض دون سابق إنذار عائلي.
“أنصح كل عائلة لديها تاريخ مرضي بنزيف الدم الوراثي بإجراء فحوصات جينية للأبناء مبكراً، لأن التشخيص المبكر يُغيّر مسار حياة الطفل كلياً ويحميه من مضاعفات خطيرة كتلف المفاصل الدائم.”
ما الفرق بين الهيموفيليا أ وب وهل يوجد نوع ثالث؟

الهيموفيليا A: النوع الكلاسيكي
يُعَدُّ هذا النوع الأكثر شيوعاً ويُشكّل نحو 80% من جميع الحالات. ينتج عن نقص أو خلل في عامل التخثر الثامن (Factor VIII). تُقدّر منظمة الصحة العالمية (WHO) أن نسبة الإصابة تبلغ حالة واحدة من كل 5,000 مولود ذكر. تتراوح الأعراض بين نزيف بسيط عند الإصابات وبين نزيف تلقائي شديد حسب مستوى العامل الثامن في الدم.
الهيموفيليا B: داء كريسماس
سُمّي بهذا الاسم نسبة إلى ستيفن كريسماس (Stephen Christmas)، أول مريض شُخِّص رسمياً بهذا النوع عام 1952 وليس نسبة إلى عيد الميلاد كما يظن البعض. ينتج عن نقص عامل التخثر التاسع (Factor IX) ويُشكّل نحو 15-20% من الحالات بمعدل حالة واحدة لكل 25,000 مولود ذكر. أعراضه مطابقة تقريباً لأعراض النوع A ولا يمكن التفريق بينهما سريرياً دون تحاليل مخبرية دقيقة.
الهيموفيليا C: النوع النادر
هذا النوع ينتج عن نقص العامل الحادي عشر (Factor XI) ويختلف جوهرياً عن النوعين السابقين. فهو لا يرتبط بالكروموسوم X بل يُورَّث بنمط جسدي صبغي متنحٍّ (Autosomal Recessive)؛ أي أنه يصيب الذكور والإناث بالتساوي. كما أنه أخف وطأة في معظم الحالات ونادراً ما يسبب نزيفاً تلقائياً. ينتشر بصورة أكبر بين يهود الأشكناز.
| وجه المقارنة | الهيموفيليا A | الهيموفيليا B | الهيموفيليا C |
|---|---|---|---|
| الاسم الشائع | الهيموفيليا الكلاسيكية | داء كريسماس | نقص العامل XI |
| العامل الناقص | العامل الثامن (VIII) | العامل التاسع (IX) | العامل الحادي عشر (XI) |
| نمط الوراثة | مرتبط بالكروموسوم X | مرتبط بالكروموسوم X | جسدي صبغي متنحٍّ |
| نسبة الانتشار | ~80% من الحالات | ~15-20% من الحالات | نادر جداً |
| معدل الإصابة | 1 من كل 5,000 ذكر | 1 من كل 25,000 ذكر | 1 من كل 100,000 |
| الجنس المصاب | الذكور بشكل رئيس | الذكور بشكل رئيس | الذكور والإناث بالتساوي |
| شدة النزيف | خفيف إلى شديد | خفيف إلى شديد | خفيف غالباً |
| النزيف التلقائي | شائع في الحالات الشديدة | شائع في الحالات الشديدة | نادر جداً |
| العلاج الأساسي | تعويض العامل VIII أو Emicizumab | تعويض العامل IX | بلازما طازجة مجمّدة |
| المصادر: الاتحاد العالمي للهيموفيليا (WFH) | مراكز السيطرة على الأمراض والوقاية منها (CDC) | |||
الفرق بين الهيموفيليا أ وب لا يمكن تحديده إلا مخبرياً عبر تحليل مقايسة عوامل التخثر (Factor Assays). فالأعراض السريرية متشابهة تماماً لكن العلاج يختلف لأن كل نوع يحتاج تعويض عامل تخثر مختلف.
كيف تُصنَّف درجات شدة مرض الناعور؟
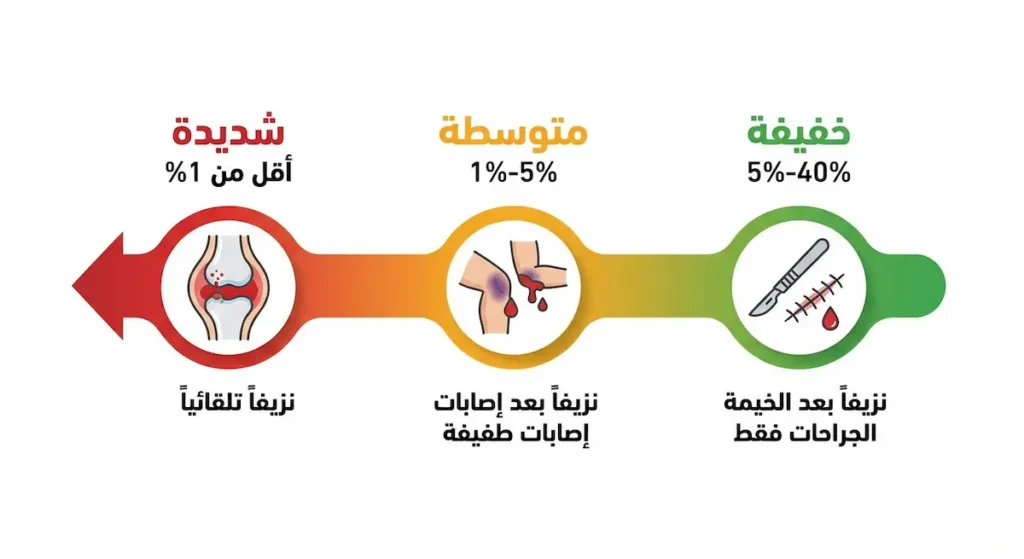
تعتمد شدة أعراض الهيموفيليا على نسبة عامل التخثر الموجود في الدم مقارنةً بالمعدل الطبيعي. الشخص السليم لديه مستوى عامل تخثر يتراوح بين 50% و150% من المعدل الطبيعي.
- الهيموفيليا الخفيفة (Mild): مستوى العامل بين 5% و40%. لا يعاني المريض من نزيف تلقائي لكنه يواجه نزيفاً مفرطاً بعد الجراحات أو إصابات الحوادث الكبيرة. قد لا يُكتشف المرض إلا بالصدفة عند إجراء عملية جراحية لأول مرة.
- الهيموفيليا المتوسطة (Moderate): مستوى العامل بين 1% و5%. يحدث نزيف بعد إصابات طفيفة نسبياً، وقد يظهر نزيف تلقائي نادر. هذه الفئة تحتاج متابعة دورية في مراكز الهيموفيليا المتخصصة.
- الهيموفيليا الشديدة (Severe): مستوى العامل أقل من 1%. يُعاني المريض من نزيف تلقائي متكرر دون إصابة واضحة خاصة في المفاصل والعضلات. هذه الفئة هي الأكثر حاجةً للعلاج الوقائي المنتظم.
| الدرجة | مستوى العامل | نمط النزيف | وقت الاكتشاف المعتاد | الحاجة للعلاج الوقائي |
|---|---|---|---|---|
| خفيفة (Mild) | 5% – 40% | نزيف مفرط بعد الجراحات والصدمات الكبرى فقط | عند إجراء أول عملية جراحية أو خلع أسنان | غير مطلوب عادةً |
| متوسطة (Moderate) | 1% – 5% | نزيف بعد إصابات طفيفة، ونزيف تلقائي نادر | في مرحلة الطفولة المبكرة | قد يكون مطلوباً |
| شديدة (Severe) | أقل من 1% | نزيف تلقائي متكرر في المفاصل والعضلات | في السنة الأولى من العمر غالباً | ضروري ومنتظم |
| المصدر: الاتحاد العالمي للهيموفيليا (WFH) — إرشادات إدارة الهيموفيليا 2020 | ||||
في المملكة العربية السعودية يُقدَّر عدد المصابين بالهيموفيليا بنحو 3,000 إلى 4,000 مريض مسجّل وفق بيانات الجمعية السعودية لأمراض الدم. وقد شهدت المملكة تطوراً ملحوظاً في إنشاء مراكز متخصصة لعلاج اضطرابات النزيف في مدن مثل الرياض وجدة والدمام.
اقرأ أيضاً: الإحصاءات الصحية: البيانات، الأساليب، والتطبيقات
ما أبرز أعراض الهيموفيليا وعلاماتها التحذيرية؟
أعراض الهيموفيليا عند الأطفال الرضع
لقد تبيّن أن بعض حالات مرض الهيموفيليا تُكتشف في الساعات الأولى بعد الولادة. من أبرز العلامات المبكرة: نزيف مستمر بعد عملية الختان لا يتوقف بالطرق التقليدية، وظهور ورم دموي تحت فروة الرأس (Cephalohematoma) بعد الولادة الطبيعية، وكدمات واسعة وغير مبررة حين يبدأ الطفل بالزحف أو محاولة الوقوف. في بعض الحالات الخفيفة قد لا تظهر أعراض واضحة حتى سنّ المدرسة.
اقرأ أيضاً: طب الأطفال (Pediatrics): التخصص، الأمراض، والرعاية
الأعراض الشائعة عند الأطفال والبالغين
تشمل الأعراض الشائعة رعافاً (Epistaxis) متكرراً يصعب إيقافه، ونزيفاً مطوّلاً من الجروح الصغيرة، وظهور كدمات عميقة وكبيرة بعد صدمات بسيطة جداً. كما قد يلاحظ المريض وجود دم في البول (Hematuria) أو البراز. من ناحية أخرى فإن نزيف اللثة المفرط عند تنظيف الأسنان يُعَدُّ من العلامات المهمة التي يتجاهلها كثيرون.
لماذا يُعَدُّ نزيف المفاصل أخطر مضاعفات الهيموفيليا؟

نزيف المفاصل — أو ما يُعرف طبياً بـ “التهاب المفصل النزفي” (Hemarthrosis) — هو العَرَض الأكثر تأثيراً على جودة حياة مرضى الهيموفيليا الشديدة. يحدث حين يتسرب الدم إلى تجويف المفصل، خاصة الركبتين والمرفقين والكاحلين. يبدأ المريض بالشعور بوخز أو حرارة داخل المفصل قبل أن يتورّم ويصبح مؤلماً وصعب الحركة.
ما يجعل هذا الأمر كارثياً هو التراكم. فكل نوبة نزيف داخل المفصل تُسبب تلفاً طفيفاً في الغضروف والغشاء الزليلي (Synovial Membrane). ومع تكرار النوبات يتطور ما يُسمّى “اعتلال المفاصل الهيموفيلي” (Hemophilic Arthropathy) الذي يُشبه التهاب المفاصل التنكّسي المتقدّم ويؤدي في نهاية المطاف إلى تشوّه المفصل وفقدان وظيفته. لقد أثبتت دراسة منشورة في مجلة Haemophilia عام 2020 أن نحو 90% من مرضى الهيموفيليا الشديدة الذين لا يتلقون علاجاً وقائياً يُصابون بتلف مفصلي دائم قبل سن الثلاثين.
رئيسة قسم الهيموفيليا — مستشفى رويال فري، لندن
“الوقاية من اعتلال المفاصل الهيموفيلي يجب أن تبدأ في السنوات الأولى من حياة الطفل. كل نوبة نزيف داخل المفصل تُحدث ضرراً تراكمياً لا رجعة فيه، والعلاج الوقائي المبكر هو الفارق بين مفصل سليم ومفصل مشوّه.”
مثال تطبيقي من الواقع: تخيّل أن طفلاً اسمه سعد يبلغ ستّ سنوات ومصاب بهيموفيليا شديدة من النوع A. استيقظ ذات صباح يشكو من ألم في ركبته اليسرى دون أن يكون قد سقط أو تعرّض لأي إصابة. لاحظت والدته أن الركبة بدأت تتورّم وأصبحت دافئة عند اللمس. هذا هو النزيف التلقائي داخل المفصل. الخطوة الأولى التي يجب أن تقوم بها الأم: تثبيت المفصل وعدم تحريكه ووضع كمّادة باردة ثم إعطاء الطفل جرعة عامل التخثر الثامن فوراً إن كانت متوفرة في المنزل والتوجه إلى المستشفى. التأخر ساعات قليلة في العلاج قد يعني الفرق بين مفصل سليم ومفصل متضرر بشكل دائم.
وفقاً للاتحاد العالمي للهيموفيليا (WFH) يوجد نحو 400,000 شخص مصاب بالهيموفيليا حول العالم، لكن 75% منهم لا يتلقون علاجاً كافياً أو لم يُشخَّصوا أصلاً خاصة في الدول النامية.
متى يجب التوجه إلى الطوارئ فوراً عند مريض الهيموفيليا؟
ثمة أعراض تُعَدُّ “أعلاماً حمراء” (Red Flags) تستوجب التوجه الفوري إلى قسم الطوارئ دون أي تردد. أخطرها على الإطلاق: علامات النزيف الدماغي. فما هي هذه العلامات؟ صداع مفاجئ وشديد غير معتاد، قيء متكرر لا يرتبط بالطعام، تشنّجات، ازدواجية في الرؤية أو ضعف مفاجئ في أحد جانبي الجسم، وتغيّر في مستوى الوعي أو نعاس شديد غير مبرر. النزيف الدماغي يُعَدُّ السبب الأول للوفاة عند مرضى الهيموفيليا الشديدة.
من جهة ثانية يجب الذهاب للطوارئ إذا استمر نزيف من جرح ولم يتوقف رغم الضغط المباشر لأكثر من عشرين دقيقة. كذلك إذا ظهر تورّم سريع في الرقبة أو الحلق؛ لأن النزيف في هذه المنطقة قد يضغط على مجرى الهواء ويسبب الاختناق. بالإضافة إلى ذلك فإن أي إصابة مباشرة في الرأس — حتى لو بدت بسيطة — تستدعي تقييماً طبياً عاجلاً عند مريض الهيموفيليا.
| العلامة التحذيرية | الموقع المحتمل للنزيف | مستوى الخطورة |
|---|---|---|
| صداع مفاجئ شديد غير معتاد | نزيف دماغي | حرج — مهدد للحياة |
| قيء متكرر مع تشنجات أو ازدواجية الرؤية | نزيف دماغي | حرج — مهدد للحياة |
| تورّم سريع في الرقبة أو الحلق | نزيف في مجرى الهواء | حرج — خطر اختناق |
| نزيف مستمر لا يتوقف رغم الضغط لأكثر من 20 دقيقة | أي موقع | عالي الخطورة |
| أي إصابة مباشرة في الرأس حتى لو بدت بسيطة | نزيف دماغي محتمل | عالي الخطورة |
| تغيّر مفاجئ في الوعي أو نعاس غير مبرر | نزيف دماغي | حرج — مهدد للحياة |
| المصدر: المؤسسة الوطنية للهيموفيليا (NHF) — توصيات MASAC | ||
اقرأ أيضاً: الإنعاش القلبي الرئوي (CPR): متى وكيف يتم تطبيقه؟
كيف يتم تشخيص الهيموفيليا بدقة وما التحاليل المطلوبة؟
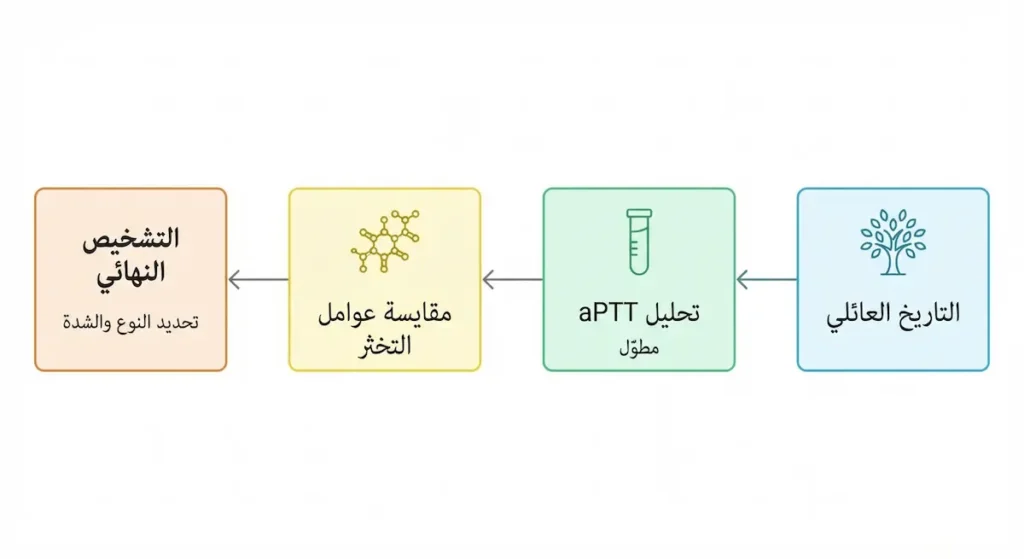
يبدأ تشخيص نزف الدم الوراثي بالتاريخ الطبي العائلي. هل يوجد أقارب ذكور عانوا من نزيف مفرط؟ هل توفي أحدهم بسبب نزيف بعد عملية جراحية؟ هذه الأسئلة توجّه الطبيب نحو الاشتباه بالمرض.
بعد ذلك تأتي مرحلة الفحوصات المخبرية. يُجري الطبيب أولاً تحاليل دم عامة تشمل: تعداد الدم الكامل (CBC) الذي يكون طبيعياً عادةً في الهيموفيليا، وزمن البروثرومبين (Prothrombin Time – PT) الذي يكون طبيعياً أيضاً لأنه يقيس المسار الخارجي للتخثر. أما الاختبار الأهم فهو زمن الثرومبوبلاستين الجزئي المُفعَّل (Activated Partial Thromboplastin Time – aPTT) الذي يكون مطوّلاً لأنه يقيس المسار الداخلي للتخثر حيث يعمل العاملان الثامن والتاسع.
إذاً كيف نحدد النوع والشدة بالتحديد؟ يتم ذلك عبر تحليل مقايسة عوامل التخثر (Factor Assays) الذي يقيس مستوى كل عامل على حدة في الدم. فإذا كان العامل الثامن منخفضاً فالتشخيص هيموفيليا A، وإذا كان التاسع منخفضاً فالتشخيص هيموفيليا B. النسبة المئوية للعامل تحدد درجة الشدة كما ذكرنا سابقاً.
كما أن الفحوصات الجينية (Genetic Testing) أصبحت متاحة وتُستخدم لتأكيد التشخيص وتحديد نوع الطفرة بدقة، وهذا مفيد جداً للاستشارة الوراثية وتحديد الإناث الحاملات في العائلة. في السعودية تتوفر هذه الفحوصات في مراكز متخصصة مثل مستشفى الملك فيصل التخصصي ومركز الأبحاث بالرياض.
“من أكثر الأخطاء شيوعاً التي أراها في الصيدلية السريرية هو وصف أدوية مضادة للالتهاب غير الستيرويدية (NSAIDs) كالإيبوبروفين لمرضى الهيموفيليا دون الانتباه إلى أنها تُثبّط وظائف الصفائح الدموية وتزيد خطر النزيف. البديل الآمن هو الباراسيتامول (الأسيتامينوفين).”
اقرأ أيضاً: مسكنات الألم: ما أنواعها وكيف تعمل في الجسم؟
ما أحدث بروتوكولات علاج مرض الهيموفيليا المتاحة اليوم؟
العلاج التعويضي: العمود الفقري لعلاج النزيف
يقوم العلاج التعويضي (Replacement Therapy) على حقن عامل التخثر الناقص وريدياً. يتوفر بصورتين: مشتقّات بلازما الدم البشري المنقّى، ومنتجات مُصنَّعة عبر تقنية الحمض النووي المؤتلف (Recombinant) التي لا تعتمد على بلازما بشرية وبالتالي تكون أكثر أماناً من حيث العدوى الفيروسية.
يُعطى العلاج التعويضي بأسلوبين. الأول “حسب الحاجة” (On-demand) حين يحدث نزيف فعلي. الثاني هو العلاج الوقائي (Prophylaxis) الذي يُعطى بانتظام — عادة كل يومين أو ثلاثة — لمنع النزيف قبل حدوثه. لقد أثبتت دراسة محورية نُشرت في مجلة New England Journal of Medicine عام 2007 أن العلاج الوقائي يقلّل عدد نوبات نزيف المفاصل بنسبة تصل إلى 85% مقارنة بالعلاج حسب الحاجة.
أستاذ طب أمراض الدم للأطفال — جامعة ميشيغان، الولايات المتحدة
“العلاج الجيني لا يعني نهاية الهيموفيليا بعد، لكنه يمثّل أول مرة في التاريخ يستطيع فيها مريض الهيموفيليا الشديدة أن يعيش أشهراً دون حقنة واحدة. نحتاج إلى متابعة طويلة الأمد لفهم ديمومة الاستجابة، لكن النتائج الأولية مشجعة للغاية.”
أدوية التخثر البديلة
دواء ديزموبريسين (Desmopressin – DDAVP) يُستخدم في حالات الهيموفيليا A الخفيفة فقط. يعمل هذا الدواء على تحفيز إفراز مخزون العامل الثامن من بطانة الأوعية الدموية. يُعطى بالرذاذ الأنفي أو الحقن الوريدي قبل الإجراءات الجراحية البسيطة أو عند حدوث نزيف طفيف. على النقيض من ذلك لا يفيد هذا الدواء في الهيموفيليا B ولا في الحالات الشديدة من النوع A.
أما أدوية حفظ التخثر المعروفة باسم مضادات انحلال الفيبرين (Antifibrinolytics) مثل حمض الترانيكساميك (Tranexamic Acid) وحمض الأمينوكابرويك (Aminocaproic Acid) فتعمل على منع تحلّل الخثرة بعد تكوّنها. تُستخدم كعلاج مساعد خاصة في نزيف الفم واللثة وبعد إجراءات طب الأسنان.
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
الثورة الحقيقية: العلاج الجيني للهيموفيليا
هذا هو الجزء الأكثر إثارة في عالم علاج الهيموفيليا اليوم. العلاج الجيني (Gene Therapy) يهدف إلى إدخال نسخة سليمة من الجين المعيب إلى خلايا كبد المريض باستخدام ناقل فيروسي مُعدَّل (Adeno-Associated Virus – AAV). بمجرد وصول الجين السليم إلى خلايا الكبد يبدأ الجسم في إنتاج عامل التخثر بنفسه دون الحاجة لحقن خارجية.
في عام 2022 وافقت وكالة الأدوية الأوروبية (EMA) على أول علاج جيني للهيموفيليا B وهو عقار Hemgenix (etranacogene dezaparvovec) الذي تُصنّعه شركة CSL Behring. يُعطى بجرعة وريدية واحدة فقط مدى الحياة. بلغ سعر هذا العلاج 3.5 مليون دولار للجرعة الواحدة ليصبح أغلى دواء في التاريخ. لكن التحليلات الاقتصادية أظهرت أنه قد يوفّر المال على المدى الطويل مقارنة بتكلفة العلاج التعويضي المستمر طوال حياة المريض.
كذلك حصل عقار Roctavian (valoctocogene roxaparvovec) على موافقة لعلاج الهيموفيليا A الشديدة. أظهرت نتائج التجارب السريرية المنشورة في مجلة NEJM عام 2022 أن المرضى الذين تلقوا هذا العلاج انخفض معدل النزيف السنوي لديهم بنسبة 85% تقريباً واستغنى كثير منهم عن العلاج التعويضي المنتظم لسنوات.
من جهة ثانية يجب التنويه إلى أن العلاج الجيني لا يزال في مراحله الأولى ولا يناسب جميع المرضى. المرضى الذين لديهم أجسام مضادة للفيروس الناقل (AAV) لا يستفيدون من العلاج. كما أن فعالية العلاج قد تتراجع تدريجياً مع مرور السنوات عند بعض المرضى. لكنه يمثّل بلا شك نقلة نوعية تبشّر بمستقبل قد يتحرر فيه المرضى من الحقن المتكررة.
اقرأ أيضاً: الهندسة الوراثية: ما هي وكيف تُغيّر مستقبل البشرية؟
| العلاج | آلية العمل | طريقة الإعطاء | تكرار الجرعات | النوع المستهدف |
|---|---|---|---|---|
| العلاج التعويضي (Factor Replacement) | تعويض العامل الناقص مباشرة | حقن وريدي | كل 2-3 أيام (وقائي) أو عند النزيف | A و B |
| إيميسيزوماب (Emicizumab) | يقلّد وظيفة العامل VIII | حقن تحت الجلد | أسبوعياً أو كل أسبوعين أو شهرياً | A فقط (بما فيها حالات المثبّطات) |
| ديزموبريسين (DDAVP) | يحفّز إفراز مخزون العامل VIII | رذاذ أنفي أو وريدي | عند الحاجة | A الخفيفة فقط |
| Fitusiran | يثبّط مضاد الثرومبين لتعزيز التخثر | حقن تحت الجلد | مرة شهرياً | A و B (بما فيها حالات المثبّطات) |
| العلاج الجيني (Gene Therapy) | إدخال جين سليم لخلايا الكبد | حقنة وريدية واحدة | جرعة واحدة مدى الحياة | A الشديدة (Roctavian) و B (Hemgenix) |
| المصادر: إدارة الغذاء والدواء الأمريكية (FDA) | وكالة الأدوية الأوروبية (EMA) | ||||
عقار إيميسيزوماب (Emicizumab) — الذي يُباع تحت الاسم التجاري Hemlibra — لا يحتوي على عامل تخثر ثامن على الإطلاق! بل هو جسم مضاد ثنائي الخصوصية (Bispecific Antibody) يعمل كجسر يربط بين العاملين IXa وX ويقلّد وظيفة العامل الثامن. يُعطى بالحقن تحت الجلد أسبوعياً أو نصف شهرياً بدلاً من الحقن الوريدي المتكرر. لقد غيّر هذا الدواء حياة مرضى الهيموفيليا A بمن فيهم أولئك الذين طوّروا أجساماً مضادة (Inhibitors) ضد العامل الثامن.
ما المضاعفات التي يسببها مرض الهيموفيليا وكيف نتجنبها؟
أخطر المضاعفات طويلة الأمد هو تلف المفاصل الدائم الذي تحدثنا عنه سابقاً. لكن ثمة مضاعفة أخرى تؤرق الأطباء وهي تكوين الأجسام المضادة المثبّطة (Inhibitors). تحدث هذه المشكلة حين يتعرّف الجهاز المناعي على عامل التخثر المحقون ويعتبره جسماً غريباً فينتج أجساماً مضادة تُبطل مفعوله. تظهر هذه المضاعفة لدى نحو 25-30% من مرضى الهيموفيليا A الشديدة و3-5% من مرضى الهيموفيليا B.
إذاً كيف يُعالَج هؤلاء المرضى؟ يُستخدم بروتوكول يُسمّى “تحمّل المناعة” (Immune Tolerance Induction – ITI) يقوم على إعطاء جرعات عالية ومتكررة من عامل التخثر على مدار أشهر أو سنوات لإقناع الجهاز المناعي بالتوقف عن إنتاج المثبّطات. تنجح هذه الطريقة في نحو 60-80% من الحالات.
أما العدوى الفيروسية فقد كانت كارثة حقيقية في ثمانينيات وتسعينيات القرن العشرين حين أُصيب آلاف مرضى الهيموفيليا بفيروس نقص المناعة البشرية (HIV) والتهاب الكبد C عبر منتجات الدم الملوّثة. لقد كانت تلك مأساة طبية بكل المقاييس. لكن اليوم أصبحت عمليات فحص وتنقية منتجات الدم دقيقة للغاية ومنتجات العامل المؤتلف لا تعتمد على بلازما بشرية أصلاً. وعليه فإن خطر العدوى الفيروسية أصبح شبه معدوم مع المنتجات الحديثة.
مدير برنامج اضطرابات التخثر — مستشفى الأطفال في لوس أنجلوس، جامعة جنوب كاليفورنيا
“تكوين المثبّطات يظل التحدي الأكبر الذي يواجهنا في علاج الهيموفيليا A الشديدة. لكن ظهور أدوية مثل Emicizumab وFitusiran أعطانا خيارات لم تكن موجودة قبل عشر سنوات، وأعتقد أن الجيل القادم من مرضى الهيموفيليا سيعيش حياة مختلفة جذرياً.”
في المملكة العربية السعودية أُنشئ البرنامج الوطني لعلاج الهيموفيليا تحت مظلة وزارة الصحة ويتضمن توفير عوامل التخثر مجاناً للمرضى المسجّلين وبرامج رعاية منزلية تُمكّن الأسر من حقن العلاج في المنزل بعد تدريب متخصص. هذا البرنامج ساهم بشكل ملحوظ في تقليل حالات الطوارئ وتحسين جودة حياة المرضى.
اقرأ أيضاً: الاقتصاد السعودي: كيف تحول من الاعتماد على النفط إلى التنويع الشامل؟
كيف يتعايش مريض الهيموفيليا مع حياته اليومية؟

التعايش مع مرض الناعور يتطلب وعياً والتزاماً لكنه لا يعني التوقف عن الحياة. إن مرضى الهيموفيليا الذين يتلقون علاجاً وقائياً منتظماً يستطيعون أن يعيشوا حياة قريبة جداً من الطبيعية.
من الناحية الغذائية ينصح الأطباء بنظام غذائي متوازن يحافظ على وزن صحي؛ لأن السمنة تزيد الضغط على المفاصل وتفاقم اعتلال المفاصل الهيموفيلي. الأطعمة الغنية بالحديد مهمة لتعويض ما يُفقد مع نوبات النزيف المتكررة. كما أن الأطعمة الغنية بفيتامين K مثل الخضروات الورقية الداكنة تدعم عملية التخثر بشكل عام رغم أن نقص فيتامين K ليس هو سبب الهيموفيليا.
“أنصح مرضى الهيموفيليا بالتركيز على مصادر الحديد الحيواني كالكبد واللحم الأحمر مع تناول فيتامين C من الحمضيات لتعزيز امتصاص الحديد. كذلك يجب الحذر من الإفراط في تناول المكملات مثل زيت السمك (أوميغا 3) بجرعات عالية لأنها قد تزيد سيولة الدم.”
اقرأ أيضاً: الدليل الطبي الشامل: كل ما تحتاج معرفته عن أحماض أوميغا 3 الدهنية
أما الرياضة فهي ليست ممنوعة كلياً بل هي ضرورية. الرياضات منخفضة التأثير كالسباحة والمشي وركوب الدراجة الثابتة تُقوّي العضلات المحيطة بالمفاصل وتحميها من النزيف. على النقيض من ذلك يجب تجنّب الرياضات العنيفة والالتحامية كالملاكمة وكرة القدم والمصارعة لأنها تحمل خطراً عالياً للإصابة والنزيف.
العناية بصحة الأسنان أمر لا يُستهان به. تسوّس الأسنان وأمراض اللثة المتقدمة قد تستوجب خلعاً أو جراحة فموية وهي إجراءات تحمل مخاطر نزيف عالية لمرضى الهيموفيليا. لذلك فإن الوقاية بتنظيف الأسنان بالفرشاة الناعمة واستخدام الخيط بلطف وزيارة طبيب الأسنان بانتظام كل ستة أشهر هي خطوات حاسمة.
كذلك يُنصح كل مريض بحمل بطاقة هوية طبية (Medical ID) أو سوار تعريفي يوضّح تشخيصه ونوع الهيموفيليا وشدتها وفصيلة دمه والأدوية التي يجب تجنبها. هذه البطاقة قد تُنقذ حياته إذا فقد الوعي ولم يستطع التواصل مع فريق الطوارئ.
اقرأ أيضاً: المكملات الغذائية: الأنواع، الفوائد، والمخاطر
احرص على إبلاغ أي طبيب أسنان أو جرّاح بتشخيصك قبل أي إجراء حتى لو كان بسيطاً كحشو ضرس. فالتنسيق المسبق مع طبيب أمراض الدم لتحضير جرعة عامل التخثر الوقائية يمنع مفاجآت النزيف غير المتوقع.
ما أهمية الاستشارة الوراثية في الزواج لمن يحمل جين الهيموفيليا؟
تُعَدُّ الاستشارة الوراثية (Genetic Counseling) خطوة بالغة الأهمية لأي شخص لديه تاريخ عائلي بمرض الهيموفيليا. في المملكة العربية السعودية أصبح فحص ما قبل الزواج إلزامياً منذ عام 2004 وإن كان يركّز أساساً على الثلاسيميا وفقر الدم المنجلي. لكن الأسر التي تحمل تاريخاً مع نزف الدم الوراثي يجب أن تطلب فحوصات جينية إضافية.
لنتأمل هذا السيناريو: إذا كانت المرأة حاملة للطفرة (أي لديها كروموسوم X سليم وآخر يحمل الطفرة) وتزوّجت رجلاً سليماً فإن احتمالات الإنجاب تكون كالتالي: كل ابن ذكر لديه نسبة 50% للإصابة بالهيموفيليا و50% أن يكون سليماً تماماً. أما كل بنت فلديها 50% أن تكون حاملة و50% أن تكون سليمة. فما هي الخيارات المتاحة أثناء الحمل؟ يمكن إجراء فحص الزغابات المشيمية (CVS) في الأسبوع 11-14 من الحمل أو بزل السائل الأمنيوسي (Amniocentesis) في الأسبوع 15-20 لمعرفة جنس الجنين وفحص وجود الطفرة.
كما أن تقنية التشخيص الجيني قبل الانغراس (PGD) أصبحت متاحة في مراكز الإخصاب المساعد المتقدمة؛ إذ تسمح باختيار الأجنة السليمة قبل زراعتها في رحم الأم. هذه التقنية تُقدّم حلاً للعائلات التي تريد تجنّب نقل المرض لأبنائها.
اقرأ أيضاً: ما هي الوراثة السائدة: وكيف تنتقل الصفات من جيل لآخر؟
ما الجديد في أبحاث الهيموفيليا عام 2025؟
يشهد مجال علاج اضطرابات النزيف تطورات متسارعة. بالإضافة إلى العلاج الجيني الذي ذكرناه تُجرى حالياً تجارب سريرية على عوامل تخثر جديدة ذات عمر نصفي مطوّل (Extended Half-Life) تسمح بتقليل عدد مرات الحقن. مثلاً عامل التخثر التاسع المعدّل بتقنية ربط الألبومين (Albumin Fusion) يُعطى مرة واحدة كل أسبوعين بدلاً من مرتين أسبوعياً.
هذا وقد أظهرت دراسة منشورة في مجلة Blood عام 2023 نتائج واعدة لعلاج Fitusiran وهو جسم مضاد يستهدف بروتين مضاد الثرومبين (Antithrombin) لتقليل تثبيط التخثر. يُعطى بالحقن تحت الجلد مرة شهرياً ويصلح لكلا نوعي الهيموفيليا A وB بما فيها الحالات المصحوبة بأجسام مضادة مثبّطة.
أما على صعيد تقنية كريسبر (CRISPR-Cas9) لتعديل الجينات فلا تزال الأبحاث قبل السريرية جارية لتصحيح الطفرة مباشرة في خلايا الكبد. النتائج الأولية في النماذج الحيوانية مُبشّرة لكن التطبيق البشري يحتاج سنوات إضافية من البحث والتحقق من الأمان.
في القرن التاسع عشر كان الراهب الروسي راسبوتين يُزعم أنه “يُشفي” الأمير أليكسي — ابن القيصر نيقولا الثاني — من نوبات نزيف الهيموفيليا عبر الصلاة والتنويم. يعتقد بعض المؤرخين الطبيين أن سرّ “نجاحه” كان ببساطة أنه كان يمنع الأطباء من إعطاء الطفل الأسبرين — الذي كان يُستخدم كمسكّن شائع آنذاك — وهو مضاد لتخثر الدم يزيد النزيف سوءاً!
اقرأ أيضاً: مميعات الدم: ما هي وكيف تعمل في جسمك؟
| وجه المقارنة | العلاج التعويضي التقليدي | العلاج الجيني |
|---|---|---|
| المبدأ | تعويض العامل الناقص من مصدر خارجي | تمكين الجسم من إنتاج العامل بنفسه |
| عدد الجرعات | عشرات إلى مئات الحقن سنوياً | جرعة واحدة مدى الحياة |
| طريقة الإعطاء | حقن وريدي متكرر | حقنة وريدية واحدة |
| التكلفة السنوية التقديرية | $150,000 – $300,000 سنوياً | ~$3,500,000 لمرة واحدة |
| مدة الفعالية | ساعات إلى أيام لكل جرعة | سنوات (قيد المتابعة طويلة الأمد) |
| خطر تكوين مثبّطات | 25-30% في الهيموفيليا A الشديدة | لم يُبلَّغ عنه حتى الآن |
| التوفر العالمي | متوفر في معظم الدول | محدود جداً (مراكز متخصصة فقط) |
| تأثيره على جودة الحياة | تحسّن كبير لكن مع عبء الحقن المتكرر | تحرر شبه كامل من العلاج الروتيني |
| المصادر: مجلة NEJM — دراسة HOPE-B 2023 | إدارة الغذاء والدواء الأمريكية (FDA) | ||
ما التحديات الخاصة بمرضى الهيموفيليا في العالم العربي؟
تواجه رعاية مرضى الهيموفيليا في المنطقة العربية تحديات متعددة. ففي بعض الدول لا تتوفر عوامل التخثر بشكل مستمر بسبب تكلفتها العالية. كما أن وصمة المرض الوراثي تجعل بعض العائلات تتردد في إجراء الفحوصات الجينية أو الإفصاح عن التشخيص.
في المقابل حققت دول مثل السعودية والإمارات والأردن تقدماً ملحوظاً في إنشاء سجلات وطنية للمرضى وتدريب فرق طبية متخصصة. الجمعية السعودية للهيموفيليا تنشط في تنظيم فعاليات توعوية بالتزامن مع اليوم العالمي للهيموفيليا في 17 أبريل من كل عام. لكن الفجوة بين الدول العربية لا تزال واسعة والحاجة ملحّة لتحسين الوصول إلى العلاجات الحديثة في الدول الأقل دخلاً.
الجدير بالذكر أن برنامج المساعدات الإنسانية التابع للاتحاد العالمي للهيموفيليا (WFH) يقدّم عوامل تخثر مجانية لعدد من الدول النامية والعربية منها. لكن هذه المساعدات لا تُغطي سوى جزء بسيط من الاحتياج الفعلي.
اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
- إرشادات الاتحاد العالمي للهيموفيليا (WFH) — الإصدار الثالث 2020: الدليل الإرشادي الأشمل عالمياً لتشخيص وعلاج وإدارة الهيموفيليا بجميع أنواعها.
- توصيات MASAC — المؤسسة الوطنية للهيموفيليا (NHF) 2024: تحديثات سنوية حول أحدث العلاجات المعتمدة وبروتوكولات الطوارئ.
- إدارة الغذاء والدواء الأمريكية (FDA) — قائمة منتجات الدم المعتمدة 2024: تشمل العلاجات الجينية المعتمدة حديثاً (Hemgenix وRoctavian).
- وزارة الصحة السعودية — البرنامج الوطني لعلاج الهيموفيليا: يوفّر عوامل التخثر مجاناً للمرضى المسجّلين مع برامج رعاية منزلية.
الأسئلة الشائعة
اضغط على السؤال لتعرف الإجابة
خاتمة
إن مرض الهيموفيليا رغم كونه حالة مزمنة لا شفاء نهائياً منها بعد — باستثناء الآمال الواعدة للعلاج الجيني — إلا أنه لم يعد حكماً بالعجز أو الموت المبكر كما كان قبل عقود. التشخيص المبكر والعلاج الوقائي المنتظم والوعي الأسري حوّلوا حياة آلاف المرضى من معاناة يومية إلى حياة شبه طبيعية. لقد تغيّر متوسط العمر المتوقع لمرضى الهيموفيليا الشديدة من أقل من عشرين سنة في الستينيات إلى أكثر من ستين سنة اليوم في الدول التي توفّر رعاية متكاملة.
المعرفة سلاحك الأول. شارك هذه المعلومات مع من حولك فقد تُحدث فارقاً في حياة طفل لم يُشخَّص بعد.
هل أجريت فحوصات ما قبل الزواج الموسّعة التي تشمل اضطرابات النزيف الوراثية؟
إذا كنت أنت أو أحد أفراد عائلتك مصاباً بمرض الهيموفيليا أو تشتبه في ذلك فلا تتردد في التواصل مع أقرب مركز متخصص في أمراض الدم. اطلب من طبيبك إحالتك لاستشارة وراثية وابدأ بتسجيل نفسك في السجل الوطني لمرضى الهيموفيليا في بلدك. هذه الخطوة البسيطة قد تفتح لك باب الحصول على أحدث العلاجات المتاحة مجاناً أو بتكلفة مدعومة.
اقرأ أيضاً: متلازمة انحلال الدم اليوريمية: ما الذي يحدث حين تتحول عدوى بسيطة إلى تهديد للكلى؟
المعلومات الواردة في هذا المقال على موسوعة خلية مُعدّة لأغراض تثقيفية وتوعوية فقط، ولا تُغني بأي حال عن استشارة طبيب مختص أو أخصائي أمراض دم. لا تبدأ أو توقف أو تُعدّل أي علاج دوائي دون إشراف طبي مباشر. إذا كنت تعاني من أعراض نزيف غير طبيعي أو تشتبه في إصابتك بمرض الهيموفيليا، فتوجّه إلى أقرب مرفق صحي فوراً. موسوعة خلية لا تتحمل أي مسؤولية قانونية أو طبية عن سوء استخدام المعلومات المنشورة.
جرت مراجعة هذا المقال من قبل هيئة التحرير العلمية في موسوعة خلية لضمان الدقة والمعلومة الصحيحة. تستند جميع المعلومات إلى مصادر طبية موثّقة تشمل دراسات محكّمة من مجلات عالمية (NEJM, The Lancet, Blood) وتقارير رسمية من منظمات دولية (WHO, CDC, FDA, WFH). تمت المراجعة الطبية بواسطة د. زيد مراد (اختصاصي طب عام)، ومراجعة المحتوى التغذوي بواسطة د. علا الأحمد (اختصاصية تغذية علاجية)، والمراجعة الدوائية بواسطة جاسم محمد مراد (مستشار دوائي). آخر تحديث: مارس 2026.
المصادر والمراجع
الدراسات والأوراق البحثية
- Manco-Johnson, M. J., et al. (2007). Prophylaxis versus episodic treatment to prevent joint disease in boys with severe hemophilia A. New England Journal of Medicine, 357(6), 535-544.
https://doi.org/10.1056/NEJMoa067659
دراسة محورية أثبتت تفوق العلاج الوقائي على العلاج حسب الحاجة في منع تلف المفاصل. - Mahlangu, J., et al. (2023). Fitusiran prophylaxis in people with haemophilia A or B (ATLAS-A/B and ATLAS-INH): results of two randomised, multicentre, phase 3 trials. The Lancet Haematology, 10(5), e322-e332.
https://doi.org/10.1016/S2352-3026(23)00037-6
نتائج تجارب المرحلة الثالثة لعقار Fitusiran كعلاج وقائي جديد. - Pipe, S. W., et al. (2023). Gene therapy with etranacogene dezaparvovec for hemophilia B. New England Journal of Medicine, 388(8), 706-718.
https://doi.org/10.1056/NEJMoa2211644
دراسة HOPE-B التي أدت لاعتماد أول علاج جيني للهيموفيليا B. - Ozelo, M. C., et al. (2022). Valoctocogene roxaparvovec gene therapy for severe hemophilia A. New England Journal of Medicine, 386(11), 1013-1025.
https://doi.org/10.1056/NEJMoa2113708
نتائج العلاج الجيني Roctavian للهيموفيليا A الشديدة. - Oldenburg, J., et al. (2020). Emicizumab prophylaxis in hemophilia A with inhibitors. Haemophilia, 26(4), 571-579.
https://doi.org/10.1111/hae.14003
دراسة عن فعالية إيميسيزوماب في المرضى ذوي الأجسام المضادة المثبّطة. - Iorio, A., et al. (2019). Establishing the prevalence and prevalence at birth of hemophilia in males: a meta-analytic approach using national registries. Annals of Internal Medicine, 171(8), 540-546.
https://doi.org/10.7326/M19-1208
تحليل تلوي يحدد معدلات انتشار الهيموفيليا عالمياً.
الجهات الرسمية والمنظمات
- World Federation of Hemophilia (WFH). (2024). Annual Global Survey 2023.
https://www.wfh.org/en/data-collection
التقرير السنوي لأعداد مرضى الهيموفيليا المسجّلين عالمياً. - National Hemophilia Foundation (NHF). MASAC Recommendations.
https://www.hemophilia.org/healthcare-professionals/guidelines-on-care/masac-documents
إرشادات اللجنة الاستشارية الطبية والعلمية لعلاج الهيموفيليا. - Centers for Disease Control and Prevention (CDC). (2024). Hemophilia: Data & Statistics.
https://www.cdc.gov/hemophilia/data-research/index.html
إحصائيات ومعلومات رسمية عن الهيموفيليا من مراكز السيطرة على الأمراض. - World Health Organization (WHO). (2024). Genomics and World Health: Haemophilia.
https://www.who.int/health-topics/haemophilia
الموقف الرسمي لمنظمة الصحة العالمية تجاه الهيموفيليا. - U.S. Food and Drug Administration (FDA). (2022). FDA Approves First Gene Therapy for Hemophilia B.
https://www.fda.gov/news-events/press-announcements/fda-approves-first-gene-therapy-treat-adults-hemophilia-b
بيان الموافقة على أول علاج جيني للهيموفيليا B.
الكتب والموسوعات العلمية
- Hoffman, R., et al. (2022). Hematology: Basic Principles and Practice (8th ed.). Elsevier.
المرجع الأكاديمي الأشهر في أمراض الدم ويتضمن فصولاً مفصلة عن اضطرابات التخثر. - Kaushansky, K., et al. (2021). Williams Hematology (10th ed.). McGraw-Hill Education.
موسوعة ويليامز لأمراض الدم — المرجع الطبي الأكثر شمولاً في هذا التخصص. - Lee, C. A., Berntorp, E., & Hoots, W. K. (2021). Textbook of Hemophilia (4th ed.). Wiley-Blackwell.
https://doi.org/10.1002/9781119423997
كتاب متخصص حصرياً في الهيموفيليا ويُعَدُّ المرجع الأول في هذا المجال.
مقالات علمية مبسطة
- Scientific American. (2023). Gene Therapy Is Poised to Transform Hemophilia Treatment.
https://www.scientificamerican.com/article/gene-therapy-hemophilia/
مقال مبسّط عن ثورة العلاج الجيني في تغيير مستقبل مرضى الهيموفيليا.
قراءات إضافية ومصادر للتوسع
- Mannucci, P. M., & Tuddenham, E. G. D. (2001). The Hemophilias — From Royal Genes to Gene Therapy. New England Journal of Medicine, 344(23), 1773-1779.
https://doi.org/10.1056/NEJM200106073442307
لماذا نقترح عليك قراءته؟ هذه المراجعة الكلاسيكية تروي القصة الكاملة لمرض الهيموفيليا من اكتشافه في العائلات الملكية وصولاً إلى بدايات أبحاث العلاج الجيني. مثالية لمن يريد فهم السياق التاريخي والعلمي معاً. - Srivastava, A., et al. (2020). WFH Guidelines for the Management of Hemophilia, 3rd edition. Haemophilia, 26(S6), 1-158.
https://doi.org/10.1111/hae.14046
لماذا نقترح عليك قراءته؟ هذه الإرشادات الشاملة من الاتحاد العالمي للهيموفيليا تُعَدُّ “دستور” علاج المرض عالمياً وتغطي كل جانب من التشخيص والعلاج والتأهيل في أكثر من 150 صفحة. - Berntorp, E., et al. (2021). Haemophilia. Nature Reviews Disease Primers, 7, Article 45.
https://doi.org/10.1038/s41572-021-00278-x
لماذا نقترح عليك قراءته؟ مراجعة حديثة من سلسلة Nature Reviews تقدّم نظرة شاملة ومحدّثة على كل ما يتعلق بالهيموفيليا من الآلية الجزيئية إلى العلاجات المستقبلية، وهي مثالية لطلاب الطب والباحثين الراغبين في التعمّق.

