سرطان الثدي: دليلك الشامل من التشخيص إلى التعافي
كيف تواجهين المرض وتتخذين القرارات الصحيحة في كل مرحلة؟

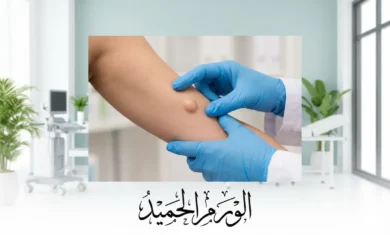
سرطان الثدي هو نمو خبيث غير منضبط ينشأ في خلايا أنسجة الثدي، غالباً في بطانة القنوات اللبنية (Milk Ducts) أو الفصيصات الغدية (Lobules). يمثّل هذا المرض أكثر أنواع السرطان شيوعاً لدى النساء عالمياً، ويصيب نحو 2.3 مليون امرأة سنوياً وفق تقديرات منظمة الصحة العالمية لعام 2024. يتفاوت مساره بين بطيء النمو وشديد العدوانية، والاكتشاف المبكر يرفع نسب الشفاء إلى ما يتجاوز 90%.
✓ مقالة مُراجَعة طبياً
المراجعة الطبية: د. زيد مراد — اختصاصي طب عام
مراجعة التغذية: د. علا الأحمد — اختصاصية تغذية علاجية
المراجعة الدوائية: جاسم محمد مراد — مستشار دوائي
اعتمدتها: هيئة التحرير العلمية | آخر تحديث: مارس 2026
لديكِ سؤال؟ تواصلي معنا
هل لاحظتِ يوماً تغيراً صغيراً في ثديكِ ثم ترددتِ طويلاً قبل أن تسألي طبيبكِ عنه؟ ربما أحسستِ بكتلة بحجم حبة العدس فتجاهلتِها، أو رأيتِ تغيراً في جلد الثدي فأقنعتِ نفسكِ أنه أمر عابر. هذا التردد طبيعي ومفهوم تماماً. لكنّ ما ستقرئينه هنا سيمنحكِ المعرفة التي تحوّل القلق إلى فعل، والخوف إلى قرار واعٍ. لقد جمعنا في هذا المقال أحدث المعلومات الطبية المراجعة من أطباء مختصين، مع إحصائيات محدثة حتى عام 2025، لنقدم لكِ خريطة واضحة تبدأ من فهم المرض وتنتهي بالتعافي. لا تبحثي في عشرات الصفحات المتفرقة؛ كل ما تحتاجينه موجود أمامكِ الآن.
🔑 خلاصة المقال في دقيقة واحدة
🎯 حقائق جوهرية
- سرطان الثدي هو الأكثر شيوعاً عالمياً بين النساء: 2.3 مليون إصابة سنوياً.
- 5% إلى 10% فقط من الحالات مرتبطة بطفرات وراثية (BRCA1/BRCA2)، والباقي ناتج عن عوامل مكتسبة.
- نسبة الشفاء في المرحلة الأولى تتجاوز 99% — الاكتشاف المبكر ينقذ الحياة فعلاً.
✅ خطوات عملية الآن
- أجري الفحص الذاتي شهرياً بعد انتهاء الدورة الشهرية بـ 3-5 أيام.
- ابدئي الماموجرام السنوي من سن 40 (أو قبل ذلك إن كان لديكِ تاريخ عائلي).
- حافظي على وزن صحي، وامشي 150 دقيقة أسبوعياً، وقللي السكريات المصنعة.
⚡ تطورات علاجية حديثة
- عقار T-DXd (Enhertu) وسّع العلاج الموجه ليشمل فئة HER2-low لأول مرة (2022-2024).
- العلاج المناعي (Pembrolizumab) أصبح معياراً لسرطان الثدي ثلاثي السلبية.
- مثبطات CDK4/6 غيّرت قواعد علاج السرطان الهرموني المتقدم.
⚠️ تحذير طبي
- أي كتلة جديدة أو تغير في الثدي يستوجب زيارة الطبيب خلال أسبوعين — لا تنتظري.
- احمرار الثدي المفاجئ مع تورم قد يكون سرطاناً التهابياً وليس التهاباً عادياً.
مثال تطبيقي من الواقع:
سارة، معلمة في الرياض عمرها 38 عاماً، كانت تستحم حين لاحظت كتلة صغيرة صلبة تحت جلد ثديها الأيسر. لم تشعر بألم. انتظرت أسبوعين ظناً أنها مرتبطة بالدورة الشهرية، لكنّ الكتلة لم تختفِ. قررت زيارة طبيبتها التي طلبت صورة ماموجرام (Mammogram) ثم موجات فوق صوتية (Ultrasound). أظهرت النتائج كتلة مشبوهة بقطر 1.2 سم. أُخذت خزعة بالإبرة (Core Needle Biopsy)، وجاء التقرير: سرطان قنوي غازٍ في المرحلة الأولى (Stage I Invasive Ductal Carcinoma)، إيجابي لمستقبلات الهرمونات. خضعت سارة لاستئصال جزئي مع علاج إشعاعي وهرموني. اليوم، بعد ثلاث سنوات، تعيش حياة طبيعية تماماً. ما أنقذ سارة ليس الحظ، بل قرارها بعدم التأجيل.
ما هو سرطان الثدي وكيف يبدأ؟
كيف يبدو تشريح الثدي من الداخل؟
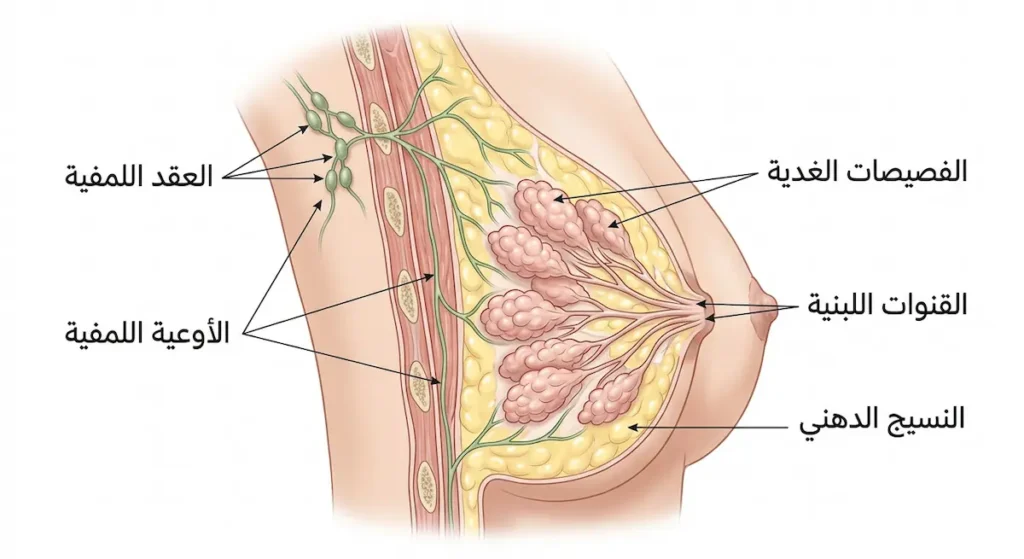
يتكون الثدي من ثلاثة مكونات رئيسة. أولاً، الفصيصات الغدية (Lobules) التي تنتج الحليب. ثانياً، القنوات اللبنية (Ducts) التي تنقل الحليب إلى الحلمة. ثالثاً، النسيج الضام والدهني (Connective and Fatty Tissue) الذي يملأ الفراغات ويمنح الثدي شكله. كذلك يحتوي الثدي على أوعية دموية وأوعية لمفية (Lymphatic Vessels) متصلة بعقد لمفية (Lymph Nodes) تقع تحت الإبط وخلف عظمة القص وفوق الترقوة.
فهم هذا التركيب مهم لأنه يفسّر لماذا ينتشر المرض أحياناً إلى مناطق بعيدة. الأوعية اللمفية تعمل كطرق سريعة قد تحمل الخلايا السرطانية إلى أجزاء أخرى من الجسم إذا لم يُكتشف الورم مبكراً.
اقرأ أيضاً: علم التشريح (Anatomy): دراسة بنية الكائنات الحية
كيف تتحول الخلايا السليمة إلى خلايا سرطانية؟
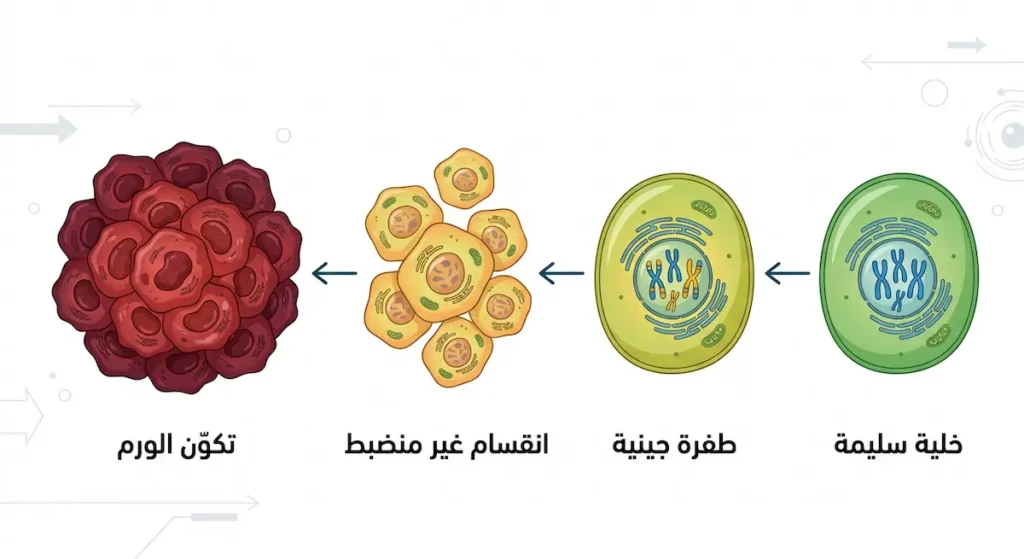
كل خلية في جسمكِ تحمل شفرة وراثية (DNA) تتحكم في نموها وانقسامها وموتها المبرمج (Apoptosis). حين تحدث طفرات في جينات معينة تنظم هذه العمليات، تفقد الخلية قدرتها على التوقف عن الانقسام. بدلاً من أن تموت في موعدها الطبيعي، تستمر في التكاثر دون ضابط.
مع مرور الوقت، تتراكم هذه الخلايا الشاذة مكوّنة كتلة تُسمى ورماً (Tumor). ليس كل ورم خبيثاً بالضرورة؛ إذ قد يكون حميداً (Benign) ولا يغزو الأنسجة المجاورة. لكن حين تكتسب الخلايا القدرة على اختراق الأغشية القاعدية (Basement Membrane) والانتقال عبر الدم أو اللمف، يصبح الورم خبيثاً وغازياً (Invasive Malignant Tumor). هذا التحول لا يحدث بين عشية وضحاها. في معظم الحالات، يستغرق سنوات طويلة قبل أن يصل الورم إلى حجم يمكن اكتشافه سريرياً.
💡 حقيقة طبية مدهشة
يحتاج الورم عادةً إلى الانقسام نحو 30 مرة قبل أن يصل إلى حجم 1 سم — وهو أصغر حجم يمكن تحسسه يدوياً — وهذا قد يستغرق ما بين 2 إلى 10 سنوات حسب سرعة نمو الخلايا. لذلك فإن الكشف المبكر عن سرطان الثدي عبر الماموجرام يكشف الورم قبل أن تشعري به بيدكِ بكثير.
المصدر: المعهد الوطني للسرطان (NCI)
ما هي أعراض سرطان الثدي ومتى يجب عليكِ زيارة الطبيب؟
ما هي الأعراض المبكرة جداً التي قد يتم تجاهلها؟
كثير من النساء يظنّنَّ أن سرطان الثدي يبدأ دائماً بكتلة واضحة. هذا ليس صحيحاً في كل الحالات. فقد تظهر أعراض مبكرة خفية للغاية:
- تغير طفيف في ملمس جلد الثدي، كخشونة تشبه قشرة البرتقال (Peau d’orange) في منطقة صغيرة.
- إفراز شفاف أو مدمى من الحلمة دون ضغط عليها.
- انكماش أو انقلاب مفاجئ في الحلمة لم يكن موجوداً من قبل.
- عدم تناظر مستجد بين الثديين في الحجم أو الشكل.
- شعور بثقل أو شد في ثدي واحد دون سبب واضح.
هذه الأعراض لا تعني بالضرورة وجود ورم خبيث، لكنها تستوجب زيارة الطبيب دون تأخير.
“أنصح كل امرأة تلاحظ أي تغيّر جديد في ثديها — مهما بدا بسيطاً — بتسجيل ملاحظاتها وزيارة الطبيب خلال أسبوعين على الأكثر. الاكتشاف المبكر يختصر رحلة العلاج بشكل لا يُصدَّق.”
— د. زيد مراد، اختصاصي طب عام
ما هي الأعراض المتقدمة؟
حين يتأخر التشخيص، تصبح العلامات أكثر وضوحاً. قد تظهر كتلة صلبة غير مؤلمة في معظم الأحيان، مع تورم في العقد اللمفية تحت الإبط. من الممكن أيضاً أن يتغير لون جلد الثدي إلى الاحمرار أو يصبح سميكاً ومتيبساً. في المراحل الأكثر تقدماً، قد تظهر تقرحات جلدية على سطح الثدي لا تلتئم. كما أن الألم — رغم أنه ليس من الأعراض الأولى عادةً — قد يظهر حين يضغط الورم على الأعصاب المحيطة أو حين يغزو جدار الصدر.
لماذا يستحق سرطان الثدي الالتهابي اهتماماً خاصاً؟
سرطان الثدي الالتهابي (Inflammatory Breast Cancer — IBC) نوع نادر لكنه شديد العدوانية. لا يظهر عادةً ككتلة واضحة، بل يتجلى باحمرار منتشر وتورم سريع في الثدي مع ارتفاع حرارة الجلد، مما يجعله يُشبه التهاباً عادياً (Mastitis). هذا الشبه الخادع يتسبب أحياناً في تأخر التشخيص لأسابيع أو أشهر.
الجدير بالذكر أن هذا النوع يمثل نحو 1% إلى 5% من جميع حالات أورام الثدي الخبيثة، لكنه ينتشر بسرعة لأن الخلايا السرطانية تسد الأوعية اللمفية في الجلد. إذا وصف لكِ الطبيب مضاداً حيوياً لعلاج “التهاب” مشتبه ولم تتحسن الحالة خلال أسبوع، فاطلبي فحصاً إضافياً فوراً.
ما الفرق بين أعراض ورم الثدي الحميد والخبيث؟
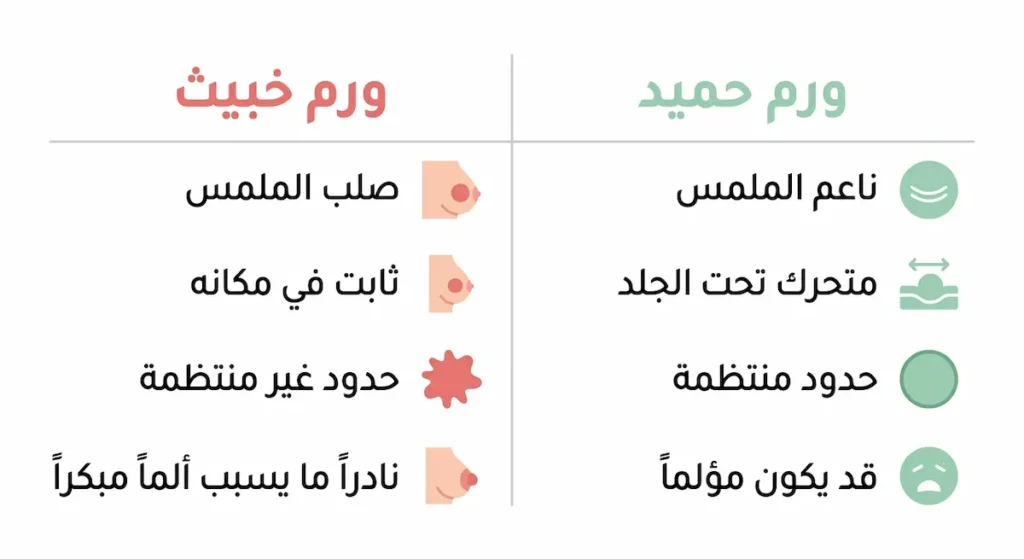
التمييز بين الورمين الحميد والخبيث بالفحص اليدوي وحده صعب حتى على الأطباء ذوي الخبرة. ومع ذلك، توجد فروق عامة مبدئية. الورم الحميد — كالكيس الليفي (Fibrocystic Changes) أو الورم الغدي الليفي (Fibroadenoma) — يميل لأن يكون ناعم الملمس ومتحركاً تحت الجلد وقد يكون مؤلماً بالضغط، وغالباً يتغير حجمه مع الدورة الشهرية. على النقيض من ذلك، يميل الورم الخبيث إلى أن يكون صلباً وغير منتظم الحدود وثابتاً في مكانه، ونادراً ما يسبب ألماً في مراحله الأولى.
لكن — وهذا جوهري — لا يمكن الاعتماد على هذه الفروق وحدها لتأكيد التشخيص. الخزعة وحدها هي القول الفصل.
جدول (1): مقارنة بين ورم الثدي الحميد والخبيث
| وجه المقارنة | الورم الحميد (Benign) | الورم الخبيث (Malignant) |
|---|---|---|
| الملمس | ناعم ومطاطي غالباً | صلب وغير منتظم |
| الحدود | واضحة ومنتظمة | غير واضحة وغير منتظمة |
| الحركة تحت الجلد | متحرك بسهولة | ثابت في مكانه غالباً |
| الألم | قد يكون مؤلماً بالضغط | غير مؤلم في المراحل المبكرة عادةً |
| التغير مع الدورة الشهرية | يتغير حجمه غالباً | لا يتأثر بالدورة |
| سرعة النمو | بطيء أو ثابت | متسارع في الغالب |
| الانتشار | لا ينتشر أبداً | قد ينتشر للعقد اللمفية وأعضاء بعيدة |
| تغيرات الجلد | نادرة | محتملة (احمرار، تجعد، قشرة برتقال) |
| التشخيص النهائي | خزعة (Biopsy) | خزعة (Biopsy) |
| المصدر: جمعية السرطان الأمريكية (ACS) | المعهد الوطني للسرطان (NCI) | ||
اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
ما هي أسباب سرطان الثدي وعوامل الخطر المعروفة؟
هل العامل الوراثي يسبب سرطان الثدي دائماً؟
العامل الوراثي مهم لكنه ليس حتمياً. طفرات جينية مثل BRCA1 وBRCA2 ترفع خطر الإصابة بشكل كبير. المرأة التي تحمل طفرة BRCA1 تواجه خطراً يصل إلى 72% للإصابة بسرطان الثدي خلال حياتها، وفق دراسة منشورة في مجلة JAMA عام 2017 (Kuchenbaecker et al.). لكن الحقيقة أن 5% إلى 10% فقط من حالات أورام الثدي الخبيثة مرتبطة بطفرات وراثية موروثة.
إذاً كيف نفسر الأغلبية الساحقة من الإصابات؟ معظمها ينشأ من طفرات مكتسبة (Acquired Mutations) تحدث خلال حياة الشخص بسبب عوامل بيئية وهرمونية وأخرى لم يفهمها العلم بعد. كذلك توجد جينات أخرى أقل شهرة مثل PALB2 وATM وCHEK2 ترفع الخطر بنسب متفاوتة.
بالنسبة للواقع السعودي، أشارت دراسة سعودية منشورة في مجلة Annals of Saudi Medicine عام 2020 إلى أن نسبة حاملات طفرات BRCA بين مريضات سرطان الثدي السعوديات أعلى مما كان متوقعاً سابقاً، خاصة مع ارتفاع معدلات زواج الأقارب في بعض المناطق.
“اكتشاف جين BRCA1 لم يكن مجرد إنجاز علمي، بل غيّر طريقة تفكيرنا بالكامل حول الوقاية من سرطان الثدي. اليوم نستطيع أن نحدد النساء الأكثر عرضة للخطر ونقدم لهن خيارات وقائية قبل أن يظهر المرض.”
— Dr. Mary-Claire King, Ph.D. — أستاذة علم الوراثة، جامعة واشنطن (مكتشفة جين BRCA1)
اقرأ أيضاً: علم الوراثة (Genetics): المبادئ الأساسية وتطبيقاتها
كيف تؤثر الهرمونات في خطر الإصابة؟
الإستروجين (Estrogen) يعمل كمحفز لنمو خلايا الثدي. كلما زادت فترة تعرض الثدي للإستروجين، ارتفع الخطر. وعليه فإن النساء اللواتي بدأ لديهن البلوغ قبل سن 12 أو تأخر انقطاع الطمث (Menopause) لديهن بعد سن 55 يتعرضن لمستويات إستروجين تراكمية أعلى.
من ناحية أخرى، الاستخدام المطول للعلاج بالهرمونات البديلة (Hormone Replacement Therapy — HRT) بعد انقطاع الطمث — خاصة المركب من إستروجين وبروجستيرون — يرفع الخطر بنسبة ملحوظة. أثبتت دراسة منشورة في مجلة The Lancet عام 2019 (Collaborative Group on Hormonal Factors in Breast Cancer) أن هذا الخطر يظل مرتفعاً حتى بعد التوقف عن العلاج الهرموني بأكثر من عقد.
بالإضافة إلى ذلك، يُعَدُّ عدم الإنجاب أو تأخر الإنجاب الأول بعد سن 30 من العوامل التي ترفع الخطر بشكل طفيف، بينما الرضاعة الطبيعية تمنح حماية نسبية.
📌 معلومة سريعة
الرضاعة الطبيعية لمدة تتجاوز 12 شهراً تراكمياً تقلل خطر الإصابة بنحو 4.3% لكل 12 شهراً إضافياً من الرضاعة، وفق بيانات منظمة الصحة العالمية. هذه الحماية تتضاعف مع تعدد مرات الرضاعة عبر عدة حمول.
المصدر: منظمة الصحة العالمية (WHO)
ما دور نمط الحياة والعوامل البيئية؟
السمنة بعد انقطاع الطمث تُعَدُّ عامل خطر مؤكداً. النسيج الدهني ينتج إستروجين إضافي عبر إنزيم الأروماتاز (Aromatase)، مما يغذي الخلايا السرطانية الحساسة للهرمونات. أما الكحول فكل مشروب يومي يرفع الخطر بنسبة 7% إلى 10%. التدخين، رغم ارتباطه الأقوى بسرطانات الرئة، يزيد أيضاً من خطر أورام الثدي الخبيثة، خاصة لدى النساء اللواتي بدأن التدخين قبل إنجابهن الأول.
“أرى في عيادتي كثيراً من النساء السعوديات اللواتي يعانين من السمنة بعد انقطاع الطمث مع نمط حياة قليل الحركة. أنصح دائماً بالمشي 150 دقيقة أسبوعياً على الأقل، وبتقليل السكريات المكررة واللحوم المصنعة. هذه التغييرات البسيطة تقلل خطر الإصابة بنسبة ملحوظة.”
— د. علا الأحمد، اختصاصية تغذية علاجية
اقرأ أيضاً: الطعام: ما هي أسس التغذية السليمة وكيف يؤثر على صحتنا؟
ما هي أنواع سرطان الثدي الأساسية والفرعية؟
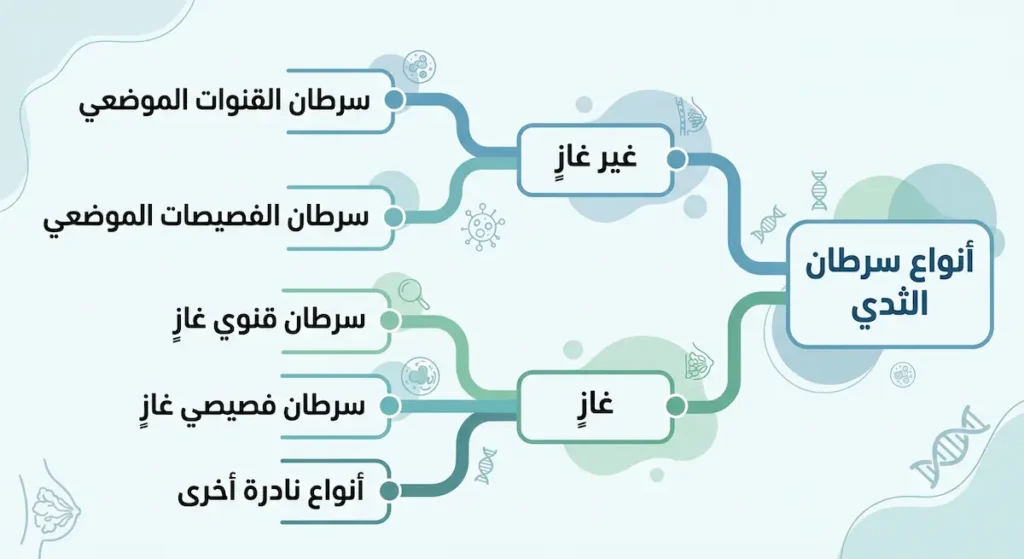
ما المقصود بالسرطان غير الغازي (In Situ)؟
السرطان الموضعي يعني أن الخلايا الشاذة لم تخترق الغشاء القاعدي بعد. أهم نوعين:
- سرطان القنوات الموضعي (Ductal Carcinoma In Situ — DCIS): الأكثر شيوعاً ويمثل نحو 20% من جميع حالات سرطان الثدي المكتشفة عبر الماموجرام. يبقى محصوراً داخل القنوات اللبنية. لا يُعَدُّ مهدداً للحياة بذاته، لكنه يرفع خطر التحول إلى سرطان غازي إن تُرك دون علاج.
- سرطان الفصيصات الموضعي (Lobular Carcinoma In Situ — LCIS): أقل شيوعاً ولا يُعَدُّ سرطاناً حقيقياً بالمعنى الدقيق، بل هو علامة إنذار تدل على ارتفاع خطر الإصابة مستقبلاً في أي من الثديين.
كيف يختلف السرطان الغازي (Invasive)؟
حين تتجاوز الخلايا السرطانية جدار القناة أو الفصيص وتبدأ بغزو الأنسجة المحيطة، يُصنَّف الورم على أنه غازٍ. السرطان القنوي الغازي (Invasive Ductal Carcinoma — IDC) يمثل نحو 70% إلى 80% من جميع الحالات. يليه السرطان الفصيصي الغازي (Invasive Lobular Carcinoma — ILC) بنسبة 10% إلى 15%.
من جهة ثانية، توجد أنواع نادرة مثل السرطان النخاعي (Medullary Carcinoma)، والمخاطي (Mucinous Carcinoma)، والأنبوبي (Tubular Carcinoma). هذه الأنواع النادرة غالباً تحمل توقعات مرضية أفضل من النوع القنوي الغازي الشائع.
لماذا يُخيف سرطان الثدي ثلاثي السلبية الكثيرين؟
سرطان الثدي ثلاثي السلبية (Triple-Negative Breast Cancer — TNBC) يمثل نحو 10% إلى 15% من حالات سرطان الثدي. يُسمى “ثلاثي السلبية” لأن خلاياه لا تحمل مستقبلات الإستروجين ولا البروجستيرون ولا البروتين HER2. هذا يعني أنه لا يستجيب للعلاج الهرموني ولا للعلاج الموجه ضد HER2، مما يجعل الخيارات العلاجية أضيق.
لكنّ هذا لا يعني انعدام الأمل. فقد شهدت السنوات الأخيرة تطورات مذهلة في العلاج المناعي (Immunotherapy) لهذا النوع تحديداً. أثبتت دراسة KEYNOTE-522 المنشورة في New England Journal of Medicine عام 2022 أن إضافة عقار بيمبروليزوماب (Pembrolizumab) إلى العلاج الكيميائي قبل الجراحة رفع نسبة الاستجابة المرضية الكاملة بشكل كبير لدى مريضات TNBC.
بالمقابل، يميل هذا النوع إلى إصابة نساء أصغر سناً، وقد يرتبط بطفرات BRCA1 في بعض الحالات.
“نتائج دراسة KEYNOTE-522 أثبتت أن الجمع بين العلاج المناعي والكيميائي قبل الجراحة يمنح مريضات سرطان الثدي ثلاثي السلبية فرصة أفضل بكثير للاستجابة المرضية الكاملة. هذا تحوّل جذري في مسار مرض كان يُعَدُّ الأصعب علاجاً بين أنواع سرطان الثدي.”
— Dr. Peter Schmid, MD, Ph.D. — أستاذ طب الأورام، جامعة كوين ماري بلندن
ما خصائص سرطان الثدي الإيجابي لبروتين HER2؟
حوالي 15% إلى 20% من أورام الثدي الخبيثة تُفرط في إنتاج بروتين HER2 (Human Epidermal Growth Factor Receptor 2)، مما يعزز نمو الخلايا السرطانية وانقسامها. كان هذا النوع يُعَدُّ من أسوأ الأنواع من حيث التوقعات المرضية قبل عقدين. لكن منذ اعتماد عقار تراستوزوماب (Trastuzumab — الاسم التجاري: Herceptin) عام 1998، انقلبت الموازين تماماً. اليوم تتوفر عدة أدوية موجهة ضد HER2 حسّنت نسب الشفاء بشكل جوهري.
جدول (2): أنواع سرطان الثدي الرئيسة وخصائصها
| النوع | نسبة الحدوث | مستقبلات الهرمونات | HER2 | الاستجابة للعلاج | التوقعات المرضية |
|---|---|---|---|---|---|
| القنوي الموضعي (DCIS) | ~20% | متغيرة | متغير | جراحة ± إشعاع | ممتازة (غير غازي) |
| القنوي الغازي (IDC) | 70% – 80% | إيجابية غالباً | متغير | جراحة + كيماوي + هرموني ± موجه | جيدة إلى متوسطة حسب المرحلة |
| الفصيصي الغازي (ILC) | 10% – 15% | إيجابية غالباً | سلبي عادةً | جراحة + هرموني ± كيماوي | جيدة عموماً |
| ثلاثي السلبية (TNBC) | 10% – 15% | سلبية | سلبي | كيماوي + مناعي (Pembrolizumab) | أقل ملاءمة لكنها تتحسن |
| الإيجابي لـ HER2 | 15% – 20% | متغيرة | إيجابي (مُفرط) | موجه (Trastuzumab) + كيماوي | تحسنت كثيراً مع العلاج الموجه |
| الالتهابي (IBC) | 1% – 5% | متغيرة | متغير | كيماوي أولاً ثم جراحة + إشعاع | عدوانية وتتطلب علاجاً مكثفاً |
| المصدر: المعهد الوطني للسرطان الأمريكي (NCI) | منظمة الصحة العالمية (WHO) | |||||
🔬 معلومة تستحق التوقف
عقار تراستوزوماب ديروكستيكان (Trastuzumab Deruxtecan — T-DXd) الذي اعتُمد مؤخراً أظهر فعالية حتى في الأورام ذات التعبير المنخفض عن HER2 (HER2-low)، مما فتح باب العلاج الموجه لفئة جديدة تماماً من المريضات كانت تُحرَم منه سابقاً. هذا التطور نُشر في دراسة DESTINY-Breast04 في NEJM عام 2022.
اقرأ أيضاً: علاج السرطان: التقنيات الحديثة والابتكارات المستقبلية
كيف تُصنَّف مراحل سرطان الثدي من الصفر إلى الرابعة؟
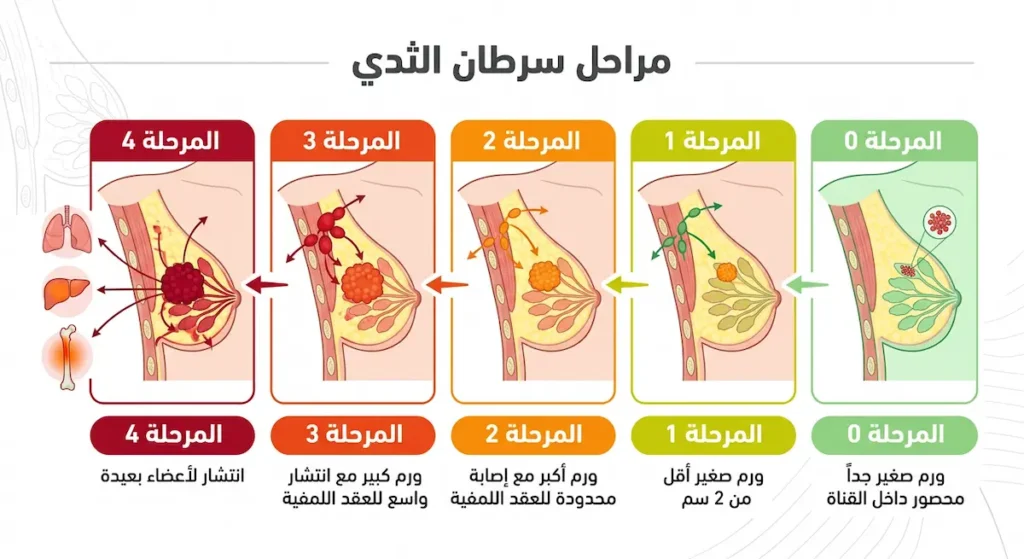
يستخدم الأطباء نظام TNM لتصنيف مراحل سرطان الثدي. الحرف T يشير إلى حجم الورم الأصلي (Tumor). الحرف N يشير إلى مدى إصابة العقد اللمفية (Nodes). الحرف M يشير إلى وجود انبثاث بعيد أو عدمه (Metastasis). وبناءً على هذه المعطيات الثلاثة، يُحدَّد مرحلة المرض الإجمالية.
ما الذي يميز المرحلة 0 والمرحلة 1 (الاكتشاف المبكر)؟
المرحلة 0 تعني سرطاناً موضعياً (In Situ)، لم ينتشر خارج مكان نشأته. المرحلة 1 تعني ورماً صغيراً لا يتجاوز 2 سم ولم يصل إلى العقد اللمفية أو وصل إلى نقاط مجهرية فقط. معدل البقاء لمدة خمس سنوات في هذه المراحل يقارب 99%، وهو رقم يبعث على التفاؤل بقوة.
هنا تكمن القوة الحقيقية للكشف المبكر عن سرطان الثدي. الماموجرام الدوري يكتشف الورم في مراحله هذه قبل أن يكبر بما يكفي ليُحَسّ يدوياً.
ما المقصود بالمرحلة 2 والمرحلة 3 (الانتشار الموضعي)؟
في المرحلة 2، يكون الورم بين 2 و5 سم، أو يكون أصغر لكنه وصل إلى عدد محدود من العقد اللمفية الإبطية. أما المرحلة 3 فتشمل أوراماً أكبر من 5 سم أو أوراماً انتشرت إلى عدد أكبر من العقد اللمفية أو غزت جدار الصدر أو الجلد. تُسمى هذه المرحلة أحياناً “متقدمة موضعياً” (Locally Advanced).
معدل البقاء لمدة خمس سنوات في المرحلة 2 يبلغ نحو 93%، وفي المرحلة 3 نحو 72%، وفق بيانات جمعية السرطان الأمريكية (ACS) لعام 2024. العلاج في هذه المراحل يكون مكثفاً ويجمع عادة بين الجراحة والكيماوي والإشعاعي.
ماذا يعني تشخيص المرحلة 4 (السرطان النقيلي)؟
المرحلة 4 تعني أن السرطان انتشر إلى أعضاء بعيدة مثل العظام أو الكبد أو الرئتين أو الدماغ. هذا التشخيص صادم ومخيف، لكن من الضروري معرفة أنه لم يعد حكماً نهائياً كما كان قبل عقود.
كثير من مريضات المرحلة 4 يعشن سنوات طويلة بنوعية حياة جيدة بفضل العلاجات الحديثة. معدل البقاء لمدة خمس سنوات يبلغ نحو 31%، لكن هذا الرقم يتحسن باستمرار مع ظهور أدوية جديدة. الهدف العلاجي هنا يتحول من الشفاء التام إلى السيطرة على المرض وإبطاء تقدمه والحفاظ على جودة الحياة.
جدول (3): مراحل سرطان الثدي ونسب البقاء لمدة 5 سنوات
| المرحلة | حجم الورم (T) | العقد اللمفية (N) | الانبثاث البعيد (M) | نسبة البقاء 5 سنوات |
|---|---|---|---|---|
| المرحلة 0 | موضعي (In Situ) | لا إصابة | لا انبثاث | ~99% |
| المرحلة 1 | ≤ 2 سم | لا إصابة أو مجهرية فقط | لا انبثاث | ~99% |
| المرحلة 2 | 2 – 5 سم | قد تصاب 1-3 عقد | لا انبثاث | ~93% |
| المرحلة 3 | > 5 سم أو غزو جدار الصدر | إصابة متعددة العقد | لا انبثاث | ~72% |
| المرحلة 4 | أي حجم | أي حالة | انبثاث بعيد (عظام، كبد، رئة، دماغ) | ~31% |
| المصدر: جمعية السرطان الأمريكية (ACS) — 2024 | برنامج SEER — المعهد الوطني للسرطان | ||||
📊 رقم يستحق التأمل
في المملكة العربية السعودية، كشف السجل الوطني للأورام أن نحو 30% من حالات سرطان الثدي لا تزال تُشخَّص في مراحل متقدمة (المرحلة 3 أو 4)، رغم توفر برامج الفحص المجانية في كثير من المستشفيات الحكومية. هذا يؤكد الحاجة الماسة لنشر الوعي بأهمية الكشف المبكر.
المصدر: المركز الوطني للمعلومات الصحية — السجل السعودي للأورام
اقرأ أيضاً: الإحصاءات الحيوية (Vital Statistics): المفهوم، الأهمية، والتطبيقات
كيف يُشخَّص سرطان الثدي بدقة؟
كيف يمكنكِ إجراء الفحص الذاتي للثدي في المنزل؟

الفحص الذاتي ليس بديلاً عن الماموجرام، لكنه أداة بسيطة تساعدكِ على معرفة شكل ثدييكِ الطبيعي حتى تلاحظي أي تغيير فوراً.
الخطوات:
- قفي أمام المرآة مع إسدال الذراعين ثم رفعهما فوق الرأس. لاحظي أي تغير في الحجم أو الشكل أو لون الجلد أو وضع الحلمة.
- أثناء الاستحمام (الجلد الرطب يسهّل الانزلاق)، ارفعي ذراعكِ اليمنى وافحصي الثدي الأيمن بأصابع اليد اليسرى مبسوطة ومتلاصقة. تحركي بحركات دائرية صغيرة من الخارج إلى الداخل، مع ضغط خفيف ثم متوسط ثم عميق.
- لا تنسي منطقة تحت الإبط والمنطقة فوق الترقوة.
- اعصري الحلمة برفق ولاحظي أي إفراز.
- كرري الخطوات على الثدي الآخر.
- أعيدي الفحص وأنتِ مستلقية على ظهركِ مع وضع وسادة صغيرة تحت الكتف الموافق للثدي المفحوص.
أفضل وقت للفحص هو بعد انتهاء الدورة الشهرية بـ 3 إلى 5 أيام، حين يكون الثدي أقل احتقاناً.
ما الذي يحدث أثناء الفحص السريري لدى الطبيب؟
يقوم الطبيب أو الطبيبة بفحص الثديين يدوياً باستخدام تقنية مماثلة للفحص الذاتي لكن بخبرة تدريبية. يتحقق من وجود كتل أو تغيرات في الجلد أو الحلمة أو العقد اللمفية. الفحص السريري يُكمل — ولا يُغني عن — الفحوصات التصويرية.
أي الفحوصات التصويرية أدق وأنسب؟
الماموجرام (Mammography): فحص الأشعة السينية الأكثر استخداماً لتصوير الثدي. يكشف التكلسات الدقيقة (Microcalcifications) والكتل قبل أن تُحَسّ يدوياً. تُوصي الجمعية الأمريكية للسرطان بالبدء بالماموجرام السنوي من سن 40 للنساء ذوات الخطر المتوسط. في السعودية، وفّرت وزارة الصحة وحدات ماموجرام متنقلة في المناطق النائية ضمن حملات “الكشف المبكر عن سرطان الثدي” التي تُكثَّف في شهر أكتوبر من كل عام.
الموجات فوق الصوتية (Ultrasound): تُستخدم كأداة مكملة، خاصة لدى النساء دون 30 عاماً اللواتي يكون نسيج الثدي لديهن كثيفاً. تساعد في التمييز بين الكتل الصلبة والأكياس المملوءة بسائل.
الرنين المغناطيسي (MRI): أعلى حساسية بين جميع الفحوصات، لكنه مكلف وقد يعطي نتائج إيجابية كاذبة. يُحجَز عادة للنساء ذوات الخطر العالي جداً أو لتقييم مدى انتشار ورم مؤكد.
جدول (5): مقارنة بين الفحوصات التصويرية لتشخيص سرطان الثدي
| وجه المقارنة | الماموجرام (Mammography) | الموجات فوق الصوتية (Ultrasound) | الرنين المغناطيسي (MRI) |
|---|---|---|---|
| الحساسية | متوسطة إلى عالية (77% – 95%) | متوسطة (مكمّل) | الأعلى (~95% – 100%) |
| الخصوصية | عالية | متوسطة | أقل (نتائج إيجابية كاذبة أكثر) |
| الإشعاع | نعم (جرعة منخفضة) | لا | لا |
| الفئة العمرية المثلى | ≥ 40 سنة | < 30 سنة أو كمكمل | ذوات الخطر العالي جداً |
| التكلفة | منخفضة نسبياً | منخفضة | مرتفعة |
| الاستخدام الأمثل | فحص دوري (Screening) | تقييم كتلة مكتشفة | تقييم الانتشار قبل الجراحة |
| المصدر: الكلية الأمريكية للأشعة (ACR) | جمعية السرطان الأمريكية (ACS) | |||
لماذا تُعَدُّ الخزعة (Biopsy) القول الفصل في التشخيص؟
مهما بدت نتائج التصوير مقلقة أو مطمئنة، لا يمكن تأكيد وجود سرطان الثدي أو نفيه إلا بأخذ عينة من النسيج المشبوه وفحصها تحت المجهر. أنواع الخزعات الشائعة:
- خزعة الإبرة الدقيقة (Fine Needle Aspiration — FNA): تسحب خلايا قليلة بإبرة رفيعة. سريعة لكن أقل دقة.
- خزعة الإبرة اللبية (Core Needle Biopsy — CNB): تأخذ عينة أسطوانية من النسيج. أكثر دقة وهي المفضلة في معظم الحالات.
- الخزعة الاستئصالية (Excisional Biopsy): تُزال الكتلة بالكامل جراحياً. تُستخدم حين لا تكون الخزعة بالإبرة كافية.
بعد الخزعة، يُحلَّل النسيج لتحديد نوع الورم ودرجته ومستقبلاته الهرمونية ومستوى HER2 ومعدل الانقسام الخلوي (Ki-67). هذه المعلومات هي أساس الخطة العلاجية.
🩺 هل تعلمين؟
تقنية الخزعة الموجهة بالتفريغ (Vacuum-Assisted Biopsy) أصبحت متاحة في عدة مراكز سعودية متقدمة، وتسمح بأخذ عينات أكبر وأكثر تمثيلاً بألم أقل ودون الحاجة لشق جراحي.
المصدر: الكلية الأمريكية للأشعة (ACR)
ما هي أحدث طرق علاج سرطان الثدي المتاحة اليوم؟

قبل الدخول في تفاصيل هذا القسم، من الضروري التأكيد على أن خطة علاج سرطان الثدي تختلف اختلافاً جوهرياً من مريضة لأخرى. العوامل المحددة تشمل نوع الورم ومرحلته وخصائصه البيولوجية وعمر المريضة وحالتها الصحية العامة ورغباتها الشخصية. لا توجد خطة واحدة تناسب الجميع. فريق علاجي متعدد التخصصات (Multidisciplinary Team) يضم جراح أورام وطبيب أورام طبية وأخصائي إشعاع وأخصائي علم أمراض هو من يضع الخطة.
متى يكون العلاج الجراحي ضرورياً وما خياراته؟
الجراحة هي الركيزة الأساسية لعلاج معظم حالات سرطان الثدي في مراحله المبكرة والمتوسطة. الخياران الرئيسان:
الاستئصال الجزئي (Lumpectomy — Breast-Conserving Surgery): يُزال الورم مع هامش من النسيج السليم المحيط. يحافظ على معظم شكل الثدي. يُتبَع دائماً تقريباً بعلاج إشعاعي. أثبتت دراسات طويلة الأمد أن نتائج البقاء مع الاستئصال الجزئي + الإشعاعي مساوية لنتائج الاستئصال الكلي في المراحل المبكرة.
الاستئصال الكلي (Mastectomy): يُزال الثدي بالكامل. يُوصى به حين يكون الورم كبيراً نسبة إلى حجم الثدي، أو حين تتعدد بؤر الورم، أو حين ترغب المريضة في ذلك لتقليل القلق من عودة المرض. هناك تقنيات حديثة مثل الاستئصال مع الحفاظ على الجلد والحلمة (Nipple-Sparing Mastectomy) تُحسّن النتائج التجميلية بشكل كبير.
بالإضافة إلى ذلك، يُجرى عادة فحص العقدة اللمفية الحارسة (Sentinel Lymph Node Biopsy — SLNB) لتحديد ما إذا كان السرطان قد وصل للعقد اللمفية. هذا الفحص قلّل كثيراً من الحاجة لاستئصال جميع العقد الإبطية (Axillary Dissection) الذي كان يسبب مضاعفات مزعجة كالوذمة اللمفية.
العلاج الكيميائي: هل يُعطى قبل الجراحة أم بعدها؟
يُعطى العلاج الكيميائي (Chemotherapy) في حالتين:
- قبل الجراحة (Neoadjuvant): لتقليص حجم الورم الكبير ليصبح الاستئصال الجزئي ممكناً. كذلك يُتيح تقييم مدى استجابة الورم للأدوية.
- بعد الجراحة (Adjuvant): لتدمير أي خلايا سرطانية متبقية ميكروسكوبياً في الجسم وتقليل خطر الانتكاس.
ليست كل الحالات تحتاج كيماوياً. فالأورام الصغيرة الإيجابية لمستقبلات الهرمونات وسالبة HER2 ذات الدرجة المنخفضة قد تُعالج بالجراحة والعلاج الهرموني فقط. اختبارات جينومية مثل Oncotype DX وMammaPrint تساعد الأطباء في تحديد ما إذا كان الكيماوي سيفيد المريضة فعلاً أم لا.
ما التقنيات الحديثة في العلاج الإشعاعي؟
العلاج الإشعاعي (Radiation Therapy) يستخدم حزماً عالية الطاقة لتدمير الخلايا السرطانية المتبقية بعد الجراحة. التقنيات تطورت بشكل مذهل:
الإشعاع الموجه ثلاثي الأبعاد (3D-CRT) والإشعاع المعدّل الشدة (IMRT) يستهدفان الورم بدقة عالية مع تقليل الضرر على القلب والرئتين المجاورين. هذا مهم جداً في أورام الثدي الأيسر حيث يقع القلب قريباً.
تقنية التنفس العميق المتحكم به (Deep Inspiration Breath Hold — DIBH): تطلب من المريضة أخذ نفس عميق أثناء جلسة الإشعاع، مما يبعد القلب عن مجال الإشعاع ويقلل التعرض القلبي بنسبة تصل إلى 50%.
الإشعاع المسرّع الجزئي للثدي (Accelerated Partial Breast Irradiation — APBI): يقصر مدة العلاج من 3 إلى 6 أسابيع إلى أسبوع واحد فقط، لكنه مناسب لحالات مختارة بعناية.
كيف يعمل العلاج الهرموني ولمن يُوصف؟
نحو 70% من أورام الثدي الخبيثة تحمل مستقبلات الإستروجين (ER+) أو البروجستيرون (PR+) أو كليهما. العلاج الهرموني (Endocrine Therapy) يمنع الهرمونات من الوصول إلى الخلايا السرطانية أو يقلل إنتاجها. الأدوية الشائعة:
تاموكسيفين (Tamoxifen): يُعطى لمدة 5 إلى 10 سنوات. يُناسب النساء قبل وبعد انقطاع الطمث.
مثبطات الأروماتاز (Aromatase Inhibitors): مثل ليتروزول (Letrozole) وأناستروزول (Anastrozole). تُعطى للنساء بعد انقطاع الطمث فقط. تمنع تحويل الأندروجينات إلى إستروجين في النسيج الدهني.
“كثير من المريضات يتوقفن عن تناول تاموكسيفين بسبب أعراضه الجانبية مثل الهبّات الساخنة وآلام المفاصل. أنصح بشدة بعدم التوقف دون استشارة الطبيب، لأن فوائد الالتزام بالعلاج لمدة خمس سنوات كاملة تفوق بكثير مضاعفاته. ويمكن للطبيب تعديل الجرعة أو تبديل الدواء إذا كانت الأعراض لا تُحتمل.”
— جاسم محمد مراد، مستشار دوائي
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
ما الجديد في العلاج الموجه والعلاج المناعي؟
العلاج الموجه (Targeted Therapy): يهاجم أهدافاً جزيئية محددة في الخلية السرطانية. من أبرز الأدوية:
- تراستوزوماب (Trastuzumab) وبيرتوزوماب (Pertuzumab) ضد HER2.
- مثبطات CDK4/6 مثل بالبوسيكليب (Palbociclib) وريبوسيكليب (Ribociclib) للسرطانات الإيجابية لمستقبلات الهرمونات المتقدمة. هذه الأدوية غيّرت قواعد اللعبة في المرحلة 4.
- مثبطات PARP مثل أولاباريب (Olaparib) لمريضات طفرات BRCA.
العلاج المناعي (Immunotherapy): بيمبروليزوماب (Pembrolizumab) اعتُمد من إدارة الغذاء والدواء الأمريكية (FDA) عام 2021 لعلاج سرطان الثدي ثلاثي السلبية المتقدم موضعياً. كذلك ظهرت أجسام مضادة مقترنة بأدوية (Antibody-Drug Conjugates — ADCs) مثل ساسيتوزوماب جوفيتيكان (Sacituzumab Govitecan) أحدثت ثورة في علاج TNBC المتقدم.
جدول (4): أحدث الأدوية الموجهة والمناعية المعتمدة لعلاج سرطان الثدي
| الدواء | الآلية | النوع المستهدف | سنة اعتماد FDA | ملاحظات |
|---|---|---|---|---|
| Trastuzumab (Herceptin) | جسم مضاد وحيد النسيلة ضد HER2 | HER2 إيجابي | 1998 | غيّر تاريخ علاج HER2+ |
| Pertuzumab (Perjeta) | جسم مضاد ضد HER2 (موقع مختلف) | HER2 إيجابي | 2012 | يُعطى مع Trastuzumab |
| T-DXd (Enhertu) | جسم مضاد مقترن بدواء (ADC) | HER2+ و HER2-low | 2019 (توسع 2022) | فتح باب العلاج لفئة HER2-low |
| Palbociclib (Ibrance) | مثبط CDK4/6 | HR+ / HER2- متقدم | 2015 | يُعطى مع مثبطات الأروماتاز |
| Olaparib (Lynparza) | مثبط PARP | حاملات طفرات BRCA | 2018 | أول مثبط PARP لسرطان الثدي |
| Pembrolizumab (Keytruda) | علاج مناعي (Anti-PD-1) | ثلاثي السلبية (TNBC) | 2021 | يُعطى مع الكيماوي قبل الجراحة |
| Sacituzumab Govitecan (Trodelvy) | جسم مضاد مقترن بدواء (ADC) | TNBC المتقدم | 2020 | ثورة في علاج TNBC النقيلي |
| المصدر: إدارة الغذاء والدواء الأمريكية (FDA) | المعهد الوطني للسرطان (NCI) | ||||
“عقار Trastuzumab Deruxtecan أعاد تعريف مفهوم HER2 في سرطان الثدي بالكامل. لم نعد نتحدث عن إيجابي أو سلبي فحسب، بل أصبح هناك طيف كامل من التعبير عن HER2 يمكننا استهدافه علاجياً. هذا يفتح الباب لعلاج فئة ضخمة من المريضات كانت تُحرم سابقاً.”
— Dr. Shanu Modi, MD — أخصائية الأورام الطبية، مركز ميموريال سلون كيتيرينغ للسرطان، نيويورك
⚡ معلومة صادمة تعيد حماسك
في عام 2024، وافقت FDA على توسيع استخدام عقار تراستوزوماب ديروكستيكان ليشمل أوراماً كانت تُصنَّف سابقاً على أنها “سلبية HER2”. هذا يعني أن حوالي 50% إلى 60% من جميع مريضات سرطان الثدي النقيلي أصبحن مؤهلات لعلاج موجه كان محصوراً في 15% فقط. أي تحول كهذا في الأورام لا يحدث كل يوم.
اقرأ أيضاً: علم المناعة (Immunology): الجهاز المناعي والأمراض
هل تساعد جراحات ترميم الثدي في التعافي النفسي والجسدي؟
بعد استئصال الثدي، تواجه كثير من النساء صدمة نفسية عميقة ترتبط بصورة الجسد والأنوثة. جراحة إعادة البناء (Breast Reconstruction Surgery) ليست ترفاً تجميلياً، بل جزء أصيل من خطة التعافي.
الخيارات المتاحة:
زراعة السيليكون (Silicone Implants): الأكثر شيوعاً. تُجرى إما فور الاستئصال (ترميم فوري) أو بعد إتمام العلاجات الأخرى (ترميم مؤجل). تتطلب عادة مرحلة توسيع الأنسجة (Tissue Expander) قبل وضع الزرعة النهائية.
استخدام أنسجة الجسم الطبيعية (Autologous/Flap Reconstruction): تُنقل أنسجة من البطن أو الظهر أو الفخذ لبناء ثدي جديد. النتائج تبدو وتشعر طبيعية أكثر، لكن الجراحة أطول وأكثر تعقيداً.
في السعودية، تتوفر كلتا التقنيتين في مراكز متقدمة مثل مركز الملك فهد الوطني للأورام ومستشفى الملك فيصل التخصصي. الجدير بالذكر أن التأمين الصحي في المملكة يغطي غالباً جراحات الترميم بعد استئصال الثدي لأسباب سرطانية.
هل يمكن الوقاية من سرطان الثدي فعلاً؟
ما تغييرات نمط الحياة التي تقلل الخطر؟
لا توجد طريقة مضمونة للوقاية التامة، لكن يمكن تقليل الخطر بشكل ملموس. الحفاظ على وزن صحي بعد انقطاع الطمث، وممارسة النشاط البدني المنتظم (150 دقيقة من المشي السريع أسبوعياً على الأقل)، وتجنب الكحول، والحد من العلاج الهرموني البديل — كل ذلك يقلل الخطر بنسب موثقة علمياً.
كما أن الرضاعة الطبيعية لأطول فترة ممكنة توفر حماية إضافية. وبالتالي فإن تعديل نمط الحياة ليس مجرد نصيحة عامة بل أداة وقائية مبنية على أدلة.
ما قصة الجراحة الوقائية وكيف أعادت أنجلينا جولي تعريف النقاش؟
في عام 2013، كشفت الممثلة أنجلينا جولي أنها تحمل طفرة BRCA1 تمنحها خطراً يقدّر بـ 87% للإصابة بسرطان الثدي. اختارت إجراء استئصال ثنائي وقائي (Bilateral Prophylactic Mastectomy) لتقليل خطرها إلى أقل من 5%. هذا القرار أثار موجة عالمية من النقاش حول الجراحة الوقائية.
ليست كل امرأة تحمل طفرة BRCA بحاجة لهذا الإجراء الجذري. الخيارات تشمل أيضاً المراقبة المكثفة بفحوصات دورية كل ستة أشهر أو الأدوية الوقائية. القرار يجب أن يكون فردياً ومبنياً على استشارة وراثية (Genetic Counseling) متعمقة.
هل توجد أدوية وقائية للنساء المعرضات لخطر عالٍ؟
نعم. أدوية مثل تاموكسيفين ورالوكسيفين (Raloxifene) ومثبطات الأروماتاز (خارج نطاق ترخيصها الأصلي) أظهرت قدرة على تقليل خطر الإصابة بنسبة تصل إلى 50% لدى النساء ذوات الخطر العالي. لكنها ليست خالية من الآثار الجانبية، لذلك تُوصف فقط بعد تقييم دقيق للمخاطر والفوائد.
📋 بروتوكولات الفحص والوقاية الرسمية (2024-2025)
| جمعية السرطان الأمريكية (ACS) | ماموجرام سنوي من سن 40 للنساء ذوات الخطر المتوسط. MRI + ماموجرام سنوياً من سن 30 لذوات الخطر العالي (≥ 20%). |
| الشبكة الوطنية الشاملة للسرطان (NCCN) | فحص جيني واستشارة وراثية لمن لديهن تاريخ عائلي قوي. بدء الماموجرام من سن 25 لحاملات BRCA. |
| وزارة الصحة السعودية | ماموجرام مجاني كل سنتين للنساء بين 40 و69 عاماً ضمن برنامج الكشف المبكر الوطني. |
| منظمة الصحة العالمية (WHO) | توصي بالماموجرام المنظم كل سنتين للنساء بين 50 و69 عاماً في الدول ذات الموارد الكافية. |
المصادر: ACS | NCCN | وزارة الصحة السعودية | WHO
ما نسب الشفاء من سرطان الثدي ومتوسط العمر المتوقع؟
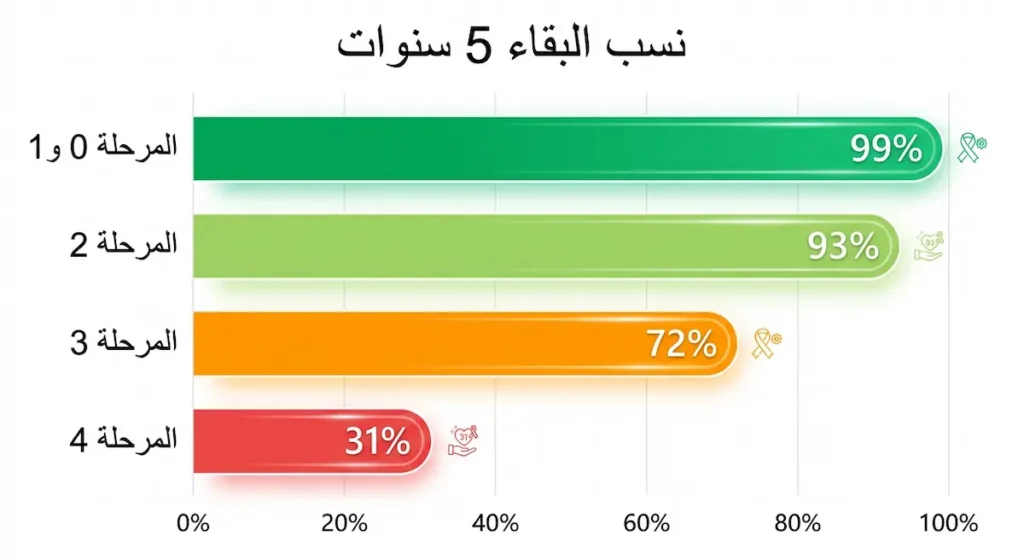
الأرقام هنا تبعث على الأمل الحقيقي. وفق بيانات جمعية السرطان الأمريكية (ACS) المحدثة عام 2024:
- المرحلة 0 و1: نسبة البقاء لمدة 5 سنوات تقارب 99%.
- المرحلة 2: نحو 93%.
- المرحلة 3: نحو 72%.
- المرحلة 4: نحو 31%، لكن مع الأدوية الحديثة هذا الرقم في تحسن مستمر.
هذه الأرقام تمثل متوسطات إحصائية ولا تتنبأ بمصير مريضة بعينها. عوامل كثيرة تؤثر في النتيجة الفردية: نوع الورم، واستجابته للعلاج، وصحة المريضة العامة، والتزامها بالمتابعة. ومما يستحق الإشارة أن نسبة الشفاء من سرطان الثدي في المرحلة الأولى والثانية تتجاوز 90%، وهو رقم يجعل الكشف المبكر القرار الأذكى الذي يمكن لأي امرأة اتخاذه.
🌍 معلومة تربط العلم بالواقع
في السعودية، بلغ معدل البقاء لمدة 5 سنوات لمريضات سرطان الثدي نحو 78% وفق بيانات السجل السعودي للأورام. الفجوة بين هذا الرقم والأرقام العالمية (90%) ترتبط بشكل رئيس بتأخر التشخيص. كل شهر تأخير يقلل فرص الشفاء التام.
المصدر: جمعية السرطان الأمريكية (ACS) | السجل السعودي للأورام
اقرأ أيضاً: الاحصاءات الصحية: البيانات، الأساليب، والتطبيقات
كيف تدعمين نفسكِ نفسياً وجسدياً أثناء وبعد العلاج؟
ما التغذية المناسبة أثناء تلقي العلاج الكيميائي؟
العلاج الكيميائي يسبب غثياناً وفقدان شهية وتقرحات في الفم وتغيراً في حاسة التذوق.
“أنصح مريضاتي بتقسيم الوجبات إلى 5 أو 6 وجبات صغيرة بدلاً من 3 كبيرة. التركيز على البروتين مهم جداً لإعادة بناء الخلايا — البيض والدجاج والسمك واللبن الزبادي. كذلك شرب لترين من الماء يومياً يساعد الكليتين على التخلص من الأدوية الكيميائية بكفاءة. وتجنب الأطعمة النيئة مهم لأن المناعة تكون منخفضة.”
— د. علا الأحمد، اختصاصية تغذية علاجية
من ناحية أخرى، بعض المكملات مثل فيتامين D والأوميغا-3 قد تُفيد، لكن يجب مناقشتها مع الطبيب المعالج لأن بعض المكملات تتفاعل مع أدوية العلاج الكيميائي.
اقرأ أيضاً: البروتين من منظور العلوم التطبيقية: دليلك الشامل لفهم الوظائف الحيوية والاحتياجات اليومية
كيف تتعاملين مع الآثار الجانبية المزعجة؟
تساقط الشعر (Alopecia): يبدأ عادة بعد 2 إلى 3 أسابيع من الجلسة الأولى. تقنية تبريد فروة الرأس (Scalp Cooling) باستخدام خوذ التبريد أثناء الجلسة يمكن أن تقلل تساقط الشعر بنسبة 50% في بعض الحالات. هذه التقنية أصبحت متاحة في عدة مراكز سعودية.
اقرأ أيضاً: تساقط الشعر عند النساء: ما الأسباب الطبية وكيف تختارين العلاج المناسب؟
الإرهاق (Cancer-Related Fatigue): أكثر الأعراض شيوعاً. قد يبدو غريباً، لكن النشاط البدني الخفيف مثل المشي 20 دقيقة يومياً يقلل الإرهاق أكثر من الراحة التامة. أثبتت دراسة كوكرين (Cochrane Review) عام 2019 أن التمارين الهوائية المنتظمة تحسّن مستوى الطاقة ونوعية النوم لدى مريضات سرطان الثدي أثناء تلقي العلاج.
الوذمة اللمفية (Lymphedema): تورم في الذراع الموافقة للثدي المصاب بسبب تضرر الأوعية اللمفية أثناء الجراحة أو الإشعاع. يمكن الوقاية منها بتجنب قياس ضغط الدم أو سحب الدم من الذراع المصابة، وبارتداء كُمّ ضاغط أثناء السفر بالطائرة، وبممارسة تمارين تصريف لمفية (Lymphatic Drainage Exercises) بإشراف أخصائي علاج طبيعي.
لماذا يُعَدُّ الدعم العائلي والنفسي ركيزة أساسية؟
تشخيص سرطان الثدي لا يصيب المريضة وحدها؛ يصيب العائلة بأكملها. الاكتئاب والقلق يصيبان نحو 30% من مريضات سرطان الثدي وفق دراسات متعددة. الاستعانة بمختص نفسي ليست ضعفاً بل ذكاء. مجموعات الدعم (Support Groups) — سواء حضورياً أو عبر الإنترنت — تتيح للمريضة مشاركة مخاوفها مع نساء يعشن التجربة ذاتها. في السعودية، تقدم جمعية “زهرة” لسرطان الثدي برامج دعم نفسي واجتماعي مجانية تشمل جلسات إرشادية وورش عمل.
ومما يغفل عنه كثيرون أن الزوج والأبناء أيضاً يحتاجون لدعم نفسي. الخوف من فقدان الأم أو الزوجة عبء هائل يحتاج لمساحة آمنة للتعبير عنه.
اقرأ أيضاً: الضغط النفسي المزمن: كيف يؤثر على صحتك وما الحلول المتاحة؟
الأسئلة الشائعة
اضغط على رمز + لمعرفة الإجابة
❓ أسئلة شائعة حول سرطان الثدي
خاتمة: رسالة أمل وتشجيع صارم
سرطان الثدي مرض مخيف بلا شك. لكنه أيضاً من أكثر السرطانات قابلية للعلاج والشفاء حين يُكتشف مبكراً. لقد قطع الطب أشواطاً هائلة في فهم هذا المرض وعلاجه خلال العقدين الأخيرين. أدوية لم تكن موجودة قبل خمس سنوات أصبحت اليوم تمنح الأمل لآلاف المريضات.
إلى كل محاربة تخوض هذه المعركة الآن: أنتِ أقوى مما تظنين. إلى كل امرأة تؤجل الفحص: لا تنتظري العرض. الكشف المبكر عن سرطان الثدي هو أقوى سلاح بين يديكِ. وإلى كل عائلة تدعم مريضتها: وجودكم هو الدواء الذي لا يُباع في الصيدليات.
هل أجريتِ فحص الماموجرام هذا العام؟ إن لم تفعلي، احجزي موعدكِ اليوم — ليس غداً، اليوم.
إذا وجدتِ في هذا المقال ما يُثري معرفتكِ أو يطمئن قلبكِ، فشاركيه مع صديقة أو قريبة. المعلومة الصحيحة في الوقت المناسب قد تنقذ حياة إنسانة. ولا تترددي في استشارة طبيبكِ حول أي سؤال أثاره هذا المقال في ذهنكِ.
المصادر والمراجع
الدراسات والأوراق البحثية
- Kuchenbaecker, K. B., et al. (2017). Risks of Breast, Ovarian, and Contralateral Breast Cancer for BRCA1 and BRCA2 Mutation Carriers. JAMA, 317(23), 2402–2416. DOI: 10.1001/jama.2017.7112
- دراسة مرجعية حددت نسب خطر الإصابة لدى حاملات طفرات BRCA بدقة غير مسبوقة.
- Collaborative Group on Hormonal Factors in Breast Cancer (2019). Type and timing of menopausal hormone therapy and breast cancer risk. The Lancet, 394(10204), 1159–1168. DOI: 10.1016/S0140-6736(19)31709-X
- تحليل تجميعي واسع أثبت أن العلاج الهرموني البديل يرفع خطر سرطان الثدي حتى بعد التوقف عنه.
- Schmid, P., et al. (2022). Event-free Survival with Pembrolizumab in Early Triple-Negative Breast Cancer (KEYNOTE-522). New England Journal of Medicine, 386(6), 556–567. DOI: 10.1056/NEJMoa2112651
- دراسة KEYNOTE-522 التي أثبتت فعالية العلاج المناعي في سرطان الثدي ثلاثي السلبية.
- Modi, S., et al. (2022). Trastuzumab Deruxtecan in Previously Treated HER2-Low Advanced Breast Cancer (DESTINY-Breast04). New England Journal of Medicine, 387(1), 9–20. DOI: 10.1056/NEJMoa2203690
- الدراسة التي فتحت باب العلاج الموجه لفئة HER2-low لأول مرة.
- Furmaniak, A. C., Menig, M., & Markes, M. H. (2016). Exercise for women receiving adjuvant therapy for breast cancer. Cochrane Database of Systematic Reviews, (9). DOI: 10.1002/14651858.CD005001.pub3
- مراجعة كوكرين تؤكد فعالية التمارين في تحسين نوعية الحياة أثناء علاج سرطان الثدي.
- Alghamdi, I. G., et al. (2013). The incidence rate of female breast cancer in Saudi Arabia: an observational descriptive epidemiological analysis of data from Saudi Cancer Registry 2001–2008. Breast Cancer: Targets and Therapy, 5, 103–109. DOI: 10.2147/BCTT.S50575
- دراسة وصفية عن معدلات الإصابة بسرطان الثدي في السعودية.
الجهات الرسمية والمنظمات
- World Health Organization (WHO) (2024). Breast Cancer Fact Sheet. https://www.who.int/news-room/fact-sheets/detail/breast-cancer
- صفحة الحقائق الرسمية لمنظمة الصحة العالمية عن سرطان الثدي.
- American Cancer Society (ACS) (2024). Breast Cancer Facts & Figures 2024. https://www.cancer.org/research/cancer-facts-statistics/breast-cancer-facts-figures.html
- تقرير شامل يتضمن نسب البقاء والإحصائيات المحدثة.
- U.S. Food and Drug Administration (FDA) (2024). Approved Drug Products — Oncology. https://www.fda.gov/drugs/resources-information-approved-drugs/oncology-cancer-hematologic-malignancies-approval-notifications
- قائمة الأدوية المعتمدة حديثاً لعلاج الأورام.
- National Cancer Institute (NCI) (2024). Breast Cancer Treatment (PDQ) — Health Professional Version. https://www.cancer.gov/types/breast/hp/breast-treatment-pdq
- المرجع العلاجي الأكثر تفصيلاً من المعهد الوطني للسرطان الأمريكي.
- Centers for Disease Control and Prevention (CDC) (2024). Breast Cancer Screening Guidelines. https://www.cdc.gov/breast-cancer/screening/index.html
- إرشادات الفحص المبكر من مراكز السيطرة على الأمراض.
الكتب والموسوعات العلمية
- Harris, J. R., Lippman, M. E., Morrow, M., & Osborne, C. K. (2014).Diseases of the Breast (5th Edition). Lippincott Williams & Wilkins.
- الكتاب المرجعي الأشهر عالمياً في أمراض الثدي.
- DeVita, V. T., Lawrence, T. S., & Rosenberg, S. A. (2019).DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology (11th Edition). Wolters Kluwer.
- الموسوعة الشاملة في علم الأورام.
- Bland, K. I., & Copeland, E. M. (2018).The Breast: Comprehensive Management of Benign and Malignant Diseases (5th Edition). Elsevier.
- مرجع تفصيلي يغطي الأمراض الحميدة والخبيثة للثدي.
مقالات علمية مبسطة
- Mukherjee, S. (2023). The New Promise of Targeted Therapies in Breast Cancer. Scientific American. https://www.scientificamerican.com/article/breast-cancer-targeted-therapy/
- مقال مبسط يشرح التطورات الحديثة في العلاج الموجه لسرطان الثدي.
قراءات إضافية ومصادر للتوسع
- Sørlie, T., et al. (2001). Gene expression patterns of breast carcinomas distinguish tumor subclasses with clinical implications. Proceedings of the National Academy of Sciences, 98(19), 10869–10874. DOI: 10.1073/pnas.191367098
- لماذا نقترح عليك قراءته؟ هذه الورقة الكلاسيكية هي التي أسست لتصنيف سرطان الثدي إلى أنواع فرعية جزيئية (Luminal A, Luminal B, HER2-enriched, Basal-like). فهمها ضروري لأي طالب يريد استيعاب كيف تُبنى خطط العلاج الحديثة.
- Mukherjee, S. (2010).The Emperor of All Maladies: A Biography of Cancer. Scribner.
- لماذا نقترح عليك قراءته؟ كتاب حائز على جائزة بوليتزر يروي تاريخ السرطان كأنه رواية أدبية. يمنح القارئ فهماً عميقاً للسياق التاريخي والعلمي الذي أوصلنا إلى العلاجات الحالية. ممتع حتى لغير المتخصصين.
- Cardoso, F., et al. (2019). Early breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology, 30(8), 1194–1220. DOI: 10.1093/annonc/mdz173
- لماذا نقترح عليك قراءته؟ هذا الدليل الأوروبي يمثل أحدث الإرشادات السريرية لتشخيص وعلاج سرطان الثدي المبكر. مناسب لطلاب الطب والأطباء المقيمين الذين يريدون فهم البروتوكولات العلاجية المعتمدة.
⚠️ تنبيه مهم وإخلاء مسؤولية
المعلومات الواردة في هذا المقال مقدّمة من موسوعة خلية لأغراض التثقيف الصحي العام فقط، ولا تُغني بأي حال عن الاستشارة الطبية المتخصصة أو التشخيص أو العلاج المهني. كل حالة طبية فريدة وتتطلب تقييماً فردياً من طبيب مختص.
لا تتخذي قرارات علاجية أو تُعدّلي أو تُوقفي أي دواء بناءً على ما تقرئينه على الإنترنت. استشيري طبيبكِ أو الصيدلي دائماً قبل اتخاذ أي إجراء صحي.
موسوعة خلية — khalieah.com — لا تتحمل أي مسؤولية عن سوء استخدام المعلومات الواردة في هذا المقال.
🛡️ بيان المصداقية والشفافية
تلتزم موسوعة خلية بأعلى معايير الدقة العلمية والمصداقية الطبية (E-E-A-T). جميع المعلومات الواردة في هذا المقال مستندة إلى مصادر علمية محكّمة وإرشادات جهات صحية رسمية مثل منظمة الصحة العالمية (WHO)، وجمعية السرطان الأمريكية (ACS)، وإدارة الغذاء والدواء الأمريكية (FDA)، والمعهد الوطني للسرطان (NCI).
جرت مراجعة هذا المقال من قبل فريق طبي متعدد التخصصات يضم أطباء مختصين ومستشاراً دوائياً وأخصائية تغذية علاجية. نحرص على تحديث محتوانا بشكل دوري ليعكس أحدث الأدلة العلمية المتاحة.
آخر تحديث: مارس 2026 | موسوعة خلية