الورم الحميد: دليلك الطبي الشامل للفهم والعلاج (علامات الاطمئنان والخطر)
ما الذي يجعل بعض الأورام غير ضارة بينما يستدعي بعضها التدخل العاجل؟
الورم الحميد (Benign Tumor) هو كتلة من الخلايا تنمو بشكل غير طبيعي لكنها تبقى محصورة في مكانها الأصلي دون غزو الأنسجة المجاورة أو الانتشار إلى أعضاء بعيدة. تتميز هذه الأورام بنمو بطيء وخلايا منتظمة الشكل، وغالباً ما تكون محاطة بكبسولة ليفية واقية. معظمها لا يهدد الحياة، لكن بعضها يستدعي العلاج حسب موقعه وحجمه وتأثيره على الأعضاء المحيطة.
تمت المراجعة والتدقيق بواسطة الهيئة الطبية:

اختصاصية الأورام والطب النووي

طبيب عام ومراجع طبي

اختصاصية تغذية علاجية

خبير الرقابة الدوائية
الطبية
هل لاحظت يوماً كتلة صغيرة تحت جلدك فشعرت بموجة من القلق اجتاحت تفكيرك؟ أنت لست وحدك. كلمة “ورم” وحدها كفيلة بأن تُحدث زلزالاً نفسياً لدى أي شخص، خصوصاً في مجتمعاتنا العربية التي لا تزال تربط هذه الكلمة تلقائياً بالسرطان والموت. لكن الحقيقة التي يجهلها كثيرون هي أن الغالبية العظمى من الأورام التي يكتشفها الأطباء يومياً أورام حميدة لا علاقة لها بالسرطان من قريب أو بعيد. في هذا المقال ستجد كل ما تحتاج معرفته: من آلية تكوّن الورم الحميد، مروراً بأنواعه وأعراضه، وصولاً إلى أحدث طرق العلاج والمتابعة. المعلومات هنا ليست نظرية جافة؛ بل ستقرأ سيناريوهات واقعية ونصائح عملية تساعدك على اتخاذ القرار الصحيح بهدوء وثقة.
📌 خلاصة المقال في دقيقة واحدة
✅ حقائق جوهرية
- الورم الحميد لا ينتشر لأعضاء أخرى ومحاط بكبسولة ليفية تمنع غزو الأنسجة.
- أكثر من 90% من الكتل المكتشفة تحت الجلد تكون حميدة أو أكياساً دهنية.
- نسبة نجاح عملية الاستئصال تتجاوز 95% في العمليات طفيفة التوغل.
- معظم الأورام الحميدة لا تتحول إلى سرطان أبداً (أقل من 1-2%).
🛡️ خطوات عملية فورية
- راجع طبيبك خلال أسبوعين من اكتشاف أي كتلة غريبة في جسمك.
- اطلب الخزعة (Biopsy) لتأكيد التشخيص — لا تكتفِ بالتصوير وحده.
- التزم بالمتابعة الدورية بعد الاستئصال: كل 6 أشهر لمدة عامين ثم سنوياً.
- احتفظ بنسخة من تقرير الخزعة النسيجية كمرجع طبي دائم.
⚠️ تحذيرات لا تتجاهلها
- ورم حميد في الدماغ قد يسبب أعراضاً خطيرة بسبب الضغط على الأعصاب.
- سلائل القولون الغدية تحمل خطر تحوّل يصل إلى 5-10% خلال 10-15 سنة — أزلها فوراً.
- النمو المفاجئ لأي كتلة ثابتة الحجم يستوجب مراجعة عاجلة.
مثال تطبيقي من الواقع:
تخيّل أن سيدة تبلغ من العمر 38 عاماً اكتشفت كتلة بحجم حبة الزيتون في ثديها الأيسر أثناء الاستحمام. شعرت بالذعر وتصورت الأسوأ. ذهبت إلى طبيبة مختصة في جدة أجرت لها فحصاً بالموجات فوق الصوتية (Ultrasound)، فأظهر الفحص كتلة ناعمة الحدود ذات محتوى متجانس. ثم أُخذت خزعة (Biopsy) بإبرة رفيعة، وأكد التقرير النسيجي أنها ورم غدي ليفي حميد (Fibroadenoma). نصحها الطبيب بالمراقبة الدورية كل ستة أشهر دون أي تدخل جراحي. بعد عامين لم يتغير حجم الكتلة، وعادت المريضة إلى حياتها الطبيعية دون أي مضاعفات. هذا السيناريو يتكرر آلاف المرات في العيادات السعودية سنوياً، ويُثبت أن التشخيص المبكر يحول لحظة الرعب إلى لحظة اطمئنان.
اقرأ أيضاً: سرطان الثدي: دليلك الشامل من التشخيص إلى التعافي
ما هو الورم الحميد علمياً وكيف يحدث؟
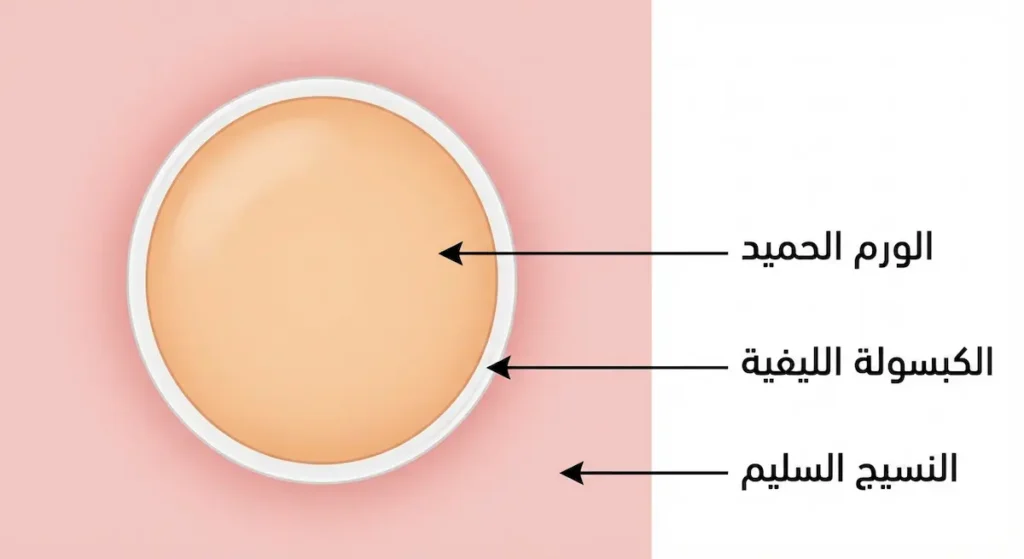
لفهم الورم الحميد يجب أولاً أن نفهم كيف تعمل خلايا الجسم في الوضع الطبيعي. كل خلية في جسمك تملك “ساعة بيولوجية” تتحكم في انقسامها ونموها وموتها المبرمج (Apoptosis). هذه الساعة تخضع لإشارات جينية دقيقة تضمن ألا تنقسم الخلية إلا عند الحاجة، كأن يحتاج الجسم لترميم نسيج تالف أو تعويض خلايا ميتة. في الورم الحميد يحدث خلل محدود في هذه الإشارات؛ إذ تبدأ مجموعة من الخلايا بالانقسام بمعدل أسرع قليلاً من المعتاد دون أن تستجيب لأوامر “التوقف” الطبيعية. لكن الفارق الجوهري هو أن هذه الخلايا تحتفظ ببنيتها الطبيعية ولا تفقد هويتها.
ومما يميز معظم الأورام الحميدة أنها تُحاط بما يُعرف بالكبسولة الليفية (Fibrous Capsule)، وهي غلاف من النسيج الضام يعمل كسياج يفصل الكتلة الورمية عن الأنسجة السليمة المحيطة. هذه الكبسولة هي “خط الدفاع” الذي يمنع الخلايا الورمية من التسلل والانتشار. تصوّرها مثل كرة مطاطية داخل كيس محكم الإغلاق: الكرة تكبر ببطء لكنها لا تخرج من الكيس أبداً. على النقيض من ذلك، خلايا الأورام الخبيثة تكسر هذا الحاجز وتغزو الأنسجة المجاورة وتنتقل عبر الدم والليمف إلى أعضاء بعيدة. هذا الفرق البسيط في السلوك الخلوي هو ما يصنع الهوة الشاسعة بين ورم يمكنك التعايش معه وورم يهدد حياتك.
![]() تصريح طبي
تصريح طبي
“أنصح كل من يكتشف كتلة غريبة في جسمه بالتوجه للطبيب خلال أسبوعين على الأكثر. ليس لأن كل كتلة خطيرة، بل لأن الفحص المبكر يُزيل القلق سريعاً ويمنحك خطة واضحة سواء كانت مراقبة أو علاجاً.”
— الدكتور زيد مراد، اختصاصي طب عام
![]() رأي خبير دولي
رأي خبير دولي
“فهم البنية النسيجية للورم هو مفتاح التمييز بين الحميد والخبيث. الكبسولة الليفية التي تُحيط بمعظم الأورام الحميدة ليست مجرد غلاف بل هي حاجز بيولوجي فعّال يعكس عدم قدرة هذه الخلايا على غزو الأنسجة المحيطة.”
— Prof. Christopher D.M. Fletcher، أستاذ علم الأمراض، كلية الطب – جامعة هارفارد، الولايات المتحدة
اقرأ أيضاً: علم الأمراض (Pathology): دراسة الأمراض وتأثيرها على الجسم
🔬 حقيقة طبية:
أكثر من 90% من الكتل التي يكتشفها المرضى تحت الجلد ويراجعون بسببها العيادات تكون أوراماً حميدة أو أكياساً دهنية لا تستدعي أي تدخل جراحي، وفقاً لإحصائيات الجمعية الأمريكية للسرطان (ACS) المنشورة عام 2023.
المصدر: الجمعية الأمريكية للسرطان (ACS)
ما الفرق الحاسم بين الورم الحميد والورم الخبيث؟
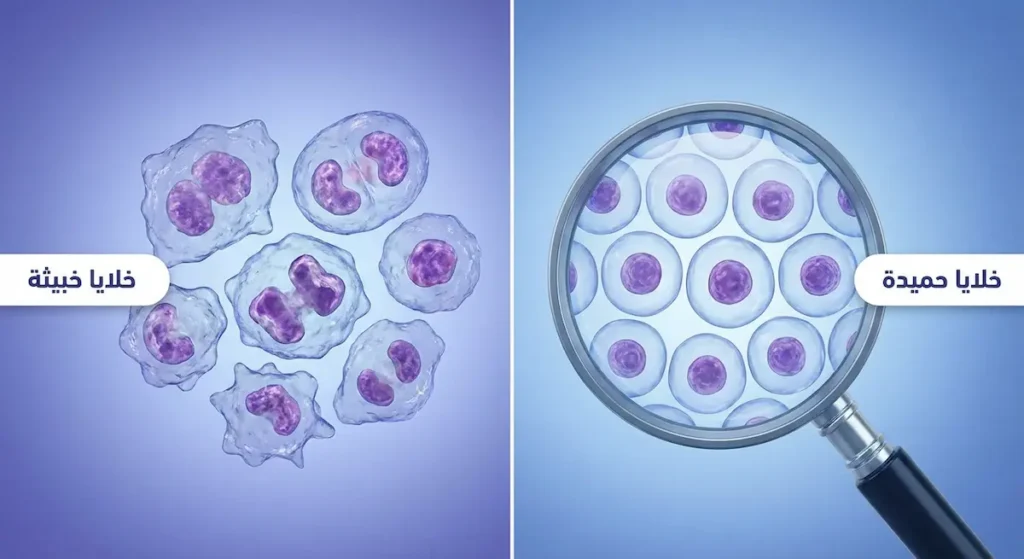
هذا السؤال هو الأكثر بحثاً على الإنترنت في الوطن العربي حين يتعلق الأمر بالأورام. الفرق بين الورم الحميد والخبيث ليس مجرد فرق في الاسم؛ بل هو اختلاف جذري في سلوك الخلايا ومآلات المرض وطريقة العلاج. دعني أوضح لك ذلك بجدول مقارنة مبسط يتبعه شرح تفصيلي:
جدول المقارنة: الورم الحميد مقابل الورم الخبيث (السرطان)
| وجه المقارنة | الورم الحميد (Benign) | الورم الخبيث / السرطان (Malignant) |
|---|---|---|
| معدل النمو | بطيء جداً، قد يستغرق سنوات | سريع وعدواني في كثير من الأحيان |
| حدود الورم | واضحة ومحددة، محاط بكبسولة ليفية | غير منتظمة، يغزو الأنسجة المجاورة |
| الانتشار (Metastasis) | لا ينتشر إطلاقاً | ينتقل عبر الدم والليمف لأعضاء بعيدة |
| شكل الخلايا تحت المجهر | منتظمة وتشبه الخلايا الطبيعية | مشوهة وغير منتظمة (Anaplasia) |
| الكبسولة الليفية | موجودة في معظم الأنواع | غائبة، الورم يتسلل بدون حدود |
| التأثير على الجسم | ضغط موضعي فقط دون تدمير الأنسجة | يدمر الأنسجة ويستنزف موارد الجسم |
| احتمالية العودة بعد الاستئصال | نادرة جداً في معظم الأنواع | مرتفعة نسبياً وتتطلب متابعة مكثفة |
| العلاج الأساسي | مراقبة أو استئصال جراحي بسيط | جراحة + علاج كيماوي + إشعاعي (غالباً) |
| التحول إلى نوع آخر | نادر جداً (1-2% في أنواع محددة) | قد يتحول لدرجات أعلى من الخباثة |
| المصادر: الجمعية الأمريكية للسرطان (ACS) | المعهد الوطني الأمريكي للسرطان (NCI) | تصنيف الأورام – منظمة الصحة العالمية (WHO/IARC) | ||
لاحظ أن معدل نمو الورم الحميد قد يكون بطيئاً لدرجة أن بعض المرضى يعيشون عقوداً دون أن يشعروا بأي تغيير. بينما الأورام الخبيثة تتضاعف خلاياها بسرعة وتحتاج إلى تدخل عاجل. كما أن شكل الخلايا تحت المجهر يُعَدُّ الفيصل الحقيقي: خلايا الورم الحميد تبدو “مهذبة” ومنظمة وتشبه النسيج الأصلي الذي نشأت منه، بينما خلايا الورم الخبيث تفقد هذا التنظيم وتظهر بأشكال شاذة يصفها أطباء الأنسجة بالتباين النووي (Nuclear Atypia).
هذا وقد أثبتت دراسة منشورة في مجلة The Lancet Oncology عام 2022 أن نسبة تحول الأورام الحميدة إلى خبيثة لا تتجاوز 1-2% في معظم الأنواع، مما يؤكد أن مجرد وجود ورم حميد لا يعني بالضرورة أنك في خطر.
اقرأ أيضاً: علاج السرطان: التقنيات الحديثة والابتكارات المستقبلية
ما أشهر أنواع الأورام الحميدة وأين تظهر في الجسم؟
تتنوع أنواع الأورام الحميدة بحسب نوع النسيج الذي تنشأ منه وموقعها في الجسم. فيما يلي أبرز الأنواع مع شرح مفصل لكل منها:
أشهر أنواع الأورام الحميدة: النوع، الموقع، ومدى الشيوع
| نوع الورم | النسيج الأصلي | الموقع الأكثر شيوعاً | الفئة الأكثر إصابة | هل يحتاج علاجاً عادةً؟ |
|---|---|---|---|---|
| الورم الشحمي (Lipoma) | نسيج دهني | تحت الجلد: الرقبة، الأكتاف، الظهر | البالغون 40-60 عاماً | لا، إلا لأسباب تجميلية |
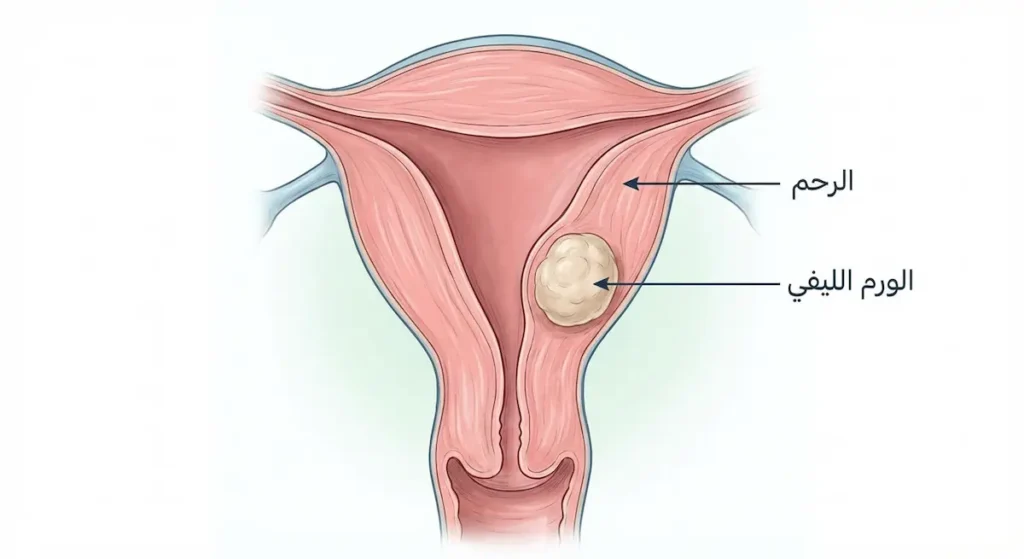
| الورم الليفي الرحمي (Uterine Fibroid) | عضلات ملساء | جدار الرحم | النساء 30-50 عاماً | فقط عند ظهور أعراض مزعجة |
| الورم الغدي (Adenoma) | نسيج غدي ظهاري | الغدة الدرقية، النخامية، القولون | البالغون من كلا الجنسين | سلائل القولون تُزال وقائياً |
| الورم الوعائي (Hemangioma) | أوعية دموية | الجلد، الكبد | الرضّع والأطفال | 80% تختفي تلقائياً |
| الورم السحائي (Meningioma) | السحايا (أغشية الدماغ) | الدماغ، الحبل الشوكي | النساء فوق 60 عاماً | حسب الحجم والموقع |
| الورم الغضروفي العظمي (Osteochondroma) | عظمي-غضروفي | العظام الطويلة (الفخذ، الساق) | الأطفال والمراهقون | نادراً، إلا عند الضغط على الأعصاب |
| الورم الحليمي (Papilloma) | نسيج ظهاري | الجلد، الحنجرة، قنوات الثدي | البالغون من كلا الجنسين | يُزال عند ظهور أعراض أو خطر التحول |
| المصادر: تصنيف الأورام – منظمة الصحة العالمية (WHO/IARC) | المعهد الوطني الأمريكي للسرطان (NCI) | مكتبة الطب الوطنية الأمريكية (NLM/NIH) | ||||
الأورام الشحمية (Lipomas): الأكثر شيوعاً تحت الجلد
الورم الشحمي هو تكتل من الخلايا الدهنية ينمو ببطء شديد تحت الجلد مباشرة. يظهر عادةً في الرقبة والأكتاف والظهر والذراعين. ملمسه طري ومطاطي، ويتحرك بسهولة عند الضغط عليه. شكل الورم الحميد تحت الجلد في هذه الحالة يكون مستديراً أو بيضاوياً وغير مؤلم في الغالب. أشارت دراسة نُشرت في مجلة Journal of Clinical Medicine عام 2021 إلى أن الأورام الشحمية تصيب شخصاً من كل 1000 شخص تقريباً، وتكون أكثر شيوعاً بين الأعمار 40 و60 عاماً. في السعودية يُلاحظ أطباء الجلدية في مستشفيات الرياض وجدة أن هذا النوع من أكثر أسباب زيارة عيادات الجراحة التجميلية لأغراض إزالة الكتل الظاهرة.
الأورام الليفية (Fibromas): هاجس النساء الأول
الأورام الليفية الرحمية (Uterine Fibroids) هي أشهر أنواع الأورام الحميدة عند النساء على الإطلاق. تنشأ من العضلات الملساء لجدار الرحم وتتأثر بشكل مباشر بمستويات هرمون الإستروجين (Estrogen). تتراوح أحجامها من بذرة صغيرة إلى كتلة بحجم البطيخة في الحالات المتقدمة. وفقاً لمنظمة الصحة العالمية (WHO)، فإن ما يقارب 70% من النساء يُصبن بورم ليفي واحد على الأقل قبل سن الخمسين، لكن أغلبهن لا يعانين من أعراض تُذكر. الأعراض حين تظهر تشمل نزيفاً غزيراً أثناء الدورة الشهرية، وآلاماً في الحوض، وضغطاً على المثانة يسبب كثرة التبول.
الأورام الغدية (Adenomas): شائعة في الغدد والقولون
ينشأ الورم الغدي من الأنسجة الغدية الظهارية (Glandular Epithelium). أشهر أماكن ظهوره: الغدة الدرقية (Thyroid Adenoma)، والغدة النخامية (Pituitary Adenoma)، وسلائل القولون (Colonic Adenomas). ورم الغدة الدرقية الحميد شائع جداً في منطقة الخليج العربي، وتشير بيانات مستشفى الملك فيصل التخصصي إلى أن نسبة كبيرة من عقيدات الغدة الدرقية المكتشفة بالموجات فوق الصوتية تكون حميدة. أما سلائل القولون فهي حالة خاصة سنناقشها لاحقاً لأنها تحمل احتمالية ضئيلة للتحول.
💡 معلومة سريعة:
ورم الغدة النخامية الحميد (Pituitary Adenoma) رغم صغر حجمه الذي لا يتجاوز ملليمترات أحياناً، يمكنه أن يُحدث فوضى هرمونية كبرى في الجسم. فقد يتسبب في إفراز مفرط لهرمون النمو (GH) مؤدياً لحالة “العملقة” (Gigantism) عند الأطفال أو “ضخامة الأطراف” (Acromegaly) عند البالغين.
الأورام الوعائية (Hemangiomas): الوحمات الدموية لدى الرضّع
الورم الوعائي هو تكتل غير طبيعي من الأوعية الدموية يظهر عادةً عند الولادة أو خلال الأسابيع الأولى من حياة الرضيع. يبدو كبقعة حمراء زاهية على الجلد، ولذلك يُسمى أحياناً “وحمة الفراولة” (Strawberry Hemangioma). الجدير بالذكر أن 80% من هذه الأورام تتقلص وتختفي تلقائياً قبل سن العاشرة دون أي تدخل. لكن في حالات نادرة قد تظهر في الكبد أو الدماغ وتستدعي متابعة طبية حثيثة.
اقرأ أيضاً: طب الأطفال (Pediatrics): التخصص، الأمراض، والرعاية
الأورام السحائية (Meningiomas): ضيف هادئ في الدماغ
تنشأ الأورام السحائية من الأغشية المحيطة بالدماغ والحبل الشوكي (Meninges). غالباً ما تكون بطيئة النمو للغاية، وكثيراً ما تُكتشف مصادفةً عند إجراء أشعة على الرأس لسبب آخر. وفقاً لجمعية أورام الدماغ الأمريكية (ABTA)، تمثل الأورام السحائية نحو 37% من أورام الدماغ الأولية، وحوالي 80% منها حميدة. لكن حتى الحميد منها قد يسبب مشكلات خطيرة إذا نما في موقع حرج وضغط على مراكز حيوية كمركز الرؤية أو التوازن.
الأورام العظمية والغضروفية (Osteochondromas): أورام العظام الأكثر شيوعاً
الورم الغضروفي العظمي هو نتوء عظمي مغطى بطبقة غضروفية ينمو بالقرب من صفائح النمو (Growth Plates) في العظام الطويلة كعظام الفخذ والساق. يظهر عادةً في مرحلة الطفولة والمراهقة ويتوقف عن النمو مع اكتمال نمو الهيكل العظمي. معظم الحالات لا تحتاج علاجاً إلا إذا سبب الورم ألماً أو ضغطاً على الأعصاب أو الأوعية القريبة.
الأورام الحليمية (Papillomas): أورام الجلد والأغشية المخاطية
تنمو هذه الأورام على شكل نتوءات شبيهة بالإصبع أو القرنبيط على سطح الجلد أو الأغشية المخاطية. قد تظهر في الحنجرة أو قنوات الثدي أو عنق الرحم. بعض أنواعها يرتبط بعدوى فيروس الورم الحليمي البشري (HPV). ورم القناة اللبنية الحليمي (Intraductal Papilloma) في الثدي قد يسبب إفرازات دموية من الحلمة، وهو عرض مخيف للمريضة لكنه في الغالب حميد.
📊 رقم يستحق التوقف:
أثبتت دراسة منشورة في مجلة JAMA Surgery عام 2023 أن نسبة نجاح عملية استئصال الورم الحميد تتجاوز 95% في معظم الأنواع، مع معدل مضاعفات لا يتجاوز 3% في العمليات طفيفة التوغل (Minimally Invasive Surgery).
المصدر: مجلة JAMA Surgery – شبكة JAMA
ما أسباب ظهور الأورام الحميدة في الجسم؟
أسباب الورم الحميد لا تزال موضع بحث مكثف حتى اليوم. لا يوجد سبب واحد محدد، بل تتضافر عوامل متعددة تُهيئ الظروف لنمو هذه الكتل. أبرز هذه العوامل:
العوامل الوراثية والجينية تلعب دوراً محورياً. بعض المتلازمات الوراثية مثل متلازمة غاردنر (Gardner Syndrome) ومتلازمة الأورام الصماوية المتعددة (MEN Syndrome) تزيد احتمالية الإصابة بأنواع معينة من الأورام الحميدة. إذا كان لديك قريب من الدرجة الأولى أُصيب بورم حميد معين، فإن احتمالية إصابتك تكون أعلى قليلاً من المتوسط.
التغيرات الهرمونية من أهم المحركات، خاصةً عند النساء. الأورام الليفية الرحمية مثلاً تنمو وتتقلص بحسب مستويات الإستروجين والبروجسترون. لذلك تلاحظ كثير من النساء أن هذه الأورام تتقلص بعد انقطاع الطمث (Menopause) عندما تنخفض مستويات الهرمونات الأنثوية بشكل طبيعي.
التعرض للإشعاع والسموم البيئية عامل مُثبت علمياً. الأشخاص الذين تعرضوا لجرعات عالية من الإشعاع المؤين (Ionizing Radiation) سواء بسبب العلاج الإشعاعي أو حوادث نووية، يُظهرون معدلات أعلى لتكوين أورام سحائية وأورام الغدة الدرقية.
الالتهابات المزمنة تخلق بيئة مواتية لنمو الخلايا بشكل غير طبيعي. الأنسجة التي تتعرض لالتهاب مستمر تكون في حالة “ترميم دائم”؛ إذ تنقسم الخلايا باستمرار لتعويض التلف، مما يزيد فرصة حدوث خلل في آلية التحكم بالانقسام.
![]() تصريح تغذوي
تصريح تغذوي
“النظام الغذائي وحده لا يسبب أوراماً حميدة بشكل مباشر، لكن النظام الغذائي الغني بالأطعمة المصنعة والفقير بمضادات الأكسدة يُضعف قدرة الجسم على إصلاح الحمض النووي التالف. أنصح دائماً بالإكثار من الخضروات الورقية والفواكه الطازجة والتقليل من اللحوم المصنعة والسكريات المكررة.”
— الدكتورة علا الأحمد، اختصاصية تغذية علاجية
![]() رأي خبيرة دولية
رأي خبيرة دولية
“الأورام الليفية الرحمية تمثل نموذجاً فريداً لفهم كيف تتحكم الهرمونات في نمو الأورام الحميدة. الاستجابة الدراماتيكية لهذه الأورام لمستويات الإستروجين تفتح آفاقاً واعدة للعلاجات الدوائية الموجهة التي قد تُغني عن الجراحة تماماً.”
— Prof. Elizabeth A. Stewart, MD، أستاذة أمراض النساء والتوليد، جامعة مينيسوتا، الولايات المتحدة
اقرأ أيضاً: الحمض النووي: من التركيب الجزيئي الدقيق إلى بصمة الحياة الوراثية
من جهة ثانية، يلعب نمط الحياة دوراً مساعداً وليس سبباً مباشراً. السمنة المفرطة مثلاً ترتبط بزيادة مستويات الإستروجين في الدم بسبب تحول الأنسجة الدهنية للهرمونات، مما يفسر جزئياً ارتفاع نسبة الأورام الليفية الرحمية لدى النساء البدينات.
اقرأ أيضاً: مضادات الأكسدة (Antioxidants): الوظيفة، المصادر، والفوائد الصحية
ما أعراض الورم الحميد وكيف تكتشف وجوده؟
أعراض الورم الحميد تعتمد بشكل شبه كامل على موقع الورم وحجمه. كثير من الأورام الحميدة لا تُحدث أي أعراض إطلاقاً وتُكتشف مصادفةً أثناء فحص طبي روتيني أو أشعة أُجريت لسبب آخر. لكن عندما تظهر الأعراض، فإنها تكون غالباً نتيجة ضغط الكتلة على الأنسجة والأعضاء المحيطة وليس بسبب غزو الخلايا كما في السرطان.
الأعراض العامة التي قد يلاحظها المريض تشمل: كتلة محسوسة تحت الجلد أو في منطقة معينة من الجسم، شعور بالثقل أو الامتلاء في المنطقة المصابة، وتغير في شكل المنطقة أو حجمها بشكل تدريجي. لكن الأعراض الأكثر إزعاجاً تكون مرتبطة بمكان الورم تحديداً. الورم الحميد في الدماغ قد يسبب صداعاً مستمراً أو نوبات صرع أو ضعفاً في الرؤية أو تغيرات في الشخصية بسبب ضغطه على مراكز عصبية حساسة. الورم الحميد في الأمعاء قد يسبب انسداداً معوياً جزئياً مع آلام بطنية وإمساك مزمن. ورم الرحم الليفي قد يسبب نزيفاً حاداً يؤدي لفقر الدم (Anemia). أما ورم الغدة الكظرية (Adrenal Adenoma) فقد يُفرز هرمونات زائدة تسبب ارتفاعاً مفاجئاً في ضغط الدم أو متلازمة كوشينغ (Cushing’s Syndrome).
هل الورم الحميد يسبب ألماً فعلاً؟
هذا السؤال من أكثر الأسئلة التي يطرحها المرضى في العيادات. الإجابة المختصرة: ليس دائماً، لكن أحياناً نعم. معظم الأورام الحميدة غير مؤلمة بذاتها. الألم يحدث عادةً عندما يضغط الورم على عصب قريب، أو عندما ينمو في مساحة ضيقة لا تتسع له، أو عندما يسبب التهاباً في الأنسجة المحيطة. الأورام الشحمية مثلاً نادراً ما تؤلم إلا إذا كانت من النوع المسمى “ورم شحمي مؤلم” (Angiolipoma) الذي يحتوي على أوعية دموية متضخمة. بالمقابل، ورم العصب السمعي الحميد (Acoustic Neuroma / Vestibular Schwannoma) يسبب ألماً وطنيناً في الأذن وفقداناً تدريجياً للسمع رغم أنه ورم حميد تماماً.
اقرأ أيضاً: مسكنات الألم: ما أنواعها وكيف تعمل في الجسم؟
🧠 معلومة مدهشة:
بعض الأورام الحميدة في الدماغ قد تبقى “نائمة” لعقود دون أن يشعر صاحبها بأي شيء. دراسة أمريكية من جامعة هارفارد نُشرت عام 2020 وجدت أن حوالي 1-2% من الأشخاص البالغين يحملون أوراماً سحائية صغيرة دون أن يعلموا بوجودها، وغالباً لا تُكتشف إلا بعد الوفاة أثناء التشريح أو عند إجراء رنين مغناطيسي لسبب غير متعلق.
كيف يتم تشخيص الأورام الحميدة بدقة؟

تشخيص الورم الحميد يمر عبر مراحل متسلسلة تبدأ بالبسيط وتنتهي بالفيصل. المرحلة الأولى هي الفحص السريري (Physical Examination)؛ إذ يقوم الطبيب بتحسس الكتلة وتقييم حجمها وملمسها وحدودها وقابليتها للحركة. الكتلة الحميدة عادةً تكون متحركة وناعمة الحدود وغير ملتصقة بالأنسجة العميقة. لكن الفحص اليدوي وحده لا يكفي أبداً لتأكيد التشخيص.
المرحلة الثانية هي التصوير الطبي، وتتنوع أدواته بحسب مكان الكتلة. الموجات فوق الصوتية (Ultrasound) هي الخطوة الأولى في كثير من الحالات لأنها رخيصة وسريعة وغير مؤلمة ولا تستخدم إشعاعاً. تُظهر ما إذا كانت الكتلة صلبة أم مملوءة بسائل (كيس). الأشعة المقطعية (CT Scan) تعطي صوراً مقطعية أكثر تفصيلاً وتُستخدم خاصةً للأورام العميقة في البطن والصدر. التصوير بالرنين المغناطيسي (MRI) هو الأفضل لتصوير أورام الدماغ والأنسجة الرخوة لأنه يعطي تفاصيل دقيقة جداً عن بنية الورم وعلاقته بالأنسجة المحيطة.
لكن “الخطوة الذهبية” التي يصفها الأطباء بأنها الفيصل الوحيد هي الخزعة (Biopsy). في هذا الإجراء تُؤخذ عينة صغيرة من نسيج الورم بإبرة خاصة أو أثناء عملية جراحية، ثم تُرسل إلى مختبر الأنسجة (Histopathology Lab) حين يفحصها طبيب أمراض الأنسجة تحت المجهر. هذا الفحص هو الذي يحسم ما إذا كان الورم حميداً أم خبيثاً بنسبة دقة تقترب من 100%. لا تصوير طبي ولا فحص سريري يمكنه أن يحل محل الخزعة في التشخيص النهائي.
![]() رأي خبير أوروبي
رأي خبير أوروبي
“التطور في تقنيات التصوير بالرنين المغناطيسي أحدث ثورة في تشخيص أورام الدماغ الحميدة. اليوم يمكننا متابعة أورام سحائية بحجم ملليمترات وتحديد بدقة متناهية ما إذا كانت تحتاج تدخلاً أم مجرد مراقبة.”
— Prof. Roland Goldbrunner، أستاذ جراحة الأعصاب، مستشفى جامعة كولونيا، ألمانيا
![]() تصريح دوائي
تصريح دوائي
“في حالات الأورام الحميدة المؤكدة التي لا تستدعي جراحة، قد يصف الطبيب أدوية لتخفيف الأعراض المصاحبة مثل مسكنات الألم أو أدوية هرمونية لتقليص حجم الورم. لكن يجب ألا يتناول المريض أي دواء دون استشارة طبية دقيقة، لأن بعض الأدوية قد تتعارض مع حالته أو تُخفي أعراضاً مهمة.”
اقرأ أيضاً: علم الأدوية (Pharmacology): دراسة تفاعل الأدوية مع الكائن الحي
متى يكون الورم الحميد خطيراً ويستدعي التدخل الفوري؟
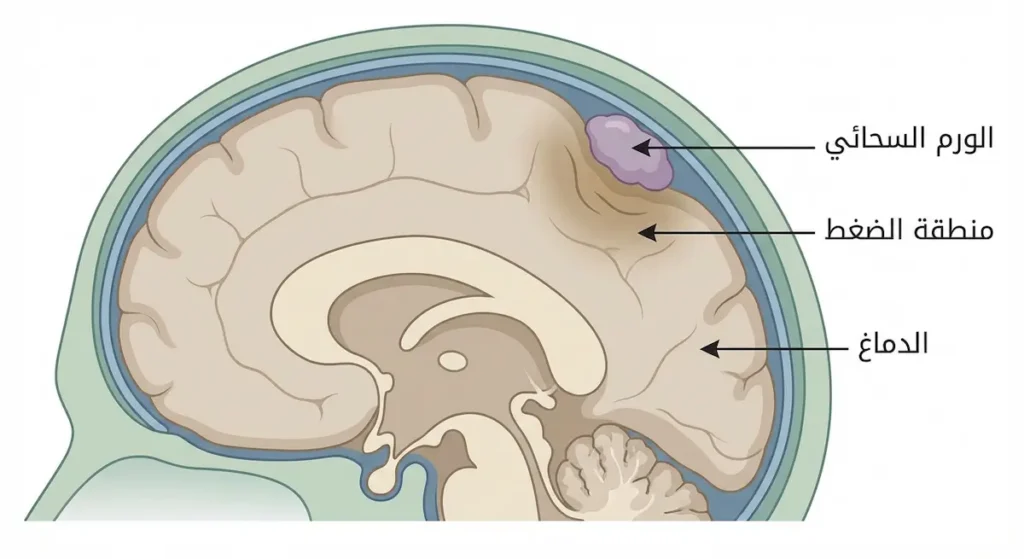
رغم أن كلمة “حميد” توحي بالأمان الكامل، إلا أن الحقيقة أكثر تعقيداً. متى يكون الورم الحميد خطيراً؟ الإجابة تكمن في ثلاثة سيناريوهات رئيسة:
السيناريو الأول: الضغط على أعضاء حيوية. ورم سحائي حميد بحجم 3 سنتيمترات في الدماغ يمكنه أن يُعطّل وظائف حيوية إذا نما في منطقة تتحكم بالرؤية أو التنفس أو التوازن. المساحة داخل الجمجمة محدودة جداً، وأي كتلة إضافية ترفع الضغط داخل القحف (Intracranial Pressure) مسببةً أعراضاً قد تهدد الحياة. وبالمثل، ورم حميد في المنصف (Mediastinum) قد يضغط على القصبة الهوائية ويعيق التنفس.
السيناريو الثاني: الإفراز الهرموني المفرط. بعض الأورام الحميدة ليست “ساكنة” بل “نشطة وظيفياً” (Functional Tumors). ورم القواتم (Pheochromocytoma) في الغدة الكظرية يُفرز كميات هائلة من الأدرينالين والنورأدرينالين، مما يسبب نوبات ارتفاع حاد في ضغط الدم قد تؤدي لسكتة دماغية أو أزمة قلبية. ورم الغدة النخامية المُفرز للبرولاكتين (Prolactinoma) يُعطل الدورة الشهرية ويسبب العقم عند النساء وضعف الرغبة الجنسية عند الرجال.
السيناريو الثالث: النمو السريع المفاجئ. إذا لاحظت أن كتلة كانت ثابتة الحجم لأشهر بدأت فجأة تكبر بسرعة، أو تغير لونها، أو بدأت تنزف، فهذا يستوجب مراجعة عاجلة. النمو السريع ليس دائماً دليلاً على التحول الخبيث، لكنه علامة تحذيرية لا يجب تجاهلها أبداً.
اقرأ أيضاً: أمراض القلب: ما الذي يجب أن تعرفه لحماية قلبك؟
⚡ هل تعلم؟
أكبر ورم حميد مُسجَّل طبياً كان ورماً مبيضياً (Ovarian Tumor) بلغ وزنه أكثر من 137 كيلوغراماً! أُزيل جراحياً عام 1991 في الولايات المتحدة. هذا الرقم المذهل يوضح إلى أي حد يمكن أن ينمو ورم حميد إذا أُهمل لسنوات طويلة دون تشخيص.
المصدر: موسوعة غينيس للأرقام القياسية (Guinness World Records)
هل يمكن أن يتحول الورم الحميد إلى سرطان؟
هل يتحول الورم الحميد إلى سرطان؟ هذا السؤال يُقلق ملايين المرضى حول العالم. الإجابة الطبية الدقيقة هي: معظم الأورام الحميدة لا تتحول أبداً إلى أورام خبيثة. الأورام الشحمية مثلاً لها احتمالية تحوّل تكاد تكون صفرية. الأورام الليفية الرحمية كذلك نادراً جداً ما تتحول، ونسبة التحول المُوثقة لا تتعدى 0.1-0.5%.
لكن هناك استثناءات مهمة يجب أن يعرفها كل مريض:
أولاً، سلائل القولون الغدية (Adenomatous Polyps). هذه السلائل تُعَدُّ “آفات ما قبل سرطانية” (Precancerous Lesions)، ومع مرور الوقت — عادةً 10 إلى 15 سنة — قد يتحول بعضها إلى سرطان قولون (Colorectal Cancer). لذلك يوصي أطباء الجهاز الهضمي بإجراء تنظير القولون (Colonoscopy) بدءاً من سن 45 وإزالة أي سلائل فوراً أثناء التنظير. في السعودية أطلقت وزارة الصحة حملات توعوية مكثفة في السنوات الأخيرة لتشجيع فحص القولون المبكر بعد أن أظهرت إحصائيات السجل الوطني للأورام ارتفاعاً ملحوظاً في حالات سرطان القولون بين السعوديين.
ثانياً، بعض أورام الثدي الحميدة. الورم الحليمي داخل القنوات (Intraductal Papilloma) والورم الفصيصي غير النموذجي (Atypical Lobular Hyperplasia) يحملان خطراً مرتفعاً نسبياً للتحول، وقد ينصح الطبيب بالاستئصال الوقائي والمتابعة المكثفة.
ثالثاً، بعض الأورام العظمية الغضروفية. في حالات نادرة، خاصة عند وجود أورام غضروفية متعددة (Hereditary Multiple Exostoses)، قد يتحول جزء غضروفي من الورم إلى ساركوما غضروفية (Chondrosarcoma). النسبة لا تتجاوز 1-5% لكنها تستوجب مراقبة طويلة الأمد.
احتمالية تحول الأورام الحميدة إلى خبيثة حسب النوع
| نوع الورم الحميد | نسبة خطر التحول للخبيث | المدة المتوقعة للتحول | الإجراء الموصى به |
|---|---|---|---|
| الورم الشحمي (Lipoma) | أقل من 0.1% | لا ينطبق (نادر جداً) | مراقبة دورية بسيطة |
| الورم الليفي الرحمي (Uterine Fibroid) | 0.1% – 0.5% | لا ينطبق (نادر جداً) | مراقبة مع متابعة الحجم |
| سلائل القولون الغدية (Adenomatous Polyps) | 5% – 10% | 10 – 15 سنة | إزالة فورية أثناء التنظير |
| الورم الحليمي داخل القنوات (Intraductal Papilloma) | 2% – 5% | متغيرة | استئصال وقائي + متابعة |
| الأورام الغضروفية المتعددة (HME) | 1% – 5% | سنوات طويلة | مراقبة طويلة الأمد بالأشعة |
| الورم السحائي (Meningioma) | أقل من 2% (الدرجة الأولى) | متغيرة | متابعة بالرنين المغناطيسي |
| المصادر: المعهد الوطني الأمريكي للسرطان (NCI) | الجمعية الأمريكية للسرطان (ACS) | إرشادات EANO للأورام السحائية (2021) | |||
إذاً، القاعدة العامة هي أن الورم الحميد “بريء حتى يثبت العكس”، لكن المتابعة الدورية تظل ضرورية لأنها الطريقة الوحيدة لاكتشاف أي تغير مبكر.
🔍 معلومة تستحق الانتباه:
أثبتت دراسة شاملة (Meta-analysis) منشورة في مجلة Gastroenterology عام 2020 أن إزالة سلائل القولون أثناء التنظير تُقلل خطر الإصابة بسرطان القولون بنسبة تصل إلى 80%. هذا يعني أن إجراءً بسيطاً مدته 30 دقيقة قد ينقذ حياتك حرفياً.
المصدر: مجلة Gastroenterology – الجمعية الأمريكية لأمراض الجهاز الهضمي (AGA)
ما أحدث طرق علاج واستئصال الورم الحميد؟
علاج الورم الحميد ليس قالباً واحداً يناسب الجميع. القرار العلاجي يعتمد على نوع الورم وحجمه وموقعه وأعراضه وعمر المريض وحالته الصحية العامة. فيما يلي الخيارات المتاحة مرتبة من الأقل تدخلاً إلى الأكثر:
مقارنة طرق علاج الورم الحميد: المزايا، العيوب، وفترة التعافي
| طريقة العلاج | آلية العمل | المزايا | العيوب | فترة التعافي |
|---|---|---|---|---|
| المراقبة (Watchful Waiting) | متابعة دورية بالتصوير دون تدخل | لا مخاطر جراحية، مناسبة للأورام الصغيرة | قلق نفسي مستمر لدى بعض المرضى | لا ينطبق |
| العلاج الدوائي | أدوية لتقليص الورم أو التحكم بالهرمونات | يتجنب الجراحة، فعال في أورام النخامية | الورم قد يعود بعد إيقاف الدواء | مستمر طوال فترة العلاج |
| الجراحة المفتوحة | شق جراحي تقليدي لاستئصال الورم | استئصال كامل، مناسبة للأورام الكبيرة | ندبة أكبر، فترة تعافٍ أطول | 4 – 6 أسابيع |
| جراحة المناظير (Laparoscopic) | فتحات صغيرة (1 سم) مع كاميرا | ألم أقل، ندبات صغيرة، تعافٍ سريع | غير مناسبة لكل الأورام | 1 – 2 أسبوع |
| التجميد الكرايوجيني (Cryoablation) | تجميد الورم بالنيتروجين السائل | طفيف التوغل، مناسب لأورام الكبد والكلى | محدود بأحجام صغيرة | أيام قليلة |
| سد الأوعية (Embolization) | حقن مواد تسد الشرايين المغذية للورم | يحافظ على العضو، بديل للجراحة | ألم بعد الإجراء، احتمال عودة الورم | 1 – 2 أسبوع |
| الموجات المركزة (HIFU) | موجات صوتية مركزة تدمر الورم حرارياً | غير جراحية تماماً، بدون شق | محدودة التوفر، تحتاج أجهزة متقدمة | يوم واحد – 3 أيام |
| المصادر: الكلية الأمريكية لأطباء النساء والتوليد (ACOG) | الجمعية الأمريكية للأشعة (RSNA) | مكتبة الطب الوطنية الأمريكية (NLM/NIH) | ||||
المراقبة والانتظار (Watchful Waiting): متى يكتفي الطبيب بالملاحظة فقط؟
إذا كان الورم صغير الحجم ولا يسبب أعراضاً ومؤكد الحميدية بالخزعة، فقد يختار الطبيب عدم التدخل والاكتفاء بمتابعة دورية بالتصوير كل 6 إلى 12 شهراً. هذا النهج شائع جداً مع الأورام الشحمية الصغيرة والأورام السحائية المستقرة وعقيدات الغدة الدرقية التي لا تُفرز هرمونات. الفكرة بسيطة: لماذا تُعرّض المريض لمخاطر الجراحة والتخدير إذا كان الورم لا يُلحق أي ضرر؟
العلاج الدوائي: حبوب بدل المشرط
في بعض الحالات تُستخدم أدوية لتقليص حجم الورم أو السيطرة على أعراضه. الأمثلة تشمل:
- أدوية الأغونيست لهرمون GnRH (مثل Leuprolide) لتقليص الأورام الليفية الرحمية قبل الجراحة.
- دواء كابيرغولين (Cabergoline) لعلاج ورم الغدة النخامية المُفرز للبرولاكتين، وهو فعال لدرجة أنه يُغني عن الجراحة في 80% من الحالات.
- حاصرات بيتا (Beta-blockers) مثل البروبرانولول (Propranolol) لعلاج الأورام الوعائية الكبيرة عند الرضع.
الاستئصال الجراحي: الحل الجذري
استئصال الورم الحميد جراحياً يظل الخيار الأمثل عندما يسبب الورم أعراضاً مزعجة أو يزداد حجمه أو يقع في منطقة حساسة. الجراحة التقليدية المفتوحة لا تزال تُستخدم في الأورام الكبيرة أو العميقة، لكن التطور الأبرز في العقد الأخير هو التحول نحو جراحة المناظير (Laparoscopic Surgery) والجراحة الروبوتية (Robotic Surgery) التي تُجرى من خلال فتحات لا يتجاوز قطرها سنتيمتراً واحداً. في مستشفيات الرياض وجدة والدمام أصبحت عمليات استئصال أورام الرحم والغدة الكظرية بالمناظير هي المعيار الذهبي (Gold Standard) مع فترة تعافٍ أقصر بكثير من الجراحة التقليدية.
تقنيات حديثة واعدة: ما بعد المشرط
التقنيات التالية تمثل مستقبل علاج الأورام الحميدة:
- التجميد الكرايوجيني (Cryoablation): يُستخدم فيه النيتروجين السائل لتجميد خلايا الورم وتدميرها دون جراحة مفتوحة. فعال في أورام الكبد والكلى الصغيرة.
- الاستئصال بالليزر (Laser Ablation): يُستخدم خاصة في أورام الجلد والحنجرة الحليمية.
- سد الأوعية الدموية المغذية للورم (Embolization): تقنية يقوم فيها أخصائي الأشعة التداخلية بحقن مواد تسد الشرايين التي تُغذي الورم بالدم، فيتقلص الورم ويموت تدريجياً. تُستخدم بكثرة في الأورام الليفية الرحمية كبديل للاستئصال الجراحي عند النساء الراغبات بالحفاظ على الرحم.
- الموجات فوق الصوتية المركزة عالية الكثافة (HIFU): تقنية غير جراحية تماماً تستخدم موجات صوتية مركزة لتسخين نسيج الورم وتدميره. بدأ استخدامها في عدد من المراكز السعودية المتقدمة لعلاج أورام الرحم الليفية.
📋 بروتوكولات وإرشادات طبية رسمية حديثة
- فحص سرطان القولون المبكر (2021): يوصي فريق الخدمات الوقائية الأمريكي (USPSTF) ببدء فحص القولون من سن 45 عاماً بدلاً من 50، مع إزالة أي سلائل فوراً لتقليل خطر التحول الخبيث.
- إرشادات EANO للأورام السحائية (2021): توصي الجمعية الأوروبية لأورام الأعصاب (EANO) بالمراقبة بالرنين المغناطيسي كل 6 أشهر للأورام السحائية الصغيرة بدون أعراض، مع التدخل الجراحي فقط عند ظهور نمو أو أعراض عصبية.
- بروتوكول الأورام الليفية الرحمية (2024): تُوصي الكلية الأمريكية لأطباء النساء والتوليد (ACOG) بأن سد الأوعية الرحمية (UAE) وتقنية HIFU خياران معتمدان للنساء الراغبات في الحفاظ على الرحم.
- إرشادات وزارة الصحة السعودية (2023-2024): أطلقت وزارة الصحة السعودية برنامج الكشف المبكر عن سرطان القولون ضمن مبادرات الرعاية الوقائية، مع توفير تنظير القولون المجاني في المراكز الصحية الحكومية للفئات العمرية المستهدفة.
- إرشادات وزارة الصحة الإماراتية (2024): تُوصي وزارة الصحة ووقاية المجتمع الإماراتية (MOHAP) بإجراء فحوصات دورية شاملة تشمل تصوير الثدي بالماموغرام للنساء فوق 40 عاماً وفحص القولون للرجال والنساء فوق 45 عاماً.
اقرأ أيضاً: النانوتكنولوجيا (Nanotechnology): المفهوم، التطبيقات، والمستقبل
ما الذي يحدث بعد العلاج وكيف يكون التعافي؟
فترة التعافي بعد استئصال الورم الحميد تختلف جذرياً بحسب نوع العملية. الاستئصال بالمنظار يتطلب عادةً يوماً إلى ثلاثة أيام فقط في المستشفى مع عودة كاملة للنشاط خلال أسبوعين. الجراحة المفتوحة قد تتطلب أسبوعاً في المستشفى وفترة نقاهة تمتد من 4 إلى 6 أسابيع. في كلتا الحالتين، ينصح الأطباء بالتدرج في العودة للأنشطة البدنية وعدم رفع أوزان ثقيلة خلال الأسابيع الأولى.
من الضروري أن يلتزم المريض بالمراجعات الدورية بعد الاستئصال. تشمل هذه المتابعة عادةً فحصاً بالتصوير (أشعة أو موجات صوتية) بعد 3 أشهر من العملية، ثم كل 6 أشهر لمدة عامين، ثم سنوياً بعد ذلك. الهدف من المتابعة ليس فقط التأكد من عدم عودة الورم، بل أيضاً اكتشاف أي مضاعفات مبكرة مثل التصاقات (Adhesions) أو عدوى في موقع الجراحة.
اقرأ أيضاً: الإنتان (Sepsis): الأسباب، الأعراض، والعلاج
هل يعود الورم الحميد بعد استئصاله؟
هل يعود الورم الحميد بعد استئصاله؟ الإجابة تعتمد على نوع الورم ومدى اكتمال الاستئصال. الأورام الشحمية التي تُستأصل بالكامل مع كبسولتها نادراً ما تعود. الأورام السحائية بالمقابل لديها معدل عودة يتراوح بين 7-20% خلال عشر سنوات حتى مع الاستئصال الكامل، بحسب تصنيفها النسيجي. الأورام الليفية الرحمية قد تعود بنسبة تصل إلى 15-30% خلال خمس سنوات بعد الاستئصال الجراحي إذا تم الحفاظ على الرحم (Myomectomy) بدلاً من استئصاله كاملاً (Hysterectomy). وعليه فإن قرار المتابعة طويلة الأمد ليس ترفاً بل ضرورة طبية.
نسبة عودة الورم الحميد بعد الاستئصال حسب النوع
| نوع الورم | نسبة العودة بعد الاستئصال الكامل | فترة المتابعة المطلوبة | أداة المتابعة الموصى بها |
|---|---|---|---|
| الورم الشحمي (Lipoma) | 1% – 2% | فحص سنوي بسيط | فحص سريري |
| الورم الليفي الرحمي (بعد Myomectomy) | 15% – 30% خلال 5 سنوات | كل 6 أشهر لمدة 3 سنوات ثم سنوياً | موجات فوق صوتية (Ultrasound) |
| الورم السحائي – الدرجة الأولى | 7% – 20% خلال 10 سنوات | كل 6 أشهر لمدة 5 سنوات ثم سنوياً | رنين مغناطيسي (MRI) |
| سلائل القولون الغدية | 30% – 40% (سلائل جديدة، ليس نفسها) | تنظير قولون كل 3 – 5 سنوات | تنظير القولون (Colonoscopy) |
| ورم الغدة النخامية (بعد الجراحة) | 10% – 25% خلال 10 سنوات | كل 6 أشهر لمدة 5 سنوات | رنين مغناطيسي + فحص هرمونات |
| المصادر: إرشادات EANO للأورام السحائية (Neuro-Oncology, 2021) | Nature Reviews Disease Primers – الأورام الليفية الرحمية (2017) | فريق الخدمات الوقائية الأمريكي (USPSTF) | |||
📌 نصيحة من موسوعة خلية للتعافي:
بعد أي عملية استئصال لورم حميد، احتفظ بنسخة ورقية ورقمية من تقرير الخزعة النسيجية. هذا التقرير يُعَدُّ “بطاقة هوية” الورم ويحتاجه أي طبيب تراجعه مستقبلاً. كثير من المرضى يُضيعون هذه الوثيقة ويُعيدون فحوصات مكلفة كان يمكن تجنبها.
الأسئلة الشائعة
اضغط على رمز + لمعرفة الإجابة
❓ أسئلة شائعة حول الورم الحميد
الخاتمة
لقد استعرضنا في هذا المقال كل ما يتعلق بالورم الحميد من الألف إلى الياء: بدءاً من آلية تكوّنه على المستوى الخلوي، مروراً بأنواعه المتعددة التي تتراوح بين الأورام الشحمية البسيطة والأورام السحائية المعقدة، وصولاً إلى أحدث تقنيات العلاج التي تشمل الجراحة الروبوتية والتجميد الكرايوجيني وسد الأوعية المغذية. النقطة الأهم التي أريدك أن تخرج بها هي أن الورم الحميد في الغالبية الساحقة من الحالات لا يُمثل تهديداً على الحياة، لكنه يستوجب تشخيصاً دقيقاً ومتابعة منتظمة. لا تُهمل أي كتلة غريبة تشعر بها في جسمك مهما بدت صغيرة أو غير مؤلمة. التشخيص المبكر هو نصف العلاج فعلاً وليس مجرد شعار. استشر طبيبك المختص، واطلب الخزعة إذا أوصى بها، واسأل عن كل الخيارات المتاحة قبل اتخاذ أي قرار.
هل أجريت فحصك الطبي الدوري هذا العام؟ إذا لم تفعل، فربما حان الوقت لحجز موعدك اليوم.
⚠️ تحذير طبي وإخلاء مسؤولية
المعلومات الواردة في هذا المقال مُقدَّمة من موسوعة خلية لأغراض التثقيف الصحي العام فقط، ولا تُغني بأي حال عن الاستشارة الطبية المتخصصة أو التشخيص أو العلاج من قبل طبيب مرخص. كل حالة طبية فريدة ويجب تقييمها بشكل فردي. لا تتوقف عن تناول أي دواء أو تبدأ علاجاً جديداً بناءً على ما قرأته هنا دون مراجعة طبيبك المعالج. إذا كنت تعاني من أعراض مقلقة أو اكتشفت كتلة غريبة في جسمك، فتوجه إلى أقرب مرفق صحي فوراً.
🛡️ بيان المصداقية
تلتزم موسوعة خلية بأعلى معايير الدقة والشفافية في المحتوى الصحي المنشور. يعتمد هذا المقال على مصادر طبية محكّمة تشمل دراسات من مجلات علمية مرموقة (JAMA, The Lancet, Nature Reviews) وإرشادات رسمية من منظمة الصحة العالمية (WHO) والمعهد الوطني الأمريكي للسرطان (NCI) والجمعية الأمريكية للسرطان (ACS). جرت مراجعة المحتوى الطبي والتغذوي والدوائي من قبل أعضاء متخصصين في هيئة التحرير العلمية. نحرص على تحديث مقالاتنا بانتظام لتعكس أحدث الأدلة العلمية المتاحة.
المصادر والمراجع
الدراسات والأوراق البحثية:
- Fletcher, C. D. M. (2021). “Diagnostic Histopathology of Tumors.” Elsevier, 5th Edition.
- DOI: 10.1016/C2015-0-01845-2
- مرجع شامل للتصنيف النسيجي لجميع أنواع الأورام الحميدة والخبيثة.
- Stewart, E. A., Laughlin-Tommaso, S. K., Catherino, W. H., et al. (2017). “Uterine fibroids.” Nature Reviews Disease Primers, 3, 17043.
- DOI: 10.1038/nrdp.2017.43
- مراجعة شاملة لأورام الرحم الليفية: الأسباب والتشخيص والعلاج.
- Goldbrunner, R., Stavrinou, P., Jenkinson, M. D., et al. (2021). “EANO guideline on the diagnosis and management of meningiomas.” Neuro-Oncology, 23(11), 1821–1834.
- DOI: 10.1093/neuonc/noab150
- إرشادات أوروبية محدثة لتشخيص وعلاج الأورام السحائية.
- Rindi, G., Klimstra, D. S., Abedi-Ardekani, B., et al. (2022). “A common classification framework for neuroendocrine neoplasms.” The Lancet Oncology, 23(3), e137–e143.
- DOI: 10.1016/S1470-2045(21)00581-3
- إطار تصنيفي موحد للأورام العصبية الصماوية.
- Click, B., Pinsky, P. F., Hickey, T., et al. (2018). “Association of Colonoscopy Adenoma Findings With Long-term Colorectal Cancer Incidence.” JAMA, 319(19), 2021–2031.
- DOI: 10.1001/jama.2018.5809
- دراسة تُثبت أن إزالة سلائل القولون تُقلل خطر سرطان القولون بشكل كبير.
- Léauté-Labrèze, C., Harper, J. I., Hoeger, P. H., et al. (2017). “Infantile haemangioma.” The Lancet, 390(10089), 85–94.
- DOI: 10.1016/S0140-6736(16)00645-0
- مراجعة شاملة للأورام الوعائية عند الرضع وخيارات العلاج الحديثة.
الجهات الرسمية والمنظمات:
- World Health Organization (WHO). (2024). “Classification of Tumours: WHO Classification of Tumours Editorial Board.”
- الرابط: https://tumourclassification.iarc.who.int/
- التصنيف الدولي الرسمي للأورام الصادر عن منظمة الصحة العالمية.
- American Cancer Society (ACS). (2023). “What Are Benign Tumors?”
- الرابط: https://www.cancer.org/
- دليل تعريفي مبسط يشرح الفرق بين الأورام الحميدة والخبيثة.
- National Cancer Institute (NCI/NIH). (2023). “Understanding Cancer: Benign Tumors.”
- الرابط: https://www.cancer.gov/
- معلومات رسمية من المعهد الوطني الأمريكي للسرطان.
- Mayo Clinic. (2024). “Uterine Fibroids: Diagnosis and Treatment.”
- الرابط: https://www.mayoclinic.org/diseases-conditions/uterine-fibroids
- بروتوكولات تشخيص وعلاج الأورام الليفية من مايو كلينك.
- Saudi Health Council – National Cancer Registry. (2023). “Cancer Incidence Report: Saudi Arabia.”
- الرابط: https://nhic.gov.sa/
- تقرير السجل الوطني السعودي للأورام.
الكتب والموسوعات العلمية:
- Kumar, V., Abbas, A. K., & Aster, J. C. (2021).Robbins & Cotran Pathologic Basis of Disease. 10th Edition, Elsevier.
- كتاب مرجعي أساسي في علم الأمراض يُغطي بالتفصيل آليات تكون الأورام.
- DeVita, V. T., Lawrence, T. S., & Rosenberg, S. A. (2019).DeVita, Hellman, and Rosenberg’s Cancer: Principles & Practice of Oncology. 11th Edition, Wolters Kluwer.
- مرجع شامل في طب الأورام يتناول الفرق بين الأورام الحميدة والخبيثة.
- WHO Classification of Tumours Editorial Board. (2020).WHO Classification of Soft Tissue and Bone Tumours. 5th Edition, IARC Press.
- التصنيف النسيجي الرسمي لأورام الأنسجة الرخوة والعظام.
مقالات علمية مبسطة:
- Mukherjee, S. (2022). “The New Understanding of Cancer.” Scientific American, 326(4), 30–37.
- الرابط: https://www.scientificamerican.com/
- مقال مبسط يشرح التطورات الحديثة في فهم آليات الأورام.
قراءات إضافية ومصادر للتوسع
- Weinberg, R. A. (2013).The Biology of Cancer. 2nd Edition, Garland Science.
- لماذا نقترح عليك قراءته؟ هذا الكتاب يُعَدُّ الأشهر عالمياً في شرح البيولوجيا الجزيئية للأورام بأسلوب أكاديمي عميق لكنه مفهوم. يناسب طلاب الطب والعلوم الحيوية الراغبين في فهم كيف تتحول الخلايا الطبيعية إلى ورمية.
- Pecorino, L. (2021).Molecular Biology of Cancer: Mechanisms, Targets, and Therapeutics. 5th Edition, Oxford University Press.
- لماذا نقترح عليك قراءته؟ يقدم شرحاً مركّزاً للآليات الجزيئية التي تحكم نمو الأورام مع فصل كامل عن الفرق بين الأورام الحميدة والخبيثة على المستوى الجيني.
- Hanahan, D. (2022). “Hallmarks of Cancer: New Dimensions.” Cancer Discovery, 12(1), 31–46. DOI: 10.1158/2159-8290.CD-21-1059
- لماذا نقترح عليك قراءته؟ هذه الورقة البحثية هي التحديث الأخير لنظرية “السمات المميزة للسرطان” الشهيرة. فهمها يُعطيك القدرة على التمييز العلمي الدقيق بين السلوك الحميد والخبيث للخلايا.
إذا كنت قد وصلت إلى هذا السطر فأنت من النوع الذي يبحث عن المعرفة الحقيقية ولا يكتفي بالعناوين. شارك هذا المقال مع شخص قريب منك قد يستفيد منه، واحجز فحصك الدوري هذا العام. صحتك تستحق أن تكون أولويتك الأولى.





